Какой маркер принят в качестве маркера выбора при незрелой тератоме
Незрелые тератомы состоят из производных трех зародышевых листков: эктодермы, мезодермы и эндодермы; в отличие от зрелых тератом они содержат незрелые или эмбриональные структуры. Эти опухоли называли по-разному: солидная тератома, злокачественная тератома, тератобластома, тератокарцинома и эмбриональная тератома. Эти названия были обусловлены тем, что незрелые тератомы неправильно считали смешанными герминогенными или вторичными злокачественными опухолями, происходящими из зрелых доброкачественных тератом. В них часто присутствуют, а иногда и преобладают зрелые ткани. Незрелая тератома яичников — редкая опухоль, составляющая менее 1 % тератом этой локализации.
В отличие от зрелой кистозной тератомы, чаще диагностируемой в репродуктивный период, хотя и встречающейся в любом возрасте, пик заболеваемости незрелой тератомой приходится главным образом на первые две декады жизни. Эти опухоли не развиваются после наступления менопаузы. По определению, незрелая тератома содержит незрелые компоненты нервной ткани. По мнению Norris и соавт., степень дифференцировки этих опухолей определяется исключительно количеством незрелой нервной ткани. Также могут присутствовать нейробластомные элементы, глиальная ткань, незрелые ткани мозжечка и коры мозга. Гистологическая дифференцировка этих опухолей основана на количестве и степени незрелости клеток.
Первая степень (G1) представлена зрелой тератомой, содержащей редкие незрелые очаги, а при G3 большая часть новообразования представлена эмбриональной тканью с атипией и митотической активностью. У старших пациенток по сравнению с молодыми первичная опухоль имеет более низкую степень дифференцировки. При зрелой опухоли с хорошо дифференцированными элементами (солидная зрелая тератома) устанавливают степень G0.
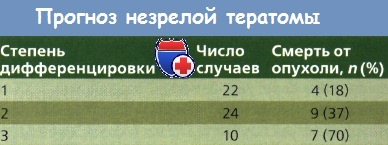
Незрелые тератомы почти никогда не бывают двусторонними; крайне редко в противоположном яичнике обнаруживают доброкачественную тератому. При первичном хирургическом лечении могут быть выявлены множественные имплантаты незрелой тератомы в брюшной полости; прогноз при этом тесно связан с гистологической степенью дифференцировки и числом метастазов. Norris и соавт. обследовали 58 пациенток и сообщили о различной 5-летней выживаемости в зависимости от степени дифференцировки первичных незрелых тератом: при высокодифференцированных (G1) — 82 %, умереннодифференцированных(G2) — 63 %, низкодифференцированных (G3) — 30 %. Эти результаты получены до применения многокомпонентной химиотерапии (ХТ).
Для точного определения степени дифференцировки необходимы множественные биопсии первичной опухоли и широкие срезы биоптатов или полное удаление имплантатов. В большинстве случаев последние более дифференцированы, чем первичная опухоль. Степень дифференцировки как самой опухоли, так и ее имплантатов устанавливают по наименее зрелой ткани. Для больных со зрелыми глиальными метастазами прогноз хороший, с незрелыми — плохой.
Степень дифференцировки опухоли и желание пациентки иметь детей — факторы, определяющие объем хирургического вмешательства и последующей адъювантной терапии. Поскольку опухоль редко бывает двусторонней, выполняют одностороннюю аднексэктомию с удалением многочисленных имплантатов. Абдоминальная гистерэктомия с двусторонней аднексэктомией не показана, поскольку она не влияет на исход заболевания. Хотя некоторые авторы выполняют цистэктомию при ранних стадиях и высокой степени дифференцировки опухоли, такой подход требует осторожности. ЛТ малоэффективна.
При высокодифференцированной первичной опухоли (G1) и всех метастазах брюшины, если таковые имеются, степени дифференцировки G0 дальнейшее лечение не требуется.
Однако, если основная опухоль умеренно- или низкодифференцированная (G2 или G3), а имплантаты или рецидивы имеют степень дифференцировки G1, G2 или G3, показана трехкомпонентная химиотерапия (XT). Рекомендации по использованию адъювантной химиотерапии (XT) при низкодифференцированной опухоли I стадии основаны на исследованиях, выполненных до того, как в практику вошло тщательное хирургическое стадирование. Cushing и соавт. обследовали 44 девочек и девушек моложе 15 лет после полной резекции незрелых тератом любой степени дифференцировки.
У 31 пациентки была чистая незрелая тератома, а у 13 — незрелая тератома с микроскопическими очагами опухоли желточного мешка. Общая и 4-летняя безрецидивная выживаемость в обеих группах составила 100 и 97 % соответственно. Только в 1 случае смешанной опухоли с компонентом новообразования желточного мешка понадобилась химиотерапия (XT). Авторы сделали вывод, что большинству детей и подростков с полностью удаленными незрелыми тератомами яичников любой степени дифференцировки достаточно одного хирургического лечения. Они советуют избегать адъювантной химиотерапии (XT) в этой группе пациенток. Схема VAC доказала свою высокую эффективность.
DiSaia и соавт. сообщили о нескольких больных с диссеминированной незрелой тератомой, получивших химиотерапию (XT) по этой схеме.
Во время лапаротомии «second-look» у них не обнаружили незрелых тканей, а оставшиеся перитонеальные имплантаты содержали только зрелые элементы. Этот феномен назвали химиотерапевтической ретроконверсией незрелой тератомы яичников, похожей или идентичной синдрому созревания тератомы при несеминомных герминогенных опухолях яичек. За период наблюдения у этих пациенток не возникли рецидивы, зрелые имплантаты, очевидно, оставались в статическом состоянии, подтверждая предшествующее общее правило.
Curry и соавт. представили опыт лечения 25 больных (средний возраст к моменту постановки диагноза 19 лет) с незрелыми тератомами яичников. В этом исследовании 4 пациентки получили послеоперационное дистанционное облучение таза или живота в самостоятельном виде либо в сочетании с химиотерапией (XT) одним препаратом, 2 — химиотерапии (XT) в режиме монотерапии и 2 — не получили никакого лечения, кроме хирургического. Все 8 женщин умерли от опухоли, наибольший период выживаемости составил 40 мес, 6 из 8 пациенток прожили менее 12 мес. после первичного лечения. Следующие 5 больных получили послеоперационную ПХТ по схеме MAC или ActFUCy; 2 оставались живы через 73 и 50 мес. после начала XT. ПХТ по схеме VAC (винкристин 1,5 мг/м2, дактиномицин 0,5 мг и циклофосфамид 500 мг) получили остальные 12 пациенток.
Препараты вводили в/в еженедельно в течение 12 нед., а затем 5-дневный в/в курс проводили каждые 4 нед. в течение 2 лет.
На момент публикации 10 пациенток с первоначальным ответом на химиотерапию (XT) были живы через 16—28 мес. после ее начала. Из 12 больныхдвое не прореагировали на химиотерапию (XT): одна умерла через 3 мес, а другая — через 26 мес. после лечения.
Специалисты GOG провели лечение 20 больных после полной резекции незрелых тератом по схеме VAC. Неудачное лечение отмечено только в 1 случае, причем терапия была назначена после выявления рецидива. Из 8 пациенток с поздними стадиями заболевания или рецидивными поражениями после неполной резекции только 4 прореагировали на схему VAC. Группа врачей из M.D. Anderson Hospital сообщила о ремиссии после первичной химиотерапии (XT) по схеме VAC у 15 (83 %) из 18 пациенток. GOG провела лечение поздних стадий или рецидивных незрелых тератом, используя XT по схеме VBP. Из 26 больных 14 (54 %) выжили без признаков болезни. Creasman лечил 6 пациенток с незрелыми тератомами, используя схему MAC: у всех отмечена отдаленная выживаемость. Schwartz при I стадии заболевания обычно назначает 6 циклов VAC.
При поздних стадиях заболевания автор проводил 12 циклов XT, а затем контрольную лапаротомию «second-look». Из 29 пациенток у 24 лечение было успешным. 4 из 5 больных с персистирующими остаточными опухолями удалось спасти.
В настоящее время большинство исследователей при Iа стадии высокодифференцированных(G1) незрелых тератом ограничиваются односторонней овариэктомией. При Iа стадии со степенью дифференцировки G1, G2, а также при поздних стадиях заболевания после хирургического лечения назначают схему VAC. Три курса XT столь же эффективны, как и большее их число, особенно после полного удаления опухоли.
Bonazzi и соавт. из Италии сообщили о собственном опыте лечения 32 больных с чистыми незрелыми тератомами, которые составили 28 % всех герминогенных опухолей в их практике. У 29 пациенток была I или II стадия, из них у 24 высоко- и умереннодифференцированные (G1, G2) опухоли. Только органосохраняющую операцию (одностороннюю овариэктомию или цистэктомию) выполнили 22 больным. Из 32 пациенток хирургическое вмешательство с сохранением фертильности выполнили в 30 случаях. У 5 из 6 женщин, желавших иметь детей, было 7 беременностей, закончившихся рождением 7 нормальных новорожденных. XT после хирургического лечения проводили только при опухолях I и II стадий степени дифференцировки G3 или при III стадии заболевания. Противоопухолевую XT на основе препаратов платины получило 10 пациенток. При медиане наблюдения 47 мес. (диапазон 11 — 138 мес.) все 32 больные были живы, без признаков рецидивирования.
В настоящее время консервативное лечение герминогенных опухолей стало нормой. Даже при распространенном процессе можно провести одностороннюю овариэктомию с полным хирургическим стадированием и сохранением матки и другого яичника. К счастью, большинство герминогенных опухолей яичников диагностируют на ранней стадии; они чаще всего ограничены одним яичником. Короткие курсы XT показали отличные результаты. Это важно, поскольку нарушения менструальной функции (вплоть до аменореи) во время XT обусловлены ее продолжительностью. Впоследствии может нарушаться фертильность.
Однако отмечено, что у многих пациенток с герминогенными опухолями после лечения наступила беременность и они родили здоровых детей. Чем моложе женщина, тем меньше риск нарушения менструального цикла и бесплодия, и это справедливо для большинства пациенток с герминогенными опухолями. У женщин старшего возраста, в пременопаузе, например, при РМЖ наблюдается другая ситуация.
Во время химиотерапии (XT) в большинстве случаев развивается аменорея, нормальный менструальный цикл восстанавливается у небольшого числа женщин, таким образом, имеет место преждевременное прекращение функции яичников.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Онкология»
Материалы конгрессов и конференций
Значение опухолевых маркеров в клинике герминогенных опухолей яичка.
З.Г.Кадагидзе, В.М.Шелепова, А.В.Соколов
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
АФП представляет собой гликопротеин с молекулярной массой 70 кД. Он является физиологическим продуктом желточного мешка, печени и желудочно-кишечного тракта плода. Повышенный уровень сывороточного АФП у пациентов с герминогенными опухолями яичка был впервые обнаружен Абелевым в 1997 г. В герминогенных опухолях АФП продуцируется элементами эндодермального синуса (желточного мешка). У детей старше года, как и у взрослых, сывороточный АФП имеет верхнюю границу нормы 15 нг/мл (
В клинической практике эти маркёры используются для диагностики, мониторинга и прогноза герминогенных опухолей яичка.
Скрининг на наличие герминогенных опухолей по биохимическим тестам в общей популяции проводить не рекомендуется. При клиническом подозрении герминогенной опухоли (основанном на данных пальпации и УЗИ яичка) определение опухолевых маркёров может быть иногда полезным в дифференциальной диагностике злокачественной опухоли и эпидидимитов у пациентов с безболезненным опуханием одного из яичек. Использование маркёров в дополнение к рентгенологическому и ультразвуковому исследованию брюшной полости повышает диагностическую чувствительность в отношении как гонадных, так и внегонадных (медиастинальных, забрюшинных, центральной нервной системы) герминогенных опухолей.
Как можно видеть из представленных данных, все больные с герминогенными опухолями яичка в зависимости от наличия маркёров могут быть разделены на две группы. К первой группе (
20 %) относятся больные, опухоли которых не продуцируют АФП и ХГЧ. Это семиномы (типичные, анапластические и сперматозоидные), зрелые тератомы и так называемые эмбриональные карциномы чистого типа. Если они содержат гигантские клетки синцитиотрофобласта, может выявляться небольшое количество ХГЧ, концентрация которого редко превышает 75 мМЕ/мл в основном у больных с III стадией заболевания. Таким образом, отсутствие маркёров не исключает наличия опухолевого процесса. Ко второй группе (около 80% больных с герминогенными опухолями) относятся «маркёрные» больные. Это пациенты с опухолями желточного мешка, продуцирующими АФП, хорионкарциномами, продуцирующими ХГЧ, и со смешанными опухолями (эмбриональные карциномы или тератокарциномы с наличием других гистологических элементов), продуцирующими обычно АФП и/или ХГЧ. Данные по чувствительности маркёров в соответствии с гистологическим типом опухоли приведены в таблице 2.
| Гистологическое строение | АФП+ | ХГЧ+ |
| Несеминомные опухоли | ||
|---|---|---|
| Низко- и средне-дифференцированная злокачественная тератома | 70-72% | 55-60% |
| Зрелая тератома | 0% | 0% |
| Желточный мешок | 64% | 0% |
| Трофобластическая дифференцировка | 0% | 100% |
| Смешанные опухоли | 50-80% | 50-60% |
| Все | 60-80% | 40-60% |
| Семинома | ||
| Семинома | 0% | 15-20% |
Роль маркёров в лечении и наблюдении за больными.
Рациональное использование маркёров находится в соответствии со стадией заболевания.
Распространённые стадии II и III. Скорость снижения опухолевых маркёров после химиотерапии прогнозирует ответ на лечение. Устойчивое повышение уровня маркёра или удлинение полупериода его жизни в первые 6 недель после специфической химиотерапии указывают на резистентность опухоли и плохой прогноз. Пациенты с остаточной опухолевой массой после проведения химиотерапии могут быть подвергнуты оперативному лечению. Однако, в тех случаях, когда уровни маркёров устойчиво повышаются, пациенты чаще всего оказываются иноперабельными, и вместо операции им показана химиотерапия.
Таблица 3.
Вклад опухолевых маркёров в классификацию прогноза метастатических герминогенных опухолей
| Концентрация опухолевых маркёров | ||
| Группа прогноза1 | АФП (кЕ/л) ХГЧ (Е/л) ЛДГ (х RR)2 | |
| Хороший (S1) | 10 000 >50 000 >10 x (RR) | |
Таблица 4.
Прогностическая классификация для метастазирующих герминогенных опухолей, основанная на прогностических критериях UK MRC и измерении опухолевых маркёров.
| Классификация на основе | 10-летняя выживаемость | ||
| Группа прогноза | Прогностические критерии UK MRC | Полупериод жизни маркёров | |
| Хороший | Good risk | Нормальный («good») | 96% |
| Средний | Good risk | Нормальный полупериод жизни («good») | 64% |
| Poor risk | Увеличенный полупериод жизни («bad») | ||
| Плохой | Poor risk | Увеличенный («bad») | 28% |
Итак, герминогенные опухоли являются уникальным примером интеграции опухолевых маркёров в диагностику, стадирование и мониторинг терапии. При дифференциальной диагностике чистых семином и опухолей с трофобластическими элементами повышенные уровни ХГЧ более доказательны, чем гистологическое заключение, что имеет значение для выбора терапии. Помимо этого, определение опухолевых маркёров позволяет более аккуратно поставить стадию заболевания. Кинетика маркёров на протяжении первых 6 недель химиотерапии обеспечивает важную прогностическую информацию. У пациентов в ремиссии повышение уровней АФП и ХГЧ может прогнозировать рецидив за несколько месяцев до его клинического диагностирования. Определение маркёров показано при оценке ответа на терапию, а их нормализация является предпосылкой для успешной операции после воздействия химиотерапии.
Тератома яичника: разновидности, симптомы и лечение
Дермоидная киста яичника (тератома) представляет собой опухолевое образование, которое формируется в процессе внутриутробного развития. Данная опухоль в большинстве случаев доброкачественная. Тератома яичника может поражать как одну железу, так и обе одновременно. Кроме того, яичники – не единственный орган, где может локализоваться тератома. Несмотря на свою доброкачественность, опухоль следует удалить при первой возможности, поскольку она может доставлять женщине значительный дискомфорт, осложняться разрывами и нагноением, а также в редких случаях подвергаться малигнизации. В Москве лечение тератомы можно выполнить в Юсуповской больнице. Здесь работают опытные гинекологи, которые составят наиболее оптимальное лечение, позволяющее эффективно устранить проблему.
Тератома яичника: что это такое у женщин
Яичники представляют собой парные органы женской половой системы, которые продуцируют половые гормоны и в которых происходит созревание яйцеклеток. В некоторых случаях яичники могут поражаться различными патологиями, среди которых кисты – явление достаточно частое.
Тератома – это одна из разновидностей кисты, которая имеет смешанное строение. В ней обнаруживаются ткани, не характерные для данного органа: части ороговевшего эпителия и поперечнополосатых мышц, нервной ткани, фрагменты костей, зубов, волос и пр. В некоторых случаях обнаруживаются зачатки различных органов, например, глазного яблока или конечностей.
Тератома – врожденная патология, которая возникает во время внутриутробного развития. Она может локализоваться на любом органе. В области яичников она встречается в 20-30% случаев.
Длительный период времени новообразование может никак себя не проявлять. Его диагностируют либо во время профилактических посещений гинеколога, либо при диагностике нарушения работы половых органов женщины. Во многих случаях опухоль является доброкачественной, однако не исключено ее преобразование в онкологию. Поэтому заболевание требует повышенного внимания гинеколога и онколога.
Тератома яичника: причины возникновения
Тератома яичников формируется во время развития плода. Точная причина ее появления еще находится на стадии изучения. Существует ряд провоцирующих факторов, наличие которых значительно повышает вероятность возникновения тератомы. К таким факторам относятся:
Существует теория, что тератома – это следствием аномального развития однояйцевых близнецов, когда происходит поглощение одного близнеца другим. Доказательством тому является наличие в образовании не до конца сформированных элементов волос, зубов, мышечных волокон, тканей эпителия и желез.
Патология не обязательно имеет наследственную предрасположенность. То есть, если у матери была тератома яичника (или другого органа), это не говорит, о том, что у ее детей она также появится.
Специфической профилактики данного состояния не существует. Для исключения возможных рисков перед планированием и во время беременности женщине необходимо:
Тератома яичника: виды
В основной классификации тератомы разделяют на зрелые и незрелые. Зрелая тератома яичника обычно имеет кистозную (дермоидную) структуру. Для нее характерен медленный рост без поражения соседних тканей. Зрелая тератома обычно представляет собой плотный одиночный улез, покрытый фиброзной капсулой. В ней находится однокапсульная киста, ее полость заполнена содержимым, в котором обнаруживаются мышечные волокна, волосы или зубы, элементы железистой ткани, участки различного эпителия. Зрелая тератома не имеет склонности к быстрому прогрессированию и редко перерождается в злокачественную опухоль.
Настороженность онкологов вызывает незрелая тератома яичника. В ней содержатся эмбриональные ткани вместе с элементами зрелого эпителия. Чаще всего выявляются ткани нервной системы, но не исключены и элементы эмбрионального хряща и другие незрелые ткани.
Незрелые тератомы имеют признаки злокачественной опухоли, но формально онкологией не являются. Для них характерен агрессивный рост. Они могут прорастать в соседние ткани и даже метастазироваться. При этом в пораженных участках длительные период времени могут не отмечаться функциональные нарушения. Незрелые тератомы опасны тем, что могут перерождаться в раковые опухоли. При этом, чаще онкологический процесс отмечается в участках метастаз, а не в первичном новообразовании. Кроме того, незрелые тератомы могут подвергаться некротическим процессам с нагноением полости новообразования.
Тератома яичника: симптомы
Зрелая тератома яичника может длительный период времени никак себя не проявлять. Она может обнаруживаться случайно во время гинекологического осмотра или в процессе диагностики области внизу живота. Патология чаще выявляется в молодом возрасте: у детей и подростков. Новообразование также может быть обнаружено впервые у женщины во время беременности, что связано с ускорением роста опухоли в связи с изменением гормонального фона.
Кистозная тератома яичника может иметь следующие проявления:
Во время беременности тератомы требуют повышенного внимания, поскольку они могут провоцировать прерывание беременности и преждевременные роды. Тератомы могут осложняться перекрутом ножки с последующей некротизацией тканей. Такая ситуация является неотложно с обязательным срочным хирургическим вмешательством. Осложнения могут спровоцировать разрыв кисты с развитием перитонита.
При наличии незрелых тератом наблюдается общая вялость, хроническая усталость, в сочетании с болями в нижней части живота. С прогрессированием заболевания состояние женщины ухудшается, наблюдается стремительная потеря веса, бледность кожных покровов, отсутствие аппетита. На поздних стадиях с метастазами отмечается ярко выраженная раковая интоксикация с нарушением работы различных органов и систем.
Тератома яичника: диагностика
Перед назначением лечения должна быть диагностически определена тератома яичника. Размеры опухоли могут варьироваться от 1 до 15 см, что выявляется при ультразвуковом исследовании.
Во время диагностики женщине могут быть назначены следующие виды обследований:
Удаление тератомы яичника: операция
Лечение тератомы яичника выполняется при помощи хирургического вмешательства. Объемы операции будут зависеть от характера опухоли, ее размеров, сопутствующих осложнений.
Зрелые тератомы обычно удаляют лапароскопическим способом. Они имеют благоприятный прогноз с сохранением детородной функции. В процессе операции возможна резекция части яичника. У женщин в постменопаузе может быть выполнена надвлагалищная ампутация матки с пораженным яичником и фаллопиевой трубой.
При обнаружении незрелой тератомы в любом возрасте выполняют удаление матки с придатками. Лучевая терапия при этом малоэффективна, поэтому ее не назначают. Для стабилизации процесса может быть использована многокомпонентная химиотерапия.
В Юсуповской больнице можно пройти полный курс лечения тератомы яичника любого вида и на любой стадии. Современный диагностический центр позволит точно определить состояние пациентки, выявить все особенности развития патологии. Опытные врачи (гинекологи, хирурги, онкологи) подбирают наиболее оптимальный план терапии, который будет максимально эффективен в данном конкретном случае. При составлении лечения учитываются все индивидуальные характеристики пациентки для получения лучшего результата.
В дальнейшем в Юсуповской больнице можно проходить профилактические осмотры и получить консультацию о планировании беременности (при необходимости). Для записи к специалистам достаточно позвонить по телефону.