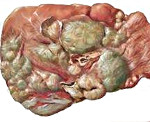
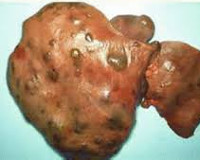
Фульминантный гепатит ( Злокачественный гепатит )
Фульминантный гепатит — это крайне тяжелый вариант воспалительно-некротического поражения печени, возникновение которого обычно не связано с предшествующей печеночной патологией. Проявляется интоксикацией, болями в эпигастрии и справа в подреберье, энцефалопатией, диспепсией, желтушностью. Диагностируется с помощью общего и биохимического анализов крови, коагулограммы, серологических методов и УЗИ печени. Для лечения проводят дезинтоксикационную, гепатопротективную, инфузионную терапию. В самых тяжелых случаях показана экстренная пересадка печени.
МКБ-10
Общие сведения
Характерная особенность фульминантного, или злокачественного, гепатита — быстрое развитие печеночной комы в течение 7-14 дней после появление первых симптомов. В литературе заболевание также упоминается под названиями молниеносного гепатита, гепатодистрофии, гепатаргии и токсической дистрофии печени. При более медленном нарастании симптоматики и возникновении печеночной комы на 3-8 неделях патологического процесса говорят о субфульминантном течении. Актуальность своевременной диагностики болезни обусловлена высокими показателями смертности и преимущественно молодым возрастом пациентов.
Причины
Возникновение фульминантного гепатита связано с действием инфекционных и неинфекционных факторов, оказывающих выраженный гепатотоксический эффект. В случае вирусного повреждения гепатоцитов определенную роль играет генетически обусловленная гиперергическая иммунная реакция на антигены вируса. По мнению специалистов в сфере гастроэнтерологии и гепатологии, причинами фульминантного воспаления печени являются:
Патогенез
Механизм развития фульминантного гепатита основан на критическом повреждении гепатоцитов с нарушением дезинтоксикационной функции печени. В результате воздействия вирусных и других токсических факторов в сочетании с гиперергическим иммунным ответом ускоряется апоптоз печеночных клеток, в тяжелых случаях происходит некроз паренхимы. Разрушение лизосомальных и митохондриальных мембран, клеточной оболочки усиливает воспаление за счет выделения активных энзимов и провоспалительных цитокинов. Наблюдается торможение регенераторных процессов.
Значительное уменьшение объема активной печеночной паренхимы сопровождается нарушением практически всех видов обмена. В организме накапливаются нейротоксичные азотистые соединения, вызывающие отек и дисфункцию астроглии, изменяющие чувствительность постсинаптических рецепторов и проницаемость гематоэнцефалического барьера. Повреждение головного мозга проявляется печеночной энцефалопатией. Ситуация усугубляется нарастающей коагулопатией, метаболическими нарушениями, системной гипотензией и острой почечной недостаточностью.
Симптомы фульминантного гепатита
Клиническая картина болезни сходна с другими некротически-воспалительными поражениями печени, но отличается быстрым ухудшением состояния пациентов. Характерный симптом фульминантного гепатита — умеренные боли в эпигастрии, правом подреберье, болезненность при пальпации в области печени. Желтушное окрашивание кожных покровов, слизистых оболочек обычно обнаруживается после появления интоксикации. У пациентов наблюдаются диспепсические расстройства: тошнота и рвота, не связанные с приемом пищи, нарушение моторной функции кишечника (чередование диареи и запоров).
Важный признак фульминантной формы заболевания — наличие печеночного (сладковатого) запаха изо рта. О тяжелом течении молниеносного гепатита свидетельствует повышение температуры тела более 39° С, значительное учащение пульса, падение артериального давления. Обязательным критерием фульминантного варианта воспаления печени является вовлечение в процесс головного мозга с появлением бессонницы, эмоциональной лабильности, периодических подергиваний отдельных групп мышц, быстро нарастающим нарушением сознания и ухудшением психического статуса.
Осложнения
На фоне массивной интоксикации и прогрессирующей гипоксии у больных с фульминантным гепатитом может возникать отек мозга, на фоне которого формируется печеночная кома. Из-за недостаточного синтеза факторов свертываемости крови существует риск профузных кровотечений из ЖКТ. Сужение мелких сосудов и уменьшение объема кровотока в почках при гепатите приводит к тяжелой почечной недостаточности и азотемическому синдрому. При снижении иммунитета возможно развитие генерализованной бактериальной инфекции. Летальность достигает 60-70%.
Диагностика
Постановка диагноза фульминантного гепатита при наличии типичной клинической картины не представляет затруднений. О возможном молниеносном некрозе печени свидетельствует крайне быстрое нарастание симптоматики вплоть до критического состояния. Диагностический поиск осуществляется гастроэнтерологом и гепатологом, предполагает проведение комплексного лабораторно-инструментального обследования для верификации первопричины болезни. Наиболее информативны:
В общем анализе крови определяется высокий лейкоцитоз, повышение СОЭ, возможны признаки гипохромной анемии (снижение уровня эритроцитов и гемоглобина). При нормальных показателях свертывания крови для изучения распространенности некроза осуществляют биопсию с морфологическим исследованием биоптатов паренхимы. Для оценки неврологического статуса рекомендовано выполнение ЭЭГ, которое позволяет обнаружить увеличение амплитуды и расширение зубцов, появление медленных волн.
Дифференциальная диагностика
В большинстве случаев дифференциальную диагностику фульминантного течения гепатита необходимо проводить с острыми отравлениями. Основные диагностические критерии — отсутствие типичного профессионального или эпиданамнеза, выделение из крови специфических маркеров HBs и HDs. В пользу молниеносного гепатита также свидетельствует быстрое ухудшение неврологического статуса вплоть до комы. При выявлении соответствующей симптоматики больному рекомендована консультация невролога.
Лечение фульминантного гепатита
Своевременное начало адекватной интенсивной терапии — ключевое условие для повышения шансов на выживание пациента. Больного срочно переводят в реанимационное отделение для проведения комплексного этиопатогенетического лечения и поддержания основных жизненных функций. При известных причинах фульминантного гепатита назначается противовирусная терапия (интерфероны, нуклеозиды), вводятся антидоты, купируется основное неотложное состояние. Рекомендована активная дезинтоксикация, направленная на снижение уровня аммиака и уменьшение его эффектов:
Для стабилизации мембран, повышения устойчивости гепатоцитов к вредным воздействиям, усиления регенерации применяют растительные и синтетические гепатопротекторы. Дезинтоксикационную и гепатотропную терапию дополняют инфузиями кристаллоидных и коллоидных растворов, нормализующих водно-электролитный и кислотно-щелочной баланс. По показаниям назначают препараты для поддержания давления и улучшения тканевой перфузии. Однако наилучшие показатели выживаемости выявляются у пациентов, которым в экстренном порядке проведена трансплантация печени.
Прогноз и профилактика
Исход заболевания зависит от своевременности лечения и обширности некроза печени. Прогноз фульминантного гепатита неблагоприятный, у 80-90% пациентов развиваются тяжелые осложнения, которые могут привести к летальному исходу. Меры специфической профилактики не разработаны. Для предупреждения перехода болезни в фульминантную форму необходимо проводить раннюю диагностику и лечение вирусных гепатитов, избегать назначения потенциально гепатотоксичных лекарственных препаратов, обеспечивать диспансерное наблюдение всем больным с патологией печени.
Вирусные гепатиты
Вирусный гепатит А
Гепатит А (ГА, hepatitis A) — острая энтеровирусная инфекция. Возбудитель — вирус гепатита А (ВГА, HAV) — энтеровирус типа 72. Геном вируса представлен однонитчатой РНК. Вирус гепатита А содержит единственный антиген (HA-Ag). Удельный вес гепатита А в суммарной заболеваемости вирусными гепатитами составляет 70–80 %. В структуре заболеваемости гепатитом А дети составляют до 80%, причем основная масса — дошкольники и школьники начальных классов.
Антитела IgM к вирусу гепатита А
Антитела IgM к вирусу гепатита А в сыворотке в норме отсутствуют. Достоверное подтверждение диагноза ГА достигается серологическими методами — обнаружением нарастания уровня специфических антител (анти-HAV), принадлежащих к иммуноглобулинам класса М (анти-HAV IgM). При гепатите А нарастание уровня антител, относящихся к IgM, начинается еще в инкубационном периоде, за 5–10 дней до появления первых симптомов болезни, и быстро прогрессирует. К моменту первичного обращения больного к врачу, уровень анти-HAV IgM успевает достичь высоких показателей, чтобы быть выявленным методом ИФА. Общепринято, что анти-HAV IgM у больных обнаруживаются в начале клинических проявлений заболевания и сохраняются до 6 мес после перенесенной инфекции.
Определение анти-HAV IgM
В настоящее время выделяют следующие формы вирусных гепатитов: гепатит А, гепатит В, гепатит С, гепатит D и гепатит Е. Для диагностики каждой из перечисленных форм вирусных гепатитов используют определенный перечень маркеров.
Определение анти-HAV IgG
Основной тест специфической диагностики гепатита А. Нарастание анти-HAV IgG происходит в более поздние сроки — в фазу реконвалесценции — и поэтому не может служить критерием ранней диагностики гепатита А. Выявление анти-HAV IgG у здоровых людей (возможно у 30–60% здорового населения) свидетельствует о предыдущей инфекции и иммунитете (ретроспективная диагностика).
Антиген гепатита А — HA-Ag
Появляется в сыворотке крови в конце преджелтушного периода. У большинства больных сохраняется в сыворотке крови на протяжение 1–2 недель заболевания. Из-за кратковременности пребывания в сыворотке крови больного для диагностических целей не используется.
Вирусный гепатит В
Гепатит В — вирусная антропонозная инфекция. Возбудитель — вирус гепатита В (ВГВ, HBV) — относится к семейству гепаднавирусов, ДНК-содержащих вирусов, поражающих клетки печени. Вирионы ВГВ имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую циркулярную ДНК и ДНК-зависимую ДНК-полимеразу.
Поверхностный антиген (HBsAg) гепатита В в сыворотке
Поверхностный антиген гепатита В в сыворотке в норме отсутствует. Обнаружение поверхностного антигена (HBsAg) гепатита В в сыворотке подтверждает острое или хроническое инфицирование вирусом гепатита В (HBV).
При остром заболевании HBsAg выявляется в сыворотке крови в последние 1–2 недели инкубационного периода и в первые 2–3 недели клинического периода. Циркуляция HBsAg в крови может ограничиваться несколькими днями, поэтому следует стремиться к раннему первичному обследованию больных. Частота выявления HBsAg зависит от чувствительности используемого метода исследования. Метод ИФА позволяет выявить HBsAg более чем у 90% больных. Почти у 5% больных самые чувствительные методы исследования не обнаруживают HBsAg, в таких случаях этиология вирусного гепатита В подтверждается наличием анти-HBcAg IgM. Концентрация HBsAg в сыворотке крови при всех формах тяжести гепатита В в разгар заболевания имеет значительный диапазон колебаний, вместе с тем имеется определенная закономерность: в остром периоде существует обратная связь между концентрацией HBsAg в сыворотке и тяжестью болезни.
Высокая концентрация HBsAg чаще наблюдается при легких и средне-тяжелых формах болезни. При тяжелых и злокачественных формах, концентрация HBsAg в крови чаще низкая, причем у 20% больных с тяжелой формой и 30% со злокачественной антиген в крови может вообще не обнаруживаться. Появление на этом фоне у больных антител к HBsAg расценивается как неблагоприятный прогностический признак; он определяется при злокачественных формах (фульминантных) гепатита В.
При остром течении гепатита В, концентрация HBsAg в крови постепенно снижается, вплоть до полного исчезновения этого антигена. HBsAg исчезает у большинства больных в течение 3 мес от начала острой инфекции. Снижение концентрации HBsAg более чем на 50 % к концу 3-й недели острого периода, как правило, свидетельствует о близком завершении инфекционного процесса. Обычно у больных с высокой концентрацией HBsAg в разгар болезни он обнаруживается в крови в течение нескольких месяцев. У больных с низкой концентрацией HBsAg исчезает значительно раньше (иногда через несколько дней после начала заболевания). В целом, срок обнаружения HBsAg колеблется от нескольких дней до 4–5 мес. Максимальный срок обнаружения HBsAg при гладком течении острого гепатита В не превышает 6 мес от начала заболевания.
HBsAg может быть выявлен у практически здоровых людей, как правило, при профилактических или случайных исследованиях. В таких случаях исследуют другие маркеры вирусного гепатита В — анти-HBcAg IgM, анти-НВс IgG, анти-HBeAg и изучают функцию печени. При отрицательных результатах необходимы повторные исследования на HBsAg. Если повторные исследования крови в течение более 3 месяцев выявляют HBsAg, такого человека относят к хроническим носителям поверхностного антигена. Носительство HBsAg — довольно распространенное явление. В мире насчитывается более 300 млн носителей; у нас в стране — около 10 млн.
Исследование крови на наличие HBsAg применяют в следующих целях:
Антитела к поверхностному антигену гепатита В
Анти-HBsAg обнаруживаются в конце острого периода вирусного гепатита В или, чаще всего, через 3 мес от начала инфекции, изредка позже (до года) и сохраняются долго, в среднем 5 лет (Хазанов А.И., 1981). Анти-HBsAg обнаруживаются не сразу после исчезновения HBsAg. Продолжительность фазы «окна» варьирует от нескольких недель до нескольких месяцев. Антитела к поверхностному антигену гепатита В нейтрализуют вирус и рассматриваются как признак иммунитета. Они относятся к классу IgG.
Определение анти-HBsAg имеет важное значение для оценки течения гепатита В и его исходов, так как характеризует иммунный ответ конкретного больного. Это надежный критерий развития постинфекционного иммунитета и выздоровления. Выявление анти-HBsAg может служить критерием ретроспективной диагностики гепатита ранее не уточненной этиологии.
Анти-HBsAg свидетельствуют о ранее перенесенной инфекции. Выявление антител к HBsAg играет важную роль в определении контингента для вакцинации против гепатита В. Согласно рекомендациям ВОЗ, если уровень анти-HBsAg составляет менее 10 мМЕ/л, таким лицам показана вакцинация против гепатита В, при уровне 10–100 мМЕ/л вакцинация должна быть отложена на один год, при уровне более 100 мМЕ/л вакцинация показана через 5–7 лет.
Общие антитела к ядерному антигену гепатита В состоят из иммуноглобулинов класса М и G. Определение общих антител к ядерному антигену гепатита В может использоваться только для ретроспективной диагностики гепатита В, так как у 5–10 % больных исследования на HBsAg дают отрицательный результат. Для того чтобы установить, в какой стадии развития находится гепатит В, необходимо дополнительное определение антител IgM. Антитела класса IgM — маркер активной репликации вируса, т.е. острой инфекции, а антитела класса IgG — перенесенной инфекции.
Антитела IgM к ядерному антигену гепатита В (анти-HBcAg IgM) в сыворотке
Анти-HBcAg IgM в сыворотке в норме отсутствуют. Анти-HBcAg IgM обнаруживаются уже в начале острой фазы болезни, еще до появления или в первые дни желтухи, иногда даже в конце инкубации. Выявление анти-HBcAg IgM расценивают как убедительный критерий диагностики гепатита В, особенно при отрицательных результатах исследования на HBsAg. Анти-HBcAg IgM циркулируют в крови больных в течение нескольких месяцев (2–5 месяца) до периода реконвалесценции, а затем исчезают, что рассматривается как признак очищения организма от вируса гепатита В.
Установлено, что высокие концентрации HBeAg соответствуют высокой ДНК-полимеразной активности и характеризуют активную репликацию вируса. Наличие HBeAg в крови свидетельствует о высокой ее инфекциозности, т.е. присутствии в организме обследуемого активной инфекции гепатита В и обнаруживается только в случае присутствия в крови HBs-антигена. У больных хроническим активным гепатитом противовирусные препараты применяют только при обнаружении в крови HBeAg.
Наличие НВе-антигена свидетельствует о продолжающейся репликации вируса и инфекциозности больного. HBeAg-антиген — маркер острой фазы и репликации вируса гепатита В.
Анти-HBeAg в сыворотке в норме отсутствуют. Появление АHTH-HBeAg-антител указывает обычно на интенсивное выведение из организма вируса гепатита В и незначительное инфицирование больного. Эти антитела появляются в острый период и сохраняются до 5 лет после перенесенной инфекции. При хроническом персистирующем гепатите, анти-HBeAg обнаруживаются в крови больного вместе с HBsAg. Сероконверсия, т.е. переход HBeAg в анти-HBeAg при хроническом активном гепатите, чаще прогностически благоприятна, но такая же сероконверсия при выраженной цирротической трансформации печени прогноза не улучшает.
Гепатит С (ГС, hepatitis С) — вирусное заболевание, наиболее часто протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации процесса. Возбудитель — вирус гепатита С (ВГС) — имеет сходство с флавови-русами, содержит РНК.
Примерно 90% всех случаев посттрансфузионных гепатитов связаны с ВГС. Среди доноров антитела к вирусу гепатита С (анти-ВГС) обнаруживают в 0,2–5% случаев. У 40–75% пациентов регистрируется бессимптомная форма болезни, у 50–75% больных острым ВГС формируется хронический гепатит, у 20% из них развивается цирроз печени. Важная роль ВГС отводится и в этиологии гепатоклеточной карциномы.
Антитела к вирусу гепатита С в сыворотке
Антитела к вирусу гепатита С в сыворотке в норме отсутствуют. Диагностика гепатита С основана на обнаружении суммарных антител к ВГС методом ИФА, которые появляются в первые 2 нед заболевания и свидетельствуют о возможной инфицированности вирусом или перенесенной инфекции. Анти-ВГС-антитела могут сохраняться в крови реконвалесцентов на протяжении 8–10 лет с постепенным снижением их концентрации. Возможно позднее обнаружение антител спустя год и более после инфицирования.
При хроническом гепатите С, антитела определяются постоянно и в более высоких титрах. Существующие в настоящее время тест-системы для диагностики ВГС основаны на определении антител класса IgG, поэтому разрабатываются тест-системы нового поколения, которые позволят верифицировать активную инфекцию (определять антитела класса IgM). Антитела класса IgM могут выявляться не только при остром ВГС, но и при хроническом гепатите С. Снижение их уровня в процессе лечения больных хроническим гепатитом С может свидетельствовать об эффективности лекарственной терапии. Обнаружение антител к ВГС методом ИФА требует подтверждения способом иммуноблотинга для исключения ложно-положительного результата исследования.
Определение антител к вирусу гепатита С используют для диагностики острого и хронического гепатита С, персистирующего хронического гепатита. Вирус гепатита С может быть причиной развития цирроза и рака печени, поэтому данное исследование показано при этих заболеваниях.
Иммуноблотинг на антитела к белкам вируса гепатита С в сыворотке
Антитела к вирусу гепатита С в норме отсутствуют. Метод иммуноферментного анализа, применяемый для определения антител к ВГС, является скрининговым. В случае получения положительного результата для подтверждения его специфичности используют метод иммуноблотинга Western-blot — встречную преципитацию в геле антител в сыворотке крови больного с различными вирусными белками, подвергнутыми разделению по молекулярной массе с помощью электрофореза и нанесенными на нитроцеллюлозу. Исследование считается положительным, если выявляются антитела к белкам интенсивностью +1 к 2 или более антителам ВГС. Специфичными для ВГС являются антитела к белкам — Core, NS3-1, NS3-2, NS1, NS5.
Иммуноблотинг на вирус гепатита С служит подтверждающим тестом специфичности метода ИФА.
Вирусный гепатит D
Гепатит D — вирусная инфекция, протекающая вследствие биологических особенностей вируса исключительно в виде ко-или суперинфекции при гепатите В, характеризующаяся тяжелым течением часто с неблагоприятным исходом.
Возбудитель — вирус гепатита D (BГD) — по своим биологическим свойствам приближается к вироидам — обнаженным молекулам нуклеиновых кислот. Печень человека — единственное место репликации BГD. Известно существование двух вариантов инфекции: коинфекция (одновременное заражение ВГВ и BГD) и суперинфекция (заражение HBsAg-позитивных пациентов). Сочетание ВГВ и BГD сопровождается развитием более тяжелых форм патологического процесса, что определяется главным образом действием BГD. Летальность при суперинфекции достигает 5–20 %. Инфицирование дельта-вирусом может вызывать острое заболевание, заканчивающееся выздоровлением, или формировать хроническое носительство BГD.
При гепатите D могут отсутствовать в крови маркеры гепатита В — анти-НВс и HBs-антиген — и наблюдается угнетение ДНК-полимеразной активности, так как BГD ингибирует репликацию вируса гепатита В.
Антитела lgM к вирусу гепатита D в сыворотке
Антитела IgM к вирусу гепатита D в сыворотке в норме отсутствуют. Антитела BГD IgM (анти-BГD IgM) появляются в острый период «дельта-инфекции». По мере выздоровления при BГD происходит элиминация вируса из печени и исчезновение анти-BГD IgM. При хронизации процесса наблюдается персистирование BГD в ткани печени и анти-BГD IgM в высокой концентрации в крови. Антитела BГD IgM говорят об активной репликации вируса.
Антитела IgG к вирусу гепатита D в сыворотке
Антитела IgG к вирусу гепатита D в сыворотке в норме отсутствуют. Антитела BГD IgG (анти-BГD IgG) появляются в период реконвалесценции, и их концентрация постепенно снижается в течение нескольких месяцев. Определение антител BГD IgG может служить критерием ретроспективной диагностики гепатита ранее не уточненной этиологии.
Возбудителем вирусного гепатита Е (ВГЕ) является РНК-вирус. Для заболевания характерен фекально-оральный путь передачи, преимущественно водный. Инкубационный период болезни — около 35 сут. Клиническое течение острого ВГЕ сходно с ВГА. Существенно тяжелее заболевание протекает у беременных, особенно в III триместре.
Для специфической диагностики ВГЕ используются методы ИФА, основанные на выявлении антител класса IgM. Обнаружение в крови повышенного уровня анти-ВГЕ IgM служит лабораторным подтверждением диагноза.
ПЕРИОДЫ ОБНАРУЖЕНИЯ В КРОВИ МАРКЕРОВ ВИРУСНОГО ГЕПАТИТА В ПРИ ОСТРОМ ПРОЦЕССЕ:
1) поверхностный HBs-антиген — с инкубационного периода до периода ранней реконвалесценции (5,5–6 мес);
2) антиген НЬе обнаруживается в инкубационный и продромальный периоды (до 3,5 мес); его выявление свидетельствует о репликации вируса;
3) антитела к Hbe-антигену появляются в острый период заболевания (3–4-й месяц) и сохраняются до нескольких лет;
4) антитела класса IgM к ядерному антигену (анти-HBc-IgM) обнаруживаются в продромальном периоде и сохраняются до периода реконвалесценции (со 2-го по 6-й месяц заболевания);
5) антитела класса IgG к ядерному антигену (анти-HBc-IgG) возникают в продромальном периоде и сохраняются на протяжении всей жизни (ведущий маркер вирусного гепатита В);
6) антитела к поверхностному Hbs-антигену (анти-HBs) появляются в стадии поздней реконвалесценции (6-й месяц) и сохраняются до 5 лет.
Маркеры гепатита В (HBeAg, anti-HBcoreM, anti-HBe, Anti-HBcore)
Гепатит В – острое или хроническое заболевание печени, вызываемое вирусом гепатита В (HBV), протекающее в различных клинических вариантах: от бессимптомных форм до злокачественных (цирроз печени, гепатоцеллюлярная карцинома). На долю ГВ приходится около 15% всех регистрируемых в РФ острых гепатитов и не менее 50% хронических.
Схематично строение вирусной частицы гепатита В можно изобразить так:
Рис.1. Структура вируса гепатита В.
Белок внешней оболочки ВГВ является его поверхностным антигеном – HBsAg. HBsAg – это основной маркёр ГВ. При остром гепатите HBsAg может быть выявлен в крови обследуемых уже в инкубационный период в первые 4–6 недель от начала клинического периода. Присутствие HBsAg более 6 мес рассматривается как фактор перехода болезни в хроническую стадию.
Следует отметить, что только часть HBsAg, образующегося при размножении вируса, используется для построения новых вирусных частиц, основное же его количество поступает в кровь инфицированных лиц, где и определяется HBsAg- антиген.
Это четвертый маркер активной репликации вируса наряду с ДНК, HBs Ag и антиHBc –IgM.
Исчезновение HBeAg и быстрое нарастание титра анти-HBе у больного практически исключает угрозу хронизации ГВ. Отсутствие такой динамики и выявление монотонно низких концентраций анти-НВе, наоборот, может свидетельствовать о развитии хронического ГВ с невысокой активностью (HBeAg-негативный хронический ГВ).
анти-HBs определяют для оценки течения инфекционного процесса и благоприятности его исхода. Факт появления анти-HBs рассматривается как надежный критерий развития постинфекционного иммунитета, т.е. выздоровления после гепатита В. Хотя при хроническом гепатите В HBsAg и анти-HBs могут иногда обнаруживаются одновременно.
Период, в который отсутствуют и HBsAg, и анти-HBs, называется фазой серологического «окна». Сроки появления анти-HBs зависят от особенностей иммунологического статуса больного. Продолжительность фазы «окна» чаще составляет 3–4 мес. с колебаниями до года.
Анти-HBs могут сохраняться пожизненно. Анти-HBs обладают протективными (защитными) свойствами. Этот факт лежит в основе вакцинопрофилактики. В настоящее время в качестве вакцины против ГВ, в основном, применяют препараты рекомбинантного HBsAg. Эффективность иммунизации оценивают по концентрации антител к HBsAg у вакцинированных лиц. Согласно данным ВОЗ, общепринятым критерием успешной вакцинации считается концентрация антител, превышающая 10 мМЕ/мл.
При интегративной фазе развития (т.е. когда вирусные частицы не подвергаются дальнейшей репликации) геном HBV встраивается в геном гепатоцита. Основную роль играет фрагмент, несущий ген, кодирующий HBs антиген Поэтому при этой фазе идет преимущественное образование HBs Ag и антител к коровскому белку и анти- HBe Ag.
Рис. 2. Динамика серологических маркёров при остром гепатите В.