Какой конечный продукт тканевого дыхания
4.1. Транспорт кислорода
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит – безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа. Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи. Hb A (HbA) – основной гемоглобин взрослых содержит 2 – альфа и 2 – бета – цепи, Hb A2 – содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 – в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде. Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови. Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови – 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной – около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов – температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении – снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 – ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
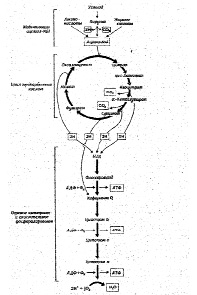
Тканевое или клеточное дыхание включает три стадии. На первой стадии пируват, аминокислоты и жирные кислоты окисляются до двухуглеродных фрагментов ацетильных групп, входящих в состав ацетилкофермента А. Последние на втором этапе окисления включаются в цикл лимонной кислоты, где происходит образование высокоэнергетических атомов водорода и высвобождение СО2 – конечного продукта окисления органических субстратов. На третьей стадии клеточного дыхания атомы водорода делятся на протоны (Н+) и «высокоэнергетические» электроны, передающиеся по дыхательной цепи на молекулярный О2 и восстанавливающие его до НО2. Перенос электронов сопряжен с запасом энергии в форме АТФ, т.е. с окислительным фосфорилированием (рис.6).
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +. Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов – кислороду.
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2. Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле. Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода
Тканевое дыхание (аэробный ресинтез АТФ) в мышечных волокнах
Дается определение тканевого дыхания — аэробного ресинтеза АТФ в мышечных волокнах. Описаны количественные критерии тканевого дыхания: максимальная мощность, время развертывания, время работы с максимальной мощностью. Дается характеристика достоинствам и недостаткам тканевого дыхания.
Тканевое дыхание в мышечных волокнах (аэробный путь ресинтеза АТФ, аэробное фосфорилирование, окислительное фосфорилирование)
Определение
Тканевое дыхание (аэробный путь ресинтеза АТФ, аэробное фосфорилирование, окислительное фосфорилирование) – основной, базовый способ образования АТФ, протекающий в митохондриях мышечных волокон.
Общая характеристика
Источниками энергии для аэробного ресинтеза АТФ являются углеводы, жиры и аминокислоты. В итоге тканевого дыхания вещество окисляется до углекислого газа и воды.
Тканевое дыхание – основной механизм энергообеспечения при работе умеренной мощности длительностью более 30 минут.
Виды спорта базирующиеся на тканевом дыхании
Виды спорта, в которых тканевое дыхание является основным механизмом обеспечения являются: спортивная ходьба на 20 и 50 км, марафонский бег; лыжные гонки на 20 и 50 км; шоссейные велогонки, плавание на 10 км в открытой воде.
Ферменты тканевого дыхания
Ферменты аэробного ресинтеза АТФ располагаются в мембране митохондрий. Эти ферменты активирует АДФ (аденозиндифосфат). В покое АДФ мало, поэтому тканевое дыхание протекает с очень низкой скоростью. При выполнении физической нагрузки в организме интенсивно используется АТФ, поэтому в мышечных волокнах накапливается АДФ. В этом случае имеет место реакция гидролиза АТФ:
Избыток АДФ ускоряет тканевое дыхание, и оно может достигнуть максимальной скорости. Тканевое дыхание характеризуется высокой экономичностью. Например, при аэробном окислении гликогена до воды и углекислого газа образуется 39 молекул АТФ в расчете на один остаток глюкозы.
Тканевое дыхание активно протекает в мышечных волокнах типа I и типа IIA.
Количественные критерии тканевого дыхания
Максимальная мощность
Максимальная мощность тканевого дыхания составляет 350-450 кал/мин кг. По сравнению с анаэробными путями ресинтеза АТФ тканевое дыхание обладает самой низкой величиной максимальной мощности. Это обусловлено возможностями доставки кислорода в митохондрии, количеством и размерами митохондрий в мышечных волокнах.
Время развертывания тканевого дыхания
Время развертывания тканевого дыхания составляет от 3 до 4 минут. Однако у хорошо тренированных спортсменов этот показатель может составлять всего 1 минуту (С.С. Михайлов, 2009). Достаточно большое время развертывания тканевого дыхания объясняется тем, что для обеспечения максимальной скорости протекания тканевого дыхания необходима перестройка всех систем организма, участвующих в доставке кислорода в митохондрии мышц.
Время работы с максимальной мощностью
Время работы с максимальной мощностью тканевого дыхания составляет десятки минут. Это связано с тем, что, для аэробного ресинтеза АТФ используются разнообразные источники энергии (аминокислоты, углеводы, жирные кислоты и др.), содержащиеся как в мышечных волокнах, так и в крови, доставляемой к мышцам. Поэтому тканевое дыхание может функционировать длительное время.
Лекция № 15. Тема «тканевое дыхание».
Состав и локализация дыхательной цепи:
а/ цитохромы, состав их молекул;
б/ роль убихинона в работе дыхательной цепи.
Окислительное фосфорилирование, его биологическая роль. Отличие от субстратного фосфорилирования.
Сущность хемиосмотической теории Митчелла.
Разобщение окислительного фосфорилирования.
ТКАНЕВОЕ ДЫХАНИЕ – это последовательность окислительно-восстановительных реакций, в результате которых происходит последовательный перенос водорода и электронов от субстрата к кислороду.
Всю систему реакций и ферментов тканевого дыхания называют дыхательной цепью.
Процесс дыхания протекает в митохондриях, которые в связи с этим называют «энергетическими станциями» клеток. Дыхательная цепь у человека и высших животных состоит из трех основных звеньев.
Первое звено – процессы дегидрирования субстратов, катализируемые преимущественно никотинамидными ферментами НАД и НАДФ.
Второе звено – процессы окисления восстановленных форм никотинамидных ферментов (НАД · Н + Н + и НАДФ · Н + Н + ), катализируемые главным образом флавиновыми ферментами.
Третье звено – процессы окисления восстановленных форм флавиновых ферментов, катализируемых системой цитохромов.
Переносчиками электронов и протонов водорода являются ферменты дыхательной цепи – оксидоредуктазы. Направление переноса протонов и электронов определяет окислительно-восстановительный потенциал – редокс-потенциал. Дыхательная цепь включает последовательно звенья с нарастающим значением окислительно-восстановительного потенциала. Для пары (НАДН + Н + )/НАД + редокс-потенциал равен 0,32 В. Следовательно, электроны будут легко отщепляться и переносится на комплексы, имеющие меньшую отрицательную и большую положительную величину редокс-потенциала.
Соединения, последовательно принимающие и отдающие протоны и электроны, играют роль промежуточных переносчиков. Окислительные реакции протекают с высвобождением энергии, т.е. они экзэргоничные. Для биологических реакций характерны сравнительно небольшие изменения энергии. Если бы реакция протекала непосредственно между субстратом и кислородом, то вся энергия окисления высвобождалась бы одновременно. Так, реакция соединения водорода с кислородом сопровождается взрывом, так как образуется «гремучий газ», выделяется большое количество тепла. Отличием биологического окисления от этой реакции является: 1) постепенное, поэтапное выделение энергии; 2) окисляется не молекулярный водород, а водород, включенный в состав субстратов – (S · Н2); 3) энергия высвобождается не только в виде тепла, но и аккумулируется в виде АТФ.
Биологическое окисление – процесс, в ходе которого окисляющиеся субстраты теряют протоны и электроны, т.е. являются донаторами водорода, промежуточные переносчики – акцепторами-донаторами, а кислород – конечным акцептором водорода.
арисовать схему биологического окисления.
На последней стадии переносчик передает электроны кислороду, который восстанавливается до воды:
Понятие биологическое окисление и тканевое дыхание однозначны, если речь идет о биологическом окислении при участии кислорода.
Такой тип окисления можно называть еще аэробным окислением. Это основной путь окисления, поставщик значительной части энергии, в которой нуждается клетка (организм). Промежуточными переносчиками в дыхательной цепи у высших организмов являются коферменты: НАД, ФАД, ФМН, Ко-Q, семейство гемсодержащих белков – цитохромов и белки, содержащие негеминовое железо. Различают цитохромы b, с1, с, а, а3, которые способны переносить электроны благодаря наличию в их составе ионов металла.
Все участники дыхательной цепи разделены на четыре окислительно-восстановительные системы (комплексы).
I комплекс дыхательной цепи: НАДН – убихинон – оксидоредуктаза.
Это сложный полиферментный комплекс, обладающий большой молекулярной массой. Он содержит более 20 различных белков, коферментом которых является ФМН – флавинмононуклеотид, который способен восстанавливаться, присоединяя два атома водорода (т.е. 2 протона и 2 электрона), отдаваемых пиридиновыми дегидрогеназами (НАД – зависимая дегидрогеназа). ФАД + 2Н ↔ ФАДН2.
Кроме ФМН-зависимых ферментов, в состав I комплекса входят пять железосерных белков, которые осуществляют разделение потока протонов и электронов. При этом электроны от ФМН · Н2 переносятся к внутренней поверхности внутренней мембраны митохондрий (обращенной к матриксу), а протоны – к внешней поверхности внутренней мембраны, здесь они выделяются в межмембранное пространство.
Символом SН2 обозначаются такие субстраты, как пировиноградная кислота, изоцитрат, малат, оксипроизводные жирных кислот, глутаминовая кислота и другие аминокислоты.
В I комплексе дыхательной цепи непосредственно АТФ не образуется, а высвобождающаяся энергия аккумулируется или рассеивается в виде тепла.
II комплекс дыхательной цепи: сукцинат – убихинон – оксидоредуктаза.
Этот комплекс отличается меньшей молекулярной массой, содержит железосерные белки. С этим комплексом взаимодействует сукцинат, поступающий из матрикса митохондрий, а также жирные кислоты, которые находятся в матриксе. Коферментом комплекса является ФАД – флавинадениндинуклеотид.
В результате включения водорода субстратов через ФАД-зависимые дегидрогеназы (II комплекс) энергия в основном рассеивается в виде тепла, так как падение редокс-потенциала на этом участке дыхательной цепи незначительное (около 0,05 В) и этой энергии недостаточно для синтеза молекулы АТФ.
Убихинон (коэнзим Q) – посредник в передаче водородов. Это небольшая молекула (производное бензохинона) с длинной боковой цепью, способная свободно перемещаться как вдоль, так и поперек мембраны. Перемещаясь, молекулы убихинона захватывают протоны и электроны от комплексов I и II дыхательной цепи, а также протоны из матрикса. При этом убихинон восстанавливается.
КоQ + 2Н + + 2е ↔ КоQН2
Восстановленная форма (убихинол, КоQН2) в свою очередь передает 2 электрона III комплексу дыхательной цепи (возможно, с участием какого-то индивидуального переносчика), а протоны при этом высвобождаются в межмембранное пространство.
III комплекс дыхательной цепи: убихинол – цитохром-с – оксидоредуктаза.
IV комплекс дыхательной цепи: цитохром-с – оксидаза.
В состав III и IV комплексов входят сложные белки – цитохромы. Цитохромы b и с1 объединены в III комплекс дыхательной цепи. Цитохромы а и а3 образуют IV комплекс дыхательной цепи.
Работа III комплекса заключается в транспорте электронов от убихинола на цитохрос с. Ферменты III комплекса способны захватывать из матрикса протоны и переносить их в межмембранное пространство. При этом существенно падает ОВ потенциал (от –0,04 В цитохрома «b» до +0,25 В цитохрома «с»), а высвободившейся энергии достаточно для синтеза одной молекулы АТФ.
От III комплекса электроны переносятся на IV при помощи очень подвижного фермента цитохромоксидазы (цитохром «с»). В своем составе этот фермент содержит 104 аминокислоты и одну гемподобную структуру. Такая молекула способна активно перемещаться, совершая челночные движения вдоль внешней поверхности мембраны от III к IV комплексу. Цитохром «с» при этом переносит только электроны, попеременно восстанавливаясь и окисляясь. В отличие от других цитохромов цитохромы а и а3 содержат, помимо железа, также медь, которая меняет свою степень окисления. При этом электроны от цитохрома «с» последовательно переносятся на цитохром «а», а затем на цитохром «а3».
Конечным акцептором электронов является молекулярный кислород воздуха. Восстановление кислорода происходит на цитохроме «а3», обращенном к матриксу:
Ионы Н + для образования молекул воды берутся из матрикса митохондрии. Редокс-потенциал IV комплекса велик (+0,57 В), его хватит на образование 2-х молекул АТФ. Важнейшей функцией IV комплекса является также активный транспорт протонов, в связи с чем этот дыхательный комплекс ферментов получил название «протонного насоса». Протоны транспортируются в межмембранное пространство митохондрий.
Нарисовать схемы: «Дыхательная цепь» и «Трансмембранный перенос протонов и синтез АТФ в митохондриях»..
Дегидрогеназа НАДН2, расположенная на поверхности мембраны митохондрии, обращенной к матриксу, отдает пару электронов на дегидрогеназу ФМН. Это позволяет ФМН принять пару протонов из матрикса с образованием ФМНН2. Пара протонов, принадлежащих НАД, выталкивается на цитоплазматическую поверхность мембраны.
Дегидрогеназа ФМНН2 выталкивает пару протонов на цитоплазматическую поверхность мембраны, а пару электронов отдает на КоQ (убихинон), который при этом получает способность присоединить пару протонов из матрикса с образованием КоQ · Н2.
КоQ · Н2 выталкивает пару протонов в цитоплазму, а электроны перебрасываются на кислород в матриксе с образованием воды. В итоге при переносе пары электронов из матрикса на цитоплазматическую поверхность перекачивается 6 протонов, что и ведет к созданию разницы потенциалов и разницы рН между поверхностями внутренней мембраны.
Разница потенциалов и разница рН обеспечивают движение протонов через протонный канал (фактор F0) в обратном направлении.
Движение протонов ведет к активации АТФ-синтетазы (фактор F1) и синтезу АТФ из АДФ и Н3РО4 (1 молекула АТФ при переносе пары протонов, соответственно 3 молекулы на 3 пары протонов или одну пару электронов).
Таким образом, работа дыхательной цепи сводится к транспорту электронов от субстрата тканевого дыхания к кислороду, а также протонов, поставляемых субстратом и матриксом митохондрий. При транспорте в связи с падением редокс-потенциала освобождается энергия и в итоге образуется вода.
Обмен веществ и энергии
Процесс распада сложных веществ на более простые называется катаболизмом. Так, поступающие в пищей белки, жиры, углеводы под действием ферментов пищеварительного тракта распадаются на более простые составные части (аминокислоты, жирные кислоты и моносахариды). При этом высвобождается энергия. Обратный процесс, т. е. синтез сложных соединений из более простых называется анаболизмом. Он идет с затратой энергии. Из образовавшихся в результате пищеварения аминокислот, жирных кислот и моносахаридов в клетках синтезируются новые клеточные белки, фосфолипиды мембран и полисахариды.
Существует понятие амфиболизм, когда одно соединение разрушается, но при этом синтезируется другое.
Интенсивность метаболизма определяется потребностью клетки в тех или иных веществах или энергии, регуляция осуществляется четырьмя путями:
1) Суммарная скорость реакций определенного метаболического пути определяется концентрацией каждого из ферментов этого пути, значением рН среды, внутриклеточной концентрацией каждого из промежуточных продуктов, концентрацией кофакторов и коферментов.
2) Активностью регуляторных (аллостерических) ферментов, которые обычно катализируют начальные этапы метаболических путей. Большинство из них ингибируется конечным продуктом данного пути и этот вид ингибирования называется «по принципу обратной связи».
4) Гормональная регуляция. Ряд гормонов способны активировать или ингибировать многие ферменты метаболических путей.
Живые организмы представляют собой термодинамически неустойчивые системы. Для их формирования и функционирования необходимо непрерывное поступление энергии в форме, пригодной для многопланового использования. Для получения энергии практически все живые существа на планете приспособились подвергать гидролизу одну из пирофосфатных связей АТФ. В связи с этим одна из главных задач биоэнергетики живых организмов это восполнение использованных АТФ из АДФ и АМФ.
Это процесс потребление клетками тканей организма кислорода, который участвует в биологическом окислении. Такой вид окисления называют аэробным окислением. Если конечным акцептором в цепи переноса водорода выступает не кислород, а другие вещества (например пировиноградная кислота), то такой тип окисления называют анаэробным.
Т. о. любое соединение может отдавать электроны только соединению с более высоким окислительно-восстановительным потенциалом. В дыхательной цепи каждое последующее звено имеет более высокий потенциал, чем предыдущее.
Дыхательная цепь состоит из:
2. ФАД- зависимой дегидрогеназы;
ФАД и ФМН-зависимые дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 ( ФАД ).
В цитохроме с порфириновая плоскость ковалентно связана с белком через два остатка цистеина, а в цитохромах b и а , она ковалентно не связано с белком.
В цитохроме а+ а3 (цитохромоксидазе) вместо протопорфирина содержатся порфирин А, который отличатся рядом структурных особенностей. Пятое координационное положение железа занято аминогруппой, принадлежащей остатку аминосахара, входящего в состав самого белка.
В отличии от гема гемолгобина атом железа в цитохромах может обратимо переходить из двух в трехвалентное состояние это обеспечивает транспорт электронов (См. подробнее приложение 1 «Атомная и электронная структура гемопротеинов «).
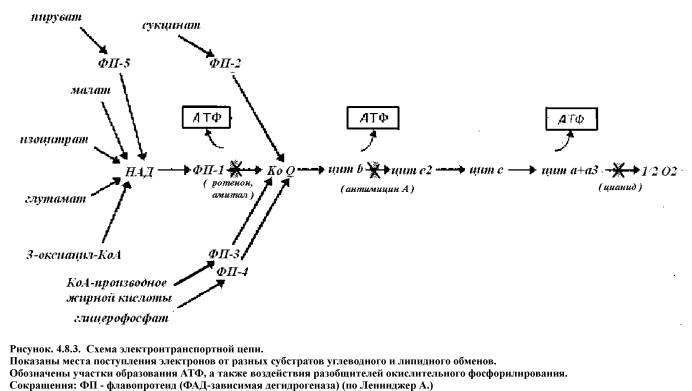
Механизм работы электронтранспортной цепи
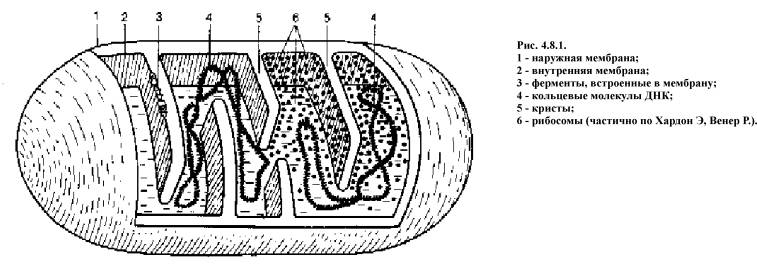
Наружная мембрана митохондрии (рис. 4.8.1) проницаема для большинства мелких молекул и ионов, внутренняя почти для всех ионов (кроме протонов Н) и для большинства незаряженных молекул.
Такая молекула содержит в себе три макроэргических связи. Макроэргической или богатой энергией называют химическую связь, при разрыве которой высвобождается более 4 ккал/моль. При гидролитическом расщеплении АТФ до АДФ и фосфорной кислоты высвобождается 7,3 ккал/моль. Ровно столько же тратится для образования АТФ из АДФ и остатка фосфорной кислоты и это один из основных путей запасания энергии в организме.
В процессе транспорта электронов по дыхательной цепи высвобождается энергия, которая тратится на присоединение остатка фосфорной кислоты к АДФ с образованием одной молекулы АТФ и одной молекулы воды. В процессе переноса одной пары электронов по дыхательной цепи высвобождается и запасается в виде трех молекул АТФ 21,3 ккал/моль. Это составляет около 40 % высвободившейся при электронном транспорте энергии.
Такой способ запасания энергии в клетке называется окислительным фосфорилированием или сопряженным фосфорилированием.
Молекулярные механизмы этого процесса наиболее полно объясняет хемоосмотическая теория Митчелла, выдвинутая в 1961 году.
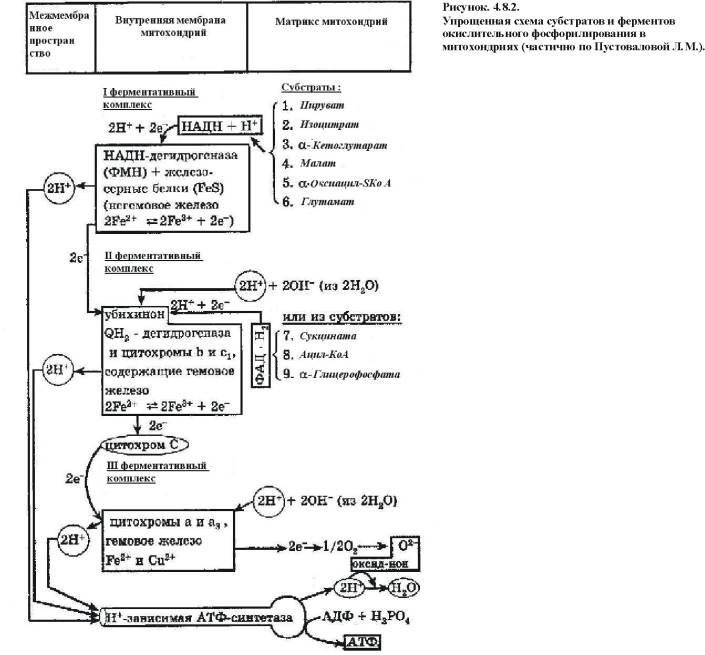
Механизм окислительного фосфорилирования (рис.4.8.2.):
1) НАД-зависимая дегидрогеназа расположена на матриксной поверхности внутренней мембраны митохондрий отдает пару электронов водорода на ФМН-зависимую дегидрогеназу. При этом из матрикса пара протонов переходит также на ФМН и в результате образуется ФМН Н2. В это время пара протонов, принадлежащих НАД выталкивается в межмембранное пространство.
2) ФАД-зависимая дегидрогеназа отдает пару электронов на Ко Q а пару протонов выталкивает в межмембранное пространство. Получив электроны Ко Q принимает из матрикса пару протонов и превращается в Ко Q Н2.
3) Ко Q Н2 выталкивает пару протонов в межмембранное пространство, а пара электронов передается на цитохромы и далее на кислород с образованием молекулы воды.
В итоге при переносе пары электронов по цепи из матрикса в межмембранное пространство перекачивается 6 протонов (3 пары), что ведет к созданию разницы потенциалов и разницы рН между поверхностями внутренней мембраны.
4) Разница потенциалов и разница рН обеспечивают движение протонов через протонный канал обратно в матрикс.
5) Такое обратное движение протонов ведет к активации АТФ-синтазы и синтезу АТФ из АДФ и фосфорной кислоты. При переносе одной пары электронов (т.е. трех пар протонов) синтезируется 3 молекулы АТФ (рис. 4.7.3.).
Образовавшаяся АТФ из матрикса в цитоплазму переносится ферментами транслоказами, при этом в обратном направлении в матрикс переносится одна молекула АДФ и одна молекула фосфорной кислоты. Понятно, что нарушение транспорта АДФ и фосфата тормозит синтез АТФ.
Скорость окислительного фосфорилирования зависит в первую очередь от содержания АТФ, чем быстрее она расходуется, тем больше накапливается АДФ, тем больше потребность в энергии и следовательно активнее идет процесс окислительного фосфорилирования. Регуляцию скорости окислительного фосфорилирования концентрацией в клетке АДФ называют дыхательным контролем.
1. Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский рабочий, 1994, 384 с.;
2. Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
3. Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.: Мир, 1974, 956 с.;
4. Пустовалова Л.М. Практикум по биохимии // Ростов-на Дону: Феникс, 1999, 540 с.;
5. Степанов В. М. Молекулярная биология. Структура и функции белков // М.: Высшая школа, 1996, 335 с.;
6. Скулачев В. П. Энергетика биологических мембран // М.: Наука, 1989, 565 с.;
7. Карякин А. В., Арчаков А. И. Межмембранный перенос электронов // Успехи современной биологии, 1981, Т. 91, вып. 1, с. 74-89;
© И н с т и т у т Ф и з и к и
им. Л.В.Киренского 1998-2007
[an error occurred while processing this directive]