Какой кальций сдавать при остеопорозе
Комплексное обследование, включающее исследование маркеров метаболизма костной ткани и маркеров состояния минерального обмена и его регуляции. Обследование будет полезно как для ранней диагностики остеопороза, так и для выбора метода адекватной терапии и оценки ее эффективности.
Электрохемилюминесцентный иммуноанализ (ECLIA):
Кинетический колориметрический метод:
Твердофазный хемилюминесцентный иммуноферментный анализ:
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Остеопороз – метаболическое заболевание, характеризующееся снижением костной массы и микроструктурной перестройкой костной ткани, в связи с чем снижается прочность кости и повышается риск переломов.
Кость формируется остеобластами. Основная их функция – синтез остеоида (протеинового матрикса), который на 90-95 % состоит из коллагена 1-го типа, на 5 % – из белка остеокальцина и затем минерализуется кальцием и фосфатом из внеклеточной жидкости. Остеобласты содержат фермент щелочную фосфатазу, несут рецепторы к паратиреоидному гормону и кальцитриолу и способны к пролиферации. Минеральная часть кости состоит из гидроксиапатита и аморфного фосфата кальция, которые связаны с белками органического матрикса.
В костях непрерывно происходят процессы ремоделирования, включающие в себя резорбцию (разрушение) существующей костной ткани и образование новой. Резорбция кости осуществляется остеокластами. Это подвижные клетки, которые выделяют протеолитические ферменты и кислую фосфатазу, вызывая деградацию коллагена, разрушение гидроксиапатита и выведение минералов из матрикса. Ежегодно в организме человека обновляется 8-10 % всей костной ткани.
В детстве формирование костей происходит значительно интенсивнее процессов резорбции. Максимальная костная масса достигается в возрасте 25-30 лет. Затем начинают преобладать процессы резорбции и костная масса постепенно уменьшается. Метаболизм костной ткани регулируется витамином D, кальцием, эстрогенами, андрогенами, паратиреоидным гормоном, кальцитонином. Дисбаланс между разрушением и восстановлением плотности костей может возникнуть при гормональных или диетических изменениях, недостаточном употреблении кальция. Преобладание процессов резорбции приводит к остеопении (снижении плотности костей), которая прогрессирует и переходит в остеопороз.
Костная щелочная фосфатаза и остеокальцин отображают активность остеобластов в костной ткани. Стимуляция остеобластов происходит при интенсивных процессах деструкции костей, которые сопровождают остеопороз, болезнь Педжета, переломы, опухоли костей. При остеопорозе уровни остеокальцина и щелочной фосфатазы увеличиваются согласованно, причем нарушения метаболизма костной ткани возникают раньше первых изменений плотности костей, которые можно выявить при денситометрии (метод лучевой диагностики). В костях щелочная фосфатаза играет важную роль в формировании и обновлении костной ткани. Чем выше активность остеобластов, тем выше активность щелочной фосфатазы в крови, поэтому у детей и лиц, перенесших переломы костей, активность щелочной фосфатазы на высоком уровне.
Витамин D и его активные метаболиты являются компонентами гормональной системы, регулирующей фосфорно-кальциевый обмен, и участвуют, с одной стороны, в минерализации костной ткани, с другой – в поддержании гомеостаза кальция. Биологическое действие активных метаболитов витамина D заключается, главным образом, в стимуляции кишечной абсорбции кальция и фосфора, активации обмена и усилении экскреции кальция с мочой. При дефиците витамина D уровень кальция компенсируется за счет его мобилизации из костной ткани, что может привести к остеомаляции, рахиту у детей и остеопорозу у взрослых.
Уровень паратиреоидного гормона (ПТГ) тесно связан с количеством кальция, витамина D, фосфора и магния в организме. Регуляция его секреции осуществляется по принципу обратной связи, поэтому важно одновременно с ПТГ оценивать уровень свободного или ионизированного кальция в крови, учитывать клинические проявления и результаты других лабораторных и инструментальных исследований. При снижении концентрации кальция в крови (гипокальциемии) выделение ПТГ паращитовидными железами усиливается, а при повышении (гиперкальциемии) – снижается. Данные механизмы направлены на поддержание стабильного уровня кальция в крови. Повышение ПТГ способствует активации остеокластов, резорбции костной ткани и высвобождению кальция из костей, усиливает всасывание кальция из кишечника, задерживает выделение кальция почками и ингибирует обратную реабсорбцию фосфора. Антагонистом ПТГ является гормон кальцитонин, секретируемый С-клетками щитовидной железы. В норме при достижении нормальной концентрации кальция в крови продукция ПТГ снижается.
Ионизированный кальций – катион, свободно циркулирующий в крови и составляющий 46-50 % от всего кальция крови. Его уровень возрастает при понижении pH крови и снижается при защелачивании. На каждые 0,1 единицы понижения pH ионизированный кальций отвечает повышением на 1,5-2,5 %. Так как уровень ионизированного кальция не зависит от количества белка крови, он иногда является более надежным показателем первичного гиперпаратиреоза для людей с низким уровнем альбумина, чем уровень общего кальция крови.
Несмотря на то что показателя общего кальция крови часто хватает для предварительной оценки кальциевого обмена, так как часто баланс между связанным и свободным кальцием – величина стабильная и достаточно предсказуемая, у некоторых людей это соотношение нарушено, поэтому уровень общего кальция не является критерием для оценки всего кальциевого обмена. В таких случаях проверка ионизированного кальция становится необходимой.
Раннее выявление остеопороза и лечение позволяют предотвратить прогрессирование заболевания и переломы, что значительно улучшает качество жизни людей старших возрастных групп.
Для чего используется исследование?
Когда назначается исследование?
При хронических заболеваниях почек;
При лечении глюкокортикоидами (выявление супрессии костного метаболизма).
Что означают результаты?
N-Остеокальцин:
Какой кальций сдавать при остеопорозе
В яичках у мужчин, яичниках у женщин, в надпочечниках у обоих полов
В молодом возрасте скорость образования новой костной ткани превышает скорость разрушения старой, в итоге происходит рост костей. Как правило, этот процесс завершается в 20 лет, когда достигается наибольшая костная масса, объем которой на 80 % зависит от генетических факторов. В 20-30 лет объем костной массы остается постоянным, после чего процесс образования новой костной ткани замедляется.
При остеопорозе существующая костная ткань разрушается быстрее, чем формируется новая. Если организм не обладает достаточным запасом костной массы, плотность костей уменьшается, они становятся хрупкими. Переломы могут происходить даже при микротравмах, при незначительных падениях.
Осложнения остеопороза не только вызывают сильную боль, но также могут приводить к инвалидности и к смерти.
Остеопороз бывает первичным и вторичным.
1. Первичный остеопороз составляет более 95 % случаев. Он может быть нескольких типов.
У пожилых женщин остеопорозы I и II типа часто сочетаются.
2. Вторичный остеопороз составляет менее 5 % случаев заболевания. Риск его развития могут увеличивать различные врождённые заболевания, дефицит или избыток гормонов, недостаточное поступление с пищей питательных веществ, хронические заболевания, алкоголизм, курение, беременность и др.
Кто в группе риска?
Остеопороз может быть заподозрен у любого взрослого человека, перенесшего перелом при минимальной травме. Его нередко выявляют случайно при рентгенологическом исследовании, назначенном по другому поводу. Наиболее надежным методом диагностики остеопороза является определение минеральной плотности костей.
Лабораторные исследования (проводятся в целях определения причин, вызвавших остеопороз)
Другие методы исследования
Целью лечения при остеопорозе является предовтвращение переломов и уменьшение болей. Для этого рекомендуется изменение образа жизни пациента, назначаются препараты кальция и витамина D, а также препараты, способствующие сохранению костной массы.
Рекомендуемые анализы
Диагностика остеопороза у женщин и мужчин: какие анализы сдавать
Что такое остеопороз
Остеопороз – заболевание, которое возникает при сильной потере массы костной ткани либо ее замедленном образовании. Это приводит к тому, что скелет слабеет, возрастает вероятность переломов. Каждый человек в возрасте после 50 лет, пострадавший от перелома, должен пройти диагностику на выявление остеопороза. Главной причиной болезни может быть длительный стаж курения, проблемы с пищеварением, сбои в работе обмена веществ. В зрелом возрасте остеопороз является следствием плохого усвоения кальция организмом. Заболевание может возникать у людей с высоким уровнем потоотделения, низким весом, а также у тех, кто ведет малоактивный образ жизни.
Признаки и симптомы остеопороза
На ранних стадиях болезнь протекает бессимптомно. Позднее она приводит к появлению болей в костях, мышцах. Прогресс недуга приводит к развитию острой боли. Часто она переносится на другие участки, продолжается в течение 7 дней, а потом стихает в течение нескольких месяцев. Диагностика остеопороза у женщин должна быть пройдена при болях в спине или нижней части спины, а также конечностях. Снижение плотности костей при остеопорозе может привести к инвалидности. На основании лабораторных анализов специалист может своевременно назначить лечение и предупредить развитие болезни.
Диагностика остеопороза у женщин и мужчин
Есть несколько методов диагностики остеопороза. Каждый из них имеет минимальную информативность, лучшие показатели получают при комплексном использовании процедур. Диагностика включает следующие виды процедур:
Анализ мочи
Анализы мочи при остеопорозе у женщин позволяют выявить наличие фосфора неорганического и дезоксипиридинолина.
В норме фосфор не должен превышать показатель от 13 до 43 ммоль/сут.
Высокий уровень свидетельствует о передозировке витамином D, рахите, появлении камней в почках.
Низкий уровень говорит о метастазах в крови, инфекционном очаге в организме.
В норме уровень ДПИД в крови должен составлять 3,6-4 у женщин и 2,3-5,6 у мужчин.
Высокий уровень говорит о наличии остеопороза, метастазах.
Низкое содержание типично для восстановления организма после болезни. За два дня до проведения диагностики состояния костной системы нужно исключить алкоголь и некоторые медикаменты.
Ультразвук
Методика состоит в анализе интенсивности прохождения ультразвукового импульса. Процедура необходима для определения уровня минерализации скелета, а также восприимчивости к механическому воздействию. В костной ткани с низкой плотностью звуковая волна проходит медленно. Из-за небольшого размера прибора исследование доступно для дистальных областей скелета. Как и анализ крови на остеопороз, метод позволяет выявить характеристики костей и определить риск переломов.
КТ-денситометрия
Как называется анализ на остеопороз, с помощью которого получают объемное изображение костной структуры? КТ-денситометрия. Устройство определяет плотность ткани, а после сравнивает ее с образцом. Этот метод устанавливает:
МРТ для анализа состояния пациента используют редко. Если врач заподозрил у вас остеопороз и определил, какие анализы надо сдать, то назначенная магнитно-резонансная томография позволит получить объемное изображение состояния внутренних органов. Процедура выявляет плотность структуры кости.
Радиоденситометрия
Этот способ диагностики при появлении симптомов остеопороза базируется на использовании рентгеновского излучения. Задействуется специальный прибор, определяющий плотность костей. Для постановки диагноза анализируется два участка: бедренная кость и позвонки в пояснице. Компьютер вычисляет плотность ткани, а после сравнивает результат с образцами.
Генетическое исследование
Процедура предполагает определение нормы коллагена, коллагеназы, кальцитонина. Позволяет выявить риск развития заболевания, уровень предрасположенности к переломам. Генетический анализ позволяет предотвратить развитие остеопороза. В процессе исследования устанавливаются генные мутации, которые могли привести к уменьшению плотности костной ткани.
Анализ крови
Анализ крови позволяет определить общее состояние организма, включая обмен фосфора и кальция. Они вымываются из организма в ходе болезни. При наличии болезни нарушается обмен этих элементов. Старые клетки уничтожаются остеокластами настолько быстро, что остеобласты не успевают заменяться новыми. Это приводит к пористости костей.
Неорганический фосфор
Главная цель фосфора – обеспечение роста костной ткани и поддержание ее целостности. Содержание элемента в крови позволяет определить скорость, с которой он всасывается в кишечник. В норме это 0,87-1,45 (моль/л).
Маркер D-Cross Laps
Определяет интенсивность вымывания из организма полезных минералов. Норма для мужчин – меньше 0,580 нг/л. Норма для женщин – меньше 0,573 нг/л.
Остеокальцин
Биохимия крови позволяет определить количество костного белка, который вырабатывается остеобластами. Норма для мужчин составляет 14-46 нг/мл, для женщин – 15-46 нг/мл.
Фермент щелочной фосфатазы
Высокий уровень фермента в организме говорит о наличии костных патологий. Норма для мужчин составляет меньше 115 е/л, для женщин – меньше 105 е/л.
Кальций
Кальций – это элемент, формирующий костную ткань. Норма для мужчин и женщин 18-60 лет – 2,15-2,56 моль/л, от 60 лет – 2,05-2,55 моль/л.
Профилактика остеопороза
Предупредить заболевание помогут следующие профилактические меры:
Боль в костях при остеопорозе
Поделиться:
Остеопороз — заболевание, приводящее к разрушению костной ткани, первым признаком которого является боль в костях. Его причина — нарушения обмена веществ, поэтому при костных болях неясного происхождения можно уточнить диагноз при помощи анализов крови.
Куда девается кальций
Кость состоит из сетчатого белкового «скелета», в ячейки которого откладываются соли кальция и фосфора. Именно этим объясняется ее прочность: если бы кость была просто твердой, она оказалась бы хрупкой, как фарфор, но белковая основа сообщает ей необходимую гибкость. В процессе развития человека — начиная еще с внутриутробного периода — формируется сперва гибкая «матрица» будущей кости, а кальцием она наполняется уже позже. Уровень насыщенности кости кальцием различается в разные периоды жизни. Отчего это зависит?
Дело в том, что обеспечение твердости нашего скелета — не единственная забота кальция. Он необходим для сокращения мышц — в том числе и сердечной. Поэтому понижение уровня кальция в крови ниже некоего «прожиточного минимума» совершенно справедливо рассматривается организмом как ситуация, угрожающая жизни. А скелет — это огромный «запас» кальция, из которого его при необходимости можно брать.
Читайте также:
Психогенная боль в спине
Костный «индикатор»
Регуляцией уровня кальция в крови занимаются два гормона: кальцитонин (его выделяет щитовидная железа) и паратгормон (продукт паращитовидных желез — маленьких образований на задней поверхности щитовидной железы). Если кальция в крови достаточно, кальцитонин «загоняет» его в кости. Но если уровень этого металла в крови падает, паратгормон «вытаскивает» его из костной ткани, чтоб не остановилось сердце.
Очевидно, что при нарушениях в выработке этих гормонов непременно возникнут симптомы со стороны костей, причем зачастую они бывают одними из первых. В зависимости от характера гормональных нарушений выделяют следующие виды остеопороза.
Тиреоидный остеопороз
Тут все несложно. Гипофункция щитовидной железы — недостаток кальцитонина: кальция много в крови, а в кости он не попадает, развивается остеопороз. Кроме ноющих неясных болей в костях снижение функции нашего «щита» проявляется и другими симптомами: вялость, слабость, ощущение общей заторможенности, сухость и бледность кожи, ломкость волос, отечность лица, урежение пульса, снижение иммунитета. Уточнить диагноз поможет анализ крови на тиреотропный гормон (ТТГ) в комплексе с кальцитонином. ТТГ изменяется и в случае понижения, и в случае повышения функции щитовидной железы, поэтому начинать обследование нужно именно с него, а не с визуализационных методов (УЗИ).
Паратиреоидный остеопороз
Здесь все наоборот. Паратгормон, как мы помним, «выгоняет» кальций из костей в кровь. При гиперфункции паращитовидных желез паратгормона слишком много, он действует очень активно, что опять способствует развитию остеопороза. Однако избыток кальция в крови тоже ни к чему хорошему не приводит. Чрезмерно длительные сокращения — спазмы — гладкой мускулатуры кишечника вызывают запоры и боли в животе. Почки, пытаясь вывести избыток кальция, работают «на износ», в них могут появляться камни-кальцинаты, мочевыделение увеличивается и ощущается сильная жажда. Разобраться в такой ситуации помогут анализ крови на кальций и фосфаты и определение кальция в суточной моче.
Эстрогензависимый остеопороз
Опосредованно на уровень кальция влияют также женские половые гормоны — эстрогены. Именно поэтому их снижение в перименопаузальном периоде может приводить к развитию остеопороза.
Воздействие эстрогенов на костную ткань — сложный многоступенчатый процесс. Интересно, что эти гормоны влияют не только на обмен кальция, но и на общее состояние «белкового скелета». С точки зрения природы все довольно логично: юная девушка (с высоким уровнем эстрогенов) должна быстро залечивать любые травмы, а вот немолодой, которая уже выполнила репродуктивную функцию, такая способность как бы уже не обязательна. Против природы не пойдешь, однако нам не хочется соглашаться с природными механизмами.
Поэтому всем женщинам, вступающим в пременопаузу, рекомендуется обсудить со своим гинекологом вопрос профилактики остеопороза — она куда эффективнее лечения. Основные анализы, которые может назначить врач: определение в крови кальция и костной фракции щелочной фосфатазы и количество кальция в суточной моче.
Любые подозрения на остеопороз должны быть подтверждены денситометрией — измерением плотности костной ткани. Наиболее точным вариантом является двуэнергетическая рентген-денситометрия. Как любой рентгеновский метод, она не совсем безвредна, однако существует альтернатива — УЗ-денситометрия. Так что поставит диагноз в любом случае несложно — главное сделать это вовремя.
Современные подходы к диагностике и лечению остеопороза
Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболи
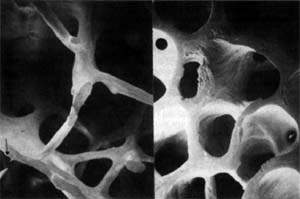 |
| Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. |
Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболизма.
Остеопороз — это системное заболевание скелета, характеризующееся снижением костной массы и нарушением микроархитектоники костной ткани, ведущими к повышенной хрупкости костей с последующим увеличением риска их переломов (рис. 1). Помимо наиболее распространенного постменопаузального остеопороза, в настоящее время в цивилизованных странах в связи с растущей продолжительностью жизни все чаще встречается сенильный остеопороз, а также вторичный остеопороз, обусловленный различными заболеваниями (эндокринная патология, ревматические болезни, заболевания желудочно-кишечного тракта и пр.) или связанный с длительным приемом некоторых лекарственных препаратов, например кортикостероидов.
В настоящее время для диагностики остеопороза используются преимущественно неинвазивные методы, которые легковыполнимы, безопасны и могут повторяться неоднократно у одного и того же больного. К таким методам относятся рентгенографическое исследование, костная денситометрия и исследование биохимических маркеров костного метаболизма. Каждый из этих методов занимает свою нишу в диагностике заболе-вания.
С целью ранней диагностики остеопороза применяются различные технологии, объединенные под общим названием «костная денситометрия», с ее помощью можно определить минимальную плотность костной ткани (МПК), являющуюся главным критерием прочности кости. В настоящее время выделяют четыре типа и два подтипа технологий для измерения МПК:
В данном перечне отсутствует фотонная денситометрия — предшественница рентгеновской денситометрии, в последнее время используемая весьма редко.
 |
| Рисунок 2 |
Системы DXA являются наиболее изученными и широко применяются в клинической практике (рис. 2). DXA позволяет измерять МПК в центральных отделах скелета: в поясничном отделе позвоночника и в проксимальном отделе бедренной кости. В этих участках происходят наиболее тяжелые переломы. Кроме того, многие из этих приборов снабжены программой «все тело», позволяющей определить содержание минералов во всем скелете, а также исследовать мягкие ткани — мышечную и жировую. В новых модификациях приборов DXA имеется возможность латерального сканирования и морфометрического измерения позвонков,что значительно повышает информативность этого метода. Метод DXA также адаптирован для оценки состояния МПК в области периферических участков скелета, в частности в области предплечья и пяточной кости (рис. 3).
Радиографическая абсорбциометрия используется редко, поскольку требует специально оборудованного центра, где при помощи микроденситометра производится сканирование рентгеновских снимков фаланг и определяется их оптическая плотность.
 |
| Рисунок 3 |
Для определения МПК позвоночника можно использовать и QCT, которая является единственным методом, представляющим результаты исследования в трехмерном измерении. Возможность проведения измерений в поперечном сечении, заложенная в QCT, позволяет выделить этот метод среди других, так как он дает возможность дифференцированно оценивать МПК в трабекулярной и кортикальной костной ткани, фиксируя истинные значения МПК в г/см3 [1]. В отличие от DXA при QCT нет искажений МПК, связанных с тучностью пациента, а также вызванных сопутствующей патологией, например спондилоартритом и остеофитами, обызвествлением стенки аорты или участками остеосклероза, развивающимися в результате дегенеративных заболеваний или переломов позвонков. Но большие дозы облучения при QCT, а также высокая стоимость обследования ограничивают широкое применение этой технологии в диагностике остеопороза, использование ее оправданно лишь в ситуациях, требующих дифференциальной диагностики (рис. 4).
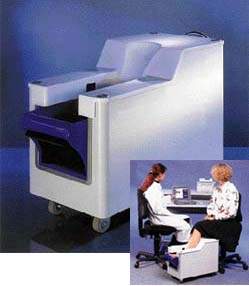 |
| Рисунок 4 |
В последние годы активно развивается ультразвуковая сонография, которая, в отличие от рентгеновской денситометрии, позволяет обследовать другие характеристики костной ткани: SOS — скорость распространения ультразвука в кости и BUA — широковолновое рассеивание (затухание) ультразвуковой волны в исследуемом участке скелета. Эти параметры, по данным многих исследователей, отражают степень эластичности и прочности костной ткани и достаточно высоко коррелируют с МПК позвоночника и шейки бедра [2]. В настоящее время многие специалисты высказывают мнение о том, что с помощью ультразвуковой денситометрии можно предсказывать риск переломов, тем самым обосновывая ее значение как метода для скрининга. Вопрос о возможности применения этих приборов в диагностике остеопороза и оценке эффективности терапии продолжает дискутироваться.
Рентгенография довольно активно используется для диагностики остеопороза и его осложнений. Однако ее нельзя отнести к методам ранней диагностики, поскольку рентгенологические признаки остеопороза появляются тогда, когда 20 — 30% костной массы уже потеряно [3]. Наиболее сложно оценить выраженность остеопороза в позвоночнике, поскольку ни один из его рентгенологических признаков не является специфичным. Часто рентгенография позволяет выявить остеопороз лишь на поздней стадии, когда уже имеются остеопоретические переломы. Для объективной оценки степени снижения минерализации костей разработаны так называемые полуколичественные методы. В основе их лежит вычисление вертебральных, феморальных и метакарпальных индексов. Но они также не могут претендовать на достаточную точность и чувствительность при выявлении ранней стадии заболевания (остеопении), хотя успешно применяются при эпидемиологических исследованиях распространенности остеопороза в популяции [4, 5]. Таким образом, основной функцией ренгенографического метода в диагностике остеопороза является обнаружение переломов, динамическое наблюдение за появлением новых переломов и дифференциальная диагностика остеопоретических переломов от других типов деформаций позвоночника.
С помощью методов «костной денситометрии» можно судить об основных параметрах прочности костной ткани, однако эти методы не дают никакой информации об уровне костного метаболизма. Уровень формирования и резорбции костной ткани может быть оценен несколькими способами: путем измерения ферментной активности костных клеток (остеобластов и остеокластов) или определения продуктов деградации костного матрикса, которые высвобождаются в циркуляцию в процессе костного обмена (табл. 1).
Таблица 1. Биохимические маркеры костного метаболизма
маркеры
мочи
Представленные в таблице костные маркеры являются предикторами потери костной массы, переломов костей скелета и используются для мониторинга антиостеопоретической терапии. По этим биохимическим показателям можно судить об эффективности терапии, об адекватности дозы препарата и о его переносимости. Особенно полезны костные маркеры для оценки эффективности терапии в сравнительно короткие промежутки времени, когда денситометрическое исследование еще не информативно (полагают, что повторные денситометрические исследования надо выполнять не чаще одного раза в год). Уровень маркеров костного метаболизма изучался в основном у женщин постменопаузального периода. Оказалось, что уровень почти всех маркеров, за исключением IPCP, повышен и коррелирует со снижением МПК [6]. Полагают, что сочетание денситометрии и исследования биохимических маркеров костного метаболизма позволит получить более полную информацию о риске развития постменопаузального остеопороза. По мнению P. Delmas (1996) увеличение скорости костной резорбции (по оценке уровней биохимических маркеров) существенно повышает риск развития переломов независимо от исходной костной массы пациентов [7]. Это связано с тем, что хрупкость кости при остеопорозе зависит не только от МПК, но и от нарушения микроархитектоники костной ткани, выраженность которой можно оценить с помощью биохимических маркеров костной резорбции. Это предположение подтверждается данными P. Garnero et al. (1996), полученными в рамках исследования EPIDOS [6]. Доказано, что увеличение уровня СТх или свободного диоксипиридинолина на 1SD от нормы ассоциировалось с 1,3- и 1,4-кратным увеличением риска переломов шейки бедра (рис. 5).
 |
| Рисунок 5. Комбинированная оценка МПК и скрытой костной резорбции для определения риска перелома шейки бедра у пожилых. МПК определялась по критериям ВОЗ с учетом показателей ниже 2,5 SD от нормальных показателей МПК у молодых здоровых женщин (Ts core |
При этом снижение МПК шейки бедра и увеличение маркеров костной резорбции, независимо друг от друга, связаны с высоким риском переломов шейки бедра. Для оценки эффективности проводимой терапии рекомендуется исследовать биохимические маркеры через каждые три месяца после начала лечения. При исследовании биохимических маркеров необходимо принимать во внимание факторы, влияющие на воспроизводимость результатов: диета, условия хранения материала, биологические факторы (циркадные и сезонные колебания, менструальный цикл, возраст, пол, наличие сопутствующих заболеваний и т. д.).
Многолетний опыт изучения остеопороза за рубежом показывает, что ни один из существующих в настоящее время лекарственных препаратов не может надежно восстановить количество и качество кости, поэтому основной мерой в борьбе с этим заболеванием является профилактика. Профилактику остеопороза надо начинать рано и уделять особое внимание средовым факторам, влияющим на достижение пика костной массы, который наступает примерно к тридцати годам. В числе этих факторов — питание и физическая активность, адекватное поступление в организм витамина D и инсоляция. К наиболее важным периодам относятся период роста кости (юношество), беременность, лактация и перименопауза. Пик костной массы может быть значительно улучшен за счет включения в рацион продуктов с повышенным содержанием кальция (прежде всего молочные и рыбные продукты). Суточное потребление кальция должно составлять в среднем 1000 — 1500 мг, предпочтительно с пищей. Регулярные физические упражнения с весовой нагрузкой в период роста кости приводят к увеличению пика костной массы. У взрослых после достижения пика костной массы адекватное потребление кальция, постоянная физическая нагрузка и наличие регулярного менструального цикла также способствует сохранению костной массы. Профилактику остеопороза среди взрослого населения нужно проводить в «группах риска».
Проблема лечения остеопороза за рубежом изучается давно, причем особенно активно в последнее десятилетие, что связано с введением денситометрии. Однако до настоящего времени не разработаны общепринятые терапевтические программы и режимы лечения этого заболевания, что, по-видимому объясняется его многофакторной природой и сложным патогенезом. Основная цель лечебных мероприятий — сбалансирование процессов костного метаболизма и сохранение или улучшение качества жизни пациента. Для этого необходимо добиться замедления или прекращения потери костной массы; уменьшить болевой синдром в позвоночнике и периферических костях; улучшить функциональное состояние больного и предотвратить возможные падения; восстановить трудоспособность и психоэмоциональное состояние. Наряду с этиопатогенетической терапией препаратами, направленными на нормализацию процессов ремоделирования костной ткани и на сохранение минерального гомеостаза, применяется и симптоматическая терапия, включающая в себя диету с повышенным содержанием солей кальция и фосфора, нестероидные противовоспалительные средства, анальгетики, миорелаксанты, которые позволяют уменьшить болевой синдром, мышечное напряжение и тем самым расширить двигательную активность пациента и ускорить начало реабилитационных мероприятий.
Реабилитация подразумевает лечебную физкультуру, ношение корсетов, плавание, курсы легкого массажа.
Все препараты для лечения остеопороза можно разделить на три группы:
В этиопатогенетической терапии остеопороза предпочтение отдается группе препаратов, подавляющих резорбцию костной ткани, вследствие их более высокой эффективности и сравнительно небольшого побочного действия.
В целом терапия остеопороза должна быть комплексной и проводить ее следует длительно в виде непрерывного или курсового лечения. Поскольку в настоящее время нет идеального препарата для лечения остеопороза, перспективна комбинированная терапия, в которой сочетаются препараты с различным механизмом действия, что позволяет потенцировать их антиостеопоретическое действие, снизить частоту и выраженность побочных эффектов.
| Профилактика остеопороза заключается в сбалансированном питании, физической активности, и адекватном поступлении в организм витамина D |
При комбинированной терапии лекарственные средства назначают одновременно или последовательно. Их выбор осуществляется индивидуально для каждого больного в зависимости от формы остеопороза, скорости костного обмена, тяжести клинического течения, сопутствующих заболеваний. Основным критерием эффективности любого антиостеопоретического средства является снижение частоты переломов, однако в каждом конкретном случае надо ориентироваться в первую очередь на показатели МПК по данным костной денситометрии и на биохимические маркеры костного обмена. Увеличение МПК более чем на 1% и нормализация биохимических показателей, если они были изменены, свидетельствуют об эффективности проводимой терапии. Учитываться должна и положительная динамика клинической картины: уменьшение болевого синдрома, повышение функциональной активности.
Таким образом, в настоящее время имеется довольно большой выбор диагностических методов, позволяющих установить диагноз остеопороза на разных стадиях, а также эффективных лекарственных препаратов, влияющих на различные звенья патогенеза остеопороза, способных уменьшить или купировать клинически выраженные симптомы заболевания, а также предупредить развитие переломов.
 Читайте также:
Читайте также: 




