Какой ион является исключением как его распознают
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Как получают галогеноводороды в промышленности и лаборатории?
Галогеноводороды в промышленности получают прямым синтезом из простых веществ:
H2 + F2 = 2HF
H2 + Cl2 = 2HCl
Фтороводород и хлороводород в лаборатории обычно получают воздействием концентрированной серной кислотой на их галогениды щелочных металлов:
CaF2 + H2SO4(конц.) = CaSO4 + 2HF↑
2NaCl + H2SO4(конц.) = Na2SO4 + 2HCl↑
Для получения иодоводорода и бромоводорода используют кислоты, не обладающие окислительными свойствами:
КI (тв) + Н3РO4 (конц.) = КН2РO4 + HI ↑
КВr(тв) + Н3РO4( конц. ) = КН2РO4 + HB ↑
Как изменяется скорость синтеза галогеноводородов в зависимости от природы галогена? Скорость синтеза галогеноводородов тем больше, чем более электроотрицателен галоген. Так, например, реакция фтора с водородом протекает со взрывом, а реакция иода с водородом — только при нагревании и является обратимой.
Задание 3
С помощью какого реактива можно распознать галогенид-ионы? Реактив качественной реакции — раствор нитрата серебра.
Ag + + Cl − ⟶ AgCl↓ — осадок белый творожистый
Аg + + Br − ⟶ AgBr↓ — осадок светло-желтый
Ag + + Br − ⟶ AgBr↓ — осадок желтый
Какой ион является исключением? Фторид-ион
Как его распознают? С помощью растворимой соли кальция: Ca 2+ + 2F − ⟶ CaF2↓ — осадок б елый
Задание 4
Составьте схему образования химической связи для молекул галогеноводородов.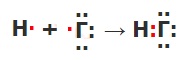
Как меняется их полярность связи и прочность молекулы от НF к НI? Полярность связи от HF к HI уменьшается, т. к. в этом ряду уменьшается электроотрицательность галогенов. Прочность молекулы уменьшается, т.к. в этом ряду увеличивается длина связи Н—Г (поскольку растёт радиус атома галогена).
Задание 5
Дайте сравнительную характеристику галогеноводородных кислот. Укажите черты сходства и различия. Сравнение химических свойств проиллюстрируйте уравнениями химических реакций.
Сходства химических свойств галогеноводородных кислот:
1) реагируют с металлами:
Zn+ 2HCl = ZnCl2 + H2↑
Zn+ 2HBr = ZnBr2 + H2↑
2) реагируют с основными оксидами:
MgO + 2HСl = MgCl2 + H2O
MgO + 2HF = MgF2 + H2O
3) реагируют с основаниями:
Mg(OH)2 + 2HBr = MgBr2 + 2H2O
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
4) реагируют с солями, если образуется газ или осадок:
2HF + Ca(NO3)2 = 2HNO3 + CaF2↓
HI + AgNO3 = HNO3 + AgI↓
Различия химических свойств галогеноводородных кислот.
В ряду HF—НСl—НВг—HI растёт сила кислот, то есть средней силы плавиковая кислота HF, в отличие от остальных сильных кислот, обладает необычным свойством: она способна реагировать с оксидом кремния (IV):
4HF + SiO2 = SiF4 + 2Н2O
Дополнительное задание
Объём производства соляной кислоты в России составляет 1 млн т в год. Сравните эти данные с объёмом производства соляной кислоты в трёх-четырёх других странах. Результат представьте в виде диаграммы в координатах: объём производства (млн т) — страна. Самостоятельно.
«Качественные реакции по химии»
Ищем педагогов в команду «Инфоурок»
« Качественные реакции в неорганической химии»
NaCI + AgNO3 =NaNO 3 + AgCI↓ 2 AgCI=2Ag + CI 2↑
Бромиды образуют осадок темно-желтого цвета.
NaBr + AgNO3=NaNO3 + AgBr↓
Иодиды образуют осадок светло-желтого цвета
В 3-х пробирках находятся растворы солей- натрий хлорида, натрий бромида и натрий иодида. Как распознать данные вещества? Записать ход рассуждения и последовательность их распознавания. Записать уравнения соответствующих уравнений реакций.
В три пробирки приливаем общий реактив- нитрат серебра. Выпадают осадки разной окрашиваемости. Это хлорид серебра, бромид и иодид. (Уравнения реакций записаны выше). Легче всего определить белый творожистый осадок. Значит, в той пробирке был натрий хлорид. Труднее будет определить два оставшихся осадка. В зависимости от концентрации они могут быть одинаковой желтой окраски. Для этого к двум оставшимся осадкам приливаем хлорную воду. Там, где был бромид серебра, наблюдается появление небольшого бурого облака. 2 AgBr + С I 2 =2 AgCI + Br 2
К третьему осадку-это иодид серебра тоже приливаем хлорную воду и небольшое количество крахмального клейстера. Наблюдается посинение раствора. Выделяющийся йод окрашивает крахмальный клейстер.
Изначально эту задачу можно было решить при помощи только хлорной воды- с хлоридом реакция не произойдет, а с оставшимися будут реакции, описанные выше.
Реактивом на сульфат-ион является раствор барий хлорида или барий нитрата. Выпадает белый нерастворимый в хлоридной или нитратной кислотах осадок.
Чтобы распознать нитрат-ион, надо к исследуемой соли добавить небольшое количество сульфатной кислоты и кусочек меди. Происходят одновременно две реакции.
б ) Cu + 4 HNO 3 = Cu(NO 3 ) 2 + 2 H 2 O +2 NO 2.↑ При этой реакции выделяющийся нитроген( IV ) оксид имеет «бурую окраску.»
По образованию бурого газа и голубого раствора соли меди можно судить о том, что это вещество нитрат.
Чтобы распознать любой карбонат, надо к нему а) прибавить
Б) Выделяющийся газ пропустить через известковую воду.
При этом образуется осадок белого цвета. При дальнейшем пропускании газа, он переходит в растворимую форму-т.к. образуется растворимая соль кальций гидрокарбонат
В 2-х пробирках находятся растворы а) калий карбоната и б)калий
сульфата. Распознать данные вещества. Описать ход рассуждения и записать уравнения реакций.
К содержимому пробирок приливаем хлоридную кислоту. Там, где был карбонат, происходит реакция и выделяется углекислый газ. Его пропускаем через известковую воду. Она « мутнеет».( уравнения аналогичных реакций записаны выше)
С калий сульфатом хлоридная кислота не реагирует. Значит в этой пробирке калий сульфат. Чтобы убедиться в правильности, у этому раствору приливаем барий хлорид. Образуется белый осадок. Реакция тоже записана.
Соли сульфитной кислоты можно распознать, действуя на них хлоридной кислотой. Выделяющаяся сульфитная кислота сразу же разлагается на воду и cульфур (IV) оксид-сернистый газ. Вот по появлению сернистого газа можно определить сульфиты.
В 3-х пробирках находятся растворы солей :сульфат, сульфит и сульфид калия.Как можно при помощи одного реактива разпознать их. Описать ход рассуждения и записать уравнения соответствующих реакций.
К содержимому всех пробирок приливаем концентрированную хлоридную кислоту. В той пробирке, где не происходит реакция, будет сульфат калия. В той пробирке, где появился запах горелой серы( сернистый газ) будет сульфит калия, в третьей пробирке появляется запах « тухлых яиц»-сероводород, там находился сульфид калия.
Реакция на соли фосфорной кислот-фосфат-ионы, дигидро и гидрофосфат-ионы.
Также можно распознать и кислые соли –дигидрофосфаты и гидрофосфаты
Силикат-ионы распознаются при реакции солей с сильной кислотой. Например, если к силикату прилить хлоридную кислоту, то выпадает белый осадок- кремниевая кислота.
В 3-х пробирках находятся растворы солей натрий хлорида, натрий ортофосфата и натрий сульфата. Как можно распознать данные соли. Записать ход рассуждения и уравнения реакций.
Вначале к содержимому пробирок приливаем нитрат бария.
Там, где находился ортофосфат, выпадет желтый осадок
Качественные реакции на катионы.
Ион аммония можно распознать, если к соли прилить немного щелочи и слегка нагреть.
Появляется у отверстия пробирки резкий запах аммика и индикаторная бумага окрашивается в синий цвет.
Соли, содержащие ионы калия окрашивают пламя в фиолетовый цвет, ионы натрия в желтый цвет, ионы кальция – в кирпично-красный цвет. В аналитической химиии есть специальные реактивы определяющие эти ионы, но они имеют очень сложные формулы. Поэтому, в школьной практике ограничимся только окраской пламени.
Ион алюминия определяется по образованию белого осадка при реакции соли со шелочью.
Гидроксид алюминия является амфотерным основанием, поэтому он будет растворяться в избытке щелочи.
Все растворимые соединения меди имеют голубую окраску. При взаимодействии любой соли меди со щелочью образуется нерастворимый синий осадок.
Если к такому синему осадку прилить гидроксид аммония, то осадок растворяется и превращается в сине-фиолетовый раствор сложной комплексной соли- купрум ( II ) аммиакат
Растворы таких солей имеют слегка зеленоватую окраску. При
Реакции со щелочами вначале образуется зеленый осадок.
Затем зеленый осадок переходит в бурый осадок.
Есть еще один реактив – это красная кровяная соль-гексоцианферрат( III ) C солями двухвалентного железа образуется осадок синий осадок-берлинская лазурь.
Растворы солей имеют желто-буроватую окраску. При действии на них щелочи выпадает бурый осадок.
Соли можно распознать при помощи роданита калия. При реакции образуется кроваво-красное окрашивание раствора.
Соли можно также распознать при помощи желтой кровяной соли
Гексоцианферрат( II )калия. Образуется темно-синий осадок-турнбулева синь.
В 3-х пробирках под номерами находятся растворы солей хлорид калия, хлорид железа ( II ) и хлорид железа ( III ). Как их можно распознать при помощи одного реактива. Записать ход рассуждения и записать уравнения реакций.
Для распознавания растворов этих солей надо взять раствор щелочи. Во всех 3- пробирках выпадут осадки. Там, где был хлорид железа( II ) будет зеленый осадок, там где хлорид железа( III ) выпадет бурый осадок, там, где был раствор хлорида алюминия-выпадет белый осадок, который растворится в избытке щелочи. ( Реакции записаны в теоретической части пособия)
В трех пробирках находятся растворы солей натрий карбонат, натрий хлорид и натрий нитрат. Распознать данные соли, записать ход рассуждения и записать уравнения реакций.
Вначале надо определить натрий карбонат. К содержимому пробирок приливает хлоридную кислоту. Она даст реакцию только с к натрий карбонатом. При этом будет выделяться углекислый газ и вода. Газ надо пропустить через известковую воду. Она помутнеет. После определения данной соли остались натрий хлорид и натрий нитрат. К содержимому двух пробирок надо прилить нитрат серебра. Он даст реакцию только с натрий хлоридом. Выпадет белый творожистый осадок. Натрий нитрат с ним не будет реагировать. Значит в третьей пробирке, где не произошла реакция- натрий нитрат. Чтобы доказать, что действительно данное вещество к нему приливаем концентрированную сульфатную кислоту и прибавляем медную проволоку. При нагревании будет выделяться бурый газ. Так можно определить данные вещества ( уравнения реакций приведены выше)
Доказать, что в состав аммоний нитрата входит азот аммонийный и нитратный.
К соли приливаем щелочь и нагреваем. Выделяется газ аммиак. Его определяем по запаху и по изменению окраски индикаторной бумаги.Так определили азот аммонийный.
К соли прибавляем сульфатную кислоту с кусочком меди и нагреваем. Выделяется бурый газ. Так мы определили наличие
нитратного азота в ионе аммония и нитратного азота в нитрат-ионе.
Проделать реакции подтверждающие качественный состав сульфатной кислоты.
Чтобы доказать в кислоте наличие иона гидрогена, надо прилить к кислоте или метилоранж или фиолетовый лакмус, или универсальную индикаторную бумагу. По изменению их окраски можно судить о наличие в кислоте ионов гидрогена.
Чтобы доказать наличие сульфат-ионов, надо прибавить раствор барий хлорида, или барий нитрата. По выпадению белого осадка барий сульфата, нерастворимого в сильных кислотах, можно доказать наличие этого иона.
Практическая работа №6. Ионные реакции.
В одну пробирку налейте 1-2 мл раствора сульфата натрия, а в другую – 1-2 мл раствора сульфата калия. В обе пробирки по каплям добавьте раствор хлорида бария. Объясните наблюдаемое.
В чём сущность обнаружения ионов с помощью реактива?
Составьте уравнения диссоциации солей, реакции обмена и полные и сокращённые ионные уравнения проведённых реакций.
В двух пробирках содержатся растворы хлорида калия и сульфата магния. С помощью каких реакций можно доказать, что в одной пробирке находится раствор хлорида калия, а в другой – раствор сульфата магния?
Раствор из первой пробирки разделите пополам и перелейте в две пробирки. Прилейте в одну пробирку раствор нитрата свинца (II), в другую – раствор хлорида бария. В какой из пробирок выпал осадок? Какая из солей – KCl или MgSO4 – содержится в первой пробирке?
Раствор из второй пробирки испытайте на присутствие аниона, не обнаруженного в первой пробирке. Для этого к испытуемому раствору прилейте раствор нитрата свинца (II). Объясните наблюдаемое.
Составьте уравнения реакций обмена проведённых вами реакций и полные и сокращённые ионные уравнения реакций обнаружения ионов.
Проделайте реакции, подтверждающие качественный состав следующих веществ: а) хлорида бария; б) сульфата магния; в) карбоната аммония. Для выполнения этого опыта используйте таблицу 12.
По таблице растворимости видно, что нерастворимым является хлорид серебра (I) и малорастворимым является хлорид свинца (II).
Опыт 4.
а) хлорид бария
б) сульфат магния
в) карбонат аммония
mozok.click
Обнаружение ионов в растворах
Понятие о качественных реакциях
Определение состава веществ и растворов — одна из задач современной химии. Качественный и количественный состав веществ и их смесей — предмет изучения аналитической химии.
Одним из способов определения качественного состава растворов является использование качественных реакций. Качественными реакциями называют реакции, позволяющие ответить на вопрос: «Содержится ли определенное вещество или ион в исследуемом образце?»
Качественные реакции — это обычные химические реакции, протекающие достаточно быстро и сопровождающиеся определенными визуальными изменениями: изменение окраски раствора, образование осадка определенного цвета или выделение газа, который также может иметь (не иметь) окраску или запах.
Известно множество качественных реакций, позволяющих выявить наличие в растворах ионов, спиртов, аминокислот, белков и других веществ. С некоторыми качественными реакциями вы ознакомитесь в этом параграфе, а с другими — при дальнейшем изучении химии.
Выявление ионов в растворах электролитов
Качественные реакции, позволяющие выявить ионы в растворе, в большинстве случаев сопровождаются образованием осадка определенного цвета. Например, обнаружение ионов Ва 2 + в растворе можно описать такой блок-схемой:
Наиболее часто употребляемые в школьном курсе химии реактивы для анализа приведены в таблице 8.
Выдающийся украинский физико-химик, член-корреспондент АН УССР. Родился в г. Сухуми, учился в Харьковском финансово-экономическом техникуме, работал на химическом факультете Харьковского университета. Основные научные исследования относятся к электрохимии растворов: изучал кислотно-основные взаимодействия в неводных растворах, развил теорию кислотно-основных реакций Брёнстеда и теорию действия стеклянного электрода, разработал количественную теорию диссоциации электролитов в растворах. Открыл метод тонкослойной хроматографии и разработал новые физико-химические методы анализа неводных растворов.
Таблица 8. Реактивы для определения некоторых анионов
Реактив для качественного анализа и пример уравнения реакции


Образование белого творожистого осадка AgCl, не растворимого в нитратной кислоте


Образование бледно-желтого осадка AgBr


Образование желтоватого осадка AgI


Образование ярко-желтого осадка Ag3PO4


Образование белого осадка BaSO4, не растворимого в кислотах


Образование белого осадка CaCO3

Выделение углекислого газа
Роль эксперимента в науке
Эксперимент — главный источник знаний. Проводя разнообразные исследования, ученые тысячелетиями накапливали знания в разных областях науки. Понятно, что, проведя один опыт, невозможно открыть закон или сформулировать теорию. На экспериментальном уровне познания происходит накопление фактов, информации о веществах и явления. Только обладая глубокими знаниями, можно
анализировать полученные данные и объяснять их, опираясь на уже существующую теорию или сформулировав свою.
Основываясь на экспериментальных фактах, ученые сформулировали большинство теорий. Так, изучая химические свойства кислорода, Лавуазье сформулировал кислородную теорию кислот, а взвешивая массы реагентов и продуктов реакции — закон сохранения массы. Изучая электропроводимость растворов, Аррениус заложил основы теории электролитической диссоциации. И таких примеров в истории химии множество.
Но некоторые теории и законы сначала были сформулированы теоретически путем анализа известных фактов. Необходимо было только «посмотреть» на эти факты с другой стороны. Анализируя свойства соединений элементов, Д. И. Менделеев открыл Периодический закон. Решая математические уравнения, Вольфганг Паули предположил существование неизвестной в то время характеристики электронов — спина, что экспериментально было подтверждено позже. Но, как говорил Нобелевский лауреат Лев Ландау: «Опыт — верховный судья теории». То есть любая теория или закон должны быть подтверждены экспериментально, как, например, открытие Галлия и Германия блестяще доказало истинность Периодического закона.
Известный украинский химик-аналитик, академик НАН Украины. Родился в поселке Кирилловка Черкасской области, окончил Киевский политехнический институт, работал в Киевском государственном университете. Занимался разработкой методов химического анализа неорганических материалов с использованием органических реактивов, применением комплексных соединений в химическом анализе. Руководил государственными программами «Чистая вода», принимал активное участие в ликвидации последствий Чернобыльской аварии, занимался созданием замкнутых циклов водоснабжения в промышленности, разработкой технологии комплексной переработки шахтных вод.
ЛАБОРАТОРНЫЕ ОПЫТЫ № 7-9
Оборудование: штатив с пробирками, пипетки.
• для опытов используйте небольшие количества веществ;
• остерегайтесь попадания веществ на кожу, одежду, в глаза; при попадании кислоты ее следует немедленно смыть большим количеством воды и протереть поврежденное место раствором соды.
Определение хлорид-ионов в растворе
В первую пробирку налейте раствор натрий хлорида объемом 1 мл, во вторую — такое же количество раствора натрий нитрата. В обе пробирки добавьте по 2-3 капли раствора аргентум(1) нитрата. Что вы наблюдаете?
По какому признаку можно определить, в какой из пробирок находятся хлорид-ионы?
Составьте молекулярные и ионно-молекулярные уравнения реакций.
Определение сульфат-ионов в растворе
В первую пробирку налейте раствор натрий хлорида объемом 1 мл, во вторую — такое же количество раствора натрий сульфата. В обе пробирки добавьте по 2-3 капли раствора барий хлорида. Что вы наблюдаете?
По какому признаку можно определить, в какой из пробирок находятся сульфат-ионы?
Составьте молекулярные и ионно-молекулярные уравнения реакций.
Выявление карбонат-ионов в растворе
1. В первую пробирку налейте раствор натрий нитрата объемом 1 мл, во вторую — такое же количество раствора натрий карбоната.
В обе пробирки добавьте по 2-3 капли раствора кальций хлорида. Что наблюдаете?
2. Повторите опыт, но вместо кальций хлорида в обе пробирки добавьте по 1 мл хлоридной кислоты. Что наблюдаете?
По каким признакам можно определить, в какой из пробирок находятся карбонат-ионы?
Составьте молекулярные и ионно-молекулярные уравнения реакций.
Качественная реакция — это химическая реакция, позволяющая выявить определенное вещество. Эксперимент является главным источником знаний. Он играет двоякую роль: доказывает или опровергает любые теоретические выводы и может стать основой новой теории или гипотезы.
159. Как вы понимаете понятие «качественные реакции»?
160. Какие химические реакции можно использовать как качественные?
Задания для усвоения материала
162. Предложите реактив, позволяющий различить пробирки с веществами в каждой из приведенных пар. Составьте соответствующие молекулярные и ионно-молекулярные уравнения реакций:
163. Охарактеризуйте роль эксперимента для: а) определения качественного и количественного состава веществ; б) открытия и доказательства истинности Периодического закона; в) становления теории электролитической диссоциации; г) развития науки.
ПРАКТИЧЕСКАЯ РАБОТА № 2
Решение экспериментальных задач
Оборудование: штатив с пробирками.
• для опытов используйте небольшие количества реактивов;
• остерегайтесь попадания реактивов на кожу, в глаза; при попадании едкого вещества смойте его большим количеством воды.
Определите необходимые реактивы и проведите реакции, которые соответствуют следующим ионно-молекулярным уравнениям:
Для всех проведенных реакций опишите свои наблюдения и составьте уравнения в молекулярной, полной и сокращенной ионномолекулярной формах.
Предложите, как можно доказать наличие каждого из ионов в растворе хлоридной кислоты.
Определите необходимые реактивы, выполните реакции и опишите визуальные изменения, по которым можно узнать состав веществ.
Для всех проведенных реакций опишите свои наблюдения и составьте уравнения в молекулярной, полной и сокращенной ионномолекулярной формах.
В пяти пронумерованных пробирках содержатся растворы следующих веществ: хлоридной кислоты, натрий хлорида, натрий сульфата, натрий гидроксида и магний нитрата. Предложите схему анализа, с помощью которого можно определить содержимое каждой пробирки, используя не более трех реактивов. Проведите химические реакции и укажите, в какой пробирке находится какое вещество. Составьте соответствующие уравнения реакций в молекулярной и сокращенной ионно-молекулярной формах.
Вывод. Сделайте обобщающий вывод к практической работе. Для этого используйте ответы на вопросы:
1. Может ли двум молекулярным уравнением реакции соответствовать одно сокращенное ионно-молекулярное уравнение?
2. Какие реакции называют качественными? По каким признакам выявляют те или иные ионы в растворе?
Темы учебных проектов по теме «Растворы»:
• Электролиты в современных аккумуляторах.
•Выращивание кристаллов солей.
•Приготовление растворов для оказания домедицинской помощи.
• Исследование pH почв своей местности.
• Исследование влияния кислотности и щелочности почв на развитие растений.
• Исследование pH атмосферных осадков и их влияния на различные материалы в окружающей среде.
• Исследование природных объектов в качестве кислотно-основных индикаторов.
• Исследование pH среды минеральных вод Украины.
Проверьте свои знания по теме «Растворы», выполнив тестовые задания на сайте.







