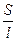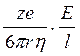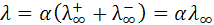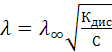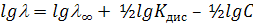Подвижность ионов
2. Подвижность ионов
Свяжем электропроводность электролита со скоростью движения его ионов в электрическом поле. Для вычисления электропроводности достаточно подсчитать число ионов, проходящих через любое поперечное сечение электролитического сосуда в единицу времени при стандартных условиях, т. е. при напряженности поля, равной 1 в/см. Так как электричество переносится ионами различных знаков, движущимися в противоположных направлениях, то общее количество электричества, проходящее через раствор в 1 сек, т. е. сила тока I, складывается из количеств электричества, перенесенных соответственно катионами I+ и анионами I—:
Обозначим скорость движения катионов через и’ (в см/сек), скорость движения анионов через v’ (в см/сек), эквивалентную концентрацию ионов через сi (в г-экв/см 3 ), поперечное сечение цилиндрического сосуда через q (в см ), расстояние между электродами через l (в см) и разность потенциалов между электродами через Е (в В). Подсчитаем количество катионов, проходящих через поперечное сечение электролита в 1 сек. За это время в одну сторону через сечение пройдут все катионы, находившиеся в начальный момент на расстоянии не более чем и’ см от выбранного сечения, т. е. все катионы в объеме u’q. Количество катионов n+, прошедших через поперечное сечение в 1 сек:
Так как каждый грамм-эквивалент ионов несет согласно закону Фарадея F = 96485 K электричества, то сила тока (в а):
Для анионов, скорость движения которых равна v’, рассуждая таким же образом, получим
Для суммарной силы тока (эквивалентные концентрации ионов одинаковы, т. е. c+ = c— = ci ):
Скорости движения ионов и’ и V’ зависят от природы ионов, напряженности поля E/l, концентрации, температуры, вязкости среды и т. д.
Пусть все факторы, кроме напряженности поля, постоянны, а скорость движения ионов в жидкости постоянна во времени при постоянной приложенной силе, если среда, в которой они движутся, обладает достаточной вязкостью. Следовательно, можно считать, что скорость ионов пропорциональна приложенной силе, т. е. напряженности поля:
где и и v—коэффициенты пропорциональности, которые равны скоростям ионов при напряженности поля, равной 1 в/см.
Величины и и v называются абсолютными подвижностями ионов. Они измеряются в см 2 /(сек·в).
Подставив выражение (25) в уравнение (24), получим
Подставляем в уравнение (27) значения К и, приравняв правые части уравнении (26) и (27) будем иметь:
Решив уравнение (28) относительно λ, получим
Для сильных электролитов, диссоциацию которых считают полной, отношение 1000 сi/с = 1; для слабых электролитов 1000 сi/с = α. Введем новые обозначения:
и назовем величины U и V подвижностями ионов. Тогда для сильных электролитов
а для слабых электролитов
При бесконечном разведении (т. е. при φ → ∞, U → U∞, V→ V∞ и α → 1) получим
как для сильных, так и для слабых электролитов. Величины U∞ и V∞, очевидно, являются предельными подвижностями ионов. Они равны эквивалентным электропроводностям катиона и аниона в отдельности при бесконечном разведении и измеряются в тех же единицах, что λ или λ∞ т. е. в см 2 / (ом • г-экв). Уравнение (33) является выражением закона К.ольрауша: эквивалентная электропроводность при бесконечном разведении равна сумме предельных подвижностей ионов.
Подвижность является важнейшей характеристикой ионов, отражающей их специфическое участие в электропроводности электролита.
Если ионы окрашены, то их перемещение при известных условиях можно измерить непосредственно и, таким образом, определить абсолютные подвижности.
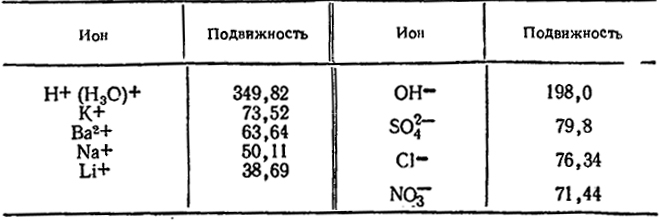
Пользуясь таблицей предельных подвижностей ионов и законом Кольрауша, можно легко вычислить предельную электропроводность соответствующих растворов.
Эквивалентная электропроводность растворов солей выражается величинами порядка 100—130 см 2 /(г-экв • ом). Ввиду исключительно большой подвижности иона гидроксония величины λ∞ для кислот в 3—4 раза больше, чем λ∞ для солей. Щелочи занимают промежуточное положение.
Движение иона можно уподобить движению макроскопического шарика в вязкой среде и применить в этом случае формулу Стокса:
где е—заряд электрона; z—число элементарных зарядов иона; r—эффективный радиус иона; η — коэффициент вязкости; Е/1 — напряженность поля.
Связь иона с молекулами растворителя, в частности с молекулами воды, ионно-дипольная, а так как напряженность поля на поверхности иона лития гораздо больше, чем на поверхности иона калия (ибо поверхность первого меньше поверхности второго, а радиус, т. е. расстояние диполей воды от эффективного точечного заряда в центре иона, меньше), то степень гидратации иона лития больше степени гидратации иона калия. Согласно формуле Стокса многозарядные ионы должны обладать большей подвижностью, чем однозарядные. Скорости движения многозарядных ионов мало отличаются от скоростей движения однозарядных, что, очевидно, объясняется большей степенью их гидратации вследствие большей напряженности поля, создаваемого многозарядными ионами.
Какой ион обладает наибольшей подвижностью
§ 2. Подвижность ионов
Наличие вакансий облегчает миграцию ионов кислорода, и при наложении разности электрических потенциалов смесь ZrO2-СаО в твердом состоянии становится анионным проводником. Это явление используется для определения термодинамических величин, важных для металлургической
практики. Доля электричества, которая переносится через электролит данным ионом, называется его числом переноса. Оно может быть найдено из уравнения, которое определяет количество электричества, прошедшего через сечение электролита, равное 1 см 2 за 1 с, и из приводившихся выше уравнений для количеств электричества, переносимого ионами. Таким образом, числа переноса
Учитывая, что υ = k при E = 1 В/см и Fk = 1, находим
Фарадея. Изменения концентраций у электродов представлены схематически на рис. VIII.1.
Грамм-эквивалент катионов обозначается знаком «плюс» и анионов знаком «минус»; вертикальные линии отделяют катодное, анодное и среднее пространства и показывают, что перемешивание растворов исключено.
Из сказанного следует, что убыль концентрации в катодном
или анодном пространствах пропорциональна подвижности иона с противоположным знаком, т.е. Δа/Δк = l+/l—. Прибавляя единицу к обеим частям равенства, найдем, t— = Δк/(Δа + Δк) и соответственно t+ = Δа/(Δа + Δк).
Основная экспериментальная трудность при определении чисел переноса таким способом заключается в устранении перемешивания растворов при электродах и в среднем пространстве. Очевидно, в среднем пространстве концентрация должна оставаться после электролиза неизменной, и необходимо аналитически найти уменьшение концентрации электролита в католите и анолите.
Более прямой способ измерения чисел переноса осуществляется при помощи метода движущейся границы, в котором определяются действительные скорости ионов. Идея этого метода поясняется рис. VIII.2.
В электролитической ячейке с кадмиевым анодом и платиновым катодом находится раствор HCl, окрашенный метилоранжем в красный цвет. В результате электролиза растворяется кадмий и вблизи анода образуется слой раствора CdCl2, который приобретает желтый цвет, свойственный метилоранжу в нейтральных растворах, так как ионы водорода из прианодного пространства уходят к катоду.
Отсюда число переноса водорода t+ = cVF/τ. Определения чисел переноса позволяют находить подвижности отдельных ионов при помощи уравнений λ∞ = l+ + l—,
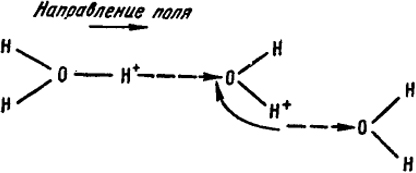
быть пояснен схемой:
Благодаря такому эстафетному механизму переноса протонов ионы гидроксония в действительности не двигаются через раствор и перенос тока осуществляется путем перераспределения электронов в молекулах воды. На схеме переход электрона в средней молекуле воды показан пунктирной стрелкой, а переходы протонов сплошными стрелками.
В неводных растворах могут иметь место и другие механизмы проводимости. Так, например, при растворении металлического натрия в жидком аммиаке образующийся раствор при низких температурах отличается сверхпроводимостью,
т.е. его электросопротивление исчезающе мало. Это обусловлено тем, что перенос тока осуществляется электронами.
ПОДВИЖНОСТЬ ИОНОВ



Свяжем электропроводность электролита со скоростью движения его ионов в электрическом поле. Для вычисления электропроводности надо подсчитать число ионов, проходящих через поперечное сечение электролитического сосуда в единицу времени. Так как электричество переносится ионами различных знаков, движущимися в противоположных направлениях, то общая сила тока складывается из количеств электричества, перенесенных катионами (I+) и анионами (I—) :
Подсчитаем количество катионов, проходящих через поперечное сечение электролита в 1 секунду. За это время через сечение пройдут все катионы, находившиеся на расстоянии не более чем u¢ см от выбранного сечения, т.е. все катионы в объеме u¢q :
Т.к. каждый г-экв ионов несет согласно закону Фарадея F =96485 к электричества, то сила тока (в А) :
Аналогично для анионов :
Для суммарной силы тока (с+ = с— = с¢) :
u¢ = u 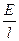
По закону Ома I = E/R = E×K = E×k
Отсюда k = (u + v)c¢qF/S = (u + v)c¢F (т.к. q º S)
l = 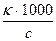
Для сильных электролитов : l = l+ + l—
Т.о., для всех электролитов можно записать :
Движение иона можно уподобить движению макроскопического шарика в вязкой среде и применить в этом случае формулу Стокса :
u =

Связь иона с молекулами растворителя ионно-дипольная, а так как напряжённость поля на поверхности иона лития гораздо больше, чем на поверхности иона калия, то степень гидратации иона лития больше степени гидратации иона калия. Согласно формуле Стокса многозарядные ионы должны обладать большей подвижностью, чем однозарядные. Однако скорости движения многозарядных ионов мало отличаются от скоростей движения однозарядных, что, очевидно, объясняется большей степенью их гидратации.
Шпаргалки к экзаменам и зачётам
студентам и школьникам
Подвижность ионов. Закон Кольрауша. Влияние природы иона на его подвижность (анализ формулы Стокса). Аномальная подвижность ионов гидроксония и гидроксила в водных растворах.
Подсчитаем количество катионов, проходящих через поперечное сечение электролита в 1 секунду. За это время через сечение пройдут все катионы, находившиеся на расстоянии не более чем u ¢ см от выбранного сечения, то есть все катионы в объеме u ¢ S :
Так как каждый г-экв ионов несет согласно закону Фарадея F = 96485 Кл электричества, то сила тока (в А)
Аналогично для анионов
Для суммарной силы тока (предполагая, что электролит бинарный и полностью диссоциированный, так что с+ = с– = с ¢ )
Отсюда k = ( u + v ) c ¢ F ;
Таким образом, для всех электролитов можно записать
200 см 2 /(Ом × г-экв). В результате эквивалентная электропроводность растворов солей выражается величинами порядка 100-130 см 2 /(г-экв × Ом). Ввиду исключительной подвижности иона гидроксония величины l ¥ для кислот в 3-4 раза больше, чем для солей; щелочи занимают промежуточное положение.
Связь иона с молекулами растворителя ионно-дипольная, а так как напряжённость поля на поверхности иона лития гораздо больше, чем на поверхности иона калия, то степень гидратации иона лития больше степени гидратации иона калия. Согласно формуле Стокса многозарядные ионы должны обладать большей подвижностью, чем однозарядные. Однако скорости движения многозарядных ионов ненамного превышают скорости движения однозарядных, что объясняется большей степенью их гидратации.
Подвижность ионов, закон Кольрауша
В бесконечно разбавленных растворах эквивалентная электропроводность достигает предела и от концентрации больше не зависит, так как в растворах слабых электролитов наступает полная диссоциация (α = 1), а в растворах сильных электролитов межионное взаимодействие исчезает.
Эквивалентная электропроводность бесконечно разбавленных растворов называется электропроводностью при бесконечном разведении и обозначается l∞ (или l0).
Эквивалентная электропроводность при бесконечном разведении, согласно закону независимого движения ионов Кольрауша, равна сумме предельных подвижностей ионов
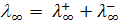
Подвижность связана с абсолютной скоростью движения ионов n:
где F – число Фарадея, 96487 к. ≈ 96500к.
Следовательно, отношение электропроводностей будет отвечать степени диссоциации слабых электролитов
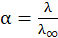
Это уравнение называют формулой Аррениуса, на практике его используют для определения степени диссоциации растворов электролитов.
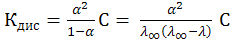
где С – концентрация электролита, моль/л.
Кроме электрофоретического и релаксационного торможения, существует третья сила, тормозящая движение ионов в растворе. Это сила трения, зависящая от вязкости растворителя, в котором движется ион. Поэтому повышение температуры вызывает увеличение скорости движения ионов, и как следствие возрастание электропроводности.
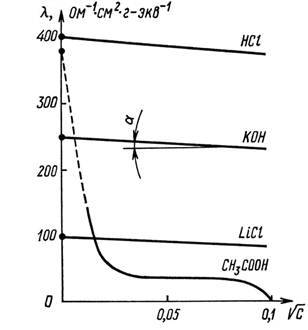
Для разбавленных растворов сильных электролитов теория дает линейную зависимость эквивалентной электропроводности от корня квадратного из концентрации (закон квадратного корня Кольрауша)
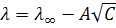
Постоянная А, зависящая от природы растворителя, температуры и валентного типа электролита, экспериментально определяется тангенсом угла наклона прямой 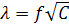
Предельную эквивалентную электропроводность 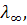
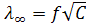

Рис. 10.2 Зависимость эквивалентной электропроводности от корня квадратного из концентрации для сильных электролитов (НСI, КОН, LiCI) 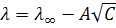
Для растворов слабых электролитов зависимость эквивалентной
электропроводности от концентрации вытекает из закона разбавления Оствальда. При α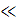
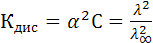
откуда
или в логарифмическом виде
Эта зависимость не является линейной, поэтому значение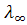
анод (+) | Н3O + 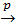
В результате такого перескока протон проходит 0,86 А, что отвечает перемещению катиона гидроксония на 3,1 Ǻ, или перенос гидроксила в электрическом поле к аноду
анод (+) | Н2O 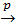
при котором перескок протона вправо имеет следствием перемещение гидроксила влево. При этом гидроксил, принимающий протон, превращается в молекулу воды, а вместо него возникает новый анион, находящийся к аноду ближе, чем тот, который исчезает вследствие присоединения протона. Естественно, что при таком механизме проводимости подвижность ионов водорода и гидроксила значительно больше, чем ионов, которые просто двигаются в электрическом поле.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет