Какой ион играет основную роль в мышечном сокращении
Гладкие мышцы содержат актиновые и миозиновые нити, имеющие химические характеристики, подобные актиновым и миозиновым нитям скелетных мышц. Но в гладких мышцах нет тропонинового комплекса, необходимого для запуска сокращения скелетной мышцы, следовательно, механизм инициации сокращения в них другой. Этот механизм подробно обсуждается далее в нашей статье.
Химические исследования показали, что актиновые и миозиновые нити, извлеченные из гладких мышц, взаимодействуют друг с другом во многом так же, как и в скелетной мышце. Более того, процесс сокращения активируется ионами кальция, а энергия для сокращения обеспечивается разрушением АТФ до АДФ.
Существуют, однако, значительные различия в морфологической организации гладких и скелетных мышц, а также в сопряжении возбуждения и сокращения, механизме запуска ионами кальция сократительного процесса, длительности сокращения и количестве энергии, необходимой для сокращения.
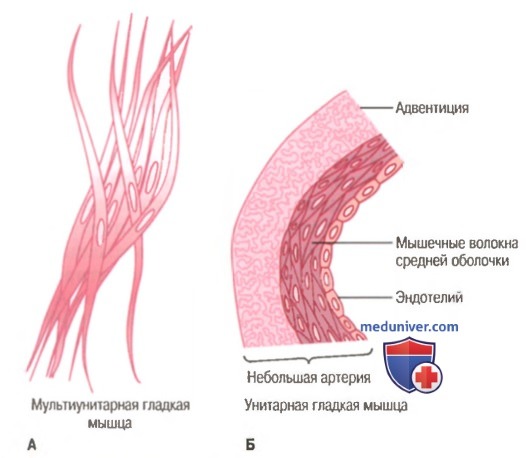
Морфологическая основа сокращения гладких мышц
Гладкие мышцы не имеют такой упорядоченной организации актиновых и миозиновых нитей, которая обнаруживается в скелетных мышцах, придавая им «полосатость». С помощью техники электронной микрофотографии выявляется гистологическая организация. Видно большое число актиновых нитей, прикрепленных к так называемым плотным тельцам. Некоторые из этих телец прикрепляются к клеточной мембране, другие распределяются внутри клетки. Некоторые из мембранных плотных телец соседних клеток связываются вместе мостиками из внутриклеточных белков. Через эти мостики в основном передается сила сокращения от одной клетки к другой.
В мышечном волокне среди актиновых нитей разбросаны миозиновые нити. Их диаметр более чем в 2 раза превышает диаметр актиновых нитей. На электронных микрофотографиях актиновых нитей обычно обнаруживают в 5-10 раз больше, чем миозиновых.
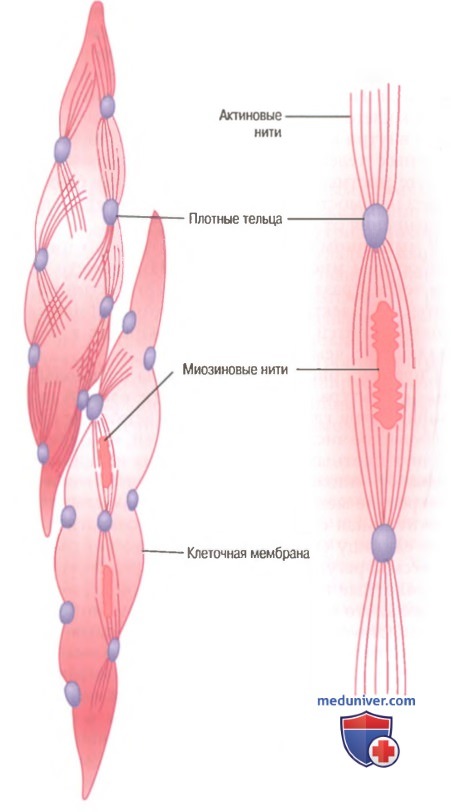
На рисунке представлена предполагаемая структура отдельной сократительной единицы внутри гладкомышечной клетки, где видно большое число актиновых нитей, исходящих от двух плотных телец; концы этих нитей перекрывают миозиновую нить, расположенную посередине между плотными тельцами. Эта сократительная единица похожа на сократительную единицу скелетной мышцы, но без специфической регулярности ее структуры. В сущности, плотные тельца гладкой мышцы играют ту же роль, что и Z-диски в скелетной мышце.
Существует и другое различие. Большинство миозиновых нитей имеют поперечные мостики с так называемой боковой полярностью. Мостики организованы следующим образом: на одной стороне они шарнирно фиксируются в одном направлении, а на другой — в противоположном направлении. Это позволяет миозину тянуть актиновую нить с одной стороны в одном направлении, одновременно продвигая с другой стороны другую актиновую нить в противоположном направлении. Такая организация позволяет гладкомышечным клеткам сокращаться с укорочением до 80% их длины вместо укорочения менее чем на 30%, характерного для скелетной мышцы.
Большинство скелетных мышц сокращаются и расслабляются быстро, но сокращения гладких мышц в основном являются длительными тоническими сокращениями, которые иногда продолжаются в течение нескольких часов или даже дней. Следовательно, можно ожидать, что морфологические и химические особенности гладких мышц должны отличаться от соответствующих характеристик скелетных мышц. Далее обсуждаются некоторые из этих отличий.
Медленная циклическая активность миозиновых поперечных мостиков. В гладкой мышце по сравнению соскелетной гораздо меньше скорость циклической активности миозиновых поперечных мостиков, т.е. скорость их прикрепления к актину, отсоединение от актина и повторное прикрепление для осуществления следующего цикла. Фактически частота циклов составляет лишь от 1/10 до 1/300 этого показателя в скелетной мышце. Однако, как считают, в гладкой мышце значительно больше относительное количество времени, в течение которого поперечные мостики остаются прикрепленными к актиновым нитям, что является главным фактором, определяющим силу сокращения. Возможной причиной медленного циклирования является гораздо меньшая по сравнению со скелетной мышцей АТФ-азная активность головок поперечных мостиков, в связи с чем скорость разрушения АТФ — источника энергии для движения головок поперечных мостиков — значительно снижена с соответствующим замедлением скорости их циклов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Какой ион играет основную роль в мышечном сокращении
Выделяют несколько последовательных этапов запуска и осуществления мышечного сокращения.
1. Потенциал действия распространяется вдоль двигательного нервного волокна до его окончаний на мышечных волокнах.
2. Каждое нервное окончание секретирует небольшое количество нейромедиатора ацетилхолина.
3. Ацетилхолин действует на ограниченную область мембраны мышечного волокна, открывая многочисленные управляемые ацетилхолином каналы, проходящие сквозь белковые молекулы, встроенные в мембрану.
4. Открытие управляемых ацетилхолином каналов позволяет большому количеству ионов натрия диффундировать внутрь мышечного волокна, что ведет к возникновению на мембране потенциала действия.
5. Потенциал действия проводится вдоль мембраны мышечного волокна так же, как и по мембране нервного волокна.
6. Потенциал действия деполяризует мышечную мембрану, и большая часть возникающего при этом электричества течет через центр мышечного волокна. Это ведет к выделению из саркоплазматического ретикулума большого количества ионов кальция, которые в нем хранятся.
7. Ионы кальция инициируют силы сцепления между актиновыми и миозиновыми нитями, вызывающие скольжение их относительно друг друга, что и составляет основу процесса сокращения мыщц.
8. Спустя долю секунды с помощью кальциевого насоса в мембране саркоплазматического ретикулума ионы кальция закачиваются обратно и сохраняются в ретикулуме до прихода нового потенциала действия. Удаление ионов кальция от миофибрилл ведет к прекращению мышечного сокращения.
Далее мы обсудим молекулярные механизмы этого процесса.
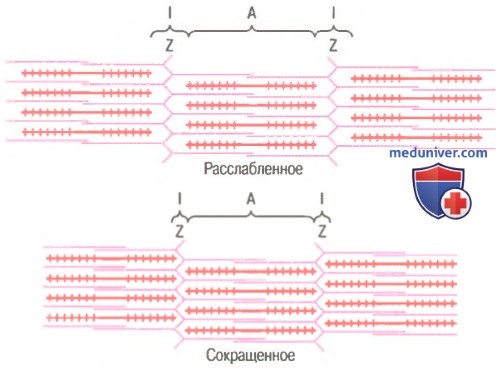
Молекулярные механизмы мышечного сокращения
Механизм скольжения нитей для мышечного сокращения. На рисунке показан основной механизм мышечного сокращения. Показано расслабленное состояние саркомера (вверху) и сокращенное состояние (внизу). В расслабленном состоянии концы актиновых нитей, отходящие от двух последовательных Z-дисков, лишь незначительно перекрываются. Наоборот, в сокращенном состоянии актиновые нити втягиваются внутрь между миозиновыми так сильно, что их концы максимально перекрывают друг друга. При этом Z-диски притягиваются актиновыми нитями к концам миозиновых. Таким образом, мышечное сокращение осуществляется путем механизма скольжения нитей.
Что заставляет нити актина скользить внутрь среди нитей миозина? Это связано с действием сил, генерируемых при взаимодействии поперечных мостиков, исходящих от нитей миозина, с нитями актина. В условиях покоя эти силы не проявляются, однако распространение потенциала действия вдоль мышечного волокна приводит к выделению из саркоплазматическо-го ретикулума большого количества ионов кальция, которые быстро окружают миофи-бриллы. В свою очередь, ионы кальция активируют силы взаимодействия между нитями актина и миозина, в результате начинается сокращение. Для осуществления процесса сокращения необходима энергия. Ее источником являются высокоэнергетические связи молекулы АТФ, которая разрушается до АДФ с высвобождением энергии. В следующих разделах мы приведем известные детали молекулярных процессов сокращения.
Молекулярные особенности сократительных нитей
Миозиновая нить. Она состоит из множества молекул миозина, молекулярная масса каждой составляет около 480000. На рисунке показана отдельная молекула; и также — объединение многих молекул миозина в миозиновую нить, а также взаимодействие одной стороны этой нити с концами двух актиновых нитей.
В состав молекулы миозина входят 6 полипептидных цепей: 2 тяжелые цепи с молекулярной массой около 200000 каждая и 4 легкие цепи с молекулярной массой около 20000 каждая. Две тяжелые цепи спирально закручиваются вокруг друг друга, формируя двойную спираль, которую называют миозиновым хвостом. С одного конца обе цепи изгибаются в противоположных направлениях, формируя глобулярную полипептидную структуру, называемую миозиновой головкой. Таким образом, на одном конце двойной спирали молекулы миозина образуются 2 свободные головки; 4 легкие цепи также включены в состав миозиновой головки (по 2 в каждой). Они помогают регулировать функцию головки во время мышечного сокращения.
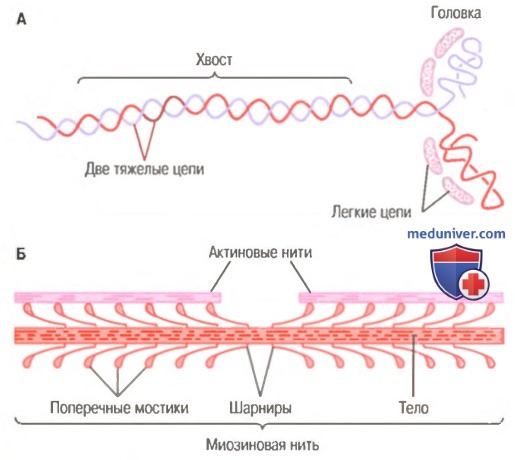
Б. Объединение многих молекул миозина в одну миозиновую нить.
Показаны также тысячи миозиновых поперечных мостиков и взаимодействие их головок с прилежащими актиновыми нитями.
Миозиновая нить состоит из 200 или более отдельных молекул миозина. Видно, что хвосты молекул миозина объединяются, формируя тело нити, а многочисленные головки молекул выдаются наружу по сторонам тела. Кроме того, наряду с головкой в сторону выступает часть хвоста каждой миозиновой молекулы, образуя плечОу которое выдвигает головку наружу от тела, как показано на рисунке. Выступающие плечи и головки вместе называют поперечными мостиками. Каждый поперечный мостик может сгибаться в двух точках, называемых шарнирами. Один из них расположен в месте, где плечо отходит от тела миозиновой нити, а другой — где головка крепится к плечу. Движение плеча позволяет головке или выдвигаться далеко наружу от тела миозиновой нити, или приближаться к телу. В свою очередь, повороты головки участвуют в процессе сокращения, что обсуждается в следующих разделах.
Общая длина каждой миозиновой нити остается постоянной и равна почти 1,6 мкм. В самом центре миозиновой нити на протяжении 0,2 мкм поперечных мостиков нет, поскольку снабженные шарнирами плечи отходят в стороны от центра.
Сама миозиновая нить сплетена таким образом, что каждая последующая пара поперечных мостиков смещена в продольном направлении относительно предыдущей на 120°, что обеспечивает распределение поперечных мостиков во всех направлениях вокруг нити.
АТФ-азная активность миозиновой головки. Есть и другая особенность миозиновой головки, необходимая для мышечного сокращения: миозиновая головка функционирует как фермент АТФ-аза. Как объясняется далее, это свойство позволяет головке расщеплять АТФ и использовать энергию расщепления высокоэнергетической связи для процесса сокращения.
Актиновая нить. Актиновая нить состоит из трех белковых компонентов: актина, тропомиозина и тропонина.
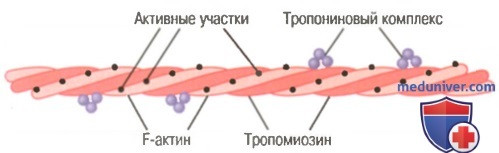
К одному концу каждой молекулы тропомиозина прикреплен тропониновый комплекс, который запускает сокращение.
Основой актиновой нити являются две цепи белковой молекулы F-актина. Обе цепи закручиваются в спираль так же, как и молекула миозина.
Каждая цепь двойной спирали F-актина состоит из полимеризованных молекул G-актина с молекулярной массой около 42000. К каждой молекуле G-актина прикреплена 1 молекула АДФ. Полагают, что эти молекулы АДФ являются активными участками на актиновых нитях, с которыми взаимодействуют поперечные мостики миозиновых нитей, обеспечивая мышечное сокращение. Активные участки на обеих цепях F-актина двойной спирали расположены со смещением таким образом, что вдоль всей поверхности актиновой нити встречается один активный участок примерно через каждые 2,7 нм.
Длина каждой актиновой нити — около 1 мкм. Основания актиновых нитей прочно встроены в Z-диски; концы этих нитей выступают в обоих направлениях, располагаясь в пространствах между миозиновыми молекулами.
Молекулы тропомиозина. Актиновая нить также содержит другой белок — тропомиозин. Каждая молекула тропомиозина имеет молекулярную массу 70000 и длину 40 нм. Эти молекулы спирально оплетают спираль из F-актина. В состоянии покоя молекулы тропомиозина располагаются поверх активных участков актиновых нитей, препятствуя их взаимодействию с миозиновыми нитями, лежащему в основе сокращения.
Тропонин и его роль в мышечном сокращении. По ходу молекул тропомиозина к ним периодически прикреплены другие белковые молекулы, называемые тропонином. Они представляют собой комплексы трех слабосвязанных белковых субъединиц, каждая из которых играет специфическую роль в регуляции мышечного сокращения. Одна из субъединиц (тропонин I) имеет высокое сродство к актину, другая (тропонин Т) — к тропомиозину, третья (тропонин С) — к ионам кальция. Считают, что этот комплекс прикрепляет тропомиозин к актину. Высокое сродство тропонина к ионам кальция, как полагают, инициирует процесс сокращения, о чем говорится в следующей статье.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Какой ион играет основную роль в мышечном сокращении
Ионы Са2+ представляют собой вторичный мессенджер, принимающий участие в многочисленных процессах передачи сигнала в различных клетках. У высших организмов внутриклеточный Са2+ участвует в таких разнообразных процессах, как синаптическая передача, мышечное сокращение, секреция инсулина, оплодотворение и экспрессия генов. В данной статье мы рассмотрим вопросы регуляции мышечного сокращения и сердечного ритма ионами Са2+.
В начале процесса сопряжения возбуждения и сокращения ионы Са2+ начинают поступать в цитозоль, а по мере возвращения клетки в состояние покоя выходят оттуда. Такое увеличение и снижение концентрации Са2+ в цитозоле представляют собой фазный момент в процессе сопряжения возбуждения и сокращения. Для его протекания необходимо участие нескольких типов Са2+-транспортных белков.
В клетках сердечной мышцы процесс возбуждения и сокращения подразделяется на четыре стадии.
На первой стадии, при деполяризации плазматической мембраны (сарколеммы) на ней генерируется электрический сигнал. При этом, благодаря входящему потенциалу действия, мембранный потенциал приобретает более положительное значение по сравнению с потенциалом покоя. Потенциал-зависимые Са2+-каналы (которые называются Cav1.2 Са2+-каналы) улавливают эти изменения мембранного потенциала и открываются (фаза 2 потенциала действия клеток миокарда). Небольшой поток ионов Са2+ начинает транспортироваться в клетку в направлении электрохимического градиента.
На второй стадии при поступлении Са2+ через Cav1.2 Са2+-каналы начинается высвобождение Са2+ из саркоплазматического ретикулума, в котором он депонирован в миллимолярных концентрациях. Выход Са2+ из саркоплазматического ретикулума происходит через особые каналы, называемые рианодиновые рецепторы (RyRs). В клетках сердечной мышцы этот процесс носит название Са2+-зависимый выход Са2+. Количество Са2+, выходящее в цитозоль из саркоплазматического ретикулума, в несколько раз превышает поступающее в цитозоль через сарколемму.
Са2+-зависимые Са2+-каналы саркоплазматического ретикулума клеток миокарда называются рианодиновыми рецепторами, поскольку они специфически связывают растительный алкалоид рианодин, блокирующий их действие. В различных клетках экспрессируются разные каналы внутриклеточного высвобождения Са2+, которые открываются в ответ на разнообразные сигналы, вызывающие мышечное сокращение. Основной вид каналов, высвобождающих Са2+ из саркоплазматического ретикулума клеток миокарда, относится к изоформе RyR2.
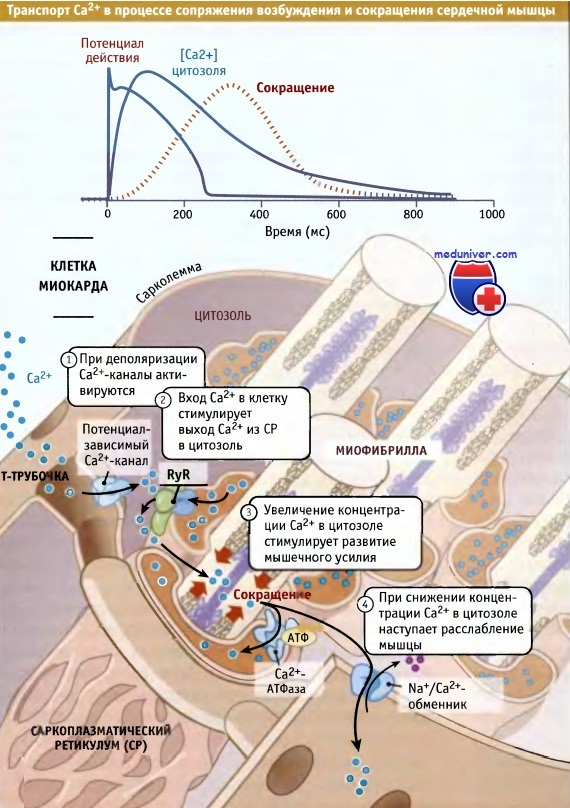
Это обеспечивается несколькими различными типами белков, транспортирующих Са2+.
На третьей стадии увеличение концентрации ионов Са2+ в цитозоле приводит к активации Са2+-зависимого белка тропонина С, который стимулирует сокращение мышечных волокон. Для эффективной активации всех внутриклеточных микрофиламентов и сокращения сердечной мышцы необходимо увеличение концентрации Са2+ в цитозоле со 100 нМ до 1,0 мкМ.
На четвертой стадии, когда Са2+ вытесняется из цитозоля, наступает расслабление мышцы. Вытеснение Са2+ происходит по нескольким механизмам. Основной из них — мобилизация Са2+ обратно в депо саркоплазматического ретикулума с помощью Са2+-АТФазы. Этот фермент осуществляет функцию насоса и направляет обратно в депо Са2+, который высвободился из саркоплазматического ретикулума при участии RyRs. Наряду с этим, Са2+ удаляется из цитозоля при участии таких Са2+- транспортных белков, как Na+/Са2+-обменник плазматической мембраны.
Этот обменник выводит из цитозоля небольшую часть Са2+, поступившего через потенциал-зависимые Cav1.2 Са2+-каналы. Немного Са2+ также обменивается между цитозолем и митохондриями.
В общем, за небольшими исключениями, процессы возбуждения и сокращения в скелетных и сердечной мышцах сходны. В отличие от клеток миокарда, потенциал-зависимые Са2+-каналы плазматической мембраны скелетных мышц представлены другой изоформой и стимулируют выход Са2+ из саркоплазматического ретикулума при физическом взаимодействии с изоформой рианодинового рецептора — RyRl. Наряду с этим, активация скелетных мышц может постепенно нарастать за счет вовлечения в процесс все большего количества мышечных волокон, что приводит к увеличению силы сокращения.
Таким образом, активация скелетных мышц может варьировать от коротких одиночных до повторяющихся тетанических сокращений и в конце концов ограничивается степенью мышечной усталости.
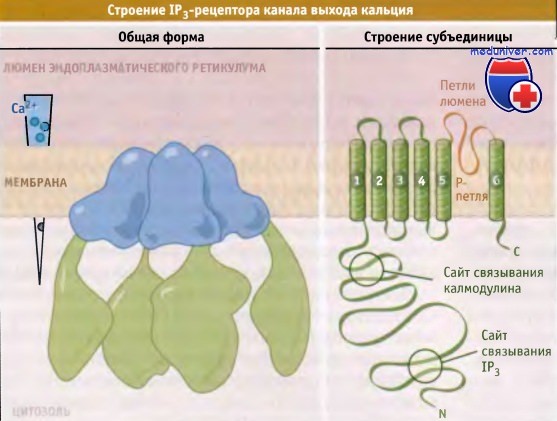
Слева показан Са2+-градиент, создающийся по сторонам мембраны эндоплазматического ретикулума в покоящихся клетках животных.
Каналы высвобождения внутриклеточного Са2+ относятся к числу уникальных ионных каналов. Они подразделяются на две группы: RyRs включаются и выключают ся под действием Са2+ или при прямом взаимодействии с Са2+-каналами плазматической мембраны, и близкие к ним рецепторы инозитол-1,4,5-трифосфата (IP3Rs), которые регулируются IР3. Четыре RyR или IP3R субъединицы собираются в симметрично организованный комплекс, образующий канал. Оба типа каналов состоят из двух доменов: порового и большого цитоплазматического, снабженного воротным механизмом. Предполагается, что канал IP3Rs имеет шесть трансмембранных сегментов и одну поровую петлю на субъединицу. Близкая структура постулируется и для RyRs.
Са2+-каналы RyR представляют собой самые большие из известных ионных каналов. Структура их доменной организации получена при трехмерном моделировании с использованием данных электронно-микроскопических исследований. Эти каналы в 10 раз больше, чем Na+-, Са2+- или К+-каналы. Каждая субъединица RyR состоит примерно из 5000 остатков аминокислот, почти вдвое превышая размер частично гомологичной IP3R субъединицы. Величина поровых доменов RyRs и IP3Rs примерно такая же, как для К+-каналов. Большие цитоплазматические домены RyRs и IP3Rs контролируют открытие-закрытие каналов с помощью Са2+ и IР3, подобно тому, как это имеет место в лиганд-зависимых К+-каналах.
Мутации, нарушающие процессы открывания-закрывания каналов внутриклеточного высвобождения Са2+, приводят к развитию различных заболеваний. Например, миссенс-мутации в гене, кодирующем белок RyR2, связаны с двумя генетическими формами аритмии и внезапной смерти при физической нагрузке. Мутантная форма RyR Са2+-канала обладает пониженным сродством к калстабину 2 (который также называется FKBP12.6). Калстабин2 представляет собой субъединицу Са2+-канала, которая стабилизирует закрытое состояние RyR миокарда, предотвращая его аберрантную активацию.
В результате мутации в белке RyR в фазе покоя или диастолы сердца, из саркоплазматического ретикулума начинается усиленный выход ионов Са2+. Более того, разрегулирование RyR2 при болезнях сердца увеличивает вероятность ухудшения сердечной функции и наступления внезапной смерти. К общему механизму, вероятно, относится внутриклеточная утечка Са2+, которая за счет аберрантной деполяризации мембраны может вызвать угрожающую аритмию.
Мутации в гене, кодирующем RyR-изоформу клеток скелетных мышц, также приводят к аберрантному выходу внутриклеточного кальция, что служит причиной заболевания, известного под названием злокачественная гипертермия. Больные крайне чувствительны к неконтролируемому внутриклеточному выходу Са2+, при этом у них поднимается температура и отмечается генерализованная мышечная контрактура. При применении в ингаляциях некоторых анестетиков и мышечных релаксантов у больных могут наступить серьезные нарушения метаболических процессов, представляющие угрозу для жизни.
Мутации в гене, кодирующем белок потенциал-зависимых Са2+-каналов плазматических мембран скелетных мышц, который физически взаимодействует с RyRs и активирует его, также обеспечивают восприимчивость к развитию злокачественной гипертермии.
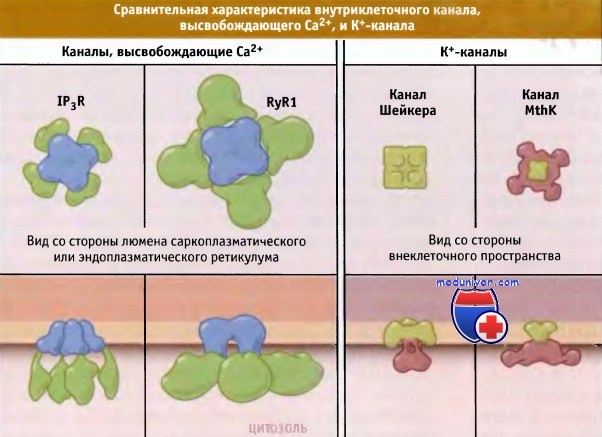
IР3-рецептор (IP3R) и рианодиновый рецептор (RyR), и два К+-канала: потенциал-зависимый канал Шейкера и Са2+-зависимый канал MthK различаются по размерам.
Поровые домены обозначены голубым и желтым цветом соответственно.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Какой ион играет основную роль в мышечном сокращении
Выделение ионов кальция из саркоплазматического ретикулума. Одним из специфических свойств саркоплазматического ретикулума является наличие внутри его везикулярных трубочек с высокой концентрацией ионов кальция, множество которых выделяются из каждой везикулы при возникновении потенциала действия в прилежащей Т-трубочке.
На рисунке показано, что потенциал действия Т-трубочки ведет к появлению местных токов, проникающих внутрь цистерн саркоплазматического ретикулума в местах их примыкания к Т-трубочке. Это, в свою очередь, ведет к быстрому открытию большого числа кальциевых каналов в мембранах цистерн и прикрепленных к ним продольных трубочек. Каналы остаются открытыми несколько миллисекунд, в течение которых в саркоплазму, окружающую миофибриллы, выделяется достаточное количество ионов кальция, запускающих сокращение.
Кальциевый насос для удаления ионов кальция из миофибриллярной жидкости после сокращения. После того, как ионы кальция выделились из саркоплазматических трубочек и диффундировали в пространство между миофибриллами, мышечное сокращение продолжается до тех пор, пока сохраняется высокая концентрация ионов кальция. Однако постоянно активный кальциевый насос, расположенный в стенках саркоплазматического ретикулума, удаляет ионы кальция из миофибрилл назад в систему продольных трубочек ретикулума. Этот насос может увеличивать концентрацию ионов кальция внутри трубочек примерно в 10000 раз. Кроме того, внутри ретикулума есть белок кальсеквестрину способный дополнительно связывать в 40 раз больше кальция.
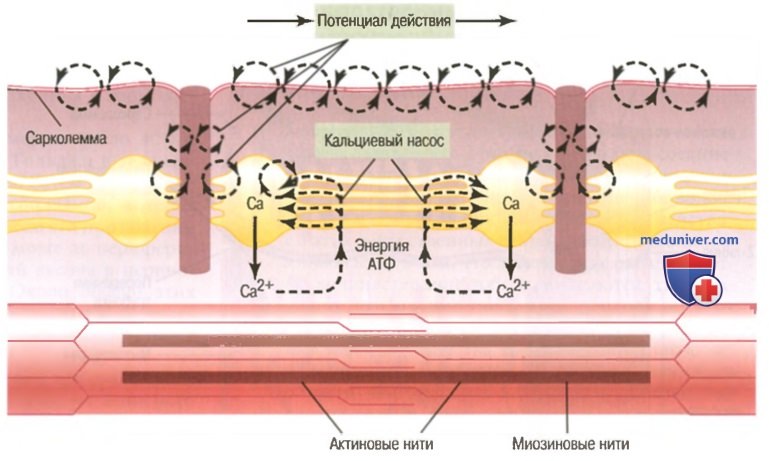
Во время кальциевого выброса происходит мышечное сокращение. Для непрерывного сокращения в течение длительного периода времени необходима серия выбросов кальция, происходящих под действием непрерывной серии повторных потенциалов действия.
Теперь обратимся к гладким мышцам, которые состоят из гораздо более мелких волокон, диаметром обычно от 1 до 5 мкм и длиной лишь 20-500 мкм. Волокна скелетных мышц примерно в 30 раз больше в диаметре и в сотни раз длиннее. Многие из основных принципов сокращения применимы как к скелетным, так и к гладким мышцам. Особенно важно, что, по существу, и в скелетных и гладких мышцах сокращение вызывают одни и те же силы притяжения между миозиновыми и актиновыми нитями, но внутренняя анатомическая структура гладкомышечных волокон иная.
Типы гладких мышц
Гладкие мышцы каждого органа отличаются от гладких мышц большинства других органов по нескольким признакам: (1) общим размером; (2) организацией в пучки или пласты; (3) реакцией на разные типы стимулов; (4) особенностями иннервации; (5) функцией. С целью упрощения гладкие мышцы можно в целом разделить на два основных типа: мультиунитарные и унитарные.
Мультиунитарные гладкие мышцы. Мышцы этого типа состоят из отдельных изолированных гладкомышечных волокон. Каждое волокно функционирует независимо от других и часто иннервируется одиночным нервным окончанием, что характерно для скелетномышечных волокон. Более того, наружные поверхности этих волокон, как и волокон скелетных мышц, покрыты тонким слоем подобного основной мембране вещества, представляющего собой мелкодисперсную смесь коллагена и гликопротеинов, помогающих изолировать отдельные волокна друг от друга.

Самая важная особенность мультиунитарных мышечных волокон: каждое из них может сокращаться независимо от других, а регуляция осуществляется главным образом нервными сигналами. И наоборот, большая доля управления унитарной гладкой мышцей осуществляется не нервными сигналами. Примером мультиунитарных гладких мышц могут служить ресничная мышца, мышца радужной оболочки глаза и мышцы, поднимающие волосы при стимуляции симпатической нервной системы.
Унитарные гладкие мышцы. Термин «унитарный» подразумевает массу из сотен и тысяч гладкомышечных волокон, которые сокращаются вместе как единое целое. Волокна обычно организованы в пласты или пучки, и их клеточные мембраны плотно прилежат друг к другу во множестве точек, поэтому сила, развиваемая одним мышечным волокном, может передаваться следующему.
Кроме того, клеточные мембраны соединяются многочисленными щелевыми контактами, через которые ионы могут свободно перетекать из одной мышечной клетки в другую, и потенциалы действия (или просто ионный ток, без потенциалов действия) могут распространяться от одного волокна к следующему, способствуя одновременному сокращению мышечных волокон. Эти гладкие мышцы также называют синцитиальными гладкими мышцами из-за синцитиальных взаимосвязей между волокнами, или висцеральными гладкими мышцами, поскольку они обнаруживаются в стенках большинства внутренних органов тела, включая кишечник, желчные пути, мочеточники, матку и многие кровеносные сосуды.



