Какой иммуноглобулин выполняет защитную функцию слизистых оболочек
Антитела класса IgA, основной функцией которых является местная гуморальная защита слизистых оболочек.
Иммуноглобулины (антитела) класса А.
Синонимы английские
Immunoglobulin A; IgA, total, Serum.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Иммуноглобулины класса А – гликопротеины, которые синтезируются в основном плазматическими клетками слизистых оболочек в ответ на местное воздействие антигена.
В организме человека IgA существует в двух формах – сывороточной и секреторной. Время их полужизни – 6-7 суток. Секреторный IgA обладает димерной структурой и устойчив к воздействию ферментов благодаря особенностям строения. Секреторный IgA находится в слезах, поте, слюне, молоке и молозиве, секретах бронхов и желудочно-кишечного тракта и защищает слизистые оболочки от инфекционных агентов. 80-90 % циркулирующих в крови IgA состоят из сывороточной мономерной формы данного класса антител. IgA входят во фракцию гамма-глобулинов и составляют 10-15 % от всех иммуноглобулинов крови.
Антитела класса IgA являются важным фактором местной защиты слизистых оболочек. Они связываются с микроорганизмами и предотвращают их проникновение с внешних поверхностей вглубь тканей, усиливают фагоцитоз антигенов путем активации комплемента по альтернативному пути. Достаточный уровень IgA в организме препятствует развитию IgЕ-зависимых аллергических реакций. IgA не проникают через плаценту, но поступают в организм ребенка с молоком матери при кормлении.
Селективный дефицит IgA является одним из наиболее распространенных иммунодефицитов в популяции. Частота – 1 случай на 400-700 человек. Данная патология часто протекает бессимптомно. Дефицит IgA может проявиться аллергическими заболеваниями, рецидивирующими респираторными или желудочно-кишечными инфекциями, нередко ассоциируется с аутоиммунной патологией (сахарным диабетом, системной красной волчанкой, ревматоидным артритом, пернициозной анемией). Дефицит IgA иногда сочетается с недостаточным уровнем IgG-2 и IgG-4, что приводит к более выраженным клиническим признакам иммунодефицита.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Возраст
Референсные значения
Причины понижения уровня IgА в сыворотке и состояния, ассоциированные с дефицитом данного класса антител:
Что может влиять на результат?
Факторы, повышающие уровни иммуноглобулинов в крови:
Факторы, снижающие уровни IgA в крови:
Кто назначает исследование?
Иммунолог, инфекционист, гематолог, онколог, ревматолог.
Секреторные иммуноглобулины А – «главная скрипка» мукозального иммунитета
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке – sIgA назального секрета.
Доминирование секреторного иммуноглобулина А среди других антител в слизистой оболочке дыхательных путей и ротоглотки
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке – sIgA назального секрета. Помогают этим антителам в нейтрализации вирусов и бактерий секреторные IgM (sIgM), но их защитное значение существенно ниже.
Помимо sIgA и sIgM, в верхних отделах дыхательных путей и ротоглотке обнаруживаются в небольших количествах и все другие известные изотипы Ig. Появление IgG и мономерного («сывороточного») IgA в слюне и назальном секрете обусловлено транссудацией этих молекул из плазмы крови. При патологических (например, воспалительных) процессах увеличивается транссудация IgG, мономерного IgA и более крупных полимерных молекул IgM. В секретах слизистых оболочек дыхательных путей выявляют еще и IgD, который тоже участвует в противоинфекционном ответе.
Особенности выработки sIgA и sIgM
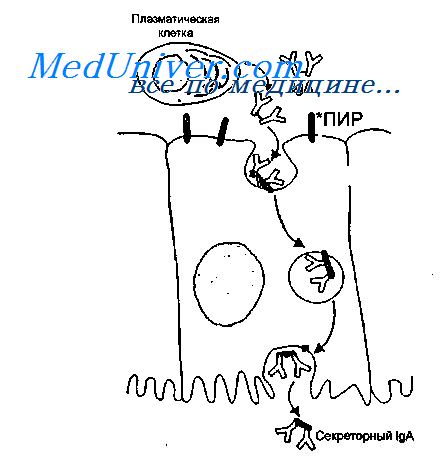
Вначале плазматические клетки слизистых оболочек синтезируют димерный IgA, в котором два мономера IgA соединены между собой J-цепью. После этого димерный IgA захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются транспорту к апикальной поверхности эпителиоцитов. Здесь происходит распад транспортирующего рецептора, в результате которого внеклеточная часть этого рецептора (так называемый «секреторный компонент») остается связанной с димерным IgA, который высвобождается в окружающую среду (слюну, слизь, другие биологические жидкости). Именно такой димерный IgA, связанный с секреторным компонентом, называют sIgA.
Как уже упоминалось, существуют еще и секреторный IgM (sIgM). Выработка sIgM напоминает таковую sIgA. Все начинается с синтеза плазматическими клетками в слизистой оболочке пентамерного IgM, который захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются трансэпителиальному транспорту. На апикальной поверхности эпителиоцитов пентамерный IgM вместе с секреторным компонентом высвобождается во внешнюю среду, превращаясь в sIgM.
Секреторные компоненты в составе sIgA и sIgM стабилизируют соответственно димерную или пентамерную структуру этих Ig и обеспечивают их длительное функционирование в биологических жидкостях.
Где происходит индукция выработки sIgA в слюне и назальном секрете?
Появление sIgA в слюне и назальном секрете происходит как следствие первичного контакта с антигенами патогенов в разных индуктивных зонах в верхних отделах респираторного и пищеварительного трактов. Главными индуктивными зонами при этом являются небные и носоглоточные миндалины, а также протоки слюнных (особенно малых, поднижечелюстных и подъязычных) желез, открытые для прямого воздействия антигенов. К индуктивным зонам относятся и другие участки слизистой оболочки полости рта, глотки, верхних и нижних дыхательных путей.
Все перечисленные индуктивные зоны доступны для стимулирующего действия топических бактериальных лизатов ИРС®19 и Имудон®.
Еще одной индуктивной зоной, антигенная стимуляция которой может привести к выработке антител в слюне и дыхательных путях, является лимфоидная ткань, ассоциированная с кишечником (Gut-Associated Lymphoid Tissue – GALT). Эта зона также доступна для действия топических бактериальных лизатов, компоненты которых неминуемо попадают в желудочно-кишечный тракт в результате проглатывания.
При раннем назначении топических бактериальных лизатов адаптивные антибактериальные механизмы (локальная продукция sIgA) включаются как раз тогда (4–5-е сутки), когда наиболее высок риск развития вторичной бактериальной инфекции.
Таким образом, ИРС®19 и Имудон® не только предотвращают развитие вторичных бактериальных осложнений вирусной инфекции, но и неспецифически усиливают противовирусную и антибактериальную защиту уже в первые часы терапевтического применения. Препараты обладают целым рядом фармакологических свойств, которые принципиально отличают их от иммуностимуляторов с системным действием, связанных со сложными маршрутами миграции иммунокомпетентных клеток. ИРС®19 и Имудон® действуют нацелено на стимуляцию противоинфекционной защиты в месте их первичного введения в организм т.е. во входных воротах для болезнетворных вирусов и бактерий и арене ключевых патогенетических событий.
Материал разработан при поддержке компании abbott в целях повышения осведомлённости пациентов о состоянии здоровья. информация в материале не заменяет консультацию специалиста здравоохранения.обратитесь к лечащему врачу.
Какой иммуноглобулин выполняет защитную функцию слизистых оболочек
Известно, что степень защиты от локальных вирусных инфекций респираторного и желудочно-кишечного трактов прежде всего зависит от содержания в организме специфического секреторного IgA, а не от наличия сывороточного IgG к энтеропатогенным или пневмотропным вирусам.
Стабильная структура, выраженный аффинитет к поверхности слизистых оболочек, преобладающее содержание в секрете молочной железы обусловливают биологическую роль секреторного IgA в защите организма от неблагоприятного воздействия различных патогенных агентов, в том числе вирусов.
IgA синтезируется в димерной форме в клетках lamina propria и после связывания с иммуноглобулиновым рецептором, синтезированным в эпителиальных клетках, транспортируется на поверхность слизистой оболочки. В момент выхода IgA в просвет кишечника рецептор частично расщепляется, в результате чего в составе IgA остается фрагмент рецептора, который называют секреторным компонентом.
Таким образом, секреторный IgA является продуктом кооперации двух типов клеток — плазматических и эпителиальных.
Секреторный IgA образуется не только в димерной, но и в тетрамерной форме, что усиливает его вируснейтрализующую способность. Секреторный компонент предохраняет IgA от расщепления протеолитическими ферментами, что обусловливает его значительные преимущества перед антителами других классов. Секреторный IgA нейтрализует вирус не только в просвете кишечника, но и при транспортировке его внутрь клетки. Димер IgA может нейтрализовать вирус в подслизистой оболочке кишечника, а затем, связавшись с рецептором, транспортировать его в просвет кишечника.
Димерные иммуноглобулины класса A (US IgA), соединенные посредством j-цепи в единую структуру с секреторным компонентом, представляют собой уникальный пример эволюционной адаптации иммуноглобулинов на слизистых покровах для эффективного функционирования в условиях постоянного воздействия антигенов различной природы.
Исходя из способности к локальному синтезу молекул секреторного компонента, а также димерной формы IgA-местно расположенными плазматическими клетками, ткани слизистых покровов можно разделить на три основных класса.
В слизистых оболочках индуктивная и продуктивная фазы гуморального иммунного ответа разобщены пространственно в большей степени, чем в других отделах иммунной системы.
Клеточные и гуморальные превращения, связанные с появлением IgA во внешних секретах, представлены на рисунке.
В молоко и, по-видимому, в другие внешние секреты молекулы IgA поступают из двух главных источников. Большая часть IgA, выделяемого со слюной, секретами слезной и молочной желез, а также пищеварительного и респираторного трактов, образуется плазматическими клетками. Однако IgA, обнаруживаемые в различных внешних секретах, могут иметь и системное происхождение. Продуцируясь клетками слизистых оболочек одних органов, они поступают в кровь и переносятся в слизистые покровы других органов.
Антиген после проникновения внутрь пейеровой бляшки активирует Т- и В-лимфоциты, которые по лимфатическому протоку поступают в мезентериальный лимфатический узел, а затем в кровь, селезенку, снова в кровь и селективно локализуются в лимфатических образованиях всех слизистых оболочек и экзокринных секреторных железах — молочных, слюнных и слезных. При этом Т-лимфоциты локализуются преимущественно между эпителиальными клетками слизистой оболочки, обеспечивая клеточный иммунный ответ, а В-лимфоциты — в lamina propria, где они дифференцируются в плазматические клетки и синтезируют IgA.
Около 90% плазматических клеток в lamina propria продуцируют IgA, в то время как в лимфатических узлах доля таких клеток составляет всего 2—5%.
Уникальна в этом отношении роль печени. Имеются убедительные данные, свидетельствующие о том, что гепатоциты избирательно связывают и в последующем транспортируют IgA в желчь, тем самым усиливая систему секреторного IgA кишечника.
Иммуноглобулины A (IgA)
Синонимы : Immunoglobulin A
Мы сократили затраты на рекламу и содержание точек забора биоматериала. Поэтому цена на анализы для вас в 2 раза ниже. Мы сделали это, чтобы вы сдавали анализы легко и управляли своим здоровьем
Срок исполнения
Анализ будет готов в течение 1 дня, исключая день забора. Срок может быть увеличен на 1 день в случае необходимости. Вы получите результаты на эл. почту сразу по готовности.
Срок исполнения: 2 дня, исключая субботу и воскресенье (кроме дня взятия биоматериала)
Подготовка к анализу
Обсудите с врачом прием лекарственных препаратов накануне и в день проведения исследования крови, а также другие дополнительные условия подготовки.
Не сдавайте анализ крови сразу после рентгенографии, флюорографии, УЗИ, физиопроцедур.
За 24 часа до взятия крови:
Не менее 8 часов до сдачи крови не принимайте пищу, пейте только чистую негазированную воду.
Перед забором крови
Информация об анализе
Иммуноглобулины A (IgA) присутствуют в сыворотке здорового человека как в виде секреторного IgA, так и в виде сывороточного IgA. Основными функциями секреторного IgA являются связывание микроорганизмов на поверхности слизистых оболочек, активация воспалительных реакций и активация альтернативного пути комплемента. Особо важную роль он играет в защите от инфекций респираторной, желудочно-кишечного тракта и мочеполовой систем.
Метод исследования — Иммунотурбидиметрия
Материал для исследования — Сыворотка крови
Состав и результаты
Иммуноглобулины A (IgA)
Иммуноглобулины A (IgA) присутствуют в сыворотке здорового человека как в виде секреторного IgA, так и в виде сывороточного IgA. Специфическая роль сывороточного IgA не ясна в отличие от IgA секреторного. IgA не обнаруживается в крови плода, т.к. не проходит через плаценту. Секреторный IgA имеет секреторный компонент и состоит из димера, соединенного J-цепью, защищающий молекулу от протеолитических ферментов. Секреторный IgA является основным секреторным иммуноглобулином, содержащимся в секретах организма, таких как слезы, слюна, молозиво, выделения из носа, секрет желудочно-кишечного тракта и трахеобронхиальная слизь. Основными функциями секреторного IgA являются связывание микроорганизмов на поверхности слизистых оболочек, активация воспалительных реакций и активация альтернативного пути комплемента. Особо важную роль он играет в защите от инфекций респираторной, желудочно-кишечного тракта и мочеполовой систем.
Изменение концентрации иммуноглобулина в сыворотке можно классифицировать следующим образом:
Интерпретация результатов исследования «Иммуноглобулины A (IgA)»
Интерпретация результатов анализов носит информационный характер, не является диагнозом и не заменяет консультации врача. Референсные значения могут отличаться от указанных в зависимости от используемого оборудования, актуальные значения будут указаны на бланке результатов.
Какой иммуноглобулин выполняет защитную функцию слизистых оболочек
Автор: Зеленов Петр Васильевич
Дыхательный тракт человека – это входные ворота для веществ, загрязняющих окружающую среду, и возбудителей различных болезней, поэтому состояние иммунной защиты в этом органе должно быть решающим фактором в элиминации неблагоприятного компонента при вдыхании. Состояние местного иммунитета слизистой оболочки зависит от ее целостности, содержания иммуноглобулинов А, G и М, состояния лимфоидной ткани [Иванов В.Д. с соавт., 2006].
Защищает организм человека от проникновения инфекции слизистая оболочка верхних дыхательных путей. Она обладает весьма совершенными и сложно организованными механизмами защиты от неблагоприятного внешнего воздействия [Рязанцев С.В. с соавт., 2000]. Среди этих механизмов ведущими являются мукоцилиарный барьер и иммунная защита. Дыхательные рефлексы, такие как кашель, чиханье и бронхоконстрикция, а также мукоцилиарный клиренс препятствуют адгезии и обеспечивают удаление микроорганизмов и инородных частиц с поверхности респираторного эпителия. Важным защитным фактором является секретируемая бокаловидными клетками и эпителиоцитами слизь, в состав которой входят обладающие антибактериальной активностью лизоцим, лактоферрин, cекреторный иммуноглобулин А (sIgA) [Лучихин Л.А., 2003].
Если возбудителю удается преодолеть мукоцилиарный барьер, срабатывают неспецифические механизмы защиты – нейтрофилы и макрофаги, мигрирующие из кровеносного русла и способные уничтожать микроорганизмы путем фагоцитоза, за счет секреторной дегрануляции, продукции активных форм кислорода и оксида азота. В противовирусных реакциях принимают участие также естественные клетки-киллеры, располагающиеся в подслизистом слое и тесно связанные с внутриэпителиальными лимфоидными фолликулами. Наконец, иммунная защита слизистой оболочки обеспечивается многими гуморальными и клеточными факторами, среди которых наиболее важную роль играет синтезируемый в ответ на воздействие специфических антигенов sIgA [Лучихин Л.А., 2003].
В дальнейшем, при продолжении контакта с неблагоприятными факторами, развивается состояние нарушения процесса адаптации (донозологическое), которое характеризуется преобладанием неспецифических изменений над специфическими. В случае дальнейшего развития патологических процессов наступает состояние срыва адаптации и развитие клинических симптомов болезни. При этом наступает повреждение внутриклеточных структур, нарушаются межклеточные кооперативные связи, развиваются аутоиммунные реакции, иммунодепрессия, формируется сенсибилизация организма, накапливаются токсичные метаболиты [Иванов В.Д. с соавт., 2006, Хаитов Р.М. с соавт., 1995].
Последние исследования показали, что уровень sIgA может иметь и прогностическую значимость в оценке состояния здоровья населения при массовых обследованиях [Иванов В.Д. с соавт., 2006]. Так установлено, что снижение sIg А может указывать на недостаточность функции местного иммунитета, а его повышенное количество – на дисбаланс в иммунной системе [Маковецкая А.К. с соавт., 2005].
В ряде исследований показано, что при снижение местного иммунитета, и в частности sIgA, возможно приводит к хронической патологии. Например, в исследовании Calvo M. с соавт. (1990) показано, что у здоровых детей, имеющих нормальный уровень sIgA, риск развития хронической легочной патологии, в том числе и бронхиальной астмы, составляет 46%, а при низком уровне sIgA повышается до 86%. В исследовании Бяховой М.М. (2008) показано, что у здоровых детей с низким sIgA повышается уровень цитогенетических показателей буккального эпителия на фоне снижения апоптического индекса, т.е. нарушается процесс удаления генетически не полноценных эпителиальных клеток.
sIgA может изменяться и при различных патологических состояниях бронхолегочной системы, и в частности при бронхиальной астме. Так известно, что у детей с этим заболеванием отмечаются различные изменения иммунной системы, сопровождающимися склонностью к частым вирусным и бактериальным инфекциям. Развитию бронхиальной астмы у детей способствуют перенесенные ранее ребенком острые респираторные инфекции, бронхиты, пневмонии. У половины детей с бронхиальной астмой первый приступ затрудненного дыхания часто возникает на фоне ОРЗ или в период реконвалесценции после него. У часто болеющих детей с этим заболеванием отмечается снижение sIgA в секрете ротоглотки [Рылеева И.В., 2003]. Так же в работе Кузьменко Л.Г. и соавторов (1999) показано, что у детей, больных бронхиальной астмой с частыми обострениями, вызываемыми вирусной инфекцией, sIgA в слюне ниже, чем у здоровых. Скорей всего, низкий уровень этого иммуноглобулина может быть связан с угнетающим действием вирусов на его синтез или истощением его продукции при чрезвычайно высокой потребности в условиях частого возникновения вирусных инфекций.
Подводя итог, можно сказать, что sIgA играет не мало важную роль в защите организма от различных факторов окружающей среды, а кроме того он имеет прогностическое значение в массовых исследованиях.
2. Бяхова М.М Цитогенетический статус, показатели пролиферации и апоптоза у детей с бронхиальной астмой, проживающих в условиях загрязнения атмосферного воздуха. Автореферат на соискание ученой степени кандидата медицинских наук. – Москва. – 2008. – 22 с.
3. Зайцева О.В. Противовоспалительная терапия в лечении заболеваний органов дыхания. // Consilium provisorum. – Том 5, №6. – 2005.
4. Иванов В.Д., Маковецкая А.К. Возможности использования неинвазивных иммунологических методов в оценке здоровья населения. // Неинвазивные методы в оценке здоровья населения. Под ред. Академика РАМН Ю.А. Рахманина. – М. – 2006. – С. 112-125.
5. Кузьменко Л.Г., Баталова Т.Н., Сойджодах Р. И др. Содержание иммуноглобулинов в слюне детей с хроническим тонзиллитом и бронхиальной астмой. // Вестник РУДН Серия «Медицина». – 1999. – №2. – С. 73-79.
7. Лучихин Л.А. Рациональные подходы к лечению и профилактики респираторных инфекций // Consilium Medicum. – 2003. – Том. 5, № 2.
8. Маковецкая А.К., Высоцкая О.В., Иванов В.Д. Изучение состояния местного иммунитета слизистых оболочек дыхательного тракта у лиц с аллергической патологией.//Материалы пленума «Экологически обусловленные ущербы здоровью: методология, значение и перспективы оценки. – Москва. – 22-23 декабря 2005г. – С.436-438.
9. Методические рекомендации. – Оценка состояния здоровья и выявления предпатологических состояний у детей. – М. – 1999. – 36 с.
14. Рылеева И.В., Балаболкин И.И. Бактериальные иммуномодуляторы ИРС19 и Имудон в педиатрической практике. // Вопросы современной педиатрии. – 2003. – Т. 2, №2. – С 78-81.
16. Хаитов Р.М., Пинегин Б.В., Истамов Х.И. Экологическая иммунология. – М.: Издательство ВНИРО. – 1995.
17. Balzar S., Strand M., Nakano T. et al. Subtle immunodeficiency in severe asthma: IgA and IgG2 correlate with lung function and symptoms. // Int. Arch. Allergy Immunol. – 2006. – Vol. 104,№2. – P. 96-102.
18. Calvo M., Grob K., Bertoglio J et al. Secretory IgA deficiency in pediatric patients: clinical and laboratory follow-up. // Allergol Immunopathol (Madr.) – 1990. – Vol. 18,№3. – P. 149-153.
20. Eccles R Rhinitis as a mechanism of respiratory defence. Eur Arch Otorhinolaryng 1995; 252: Suppl 1: 2-7.
21. Handzel Z.T. effects of environmental pollutants on airways, allergic inflammation, and the immune response. // Rev Environ Health. – 2000. – Vol. 15, №3. – P. 325-336.
22. Peebles RS Jr., Liu MC, Lichtenstein L.M. et al. IgA, IgG and IgM quantification in bronchoalveolar lavage fluids from allergic rhinitics, allergic asthmatics, and normal subjects by monoclonal antibody-based immunoenzymetric assays. // J Immunol Methods. – 1995. – Vol 179, № 1. – P. 77-86.
23. Richter J., Pelech L. Immunological findings in groups of children after compensatory measures. // Toxicol Lett. – 1996. – Vol. 88, № 1-3. – P. 165-168.
24. Salvi S., Holgate S.T. Could the airway epithelium play an important role in mucosal immunoglobulin A production? // Clin. Exp. Allergy. – 1999. – Vol. 29, №12. P. 1597-1605.
25. V.H.J. van der Velden, Savelkoul H.F.J., Versnel M.A. Bronchial epithelium: morphology, function, and pathophysiology in asthma. // Eur. Cytokine Netw. – Vol. 9,№4. – P. 585-597.
26. Wines B.D., Hogarth P.M. IgA receptors in health and disease. // Tissue Antigens. – 2006. – Vol. 68,№2. – P. 103-114.
27. Wilson R, Dowling RB, Jackson AD. The biology of bacterial colonization and invasion of the respiratory mucosa. Eur Respir J 1996; 30: 289-9.