Активность антибактериальных средств in vitro
Грамотрицательные неферментирующие микроорганизмы широко распространены в окружающей среде. Одной из серьезных проблем является диагностика вызванных ими инфекций, связанная с объективными трудностями их выделения и идентификации. Второй проблемой является то, что для них характерна полирезистентность к антимикробным препаратам, включая те, которые обычно активны против Pseudomonas aeruginosa.
В данном исследовании определялась антибактериальная активность in vitro различных препаратов по отношению к 177 выделенным в клинике штаммам неферментирующих бактерий (кроме Pseudomonas aeruginosa и Acinetobacter spp.). МПК определялась методом разведений в агаре. Использовали среду Мюллера-Хинтона. Оценивали активность ампициллина, пиперациллина, пиперациллин/тазобактама, сульбактама, цефоперазона, цефоперазон/сульбактама, цефтазидима, цефепима, азтреонама, имипенема, меропенема, колистина, гентамицина, амикацина, триметоприм/сульфаметоксазола, хлорамфеникола, эритромицина, рифампицина, норфлоксацина, ципрофлоксацина и миноциклина.
У 7 изолятов: Sphingobacterium multivorum(2), Sphingobacterium spiritivorum(1), Empedobacter brevis(1), Weeksella virosa(1), Bergeyella zoohelcum(1) и Oligella urethralis (1), вместо чувствительности к цефоперазону или сульбактаму определяли чувствительность к амоксициллин/клавуланату и ампициллин/сульбактаму.
Полирезистентность к антибактериальным препаратам была характерна для таких возбудителей, как Stenotrophomonas maltophilia, Burkholderia cepacia, Chryseobacterium spp., Myroides spp., Achromobacter xylosoxidans и Ochrobactrum anthropi.
В то же время, такие микроорганизмы, как Pseudomonas stutzeri, Shewanella putrefaciens-algae, Sphingomonas paucimobilis, Pseudomonas oryzihabitans, Bergeyella zoohelcum, Weeksella virosa и Oligella urethralis часто были чувствительны к большинству из тестируемых антибиотиков.
Учитывая, что различные виды возбудителей, образующих группу грамотрицательных неферментирующих микроорганизмов, демонстрируют различные показатели антибиотикорезистентности, для выбора оптимальной схемы лечения требуется проведение микробиологического исследования с идентификацией возбудителя и выявления показателей его антибиотикорезистентности. Феномен полирезистентности, характерный для ряда возбудителей, требует активной разработки новых антибактериальных средств или поиска новых комбинаций антибиотиков, обладающих синергизмом бактерицидного действия по отношению к данным микроорганизмам.
«In vitro» activity of different antimicrobial agents on Gram-negative nonfermentative bacilli, excluding Pseudomonas aeruginosa and Acinetobacter spp. (Vay C.A., Almuzara M.N., Rodriguez C.H., Pugliese M.L., Lorenzo Barba F., Mattera J.C., Famiglietti A.M. Rev. Argent Microbiol., 2005;37(1):34-45).
Код вставки на сайт
Активность антибактериальных средств in vitro
Грамотрицательные неферментирующие микроорганизмы широко распространены в окружающей среде. Одной из серьезных проблем является диагностика вызванных ими инфекций, связанная с объективными трудностями их выделения и идентификации. Второй проблемой является то, что для них характерна полирезистентность к антимикробным препаратам, включая те, которые обычно активны против Pseudomonas aeruginosa.
В данном исследовании определялась антибактериальная активность in vitro различных препаратов по отношению к 177 выделенным в клинике штаммам неферментирующих бактерий (кроме Pseudomonas aeruginosa и Acinetobacter spp.). МПК определялась методом разведений в агаре. Использовали среду Мюллера-Хинтона. Оценивали активность ампициллина, пиперациллина, пиперациллин/тазобактама, сульбактама, цефоперазона, цефоперазон/сульбактама, цефтазидима, цефепима, азтреонама, имипенема, меропенема, колистина, гентамицина, амикацина, триметоприм/сульфаметоксазола, хлорамфеникола, эритромицина, рифампицина, норфлоксацина, ципрофлоксацина и миноциклина.
У 7 изолятов: Sphingobacterium multivorum(2), Sphingobacterium spiritivorum(1), Empedobacter brevis(1), Weeksella virosa(1), Bergeyella zoohelcum(1) и Oligella urethralis (1), вместо чувствительности к цефоперазону или сульбактаму определяли чувствительность к амоксициллин/клавуланату и ампициллин/сульбактаму.
Полирезистентность к антибактериальным препаратам была характерна для таких возбудителей, как Stenotrophomonas maltophilia, Burkholderia cepacia, Chryseobacterium spp., Myroides spp., Achromobacter xylosoxidans и Ochrobactrum anthropi.
В то же время, такие микроорганизмы, как Pseudomonas stutzeri, Shewanella putrefaciens-algae, Sphingomonas paucimobilis, Pseudomonas oryzihabitans, Bergeyella zoohelcum, Weeksella virosa и Oligella urethralis часто были чувствительны к большинству из тестируемых антибиотиков.
Учитывая, что различные виды возбудителей, образующих группу грамотрицательных неферментирующих микроорганизмов, демонстрируют различные показатели антибиотикорезистентности, для выбора оптимальной схемы лечения требуется проведение микробиологического исследования с идентификацией возбудителя и выявления показателей его антибиотикорезистентности. Феномен полирезистентности, характерный для ряда возбудителей, требует активной разработки новых антибактериальных средств или поиска новых комбинаций антибиотиков, обладающих синергизмом бактерицидного действия по отношению к данным микроорганизмам.
In vitro и in vivo в медицине что такое
А.Н. Суворов (1), Н.В. Барышникова (1, 2), А.В. Сварваль (3), Р.М. Ниязов (4)
1) Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова Минздрава России, Санкт-Петербург, Россия; 2) Институт экспериментальной медицины, Санкт-Петербург, Россия; 3) Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера, Санкт-Петербург, Россия; 4) Клинический госпиталь ФКУЗ Медико-санитарная часть МВД России по г. Санкт-Петербургу и Ленинградской области, Санкт-Петербург, Россия
Введение
Возможным путем повышения эффективности эрадикации Helicobacter pylori и оптимизации лечения H. pylori-ассоциированных заболеваний является применение пробиотиков. Препараты с пробиотическим действием кроме коррекции дисбиотических изменений кишечной микрофлоры обеспечивают ряд дополнительных положительных эффектов, например иммунологических (улучшение показателей гуморального и клеточного иммунитета, снижение аллергизации организма), а также оказывают воздействие на H. pylori в желудке за счет прямого антагонистического влияния и стимуляции местной иммунологической защиты (укрепление слизистого защитного барьера и снижение выраженности воспаления слизистой оболочки желудка, выработка бактериоцинов) [1–3].
В ряде работ показано, что применение пробиотиков (на основе бифидобактерий, лактобацилл, культуры сенной палочки и др.) в отношении больных заболеваниями, ассоциированными с H. pylori, способствует улучшению состояния микрофлоры кишечника, снижению риска развития побочных эффектов антибактериальной терапии, в т.ч. антибиотикоассоциированной диареи, способствует наступлению более быстрой клинико-эндоскопической ремиссии заболевания и повышению эффективности эрадикации H. pylori [4–8].
В постулатах IV и V Маастрихтских консенсусов упоминается о возможной эффективности некоторых пробиотиков в качестве дополнения к стандартной эрадикационной терапии [9, 10].
Исследования, посвященные роли пробиотиков в эрадикации H. pylori, движутся по двум направлениям.
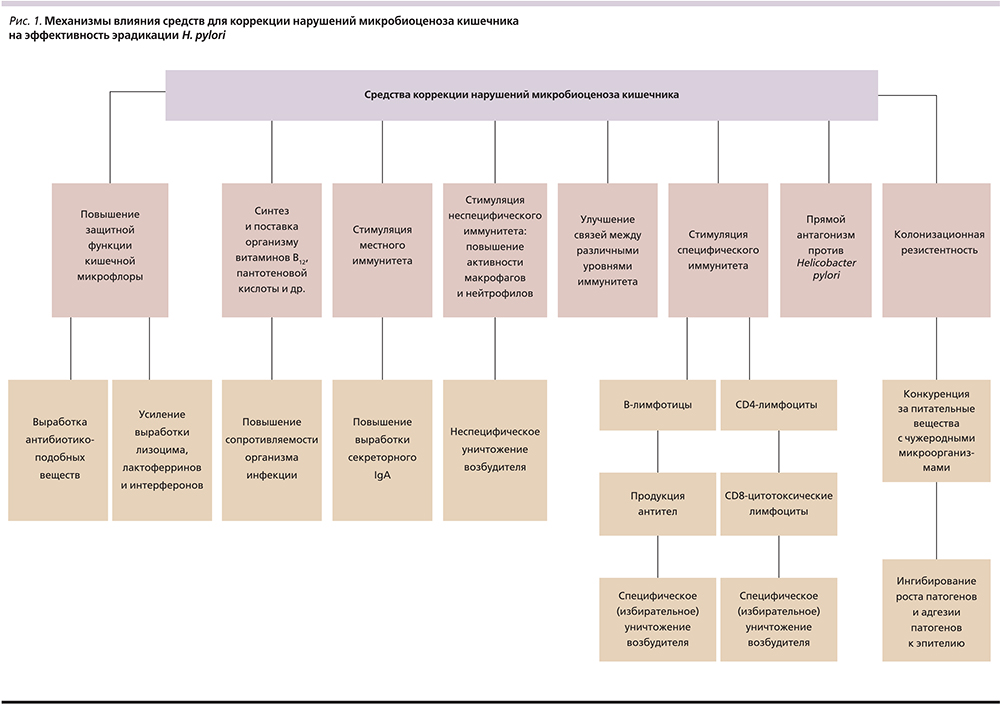
В первом случае пробиотики включают в состав стандартной эрадикационной терапии [11–13]. Второе направление изучает влияние монотерапии пробиотиками на эффективность антихеликобактерной терапии [14–18]. Важным аспектом является также подтверждение антагонистических свойств пробиотиков in vitro для более четкого понимания процессов взаимодействия пробиотических штаммов с H. pylori. Предлагается схема основных механизмов положительного влияния пробиотиков (средств коррекции нарушений микробиоценоза кишечника) на эффективность эрадикации Helicobacter pylori (рис. 1) [19–21].
Цель работы: изучить влияние некоторых пробиотиков на рост инфекции H. pylori in vitro, оценка эффективности эрадикации при использовании монотерапии пробиотиками in vivo.
Материал и методы
Исследование in vitro
Были успешно культивированы 14 штаммов H. pylori. Штаммы микроорганизма были получены при проведении бактериологического анализа биоптатов слизистой оболочки антрального отдела желудка пациентов с клиническими проявлениями диспепсии. Инкубирование проведено в стандартных условиях для роста H. pylori. Оценивалось действие трех различных пробиотиков: 1-й – на основе Enterococcus faecium strain L-3, 2-й – на основе лиофилизированной культуральной жидкости Bacillus subtilis, 3-й – на основе комбинации Bifidobacterium longum и E. faecium. Исследуемые пробиотики разводились в дистиллированной воде в соотношении 1:100 и затем добавлялись в чашку с агаром, на который высевался штамм H. pylori. Учет роста осуществлен на 6–7-е сутки.
Исследование in vivo
Под наблюдением находились 55 больных хроническим гастродуоденитом, ассоциированным с H. pylori.
В зависимости от получаемой терапии пациенты были разделены на 3 группы. 1-я группа (18 больных) получала пробиотик на основе B. subtilis, 2 капсулы 2 раза в сутки во время еды 20 дней (согласно схеме назначения в инструкции); 2-я группа (17 пациентов) – пробиотик на основе E. faecium, 3 драже 3 раза в сутки во время еды в течение 1 месяца (согласно схеме назначения в инструкции), 3-я группа (20 больных – группа сравнения) – стандартную тройную эрадикационную терапию (омепразол 20 мг 2 раза в сутки, амоксициллин 1000 мг 2 раза в сутки, кларитромицин 500 мг 2 раза в сутки 7 дней). В 1-ю и 2-ю группы вошли пациенты, у которых имела место аллергическая реакция на кларитромицин или амоксициллин и/или которые отказались от проведения тройной эрадикационной терапии. До и после лечения (через 1,5–2,0 месяца) проведен стандартизированный опрос всех больных для оценки характера жалоб, фиброэзофагогастродуоденоскопия с взятием двух биоптатов из антрального отдела желудка для верификации инфекции H. pylori (проведены быстрый уреазный тест, гистологическое исследование биоптатов, полимеразная цепная реакция с детекцией гена ureC). Статистическая обработка данных осуществлена с помощью программы Excel для Windows.
Результаты и обсуждение
Исследование in vitro
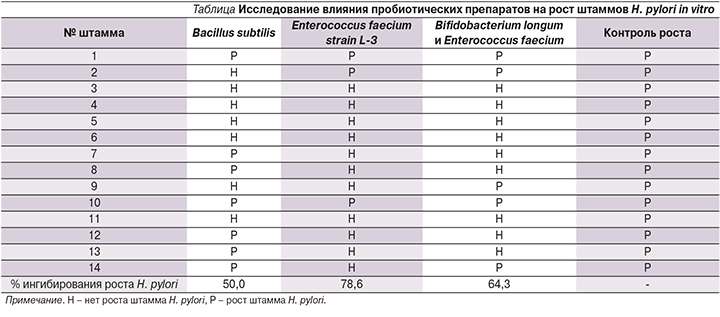
Ингибирование роста H. pylori имело место в 50% случаев при контакте культуры микроорганизма с пробиотиком на основе B. subtilis, в 78,6% случаев при контакте с пробиотиком на основе E. faecium strain L-3 и в 64% случаев при контакте с пробиотиком на основе B. longum и E. faecium (см. таблицу).
Из представленной таблицы видно, что ингибирование роста H. pylori при контакте со всеми тремя выбранными пробиотиками произошло лишь у 35,7% штаммов данного микроорганизма. Ингибирование роста 35,7% штаммов микроорганизма было отмечено в присутствии каких-либо двух из трех пробиотиков. В 14,3% случаев ингибирование роста H. pylori определено в присутствии только какого-то одного пробиотика. Это может говорить о различной реакции штаммов возбудителя на разные пробиотики и требует дальнейшего изучения.
Исследование in vivo
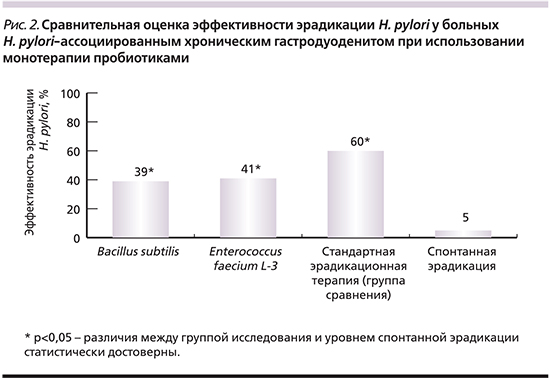
Пробиотики в качестве монотерапии H. pylori-ассоциированного гастрита показали свою эффективность (рис. 2) и безопасность. Пациенты отмечали хорошую переносимость пробиотических препаратов, побочных эффектов на фоне их приема выявлено не было.
Заключение
Результаты, полученные in vitro, могут быть следствием прямого ингибирующего (антагонистического) действия пробиотиков (возможно, за счет синтеза бактериоцинов) в отношении H. pylori. Однако данная гипотеза нуждается в дальнейшем углубленном изучении. Использование монотерапии пробиотиками обеспечивает достижение уровня успешной эрадикации H. pylori (39 и 41%), достоверно превышающего процент спонтанной эрадикации (3–5%). Лучшие показатели ингибирования H. pylori продемонстрировал пробиотический штамм E. faecium strain L-3 in vitro и in vivo. Следовательно, возможно проведение дальнейших исследований именно с этим пробиотиком. В целом монотерапия пробиотиками может быть рекомендована как альтернативный способ лечения хронического гастродуоденита, ассоциированного с H. pylori, в особенности при непереносимости компонентов стандартной антихеликобактерной терапии.
Литература
1. Ткаченко Е.И., Авалуева Е.Б., Успенский Ю.П., Волков М.Ю., Сказываева Е.В., Можелис Ю.В., Захарченко М.М. Эрадикационная терапия, включающая пробиотики: консенсус эффективности и безопасности. Клиническое питание. 2005;1:14–20.
2. Суворов А.Н. Симаненков В.И. H. рylori как возбудитель заболеваний желудочно-кишечного тракта. Генетика патогенности. Возможность эрадикации с использованием пробиотиков (лекции для врачей). СПб., 2006. 12 с.
3. Gotteland M., Brunser O., Cruchet S. Systematic review: are probiotics useful in controlling gastric colonization by Helicobacter pylori? Alimentary Pharmacology and Therapeutics. 2006;23(8):1077–86.
4. Суворов А.Н.. Алехина Г.Г. Драже «Ламинолакт» – эффективное средство для нормализации микробиоценоза кишечника. Гастробюллетень. 2001;1:24.
5. Барышникова Н.В. Эффективность пробиотической терапии в коррекции нарушений микробиоценоза кишечника у больных хроническим гастродуоденитом, ассоциированным с Helicobacter pylori. Вестник СПб., 2006;2:89–92.
6. Caramia G. Probiotics from Mechnicoff to the current preventive and therapeutics possibilities. La Pediatria medica e chirurgica: Medical and Surgical Pediatrics. 2004;26(1):19–33.
7. Limdi J.K., O’neill C., McLaughlin J. Do probiotics have a therapeutic role in gastroenterology? World J. Gastroenterol. 2006;12(34):5447–57.
8. Szajewska H., Horvath A., Piwowarczyk A. Meta-analysis: the effects of Saccharomyces boulardii supplementation on Helicobacter pylori eradication rates and side effects during treatment. Aliment. Pharmacol. Ther. 2010;32:1069–79.
9. Malfertheiner P., Megraud F., O’Morain C.A., Atherton J., Axon A.T., Bazzoli F., Gensini G.F., Gisbert J.P., Graham D.Y., Rokkas T., El-Omar E.M., Kuipers E.J. European Helicobacter Study Group Management of Helicobacter pylori infection: the Maastricht IV/Florence Consensus Report. Gut. 2012;61:646–64.
10. Malfertheiner P., Megraud F., O’Morain C.A., Gisbert J.P., Kuipers E.J., Axon A.T., Bazzoli F., Gasbarrini A., Atherton J., Graham D.Y., Hunt R., Moayyedi P., Rokkas T., Rugge M., Selgrad M., Suerbaum S., Sugano K., El-Omar E.M. et al. Management of Helicobacter pylori infection – the Maastricht V/Florence Consensus Report. Gut. 2017;66:6–30.
11. Ткаченко Е.И., Успенский Ю.П., Барышникова Н.В. Оптимизация лечения заболеваний, ассоциированных с Helicobacter pylori. Врач. 2012;1:36–8.
12. Rustamov M.N., Lazebnik L.B. Use of probiotics in the treatment of patients with Helicobacter pylori-positive duodenal ulcer. Научно-практические аспекты кардиологии и внутренних болезней. Минск, 2013. С. 298–301.
13. Rustamov M.N., Lazebnik L.B. Effect of nonpharmacologic factors in treatment of patients with Helicobacter pylori – associated duodenal ulcer. Central Asia Gastroenterology Week-2013. Consilium. 2013. 84 р.
14. Козлова Д.И. Состояние кишечного микробиоценоза и течение H. pylori-ассоциированного гастрита в условиях эрадикационной и синбиотической терапии. Дисс. канд. мед. наук. СПб., 2004.
15. Барышникова Н.В. Монотерапия пробиотиками как альтернатива стандартной эрадикационной терапии больных Helicobacter pylori-ассоциированными заболеваниями. Сборник научных материалов V конгресса «Рациональная фармакотерапия и клиническая фармакология». СПб., 2010. С. 27–32.
16. Canducci F., Cremonini F., Armuzzi A. Probiotics and Helicobacter pylori eradication // Digestive and Liver Diseases: official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver. 2002;34(Suppl. 2):81–3.
17. Plewinska E.M., Bak-Romaniszynh L., Czkwianianc E., Planeta-Malecka I. Bifidogenic properties of the probiotic bacteria in eradication Helicobacter pylori infection in children / Abstracts of World congress of gastroenterology. Montréal, Canada. 2005.
18. Vandenplas Y., Czerucha D, Surawicz C. Diarrhea: Treatment and prevention. Where do probiotics fit? Abstracts of World congress of gastroenterology. Montréal, Canada. 2005.
19. Успенский Ю.П., Барышникова Н.В., Фоминых Ю.А. Лечение инфекции Helicobacter pylori: проблемы и перспективы. Consilium Medicum. Гастроэнтерология. (Прил.). 2015;1:8–17.
20. Успенский Ю.П., Фоминых Ю.А., Иванов С.В., Менакер И.О. Эволюция в эрадикационной терапии НР-ассоциированных заболеваний. Выход за рамки стандартов? РМЖ. 2016;24(17):1144–52.
21. Успенский Ю.П.. Суворов А.Н., Барышникова Н.В. Инфекция Helicobacter pylori в клинической практике. СПб., 2011. С. 497–537.
In vitro и in vivo в медицине что такое
Усовершенствование качества медицинской помощи, увеличение спектра лечебно-профилактических и диагностических манипуляций, внедрение новых технологических подходов к сохранению здоровья людей одновременно приводит и к возникновению инфекций, связанных с оказанием медицинской помощи (ИСМП). ИСМП представляют серьезную проблему общественного здравоохранения в силу своей распространенности, отрицательного влияния на показатели заболеваемости, смертности и степени тяжести состояния пациентов, а также опасности для медицинских работников и значительного экономического ущерба. В современных условиях проблема ИСМП достаточна актуальна, т.к. заболеваемость во многих странах значительна [1].
В 2016 году в медицинских организациях Российской Федерации случаев ИСМП выявлено на 7,7 % больше, чем в 2015 году (24 771 и 23 006 случаев на 2016 и 2015 года соответственно). Официальная статистика, как правило согласно экспертным оценкам, занижает реальную заболеваемость госпитальными инфекциями. Такая разница возможна из-за несовершенства надзора и учета за ИСМП в большинстве российских медицинских учреждений, своевременного выявления случаев ИСМП и принятия адекватных мер в целях их предупреждения [5].
Наибольшее число случаев ИСМП регистрируется в учреждениях родовспоможения,хирургических стационарах.По данным, представленным в «Национальной Концепции РФ по профилактике инфекций, связанных с оказанием медицинской помощи», разработанной в 2011 г., наблюдаемые в последние годы в России случаи регистрации и внедрения в практику здравоохранения неэффективных антисептических и дезинфекционных средств связаны с нарушениями в экспертной оценке новых средств, и подчеркивается необходимость создания новых методов определения чувствительности госпитальных патогенов к антимикробным препаратам[1,3]. Возникает формирование и широкое распространение в условиях ЛПУ полирезистентных внутрибольничных штаммов условно патогенных микроорганизмов, отличающихся повышенной устойчивостью к воздействию факторов окружающей среды, в том числе и к дезинфицирующим средством,что нашло отражение в СанПиНе 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность», разделе II «Организация дезинфекционных и стерилизационных мероприятий» ( в п. 1.9. указывается, что «в целях предупреждения возможного формирования резистентных к дезинфектантам штаммов микроорганизмов следует проводить мониторинг устойчивости госпитальных штаммов с последующей их ротацией при необходимости»),а также согласно МУ 3.5.1.3439-17 “Оценка чувствительности к дезинфицирующим средствам микроорганизмов,циркулирующих в медицинских организациях”высокой эффективностью мер по предупреждению ИСМП является необходимость проводить эпидемиологический надзор за уровнем и распространенностью ИСМП,микробиологическую диагностику ИСМП, санитарно-бактериологические исследования объектов внутрибольничной среды,оценку чувствительности микроорганизмов к ДС, организацию и проведение мер по повышению эффективности дезинфекционных мероприятий[7, 8].
В настоящее время существует большое количество антисептиков и дезинфектантов под разными торговыми названиям, в основе которых могут находиться химические соединения группы галогенов (в том числе соединения активного хлора), окислители, четвертичные аммониевые соединения (ЧАС), альдегиды, спирты (этанол, изопропиловый спирт).В отличие от антибиотиков они не имеют избирательности действия на бактериальные клетки и эффективно воздействуют на покоящиеся формы.
Однако все чаще стали отмечаться случаи перекрестной резистентности к дезинфицирующим средствам и антибиотикам, что можно объяснить сходством воздействия на мишени в бактериальной клетке. Для предупреждения снижения эффективности дезинфекционных мероприятий необходимо проводить мониторинг устойчивости госпитальных штаммов с последующей их ротацией при необходимости[8].
Современный дезинфектант должен отвечать нескольким основным требованиям, без осуществления которых ни один препарат не может быть рекомендован к применению:
Факторы, оказывающие влияние на антимикробную активность растворов медицинских дезинфектантов:
Целью исследования послужило:
2) сравнение эффективности обратоки рук двумя антисептиками (“Стериллиум” и “Изосепт”).
Материалы и методы: 1)чувствительность 3 штаммов (EscherichiacoliATCC 25922, StaphylococcusaureusFDA 209P, PseudomanasaeruginosaaATCC 27853) определяли методом двукратных серийных разведений в бульоне Мюллера-Хинтона при микробной нагрузке 5×10 5 КОЕ/мл. Посевы инкубировали при 37°С в течение суток, после чего при наличии видимого роста в контроле (питательная среда без антисептика) определяли минимальную подавляющую концентрацию (МПК), для установления характера которой (бактерицидная или бактериостатическая) осуществляли высев на мясо-пептонный агар.
2) у 30 студентов стерильными ватными тампонами, смоченными в физиологическом растворе, тщательно протирали околоногтевые и межпальцевые пространства обеих рук. После отбора проб засевали чашки Петри с мясопептонным агаром. Спустя 15 минут брали повторный смыв с рук испытуемого. Посевы инкубировали при температуре 37°С в течение 24 ч и затем подсчитывали количество выделенных колоний.
Результаты и выводы: Установлено, что: 1) «Стериллиум» во всех разведениях не оказывает бактерицидного действия на штаммы E.coliATCC 25922, S.aureusFDA 209P, что не исключает его наличие при отсутствии разведения. Бактериостатическое действие его в отношении упомянутых штаммов проявилось только в первом двукратном разведении (концентрация 375000 мкг/мл). Бактерицидного и бактериостатического действия на штамм P.aeruginosaATCC 27853 данный антисептик во взятых разведениях не оказал. Антисептик «Изосепт» проявил большую антимикробную активность в отношении опытных штаммов: его МПК (бактериостатическая и бактерицидная) для P.aeruginosaATCC 27853 составила 5080мкг/мл, что соответствует разведению в 128раз. На штаммы кишечной палочки и золотистого стафилококка все опытные разведения оказали бактериостатическое и бактерицидное действие, т.е. МПК ≤ 2540 мкг/мл.
2) Установлено, что до проведения обработки количество микроорганизмов – представителей микрофлоры кожи указанных биотопов у разных студентов различно, что во многом связано с соблюдением правил личной гигиены, состоянием противомикробной резистентности. Следует отметить, что правая рука у большинства обследуемых-правшей оказалась более контаминированной по сравнению с левой, что, очевидно, связано с большим содержанием транзиторной микрофлоры на ней как на «рабочей». После обработки дезинфицирующими средствами смывы, взятые у всех обследуемых, не дали видимого роста или показали рост единичных колоний. Несмотря на то, что в условиях опыта invitro антисептики проявили разную активность, по количественной эффективности обработки рук они не уступали друг другу.
Таким образом, согласно полученным результатам «Изосепт» в условиях нашего опыта проявил большую антимикробную активность в отношении стандартных штаммов бактерий, чем «Стериллиум». Однако результаты могут измениться при тестировании химически чистых веществ, а не комплексных препаратов.