Хорион не дифференцирован что это значит
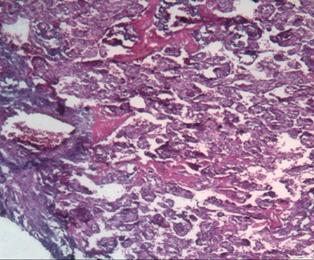
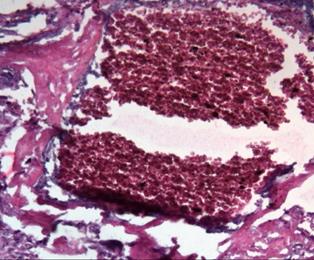
Как уже упоминалось, для беременных женщин является вполне обычным наличие скудных кровяных выделений, не сопровождающихся болями, в первые несколько недель беременности. Возможно, это связано с процессами инвазии трофобласта в дециду-альную оболочку полости матки. По мере развития плодного яйца в области периферической поверхности гиперэхогенного ветвистого хориона становятся различимы небольшие (от 2 до 5 мм) гипоэхогенные зоны, которые, по-видимому, представляют собой области скопления крови в виде лакун, окружающих ворсины хориона.
При трансвагинальном ЦДК артериальный и венозный кровоток в сосудах хориона выявляется раньше, чем начинает визуализироваться эмбрион. По мере увеличения срока беременности регистрируется постепенное увеличение скорости артериального кровотока.
При замершей или прерывающейся маточной беременности отмечается тенденция к увеличению венозного кровотока по периферии хориона. Однако статистически значимых различий между значениями скоростей кровотока в артериальных сосудах при нормальном развитии плодного яйца и при беременности, протекающей с осложнениями, выявлено не было.
У пациенток с обильным кровотечением могут возникать ретрохориальные гематомы. В этих случаях между хорионом и стенкой матки начинает визуализироваться скопление крови, которое выглядит в виде гипоэхогенной области, окружающей плодное яйцо. Используя формулу для расчета объема эллипсоида (длина (см) х ширина (см) х высота (см) х 0,5), размер ретрохориальной гематомы может быть выражен в количественной форме (в см3) относительно размеров плодного яйца. Имеются данные о взаимосвязи между относительным размером ретрохориальной гематомы и прогнозом в отношении прогрессирования беременности.
В том случае если ее объем составляет меньше четверти объема плодного яйца или менее 60 мл, вероятность благоприятного исхода остается достаточно высока.
При самопроизвольном неполном аборте обычно происходит экспульсия плодного яйца из матки и задержка в ней частей хориона, которые обычно визуализируются в просвете ее полости в виде гиперэхогенных структур. При этом контуры плодного яйца могут значительно деформироваться, а структура хориона становится неоднородной.
При неразвивающейся беременности отмечается отсутствие роста эмбриона или формирование его патологии, например в виде аномалии развития стебля тела в сочетании с аномалией пуповины. Так, даже при наличии плодного яйца нормальной формы и размеров в его полости могут отсутствовать эмбрион, а в ряде случаев и желточный мешок. Прекращение развития беременности на ранних сроках наиболее часто является следствием хромосомных нарушений, возникших при оплодотворении.
О гибели эмбриона при трансвагинальной эхографии свидетельствует отсутствие его сердцебиений в сроки, когда КТР составляет более 6 мм. В большинстве наблюдений сердечная деятельность эмбриона может быть зарегистрирована с момента начала его визуализации. Иногда при нарушении развития эмбриона внутри плодного яйца определяются аморфные тканевые массы, которые, наиболее вероятно, представляют собой сгустки крови и/или отторгнувшиеся обрывки децидуальной оболочки.
При полном выкидыше стенки полости матки смыкаются, и во время трансвагинального исследования выявляется тонкий эндометрий однородной структуры. Принимая во внимание, что при внематочной беременности может наблюдаться аналогичная эхографическая картина, для подтверждения диагноза полного аборта используется определение уровня (3-ХГ в крови пациентки в динамике.
Если беременность отсутствует, уровень бета-ХГ, как правило, быстро снижается, в то время как при наличии эктопической локализации плодного яйца такое снижение происходит медленно или приостанавливается на определенном уровне. После неосложненного искусственного аборта бета-ХГ может определяться в крови женщины в течение 16-60 дней (в среднем 30 дней), тогда как при самопроизвольных абортах он выявляется в течение 9-35 дней (в среднем 19 дней). Начиная с 5-го дня после удаления трубной беременности с помощью лапароскопии нулевые концентрации бета-ХГ начинают регистрироваться через 1-31 день (в среднем через 8 дней).
Скрининг на выявление врожденных заболеваний плода при беременности
Что собой представляет скрининг при беременности и зачем он проводится
Скрининг при беременности — это комплекс обследований, в который входят УЗИ и биохимический анализ венозной крови на гормоны. Как правило, скрининг проводят трижды — в первом, втором и третьем триместре.
Раннее обнаружение патологий имеет очень большое значение. Это дает возможность приступить к лечению генетических заболеваний как можно раньше и если не полностью вылечить их, то хотя бы максимально купировать симптомы. Если при обследовании врач замечает отклонения, беременность контролируется особенно тщательно, что дает возможность предупредить развитие осложнений или преждевременные роды. Если же обнаруженные патологии окажутся слишком тяжелыми и несовместимыми с жизнью, врач направит пациентку на прерывание беременности по медицинским показаниям.
Скрининг при беременности безвреден как для мамы, так и для малыша. Это довольно точное исследование, хотя следует четко понимать, что оно не дает стопроцентной гарантии. Точность скрининга зависит от многих факторов — профессионализма исследователей, соблюдения женщиной правил подготовки к обследованию и других факторов.
Первый скрининг при беременности
Первый скрининг при беременности проводят между и неделями. Нет смысла проходить это обследование ранее — до недели беременности многие показатели практически не поддаются определению.
Исследование включает в себя два медицинских теста — УЗИ и анализ крови.
При помощи УЗИ врач определяет точный срок беременности, оценивает телосложение ребенка, его размеры (окружность головы, длину конечностей, рост), работу сердечной мышцы, симметричность головного мозга, объем околоплодных вод, структуру и размер плаценты, а также состояние и тонус матки. Для каждого из этих параметров есть показатели нормы, с которыми врач и будет сравнивать полученные результаты. Для беременности эти нормы составляют:
Длина кости носа — 2–4,2 мм. Слишком маленькая кость носа может говорить о патологии или же просто о том, что нос у малыша будет курносым. ЧСС (частота сердечных сокращений) — 140–160 ударов в минуту. Небольшое (до 40 ударов в минуту) отклонение в ту или иную сторону считается вариантом нормы.
Размер хориона, амниона и желточного мешка. Хорион — это внешняя оболочка плода, которая со временем станет плацентой. Если он расположен на нижней стенке матки, говорят о предлежании хориона. Это потенциально опасная ситуация, чреватая выкидышем, и в этом случае беременной рекомендован постельный режим.
Амнион — внутренняя оболочка, которая удерживает околоплодные воды. Нормальный объем околоплодных вод на сроке 11–13 недель — 50–100 мл.
Желточный мешок — это зародышевый орган, который в первые недели жизни плода выполняет роль некоторых внутренних органов, которые будут сформированы позже. К сроку первого скрининга желточный мешок должен практически исчезнуть (тогда в бланке обследования будет указано «не визуализируется»). Если же размер его составляет около 6 мм, то, возможно, у плода присутствуют определенные патологии.
Шейка матки. В норме ее длина к моменту первого скрининга составляет 35–40 мм. Более короткая шейка матки означает риск преждевременных родов.
УЗИ проводят двумя способами — трансабдоминальным, при котором датчик располагается на животе, и трансвагинальным, при котором он вводится во влагалище. Трансвагинальное УЗИ дает более полную и точную информацию, но его обычно проводят только в первом триместре. Этот метод, как правило, используют при обследовании женщин с лишним весом, поскольку жировая прослойка в области живота не позволяет в деталях рассмотреть плод и матку.
К УЗИ необходимо соответствующим образом подготовиться. Перед трансабдоминальным УЗИ советуют выпить примерно литр воды, чтобы на момент обследования мочевой пузырь был заполнен — тогда матка немного сместится в сторону живота и картинка будет четче. При трансвагинальном УЗИ степень наполненности мочевого пузыря не имеет никакого значения, однако перед обследованием лучше зайти в туалет — так будет комфортнее. Перед исследованием нужно принять душ или освежиться при помощи влажных салфеток. Скопление газов способно исказить результаты УЗИ, каким бы методом оно ни проводилось. Поэтому будущим мамам, страдающим от метеоризма, советуют за день до обследования принимать средства от метеоризма и не есть ничего газообразующего.
Анализ крови
Чтобы анализ крови дал максимально точные сведения, его нужно сдавать на голодный желудок, как минимум через 8 часов после последнего приема пищи. За 2–3 дня до анализа следует воздерживаться от жареной, жирной, острой, копченой пищи, шоколада, орехов, морепродуктов. Рекомендуется также не вступать в половые контакты. Все это не столь значительно, однако может тем или иным образом повлиять на результат.
Второй скрининг при беременности
Второй скрининг при беременности проводят на сроке 16–20 недель. Как и первый, он состоит их тех же двух этапов — УЗИ и анализа крови.
На этот раз врач определяет не только размеры, но и положение плода и его костную структуру, состояние внутренних органов и место прикрепления пуповины, а также объем околоплодных вод. Вот приблизительные основные показатели нормы для срока 16–20 недель:
ИАЖ (индекс амниотической жидкости, то есть объем околоплодных вод) — 73–230 мм. Маловодие может негативно повлиять на состояние костной структуры ребенка и развитие его нервной системы.
Локализация плаценты. Некоторый риск есть лишь при расположении плаценты на передней стенке матки — при такой локализации возможно отслоение плаценты.
Пуповина. Один из важнейших параметров — место прикрепления пуповины. Краевое, расщепленное или оболочечное прикрепление чревато гипоксией плода и трудностями во время родов, нередко оно становится показанием для кесарева сечения. Пуповина подпитывается через 2 артерии и 1 вену, хотя иногда в наличии имеется только одна артерия. Это может вызвать гипоксию плода, порок сердца, нарушения в работе системы ребенка, стать причиной пониженной массы тела малыша. Впрочем, если все остальные анализы и обследования не показывают отклонений от нормы, волноваться не стоит.
Шейка матки. Длина шейки матки на этом сроке должна составлять 40–45 мм. Короткая шейка матки означает угрозу выкидыша.
Визуализация. Неудовлетворительная визуализация может быть вызвана как особенностями положения плода или лишним весом будущей мамы, так и отеками или гипертонусом матки.
Анализ крови
Третий скрининг при беременности
Третий скрининг при беременности проводят на 30- неделе. По результатам этого скрининга врач принимает решение о необходимости кесарева сечения или возможности естественных родов. Основа третьего скрининга — все те же УЗИ. Иногда назначают допплерографию — исследование работы сосудов. Вот приблизительные нормы для данного срока беременности:
Пренатальный скрининг очень важен, и пренебрегать им не стоит. Вовремя выявленные патологии и отклонения от нормы могут спасти жизнь и здоровье вашему ребенку. Об этом стоит помнить, особенно тем родителям, которые отказываются от обследования из страха узнать о том, что развитие малыша идет не по плану.
Если при ультразвуковом исследовании найдены маркеры хромосомной патологии плода
Если при ультразвуковом исследовании были найдены маркеры (признаки) хромосомной патологии плода, то это еще не означает, что у плода есть хромосомная патология, и надо обязательно прерывать беременность. Всем женщинам, у которых были найдены ультразвуковые маркеры хромосомной патологии плода, предлагается инвазивная пренатальная диагностика – хорионбиопсия/плацентобиопсия с целью взятия клеток плода и их тонкого микроскопического анализа.
Хорионбиопсия – это взятие нескольких ворсинок из хориона плода под ультразвуковым контролем и подсчет количества хромосом в его клетках. Хорион – орган плода, из которого потом образуется плацента. Его клетки идентичны клеткам плода. Поэтому если количество и структура хромосом в клетках хориона нормальны, то хромосомные болезни у плода исключаются с вероятностью более 99%.
Как проводится хорионбиопсия
Тонкой иглой через переднюю брюшную стенку делается укол, игла проходит в хорион и в нее попадает несколько ворсинок хориона. Процедура проводится в амбулаторных условиях, используются одноразовые перчатки и стерильные иглы, поэтому риск инфицирования во время процедуры практически отсутствует.
Каковы риски проведения хорионбиопсии
Любая процедура, даже простейший анализ крови, имеет риск осложнений. При проведении хорионбиопсии тоже есть риск – риск прерывания беременности. Однако, при соблюдении всех правил проведения процедуры этот риск не превышает 1%. Поэтому в тех случаях, когда индивидуальный риск хромосомной патологии плода достаточно высок, должна быть выполнена эта процедура.
На сегодняшний день в мире не разработано другого метода, позволяющего получить для исследования клетки плода, не выполняя внутриматочного вмешательства. В то же самое время, исключить или подтвердить диагноз болезни Дауна или другой хромосомной патологии можно только при исследовании клеток плода, которые были получены при внутриматочном вмешательстве.
Когда проводится хорионбиопсия
Хорионбиопсия выполняется до 14 недель беременности, после этого срока на месте хориона образуется плацента и тогда проводится уже плацентобиопсия. Техника выполнения и риск при плацентобиопсии принципиально не отличаются от хорионбиопсии.
Мы надеемся, что эта информация поможет Вам лучше понять, для чего мы проводим эти исследования, и преодолеть тот естественный страх перед процедурой, который вызывает неизвестность и те непрофессиональные сведения, которые иногда печатаются в немедицинских источниках.
В нашем центре вы можете пройти инвазивную диагностику хромосомных болезней плода и получить полный ответ уже через 3-4 дня (в некоторых случаях – через 24 часа).
Хорион не дифференцирован что это значит
Правильный рост плода и физиологическое течение беременности в основном зависят от адекватной функции плаценты с нормальной плацентарной морфометрией (размером и формой) и структурой. Нарушения в развитии плаценты, в том числе уменьшение ее размера или изменение способности транспорта питательных веществ и кислорода, способствуют дисфункции провизорного органа. Способность плаценты поддерживать достаточное количество питательных веществ обычно описывается как «эффективность плаценты» и отражается в соотношении массы тела плода к весу плаценты [1; 2]. Повышенный риск мертворождения может отражать меньший «плацентарный резерв» с высоким коэффициентом отношения массы плода к весу плаценты, но при этом максимально увеличены, хотя и ограничены, вес и рост.
Преждевременные роды имеют непредсказуемые последствия для здоровья новорожденного, всегда вызывая опасения как у докторов, так и будущих родителей. Основные факторы плацентарной недостаточности, патофизиологический механизм, можно широко разделить на нарушения кровотока и обменную способность по синцитиокапиллярным мембранам ворсин плаценты плода. Плацентарная недостаточность имеет значительные связи с неблагоприятными исходами беременности (перинатальная смертность и заболеваемость). Несколько подходов были направлены на скрининговое обнаружение плацентарной недостаточности, например единообразное определение гипотрофии плода, использование ультразвуковых профилей доплера и использование траекторий роста с помощью ультразвуковой биометрии плода. Однако роль плацентарной морфометрии и морфологии, связь между структурными поражениями плаценты и неонатальными исходами не полностью понятна и заслуживает дальнейшего изучения [1; 3].
Цель исследования: изучить морфологические особенности плаценты человека во II и III триместре беременности в норме и при различной экстрагенитальной патологии.
Материал и методы исследования
Проанализировано 22 истории родов женщин, родоразрешившихся в сроках беременности 22-40 недель, с изучением акушерско-гинекологического анамнеза, экстрагенитальной патологии, особенностей течения беременности и родов. Материалом для исследования послужили центральные и краевые участки плаценты новорожденных (размером 1 см3) в различных сроках гестации. Использовали классический метод О.В. Волковой и Ю.К. Елецкого: фиксация в 10% нейтральном формалине, промывка органа, обезвоживание в батарее спиртов и заливка в парафин. На ротационном микротоме LEICA RM 2245 получили срезы плаценты толщиной 6 мкм, с последующей окраской гематоксилином и эозином. Серийные срезы изучали с помощью светового микроскопа LEICA с цифровой фотокамерой (увеличение х100, х200, х400, х1000), описывали структуру ворсинок плаценты и межворсинчатого пространства, объемную плотность ворсинчатой ткани, средний диаметр сосудов, состояние терминальных ворсин и синцитиокапиллярных мембран. Морфометрические параметры были оценены в 50 срезах каждой плаценты. Измерения проводили с использованием компьютеризированной системы анализа видеоизображений Image scop. С помощью программы Adobe Photoshop Cs3 Extendid определяли: 1) площадь сечения ворсин (мкм2) – по внешнему контуру эпителия ворсины, 2) площадь стромы ворсины (мкм2) – по внутреннему контуру эпителия ворсины, 3) площадь, занимаемую эпителием – по разнице первой и второй площади. Статистическая обработка данных проводилась с помощью программы Sigma Stat 3.5.
Результаты исследования и их обсуждение
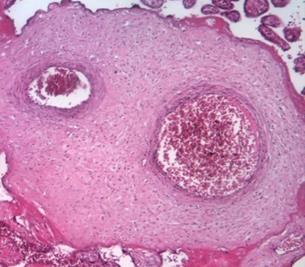
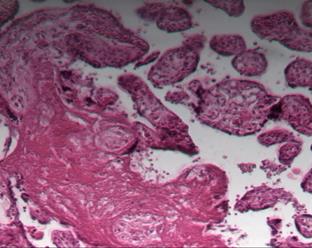
Известно, что к 12-й неделе беременности ворсины плаценты достигают определенных, основных этапов развития и дифференцируются на опорные (рис. 1), промежуточные и терминальные. В последующие недели гестации ворсины претерпевают качественное изменение, появляются недифференцированные и дифференцированные промежуточные ворсины, а также терминальные специализированные ворсины, осуществляющие основные обменные процессы.
При физиологической беременности плацента во втором триместре характеризуется преобладанием промежуточных недифференцированных и дифференцированных ворсин, в последних увеличивается количество синцитиальных почек и узлов и появляются первые синцитиокапиллярные мембраны [4; 5]. Четверть всех ворсин даже при доношенной беременности составляют крупные стволовые ворсины, характеризующиеся плотной стромой, в центре которой находятся толстостенные сосуды, окруженные муфтами гладкомышечных клеток и адвентицией (рис. 1а).
Рис. 1. Стволовые ворсины плаценты при физиологической (а) и патологической беременности (б) во II триместре. Окраска гематоксилином и эозином. Увеличение х100
Стволовые ворсины в основном осуществляют транспорт крови и в меньшей степени участвуют в диффузии газов и метаболитов. Морфометрия показала, что в данном периоде ворсины характеризуются большой площадью сечения стромы (17157±121 мкм2) и незначительной долей эндотелия по отношению к строме (около 17,9-18,6%).
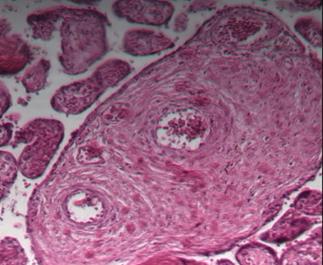
Плацента, рожденная на сроке 20-22 недели беременности, отягощенной различной экстрагенитальной патологией (гипертензия, сахарный диабет, гепатит), характеризуется преобладанием гиперплазированных ворсин, доминированием стромального компонента, сужением основных сосудов в стволовых ворсинах за счет гиперплазии стенок (рис. 1б), дефицитом промежуточных дифференцированных и терминальных ворсин, уменьшением удельного веса сосудов, а, следовательно, гипоплазией капилляров и синцитиокапиллярных мембран. В некоторых случаях ворсины имеют неровные контуры, кистозную дегенерацию, повышенный фиброзный компонент, отложения фибрина в крупных сосудах и очаги аваскуляризированных ворсин. Все эти признаки характеризуют состояние мальперфузии, которая значительно нарушает основную функцию плаценты – трофическую, и приводит к различным нарушениям у плодов: экстремально низкая масса тела, гипоксия, постгипоксическая энцефалопатия и другие нарушения центральной нервной системы [4; 5]. Все перечисленные изменения обычно входят в клиническую практику акушеров под термином «плацентарная недостаточность», которая обычно определяется косвенными методами по морфометрии плода [6].
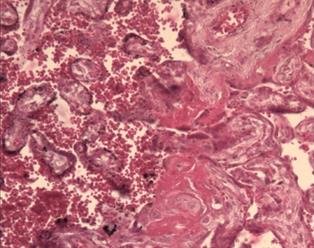
Исследование плацент женщин с патологией крови, сосудов, железодефицитной анемией показало наличие псевдоинфарктов, некрозов ворсин, склероза стромы ворсин и их тромбоз 6. В тяжелых случаях данной экстрагенитальной патологии, при отсутствии должной терапии, плацента и в третьем триместре гестации сохраняет и усугубляет морфологические проявления, такие как облитерация сосудов ворсин, фибриноидные отложения и скопление (сладжирование) эритроцитов в межворсинчатом пространстве, микроинфаркты (рис. 2).
Рис. 2. Патологические изменения в плаценте в III триместре беременности: а – фибриноидные отложения в межворсинчатом пространстве, кистозная дегенерация некоторых ворсин; б – скопление эритроцитов, расширение межворсинчатого пространства, фибриноидные изменения и склерозирование ворсин. Окраска гематоксилином и эозином. Увеличение х100
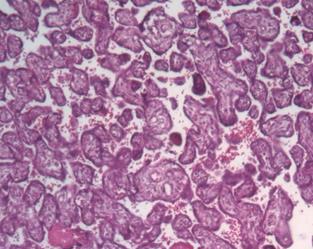
Плацента при доношенной физиологической беременности характеризуется структурными признаками зрелости, включающими все компоненты ворсинчатой части и преобладание самых мелких терминальных дифференцированных ворсин (41-47%), являющихся дивергентным адаптивным механизмом в гемохориальной плаценте. Терминальные ворсины (рис. 3) являются основными в обеспечении трофики плода, с наличием типичных синцитиокапиллярных мембран: тончайшие участки плацентарного барьера, в которых капилляры ворсин приближены к истонченному синцитиотрофобласту [8; 9]. На продольных срезах терминальных дифференцированных ворсин хорошо видно, что синцитиокапиллярные мембраны занимают большую площадь поверхности ворсины (рис. 3б), часто встречаются несколько таких образований в пределах одной ворсины, тем самым увеличивая площадь плацентарного барьера. Морфометрические показатели позволяют говорить о многократном уменьшении стромального компонента ворсинчатого дерева к концу беременности (2921±152 мкм2) и, как следствие, увеличении доли эндотелия к строме ворсины до 88%. Морфологически большинство терминальных ворсин были специализированными, содержащими капилляры синусоидного типа, которые находились в тесном контакте с синцитиотрофобластом [9; 10]. Доля терминального ворсинчатого эндотелия по отношению к строме была значительно увеличена.
Рис. 3. Основной компонент зрелой плаценты – терминальные дифференцированные ворсины: а – поперечный срез, б – продольный срез, синцитиокапиллярные мембраны показаны стрелками. Окраска гематоксилином и эозином. Увеличение: а х100, б х400
Таким образом, во II и III триместрах физиологической беременности в плаценте происходят структурные изменения, в частности капилляры превращаются в тонкостенные синусоиды, которые сближаются и тесно взаимодействуют с синцитиотрофобластом, что приводит к образованию необходимых синцитиокапиллярных мембран для адекватного удовлетворения растущих потребностей плода. Синцитиокапиллярная мембрана состоит из общего бесклеточного слоя эндотелия и эпителия толщиной 4,31±0,18 мкм. Благодаря такому строению осуществляется прямая диффузия кислорода и метаболитов в течение последнего месяца беременности и родов.
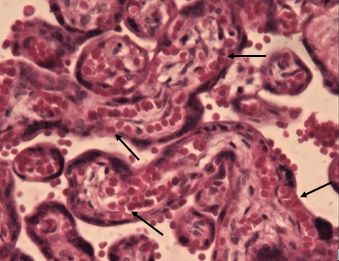
Проводя исследование, мы обратили внимание на тот факт, что даже при наличии в клиническом диагнозе различной инфекционной патологии (хронический пиелонефрит, хроническая вирусная инфекция, включая гепатит С и ВИЧ), развитии гестационных осложнений в виде гестоза, наличия хронической фетоплацентарной недостаточности и хронической гипоксии плода компенсаторные возможности плаценты достаточно велики и вес плода при доношенной беременности страдает далеко не всегда, а чаще всего остается в пределах нормы [10; 11]. В одном из случаев, сопровождающемся достаточно неблагоприятной экстрагенитальной патологией и недостаточностью плаценты (по данным истории родов), масса плода была 5190 г. По данным микроскопии такой плаценты, результаты были крайне противоположными. Наряду с участками физиологической нормы наблюдались значительные повреждения микроструктуры плаценты, такие как интраплацентарный застой, тромбоз, очаги инфарктов, участки некроза и маляции, резкий отек дистальных ворсин и межворсинчатого пространства (рис. 4) [11]. Следовательно, плацента как основной провизорный орган, осуществляющий главные функции во внутриутробной жизни плода (газообменная, транспортная, метаболическая, защитная, гормональная), обладает практически безграничными возможностями и функциональным резервом в обеспечении возрастающих потребностей плода.
Рис. 4. Морфологические признаки плацентарной дисфункции: а – интраплацентарный застой, деструкция терминальных ворсин, аваскулярные участки ворсин, отложения фибриноида; б – микроинфаркт. Окраска гематоксилином и эозином. Увеличение: а, б х200
Заключение. Структура плаценты человека на разных сроках беременности имеет свои особенности в связи с постепенной дифференцировкой ворсин хориона. В процессе преобразования ворсин барьер между материнским и плодным кровотоком уменьшается вследствие истончения синцитиотрофобласта, снижения количества клеток цитотрофобласта и диаметра ворсин. Кроме того, капилляры плода приближаются к поверхности ворсин, при этом уменьшается расстояние диффузии, что особенно необходимо во время родов. При недоношенной беременности наблюдаются различные нарушения дифференцировки ворсин хориона, отсутствуют терминальные дифференцированные ворсины и, как следствие, резко уменьшается количество синцитиокапиллярных мембран. «Эффективность плаценты» в большей степени связана с ранним ангиогенезом, так как только снижение плацентарного кровотока, преобладание аваскуляризированных терминальных ворсин резко снижает компенсаторные возможности и способствует прерыванию беременности. Но, безусловно, плацента имеет значительный функциональный резерв, что продемонстрировано разнообразием морфологических изменений в разных сроках гестации и при различной экстрагенитальной патологии. Более поздние нарушения морфологии плаценты, микроинфаркты, отек, отложение фибриноида, некроз отдельных ворсин не приводят к фатальным последствиям.
Ввиду критической роли плаценты в определении исхода беременности и роли плацентарной недостаточности в этиологии мертворождения послеродовая гистология плаценты является часто используемым исследованием, которое может предоставить важную информацию для клиницистов. Предварительные результаты нашего исследования показали, что добавление объективной оценки морфологии плаценты с использованием современной системы классификации и отработанных критериев, с качественными описаниями (аваскулярные ворсины, тромботическая васкулопатия, нарушение созревания плаценты, уменьшение доли синцитиокапиллярных мембран и другие), а также дополнительными комплексными исследованиями иммуногистохимии факторов роста сосудов, например, позволят достаточно точно диагностировать причины возникшего неблагоприятного перинатального исхода.