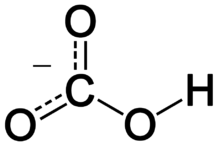
Hco3 что за кислота
При растворении углекислого газа в воде образуется очень слабая угольная кислота Н2СО3. Углекислый газ в воде находится преимущественно в виде гидратированных молекул СО2 и лишь в незначительной степени в форме угольной кислоты. При этом в растворе устанавливается равновесие:
Угольная кислота – слабая неустойчивая кислота, которую в свободном состоянии из водных растворов выделить нельзя.
Тем не менее, при разложении гидрокарбоната аммония в газовой фазе обнаружены частицы Н2СО3, довольно устойчивые в отсутствии воды.
Проявляет свойства слабых кислот. Будучи двухосновной, образует два типа солей карбонаты и гидрокарбонаты.
Карбонат-ион имеет форму правильного плоского треугольника.
Три гибридные орбитали атома углерода участвуют в образовании трех связей с атомами кислорода, оставшаяся р-орбиталь углерода перекрывается с аналогичной орбиталью кислорода.
Карбонаты двухвалентных металлов трудно растворимы в воде, но их растворимость повышается в присутствии углекислого газа за счет образования гидрокарбонатов:
Карбонаты металлов (кроме щелочных металлов) при нагревании декарбоксилируются с образованием оксида:
Температура распада карбонатов повышается по мере усиления электроположительного характера металла и ионного характера связи, карбонаты щелочных металлов не разлагаются.
Гидрокарбонаты разлагаются до карбонатов:
Качественной реакцией на карбонат и гидрокарбонат ионы является их взаимодействие с сильной кислотой, наблюдается образование углекислого газа с характерным вскипанием:
Гидрокарбонаты
Гидрокарбонаты щелочных металлов в воде растворимы. Также в воде хорошо растворимы гидрокарбонаты щелочноземельных металлов, в отличие от карбонатов.
Содержание
Получение
Гидрокарбонат натрия плохо растворим в холодной воде, поэтому его можно отделить от хлорида аммония фильтрованием.
Химические свойства
В итоге раствор гидрокарбонатов имеет щелочную реакцию.
Применение
Гидрокарбонат натрия (сода) используется в производстве искусственных минеральных вод и заправки огнетушителей, в кондитерском деле и хлебопечении, в быту, в медицине.
Физиологическое действие
Литература
Примечания
См. также
Полезное
Смотреть что такое «Гидрокарбонаты» в других словарях:
ГИДРОКАРБОНАТЫ — (бикарбонаты) кислые соли угольной кислоты Н2СО3, напр., питьевая сода NаНСО3 … Большой Энциклопедический словарь
гидрокарбонаты — – кислые соли угольной кислоты. Словарь по аналитической химии [3] … Химические термины
гидрокарбонаты — (бикарбонаты), кислые соли угольной кислоты Н2СО3, например питьевая сода NaHCO3. * * * ГИДРОКАРБОНАТЫ ГИДРОКАРБОНАТЫ (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр., питьевая сода NаНСО3 … Энциклопедический словарь
Гидрокарбонаты — бикарбонаты, двууглекислые соли, кислые соли угольной кислоты (См. Угольная кислота) H2CO3, например NaHCO3 (Гидрокарбонат натрия). Г. получают действием CO2 на карбонаты или гидроокиси в присутствии воды. При нагревании они превращаются… … Большая советская энциклопедия
ГИДРОКАРБОНАТЫ — (от гидро. и карбонаты) кислые соли угольной к ты H2CO3; Г. натрия NaHCO3 питьевая сода … Большой энциклопедический политехнический словарь
ГИДРОКАРБОНАТЫ — (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр. питьевая сода NaHCO3 … Естествознание. Энциклопедический словарь
гидрокарбонаты — гидрокарбон аты, ов, ед. ч. н ат, а … Русский орфографический словарь
гидрокарбонаты — мн., Р. гидрокарбона/тов; ед. гидрокарбона/т (2 м) … Орфографический словарь русского языка
Минеральная вода — Минеральные воды воды, содержащие в своем составе растворённые соли, микроэлементы, а также некоторые биологически активные компоненты. Среди минеральных вод выделяют минеральные природные питьевые воды, минеральные воды для наружного… … Википедия
Натрия гидрокарбонат (пищевая сода)

Гидрокарбонат натрия — химическое вещество
Натрия гидрокарбонат — лекарственное средство
Терапия гидрокарбонатом натрия беременных и кормящих матерей
В связи с нежелательными побочными эффектами натрия (отек и увеличение веса) некоторые специалисты выступают за использование у беременных альтернативных антацидов, не содержащих гидрокарбонат натрия. Категория риска для плода по FDA при терапии гидрокарбонатом натрия — «C» (исследования на животных выявили отрицательное воздействие лекарства на плод, а надлежащих исследований у беременных женщин не было, однако потенциальная польза, связанная с применением данного лекарства у беременных, может оправдывать его использование, несмотря на имеющийся риск).
В связи с отсутствие данных об экскреции натрия гидрокарбоната в материнское молоко, ограничений для терапии кормящих грудью матерей нет.
Питьевая сода — традиционное, но опасное средство для купирования изжоги
| Bсе наклоненья и залоги Изжеваны до одного. Хватить бы соды от изжоги! Так вот итог твой, мастерство? Б.Л. Пастернак. «Bсе наклоненья и залоги». 1936. |
Натрия гидрокарбонат — традиционное средство для купирования изжоги, всасывающийся антацид. Всасывающимися называют антациды, которые или сами, или продукты их реакции с кислотой желудочного сока растворяются в крови. 
После приема 3 г гидрокарбоната натрия рН желудочного содержимого сохраняется на уровне выше 3 единиц рН лишь в течение 75 минут. Образующаяся при нейтрализации углекислота вызывает отрыжку и вздутие живота. Как редкое осложнение после приема гидрокарбоната натрия, описан разрыв желудка из-за резкого освобождения большого количества газа (А.В. Охлобыстин).
В XIX веке «сода» была одним из самых популярных средств от изжоги, например, её постоянно принимал П.И. Чайковский.
Натрий гидрокарбонат в составе кислотоподавляющих лекарств
Несмотря на отрицательное отношение к гидрокарбонату натрия как средству купирования изжоги, он иногда включается в состав лекарств, предназначенных для снижения кислотности в верхних отделах желудочно-кишечного тракта, в достаточном количестве, чтобы его рассматривать, как еще одно действующее вещество (хотя в инструкции к такому препарату гидрокарбонат натрия может быть перечислен среди вспомогательных, а не активных веществ).

| Основные ингредиенты | Zegerid, капсула | Zegerid, капсула | Zegerid, пакетик* | Zegerid, пакетик* | Zegerid OTC, капсула | Омез Инста, пакетик* |
| Омепразол, мг | 20 | 40 | 20 | 40 | 20 | 20 |
| Натрия гидрокарбонат, мг | 1100 | 1100 | 1680 | 1680 | 1100 | 1680 |
Примечание. *) Пакетик содержит порошок для приготовления суспензии для приема внутрь.

| Основные ингредиенты | Гевискон, 10 мл суспензии | Гевискон, таблетка жевательная | Гевискон форте, 10 мл суспензии | Гевискон Двойное Действие, таблетка жевательная | Гевискон Двойное Действие, 10 мл суспензии |
| Натрия альгинат, мг | 500 | 250 | 1000 | 250 | 500 |
| Натрия гидрокарбонат, мг | 267 | 133,5 | — | 267 | 213 |
Натрия гидрокарбонат в составе других лекарств
Применение гидрокарбоната натрия при исследовании желудка (тест Ноллера)
Тест Ноллера (щелочной тест) выполняется с целью получения информации о количестве соляной кислоты в желудке пациента, об интенсивности кислотообразования, а также, косвенно, о количестве желудочного сока. Тест проводится одновременно с процедурой внутрижелудочной рН-метрии, через 20 минут после стабилизации кислотности в базальных условиях или через 45 минут после введения стимуляторов. При рН равном или выше 4,0 щелочной тест не проводится.
Пациент выпивает 0,5 г гидрокарбоната натрия, растворенного в 30 мл дистиллированной воды. Обычно в теле желудка рН регистрируется ниже 2,5. В результате введения в желудок щелочи показатели рН изменяются до щелочных и в течение определенного времени сохраняются на одном уровне, а затем, через некоторое время, называемое «щелочным временем», возвращаются к исходным. По щелочному времени определяется состояние кислотопродукции желудка пациента (С.И. Рапопорт и др.):
Оценка продукции соляной кислоты в желудке
Бикарбонаты, как естественное средство защиты органов ЖКТ от кислоты
Бикарбонаты вместе со слизью составляют так называемый предэпителиальный уровень защиты слизистой оболочки желудка. Слизь не может защищать эпителий от ионов Н + без постоянно поступающих в нее бикарбонатов, также секретируемых поверхностным эпителием. С помощью бикарбонатов в слизи поддерживается градиент рН: на поверхности, обращенной в просвет желудка, среда кислая, а у эпителиоцитов — нейтральная или слабощелочная. Немедленного смешивания бикарбонатов с кислым секретом в просвете и нейтрализации не происходит: слой слизи образует барьер, благодаря которому и существует градиент рН (Т.Л. Лапина ).
Бикарбонаты также секретируются протоковыми клетами поджелудочной железы и вместе с соком поджелудочной железы поступают в двенадцатиперстную кишку, где участвуют в нейтрализации соляной кислоты (О.А. Саблин и др.).
Гидрокарбонат в минеральных водах
Ионы гидрокарбонатов HCO3 – присутствуют практически во всех природных минеральных водах. Для их определения в воде применяется ГОСТ 23268.3-78 «Воды минеральные питьевые лечебные, лечебно-столовые и природные столовые. Методы определения гидрокарбонат-ионов». Согласно ГОСТ Р 54316-2011. «Воды минеральные природные питьевые. Общие технические условия» содержание гидрокарбонаты указывается на потребительской таре (на этикетках бутылок с минеральной водой).
Особенности взаимодействия кислых солей со щелочами.
Достаточно часто возникают затруднения при записи реакций кислых солей со щелочами. Ниже рассмотрим основные закономерности подобных взаимодействий. Под кислыми солями подразумеваем соли, в которых остались атомы водорода, способные к замещению на катионы металлов или аммония. Отсюда первый вывод: при добавлении щелочи водород в составе «кислого» аниона будет замещаться с образованием среднего аниона. По такой схеме будут идти простейшие примеры 1) и 2):
2) LiHS + LiOH = Li2S + H2O
Li + + HS − + Li + + OH − = 2Li + + S 2- + H2O
HS − + OH − = S 2- + H2O
При рассмотрении солей фосфорной кислоты будут возникать дополнительные варианты за счет образования двух видов кислых солей: гидрофосфатов и дигидрофосфатов. Тут следует обращать внимание на избыток/недостаток соли, либо щелочи. Сравните примеры 3) и 4):
Щелочи в примере 3) мало, не хватает для полного замещения атомов водорода в кислой соли.
В примере 4) щелочи много, заместит все возможные атомы водорода в кислой соли.
Значительно больше сложностей возникает при взаимодействии кислой соли и щелочи с разными катионами. Здесь все так же сперва происходит превращение кислого аниона в средний, а далее возможен обмен катионами. Влиять на такой обмен будет природа катионов, растворимость соответствующих средних солей, а также избыток/недостаток соли, либо щелочи. Рассмотрим возможные комбинации для солей двухосновной кислоты, например, угольной:
В описании задания случай 5) можно охарактеризовать фразой «в образовавшемся растворе практически отсутствовали гидроксид-ионы», что вполне понятно из ионного уравнения.
Для случая 6) можно записать «в образовавшемся растворе практически отсутствовали карбонат-ионы», что вполне понятно, поскольку они полностью перешли в состав осадка карбоната бария.
Различие в примерах 5) и 6) легко понять, если представить, что карбонат калия, образовавшийся на первой стадии, может далее вступить в обмен с избытком гидроксида бария.
Теперь давайте поменяем местами исходные катионы и убедимся, что тогда реакция может пойти единственным образом:
Почему невозможен вариант с получением гидроксида бария по аналогии со случаем 6)? Потому что карбонат бария уже является осадком и в дальнейшее взаимодействие с гидроксидом калия не вступает:
BaCO3 + KOH – нет реакции
Схожие рассуждения можно применить и для реакций с участием трехосновной фосфорной кислоты. Там так же будет больше вариантов протекания, если исходим из соли щелочного металла и щелочи, содержащей щелочноземельный металл:
Вариант 8) с образованием двух солей, по формулировке «в образовавшемся растворе практически отсутствовали гидроксид-ионы». Гидроксида кальция добавили мало, связать все фосфат-ионы в осадок не смог.
Вариант 9) с образованием соли и щелочи, по формулировке «в образовавшемся растворе практически отсутствовали фосфат-ионы». Гидроксида кальция взяли много, все фосфат-ионы перешли в осадок.
Если взять изначально соль щелочноземельного металла и гидроксид щелочного, то вариант будет только один:
Причина отсутствия гидроксида кальция в продуктах по аналогии с пунктом 7) – нерастворимость промежуточно образовавшегося фосфата кальция и отсутствие обмена с ним:
Реакции с дигидрофосфатами будут идти по аналогичным схемам и приводить к двум солям, либо соли и щелочи. Рассмотрим два примера из числа возможных:
Весь фосфат перешел в осадок.
Часть фосфата перешла в осадок, новый гидроксид образоваться не может.
Карбонаты
От угольной кислоты Н2СО3 происходит два ряда карбонатов щелочных металлов. При полном насыщении угольной кислоты щелочью получаются нейтральные или вторичные карбонаты М2СО3, в то время как при замещении лишь одного из двух атомов водорода образуются кислые или первичные карбонаты MHCO3. Последние называют также гидрокарбонатами, так как они еще содержат водород, который может быть замещен на металл. Их название — «бикарбонаты» (так как они образуются в результате взаимодействия одного эквивалента щелочи с двумя эквивалентами угольной кислоты) — устарело. Как «нейтральные», так и «кислые» карбонаты щелочных металлов (гидрокарбонаты) обнаруживают в водном растворе щелочную реакцию, так как вследствие слабости угольной кислоты они подвергаются частичному гидролизу:
Однако гидрокарбонаты имеют в растворе более слабую щелочную реакцию, чем нейтральные карбонаты. Щелочную реакцию последних можно обнаружить лакмусом и фенолфталеином; гидролиз бикарбонатов не удается обнаружить при помощи менее чувствительного к ионам ОН` фенолфталеина.
За исключением карбоната лития, все нейтральные карбонаты щелочных металлов легко растворимы в воде. Гидрокарбонаты также легко растворимы; лишь гидрокарбонат натрия обладает сравнительно незначительной растворимостью. Как будет видно в дальнейшем, это имеет большое техническое значение.
Карбонаты К и Rb с соответствующими фторидами образуют конгруентно плавящиеся двойные соединения состава К2СО3·KF и Rb2CO3·RbF. В противоположность этому в системах Li2CO3/LiF, Na2CO3/NaF и Cs2CO3/CsF не образуется ни двойных соединений, ни смешанных кристаллов.
Карбонат натрия. Сода Na2CO3 в безводном состоянии представляет собой белый порошок удельного веса 2,4—2,5, который плавится около 850°. В воде сода легко растворяется, причем вследствие образования гидратов растворение сопровождается разогреванием. Важнейший из гидратов, получаемых в твердом состоянии, кристаллическая сода, Na2CO3·10Н2О кристаллизуется из водных растворов при температуре ниже 32° в виде больших бесцветных моноклинных кристаллов удельного веса 1,45, которые плавятся в своей же кристаллизационной воде при 32°. Водные растворы соды обнаруживают ярко выраженную щелочную реакцию, так как вследствие слабости угольной кислоты соль подвергается далеко идущему гидролитическому расщеплению.
Помимо декагидрата, существует ромбический гептагидрат, устойчивый при соприкосновении с раствором в температурном интервале 32,017—35,3°, а также ромбический моногидрат, который, согласно Вальдеку, находясь под раствором при 112,5° и давлении 1,27 атм, переходит в безводную соль. Гептагидрат существует также еще в другой модификации, которая при соприкосновении с водным раствором не устойчива ни при какой температуре.
Сода встречается иногда в природе в водах озер, например в озере Оуэнс в шт. Калифорния, общее содержание соды в котором достигает 100 млн. т; сода, правда достаточно грязная, добывается из этого озера в результате испарения воды на солнце. Содовые озера наряду с нейтральным карбонатом содержат прежде всего гидрокарбонат. В некоторых местах осаждается двойное соединение гидрокарбоната с нормальным карбонатом Na2CO3·NaHCO3, называемое троной (trona или urao). В водах целебных щелочных источников, например в Карловых Варах, также содержатся Na2CO3 и NaHCO3.
Карбонат натрия содержится в золе некоторых морских водорослей. 100 лет назад соду добывали главным образом из золы растений.
Теперь соду получают почти исключительно способом Сольве (аммиачный способ получения соды). Более старый способ Леблана теперь почти совершенно не используют. Производство соды путем карбонизации полученной электролизом натровой щелочи в противоположность осуществляемому таким путем производству поташа имеет ограниченное значение. Как было указано, едкий натр, наоборот, часто получают каустификацией соды. В США соду отчасти получают из криолита.
По способу Леблана каменную соль обрабатывали сначала концентрированной серной кислотой, получая сульфат натрия (называемый обычно в технике коротко сульфат) и в качестве важнейшего побочного продукта соляную кислоту
Затем для получения соды сульфат смешивали с карбонатом кальция (известняк) и углем и сплавляли в пламенной печи. При этом происходили следующие реакции:
Соду извлекали из охлажденного сплава выщелачиванием водой, в то время как нерастворимый CaS оставался в качестве малоценного отброса. Способ был разработан Лебланом в 1791 г. на премию Французской академии. Вскоре после этого, сначала в Англии, затем в Германии и Франции, развилась содовая промышленность, которая до 1870 г. основывалась исключительно на процессе Леблана. Только в последнее время процесс Леблана был вытеснен рентабельным способом Сольве.
Способ получения соды по Сольве, или аммиачный способ, основан на образовании сравнительно трудно растворимого гидрокарбоната натрия NaHCO3 взаимодействием хлорида натрия с гидрокарбонатом аммония в водном растворе
В технике в почти насыщенный раствор поваренной соли пропускают сначала аммиак, затем двуокись углерода. Образующийся NaHCO3 отфильтровывают и нагреванием (кальцинирование) переводят в Na2CO3 (кальцинированная сода).
При этом выделяется половина первоначально взятой двуокиси углерода, и ее снова направляют в процесс. Чтобы вновь получить NH3, в маточный раствор, из которого осаждали гидрокарбонат, пропускают аммиак и водяной пар. Благодаря этому содержащийся там гидрокарбонат аммония переходит сначала в нейтральный карбонат
и последний при температурах выше 58° разлагается на двуокись углерода, воду и аммиак:
Аммиак, содержащийся в маточном растворе в виде NH4Cl (около 75% общего количества), выделяется оттуда при добавлении известкового молока
так что наряду с непрореагировавшим хлоридом натрия единственным отходом является хлорид кальция, который обычно спускают в реки.
Аммиачный способ получения соды был разработан в техническом отношении в 1863 г. бельгийцем Сольве. При этом способе получается очень чистая сода. Аммиачный способ более эффективен, чем способ Леблана, прежде всего потому, что в этом случае расходуется меньше топлива.
Производство соды из криолита применяют в США, правда, в небольших размерах. Способ основан на том, что криолит Na3AlF6 при нагревании до красного каления с известняком разлагается по реакции
Полученный таким образом алюминат натрия Na3AlO3 разлагают затем водой и двуокисью углерода
Сода, полученная из криолита, отличается особой чистотой.
Сода является одним из важнейших продуктов химической промышленности. В больших количествах ее используют в стекольном и мыловаренном производствах. Она является также исходным продуктом для получения многих других важных соединений натрия, таких, как едкий натр, бура, фосфат натрия, растворимое стекло и др. Большое количество соды употребляют, кроме того, в прачечных, на бумажных фабриках, в красильном производстве, а также для смягчения воды паровых котлов. В домашнем хозяйстве сода применяется как средство для чистки.
Гидрокарбонат натрия, кислый карбонат натрия —«двууглекислый натрий» NaHCO3 представляет собой белый, устойчивый в сухом воздухе порошок с щелочным вкусом (удельный вес 2,2). Его получают пропусканием двуокиси углерода через холодный насыщенный раствор Na2CO3.
Гидрокарбонат натрия получают как промежуточный продукт в способе Сольве. Чтобы получить чистый гидрокарбонат натрия, продукт, загрязненный гидрокарбопатом аммония, растворяют в теплой воде; при охлаждении осаждается чистый гидрокарбонат натрия. Реакцию по уравнению (18) используют в лабораториях для очистки карбоната натрия. Нагреванием примерно до 300° гидрокарбонат можно легко снова перевести в карбонат
Вследствие гидролитического разложения раствор проявляет щелочную реакцию, правда очень слабую. Она обнаруживается лакмусом и метиловым оранжевым, но не обнаруживается (при 0°) фенолфталеином. Гидрокарбонат натрия применяют главным образом в качестве заменителя дрожжей, как медицинское средство для нейтрализации желудочной кислоты (соль Бульриха), а также для приготовления шипучих порошков.
Карбонат калия — поташ — К2СО3. Белая гигроскопичная масса удельного веса 2,30 с температурой плавления 894°, легко растворяется в воде, причем растворение сопровождается разогреванием (9,5 ккал/моль). В 100 г воды при 0° растворяется 105, при 25° 113,5, при 100° 156 г К2СО3. Среди получающихся в твердом состоянии гидратов при обычной температуре устойчив дигидрат К2СО3·2Н2О.
Техническое получение поташа ведут преимущественно двумя путями: 1) карбонизацией калийного щелока, 2) непосредственно из калиевых солей либо Стассфуртским способом, либо, в последнее время, формиатным способом. Наряду с этим поташ получают также из золы мелассы и из золы овечьей шерсти, а в странах, богатых лесом, из древесной золы.
Еще в древние времена было известно моющее действие золы растений, которое связано с присутствием в ней карбоната калия. Получение карбоната калия из древесной золы было известно уже древним грекам и римлянам, однако они не отличали полученную таким образом соль от встречающейся в природе соды. Алхимики готовили чистый карбонат калия прокаливанием виннокаменной соли КНС4Н4О6, а позднее путем сжигания ее с селитрой.
Для получения поташа Леблан разработал способ, совершенно аналогичный его способу получения соды. Долгое время этот способ имел большое техническое значение.
Карбонизация калийного щелока происходит непосредственно вслед за его электролитическим получением при пропускании через него двуокиси углерода
По предложению Харгревса (Hargreaves) двуокись углерода вводят непосредственно в камеру для электролиза, так что там тотчас образуется К2СО3; однако в этом случае поташ трудно отделить от хлорида.
Стассфуртский способ основан на плохой растворимости двойной соли гидрокарбоната калия и карбоната магния. По этому способу двуокись углерода пропускают в раствор хлористого калия, в котором суспендирован MgCO3·3H2O:
Выпадающая труднорастворимая двойная соль разлагается в воде при температуре около 60° с выделением двуокиси углерода
По формиатному способу (способ Гольдшмидта) поташ получают через формиат калия КНСО2, для чего раствор сульфата смешивают в молярном отношении с известковым молоком и эту смесь насыщают окисью углерода при повышенной температуре (около 220°) и давлении 30 ат. Реакция идет по уравнению
в результате чего образуется раствор формиата калия, который после отделения гипса упаривают досуха. Методом окислительного кальцинирования получают затем карбонат по уравнению
Карбонат калия применяют в мыловаренном и стекольном производствах, при крашении, белении и отмывке шерсти. Его используют также для получения цианида калия, а в препаративной химии — часто в качестве воду-отнимающего средства.
Гидрокарбонат калия. Кислый или первичный карбонат калия КНСО3 несколько более трудно растворим, чем нейтральный карбонат калия, но существенно легче растворим, чем гидрокарбонат натрия (а именно 36,1 г КНСО3 в 100 г воды при 26°). Он имеет бесцветные моноклинные кристаллы удельного веса 2,17. При нагревании он распадается так же, как гидрокарбонат натрия:
Карбонаты рубидия и цезия. Rb2CO3 и Cs2CO3 удобнее всего получать взаимодействием сульфатов с гидроокисью бария и последующим упариванием с карбонатом аммония. Обезвоженные прокаливанием соли расплываются на воздухе и растворяются в воде со значительным выделением тепла (8,75, соответственно 11,84 ккал). В спирте карбонат рубидия, так же как другие карбонаты щелочных металлов, незначительно растворим, карбонат цезия, напротив, легко растворим. В 100 г спирта при 19° растворяется 0,74 г Rb2СО3 и 11,1 г Cs2CO3. Это используют для разделения рубидия и цезия. Гидрокарбонаты рубидия и цезия еще лучше растворимы, чем гидрокарбонат калия.
Карбонат лития. Li2CO3 выделяется при смешивании растворов солей лития с растворами, содержащими ионы СО3 2- в виде труднорастворимой в воде и нерастворимой в спирте белой кристаллической соли. Удельный вес его 2,11. Точка плавления 618°.
При техническом получении карбоната лития большей частью исходят из амблигонита LiAl[PO4]F, встречающегося в виде больших залежей в Америке. Его растворяют в горячей концентрированной серной кислоте. Примеси алюминия и железа осаждают добавлением аммиака и сульфида аммония и водную вытяжку смешивают с карбонатом натрия. Выделившийся при этом карбонат лития очищают растворением в соляной кислоте, осаждением примесей серной кислоты хлоридом бария и повторным осаждением соли в виде карбоната. Получение лития из других минералов проводят аналогично, с той только разницей, что вскрытие производят по-другому — например, в случае сподумена LiAl[Si2O6] путем сплавления с содой. Силикаты можно вскрывать также прокаливанием с СаСО3 или с СаО. Для вскрытия трифилина лучше всего применять концентрированную серную кислоту с небольшим добавлением азотной кислоты. Отделение лития от других щелочных металлов можно производить, используя плохую растворимость фосфата в воде или определенную растворимость хлорида в смеси спирта с эфиром.
Карбонат лития лучше растворим в холодной воде, чем в горячей. При нагревании от 0 до 100° растворимость падает от 1,54 до 0,73 ч. Li2CO3 на 100 ч. воды. Растворимость значительно увеличивается при добавлении в воду СО2. Этим иногда пользуются для очистки карбоната. Можно предположить, что в воде, содержащей СО2, образуется гидрокарбонат, так же как в случае щелочноземельных металлов. В твердом состоянии гидрокарбонат лития не получен.
Карбонат лития является исходным продуктом для получения большинства других, солей лития. Ранее его применяли для лечения подагры. Теперь для этой цели используют органические соли лития, такие, как цитрат лития или салицилат лития.