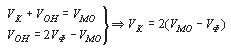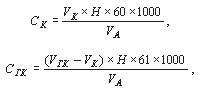Чем нам помогут гидрокарбонатные воды
Польза от употребления минеральных щелочных вод с высоким содержанием гидрокарбонатных ионов (щелочные воды) охватывает широкий спектр проблем со здоровьем. Это и избавление от изжоги, и выведение слизи из желудка, метаболитов и токсинов.
Они эффективны при болезнях желудочно-кишечного тракта: гастритах, колитах и панкреатитах, язвенной болезни и сахарном диабете, дискинезии желчевыводящих путей, хронических заболеваниях желчного пузыря и печени, нарушении обмена веществ и многих других.
Щелочные минеральные воды полезно употреблять и здоровым людям, ведущим активный образ жизни. Минералы и микроэлементы, содержащиеся в воде, проникают в клетки организма. Там они улучшают процесс обмена веществ и метаболизм, не допускают закисления, стабилизируют водный баланс, выводят ионы водорода из организма.
Кишечник
Гидрокарбонаты позволяют связать свободную соляную кислоту в желудке, оказывая, таким образом, антацидный эффект (уменьшение 
Болезни желчного пузыря, желчевыводящих путей, печени
Непосредственно после приема гидрокарбонатные воды стимулирует выделение и секрецию желчи печенью, что способствует вымыванию застоев желчи и очищению желчевыводящих путей и печени, ускоряется восстановление поврежденной ткани печени. Поэтому их применяют при дискинезии желчевыводящих путей, хронических заболеваниях печени и желчного пузыря.
Заболевания мочевыводящих путей
Болезни поджелудочной железы
Гидрокарбонатные воды участвуют в нейтрализации и ощелачивании кислого пищевого содержимого желудка в двенадцатиперстной кишке. Обеспечивают панкреатическому секрету поджелудочной железы щелочную среду, что является одной из задач при ее лечении.
Поддержание гормонального баланса
Сахарный диабет
Высокое содержание гидрокарбонатов благодаря нормализации гормонального баланса, увеличению выработки инсулина и поступлению его в кровь в нужное время (к началу пищеварения) играет существенную роль для предупреждения и при лечении сахарного диабета. Гидрокарбонаты оказывают благоприятное влияние на углеводный и белковый обмен, снижая уровень сахара и холестерина. При нормализаци этих процессов можно уменьшить, а со временем кому-то и отказаться от приема препаратов, понижающих сахар в крови.
Лишний вес
Гидрокарбонатные воды успешно применяются в целях борьбы с лишним весом, включая ожирение, и занимают особое место в предупреждении и лечении этого состояния.
Они оптимизируют гормональные взаимосвязи в организме, оказывают положительное влияние на все виды обмена веществ и функциональные системы человека. Гидрокарбонаты являются «пусковым» средством выработки собственных гормонов во всей пищеварительной системы. Самым главным результатом этого является регулирующее влияние гидрокарбонатых вод на углеводный обмен, который обычно нарушен у людей с лишним весом и при ожирении (как и при сахарном диабете). При этом происходит снижение излишков глюкозы, нормализация холестерина и других «плохих» жиров в организме, способствуя увеличению резервов организма в борьбе с лишним весом и с проявлениями метаболического синдрома. Гидрокарбонатов в воде, необходимой для нормализации веса, должно быть не меньше 1300 мг на литр.
Сердечно-сосудистая система
Сосуды подчиняются головному мозгу и управляются его сигналами. Это управление жестко связано с указаниями иммунной сисетемы и 
Гидрокарбонатные минеральные воды при курсовом приеме значительно увеличивают выработку пищеварительных гормонов. Поэтому, когда минеральная вода, транспортируясь по желудку и кишечнику, попадает в то самое место, где продуцируются эти гормоны, она их активизирует. Эти гормоны ускорят выработку других гормонов, например, инсулина поджелудочной железой, то есть возникает мощнейшая перестройка гормонального аппарата, что непосредственно воздействует на первооснову не только ССЗ, но и многих других заболеваний.
Прочие воздействия
Нормализация выработки пищеварительных гормонов в результате приема гидрокарбонатных вод не только ускоряет производство инсулина и восстанавливает ритм его поступления. Пищеварительные гормоны регулируют кроветворение и влияют на активность структур головного мозга, контролируют голод и сытость, передают информацию о степени переваривания пищи. То есть, несут ответственность практически за все обменные процессы организма.
Именно в оптимизации обмена веществ проявляются лечебные эффекты таких вод при многих заболеваниях (сахарном диабете, большинстве заболеваний сердечно-сосудистой системы, ожирения, гипертонии, органов пищеварения), а также профилактическое воздействие на организм. Достоверно увеличивается стойкость организма человека к повреждающему действию стрессорных факторов различной природы.
Водами – рекордсменами по содержанию гидрокарбонатов являются: «Donat Mg» (около 8000 мг/л), «Sulinka» (около 5000 мг/л), ЙОДИКА (3200-3700 мг/л). Значительное количество гидрокарбонатов присутствует также в водах «Sulinka Si» (1400-2400мг/л), «Stelmas Mg» (2200-2500 мг/л).
Уважаемые читатели!
Спасибо, что читаете наш блог! Получайте самые интересные публикации раз в месяц оформив подписку. Новым покупателям при первом заказе дарим 12 бутылок (2 упаковки) минеральной воды BioVita или питьевой воды Stelmas. Операторы свяжутся с Вами и уточнят детали. Тел. 8 (800) 100-15-15
* Акция для Москвы, МО, Санкт-петербурга, ЛО
Гидрокарбонаты в питьевой воде
Гидрокарбонаты в питьевой воде – это компоненты, определяющие ее щелочность. Их содержание в воде объясняется несколькими процессами:
Гидрокарбонаты в питьевой воде уменьшают количество водородных ионов, приводят к уменьшению кислотности и повышению щелочности. Благодаря высокой концентрации гидрокарбонатов некоторые минеральные воды могут использоваться для лечения гастритов и повышенной кислотности желудочного сока. В умеренных концентрациях гидрокарбонат-ионы необходимы качественной питьевой воде для поддержания нормальной щелочности, оптимального значения рН и приемлемых органолептических характеристик.
Зачем насыщать воду гидрокарбонатами
Гидрокарбонаты в воде нужны для того, чтобы корректировать водородный показатель pH воды и улучшить ее вкусовые свойства. Если щелочность низкая, уровень pH будет нестабилен вследствие низкой буферной емкости такой воды. Низкая (практически нулевая) щелочность и пониженные уровни рН характерны, в частности, для воды после очистки обратным осмосом.
Гидрокарбонаты в воде (природной) – это прежде всего соли кальция и магния (гидрокарбонаты этих элементов существуют только в растворенном состоянии). При нагреве и кипячении растворенные гидрокарбонаты элементов жесткости частично перейдут в нерастворимые карбонаты, и вода станет мягче.
При необходимости (например, после обратного осмоса) гидрокарбонаты в воде можно повысить, используя специально разработанные для этого модификации минеральной добавки «Северянка Бикарбонат». Помимо повышения щелочности питьевой воды и коррекции рН, эта добавка улучшает её вкусовые качества.
Гидрокарбонаты
Гидрокарбонаты щелочных металлов в воде растворимы. Также в воде хорошо растворимы гидрокарбонаты щелочноземельных металлов, в отличие от карбонатов.
Содержание
Получение
Гидрокарбонат натрия плохо растворим в холодной воде, поэтому его можно отделить от хлорида аммония фильтрованием.
Химические свойства
В итоге раствор гидрокарбонатов имеет щелочную реакцию.
Применение
Гидрокарбонат натрия (сода) используется в производстве искусственных минеральных вод и заправки огнетушителей, в кондитерском деле и хлебопечении, в быту, в медицине.
Физиологическое действие
Литература
Примечания
См. также
Полезное
Смотреть что такое «Гидрокарбонаты» в других словарях:
ГИДРОКАРБОНАТЫ — (бикарбонаты) кислые соли угольной кислоты Н2СО3, напр., питьевая сода NаНСО3 … Большой Энциклопедический словарь
гидрокарбонаты — – кислые соли угольной кислоты. Словарь по аналитической химии [3] … Химические термины
гидрокарбонаты — (бикарбонаты), кислые соли угольной кислоты Н2СО3, например питьевая сода NaHCO3. * * * ГИДРОКАРБОНАТЫ ГИДРОКАРБОНАТЫ (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр., питьевая сода NаНСО3 … Энциклопедический словарь
Гидрокарбонаты — бикарбонаты, двууглекислые соли, кислые соли угольной кислоты (См. Угольная кислота) H2CO3, например NaHCO3 (Гидрокарбонат натрия). Г. получают действием CO2 на карбонаты или гидроокиси в присутствии воды. При нагревании они превращаются… … Большая советская энциклопедия
ГИДРОКАРБОНАТЫ — (от гидро. и карбонаты) кислые соли угольной к ты H2CO3; Г. натрия NaHCO3 питьевая сода … Большой энциклопедический политехнический словарь
ГИДРОКАРБОНАТЫ — (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр. питьевая сода NaHCO3 … Естествознание. Энциклопедический словарь
гидрокарбонаты — гидрокарбон аты, ов, ед. ч. н ат, а … Русский орфографический словарь
гидрокарбонаты — мн., Р. гидрокарбона/тов; ед. гидрокарбона/т (2 м) … Орфографический словарь русского языка
Минеральная вода — Минеральные воды воды, содержащие в своем составе растворённые соли, микроэлементы, а также некоторые биологически активные компоненты. Среди минеральных вод выделяют минеральные природные питьевые воды, минеральные воды для наружного… … Википедия
Природные воды и их основной состав. Часть II
Природные воды представляют собой сложную многокомпонентную систему, в чей химический состав входит комплекс минеральных и органических веществ в разных формах ион-молекулярного и коллоидного состояния.
Качественный состав природных вод
Л.А. Кульский предложил классифицировать примеси, основываясь на их фазовом состоянии и дисперсности:
Выделим наиболее основные на наш взгляд примеси и рассмотрим их влияние на свойства воды.
Главнейшие ионы
В зависимости от преобладающего аниона О.А. Алекин предложил классифицировать природные воды на три больших класса:
Каждый класс по преобладающему катиону разделяют на три группы:
В свою очередь в группах различают три типа вод:
Превышение ионов Na + над ионами K + объясняется высоким поглощением калия почвами и извлечением его растениями из воды.
Ионы Ca 2+ и Mg 2+ по большей степени обуславливают жесткость воды, которая не должна превышать 7 мг-экв./л.
В поверхностных водах средней полосы России содержится от 0,1 до 1мг/л железа и от 0 до 0,05 мг/л марганца, в подземных же водах содержание железа часто превышает 15 – 20 мг/л, концентрация марганца колеблется в пределах 0,5 – 3 мг/л.
Бор. При концентрации в питьевой воде выше 0,5 мг/л негативно воздействует на организм человека, ухудшая обмен веществ, вызывая заболевание печени и желудочно-кишечного тракта.
Бром. При концентрации в питьевой воде выше 0,2 мг/л снижает скорость импульса по нервным волокнам, что отрицательно сказывается на функции печени и почек, обуславливает снижения калия в крови и увеличивает содержание азота в мочевине.
Нитраты и нитриты. Нитраты содержатся в основном в поверхностных водах (0,001 – 0,003 мг/л), нитриты (десятые доли миллиграммов в литре) – в артезианских. При употреблении воды с содержанием нитратов свыше 45 мг/л в организме человека синтезируются нитрозамины, способствующие образованию злокачественных опухолей, перерастающих в рак желудка, у детей возникает нарушение окислительной функции крови. ПДК нитрит-иона не должна превышать 3 мг/л.
Очистку воды от нитратов осуществляют на колонных анионитовых фильтрах с использованием в качестве фильтрующей среды высокоосновную анионообменную смолу А520Е
Кремний. В природных водах присутствует в виде ионов, молекул и коллоидных частичек. Форма кремниевой кислоты в сильной степени зависит от ее ионного состава и значения pH.
Содержание кремния в природных водах колеблется от 0,6 – 40 мг/л и лишь в исключительных случаях может превышать 65 мг/л. Кремниевая кислота не представляет опасности для здоровья, но повышенное ее содержание делает воду непригодной для подпитки паровых котлов вследствие образования силикатной накипи. По санитарным правила концентрация кремния не должна превышать 10 мг/л.
Для исключения образования силикатной накипи на поверхностях трубопроводов и аппаратов в промышленных установках обессоливания воды в качестве фильтрующей загрузки рекомендуется применять сильноосновный анионит Purolite A400
Повышенное содержание хлоридов и сульфатов обуславливает коррозийную активность воды, некарбонатную жесткость, разрушающе воздействует на железобетонные конструкции.
Соединения фосфора. Встречаются в виде ионов ортофосфорной кислоты, сложных органических комплексов, суспендированных частиц минерального и органического происхождения. В природных водах концентрация соединений фосфора довольно мала, но их присутствие в сильной степени оказывает влияние на водную растительность. Для питьевой воды концентрация фосфора элементарного должна составлять не более 0,0001 мг/л.
Фтор. В артезианских скважинах содержание фтора не превышает 12 мг/л, в природных водах, как правило, не более 0,5 мг/л фтор-иона. Фтор является биологически активным микроэлементом, концентрация которого в питьевой воде не должно превышать 0,7 – 1,5 мг/л во избежание развития кариеса или флюороза зубов.
Йод. Содержание данного элемента довольно мало, но вследствие его высокой биологической ценности должно быть не менее 10-8 мг/л в питьевой воде.
Стронций. При концентрации свыше 7 мг/л вызывает ломкость костей, рахит.
Кадмий. При концентрации свыше 0,001 мг/л вызывает болезнь «Итай-итай».
Ртуть. При концентрации свыше 0,0005 мг/л вызывает болезнь Минамата.
Цинк. При концентрации свыше 5 мг/л угнетает окислительные процессы в организме, вызывает анемию.
Молибден. При содержании свыше 0,25 мг/л вызывает подагру и молибденувую болезнь.
Медь. При содержании свыше 1 мг/л вызывает заболевание печени, анемию, гепатит.
As, Be, Cu, Mo, Pb, Se, Sr, Zn и др. Эти элементы относятся к ядовитым и в природных водах встречаются крайне редко. Как правило, их попадание в водоемы и реки вызвано промышленной деятельностью человека и ведет к серьезным негативным последствиям для живых организмов, как населяющих эти воды, так и питающихся из них.
Кислород, оксид углерода, сероводород. Удаление этих газов происходит в основном при использовании воды в котлах, т.к. они обуславливают коррозийные свойства воды.
Кислород попадает в воду при контакте с воздухом. В поверхностных водах концентрация кислорода меньше теоретического за счет потребления его различными организмами, процессов брожения и гниения органических остатков. Низкое же содержание кислорода в поверхностных водах указывает на их повышенную загрязненность. В артезианских водах он отсутствует.
Азот. Попадает в воду из воздуха, при разложении органических остатков, а также при восстановлении соединений азота денитрифицирующими бактериями. За счет высокого парциального давления концентрация азота в воде сильно превышает концентрацию кислорода. Образующийся в процессе гниения аммиак существенно оказывает влияние на технологию хлорирования воды.
Метан. В природных водах его концентрация не значительна, но в подземных водах газонефтеносных районов и в болотных водах его содержание доходит до 50 мг/л. При концентрации метана в воздухе 5,3 – 14 % создается взрывоопасная ситуация.
Оксид углерода IV. В поверхностных водах концентрация углекислого газа находится в пределах 20 – 30 мг/л, в подземных не минерализованных водах – 90 мг/л. В подземных водах он появляется в результате процессов разложения органических соединений и биохимических процессов.
Сероводород, H2S. Его присутствие характерно для подземных источников, где он образуется в результате процессов разложения и восстановления некоторых минеральных солей (гипса, серного колчегана и пр.). Вследствие способности легко окисляться, в поверхностных водах сероводород практически не встречается. Появление же его в поверхностных источниках может быть вызвано протеканием гнилостных процессов или сброса неочищенных сточных вод.
Сероводород придает воде неприятный запах, ощутимый при его концентрации от 0,5 мг/л, а также вызывает процесс коррозии и размножению серобактерий. Санитарными правилами концентрация сероводорода должна быть не более 0,003 мг/л.
Взвешенные вещества
Появляются в воде в результате смыва твердых частичек песка, глины, илистых веществ с верхнего покрова земли талыми водами весенних и осенних паводков, а также дождями и водами разлившихся рек и ручьев.
Повышение мутности воды может быть вызвано выделением гидроксидов алюминия, марганца, железа (III), высокомолекулярных органических примесей гумусового происхождения, сбросом неочищенных сточных вод.
Взвешенные вещества различаются по своему гранулометрическому составу. Для питьевой воды мутность должна составлять не более 1,5 мг/л.
Удаление из воды взвешенных веществ проходит на колонных осветлительных фильтрах, а сам процесс называется осветлением. В качестве фильтрующей среды для осветления воды используют песок, угль и другие засыпки.
Органические вещества
Наиболее значительными поставщиками органических веществ в природные воды являются почвенный и торфяной гумус, продукты жизнедеятельности и разложения растительных и животных организмов, сточные воды промышленных предприятий.
Наиболее сильно окрашивают воду гумусовые вещества, придающие ей оттенки желтого или бурого цветов. Они представляют собой высокомолекулярные соединения, содержащие плоские сетки циклически полимеризованного углерода с атомами H, O и др. и функциональными группами – OH, – COOH. Гумусовые вещества разделяются на гуминовые, ульминовые, креновые, апокреновые (фульвокислоты) и прочие кислоты, а также их растворимые в воде соли.
Наибольшую угрозу для водоемов с точки зрения загрязнения органическими веществами представляют неочищенные стоки промышленных предприятий, в состав которых могут входить белки, жиры, углеводы, органические кислоты, эфиры, спирты, фенолы, нефть и др.
Гидробионты
В процессе жизнедеятельности влияют как на состав окружающей среды, так и на качество воды.
Гидрофлора водоема
Определяется макрофитами (высшая водная растительность) и микрофитами ( водоросли – фитопланктон и фитобентос). При отмирании и разложении макрофитов вода обогащается органическими веществами, появляется запах, ухудшаются органолептические свойства воды.
Бактерии и вирусы
Из тех, кто является патогенными, т.е. паразитами, живущими на живом субстрате, могут вызвать заболевания брюшным тифом, парафитом, дизентерией, гепатитом и прочими малоприятными заболеваниями.
При биологическом анализе определение патогенных бактерий затруднено, то при бактериологическом анализе воды выявляют общее число бактерий в 1 мл воды, растущих при 37 0 C, и кишечных палочек – бактерий коли, наличие которых свидетельствует о загрязнении воды выделениями людей и животных.
Что бы исключить возможность попадания в питьевую воду различных бактерий и вирусов мы рекомендуем комплексно очищать и обеззараживать воду применяя современные системы очистки воды для бытовых и питьевых нужд.
Hco3 что это в воде
Как отмечалось выше (в разделе «Щелочность и кислотность»), карбонаты и гидрокарбонаты представляют собой компоненты, определяющие природную щелочность воды. Их содержание в воде обусловлено процессами растворения атмосферной СО2, взаимодействия воды с находящимися в прилегающих грунтах известняками и, конечно, протекающими в воде жизненными процессами дыхания всех водных организмов.
Определение карбонат- и гидрокарбонат-анионов является титриметрическим и основано на их реакции с водородными ионами в присутствии фенолфталеина (при определении карбонат-анионов) или метилового оранжевого (при определении гидрокарбонат-анионов) в качестве индикаторов. Используя эти два индикатора, удается наблюдать две точки эквивалентности: в первой точке (рН 8,0–8,2) в присутствии фенолфталеина полностью завершается титрование карбонат-анионов, а во второй (рН 4,1–4,5) – гидрокарбонат-анионов. По результатам титрования можно определить концентрации в анализируемом растворе основных ионных форм, обуславливающих потребление кислоты (гидроксо-, карбонат- и гидрокарбонат-анионов), а также величины свободной и общей щелочности воды, т.к. они находятся в стехиометрической зависимости от содержания гидроксил-, карбонат- и гидрокарбонат-анионов. Для титрования обычно используют титрованные растворы соляной кислоты с точно известным значением концентрации – 0,05 моль/л либо 0,1 моль/л.
Определение карбонат-анионов основано на реакции:
Присутствие карбонат-аниона в концентрациях, определяемых аналитически, возможно лишь в водах, рН которых более 8,0–8,2. В случае присутствия в анализируемой воде гидроксо-анионов при определении карбонатов протекает также реакция нейтрализации:
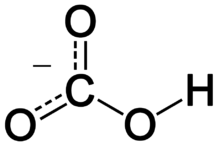
Определение гидрокарбонат-анионов основано на реакции:
Величина карбонатной жесткости рассчитывается с учетом эквивалентных масс участвующих в реакциях карбонат- и гидрокарбонат-анионов.
При анализе карбонатных природных вод правильность получаемых результатов зависит от величины потребления кислоты на титрование по фенолфталеину и метилоранжу. Если титрование в присутствии фенолфталеина обычно не вызывает трудностей, т.к. происходит изменение окраски от розовой до бесцветной, то в присутствии метилового оранжевого, при изменении окраски от желтой до оранжевой, определить момент окончания титрования иногда довольно сложно. Это может привести к значительной ошибке при определении объема кислоты, израсходованной на титрование. В этих случаях, для более четкого выявления момента окончания титрования, определение полезно проводить в присутствии контрольной пробы, для чего рядом с титруемой пробой помещают такую же порцию анализируемой воды (во второй склянке), добавляя такое же количество индикатора.
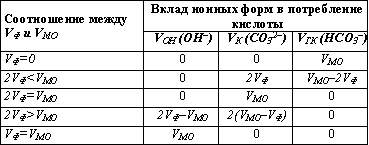
В результате титрования карбоната и гидрокарбоната, которое может выполняться как параллельно в разных пробах, так и последовательно в одной и той же пробе, для расчета значений концентраций необходимо определить общее количество кислоты в миллилитрах, израсходованной на титрование карбоната (VK) и гидрокарбоната (VГК). Следует иметь в виду, что при определении потребления кислоты на титрование по метилоранжу (VМО) происходит последовательное титрование и карбонатов, и гидрокарбонатов. По этой причине получаемый объем кислоты VМО содержит соответствующую долю, обусловленную присутствием в исходной пробе карбонатов, перешедших после реакции с катионом водорода в гидрокарбонаты, и не характеризует полностью концентрацию гидрокарбонатов в исходной пробе. Следовательно, при расчете концентраций основных ионных форм, обуславливающих потребление кислоты, необходимо учесть относительное потребление кислоты при титровании по фенолфталеину (VФ) и метилоранжу (VМО). Рассмотрим несколько возможных вариантов, сопоставляя величины VФ и VМО.
VФ = 0. Карбонаты, а также гидроксо-анионы в пробе отсутствуют, и потребление кислоты при титровании по метилоранжу может быть обусловлено только присутствием гидрокарбонатов.
VФ
VФ = VМО. В исходной пробе отсутствуют и карбонаты, и гидрокарбонаты, и потребление кислоты обусловлено присутствием сильных щелочей, содержащих гидроксо-анионы.
Присутствие свободных гидроксо-анионов в заметных количествах (случаи 4 и 5) возможно только в сточных или загрязненных водах.
Массовые концентрации анионов (не солей!) рассчитываются на основании уравнений реакций потребления кислоты карбонатами (СК) и гидрокарбонатами (СГК) в мг/л по формулам:
где:
VК и VГК – объем раствора соляной кислоты, израсходованный на титрование карбоната и гидрокарбоната соответственно, мл;
Н – точная концентрация титрованного раствора соляной кислоты (нормальность), моль/л экв.;
VА – объем пробы воды, взятой для анализа, мл;
60 и 61 – эквивалентная масса карбонат- и гидрокарбонат-аниона соответственно, в соответствующих реакциях;
1000 – коэффициент пересчета единиц измерений.
Результаты титрования по фенолфталеину и метилоранжу позволяют рассчитать показатель щелочности воды, который численно равен количеству эквивалентов кислоты, израсходованной на титрование пробы объемом 1 л. При этом потребление кислоты при титровании по фенолфталеину характеризует свободную щелочность, а по метилоранжу – общую щелочность, которая измеряется в ммоль/л. Показатель щелочности используется в России, как правило, при исследовании сточных вод. В некоторых других странах (США, Канаде, Швеции и др.) щелочность определяется при оценке качества природных вод и выражается массовой концентрацией в эквиваленте СаСО3.
Следует иметь в виду, что, при анализе сточных и загрязненных природных вод, получаемые результаты не всегда корректно отражают величины свободной и общей щелочности, т.к. в воде, кроме карбонатов и гидрокарбонатов, могут присутствовать соединения некоторых других групп (см. «Щелочность и кислотность»).
Оборудование и реактивы
Пипетка на 2 мл или на 5 мл, мерный шприц с наконечником и соединительной трубкой; пипетка-капельница; склянка с меткой «10 мл».
Раствор индикатора метилового оранжевого (0,1%) водный; раствор индикатора фенолфталеина; раствор соляной кислоты титрованный (0,05 моль/л).
Приготовление растворов см. приложение 3.
Выполнение анализа
А. Титрование карбонат-аниона
 |
 |