Гафниоз (паратиф) пчел

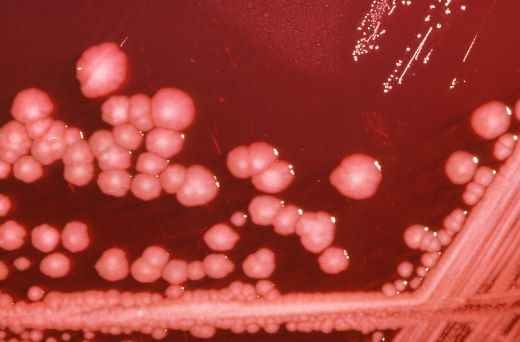
Возбудитель болезни — Hafnia alvei (синоним — Bacterium paratyphi alvei) — маленькая, с закругленными концами полиморфная палочка, длиной 1—2 мкм и шириной 0,3—0,5 мкм. Спор не образует, подвижная, растёт на всех обычных питательных средах слабощелочной реакции.
Бактерия Hafnia alvei отличается от собственно паратифозных бактерий тем, что она при 20° приобретает подвижность, а при 37° подвижность отсутствует, при 20° C она обладает газообразованием, а при 37° C — нет, при 20° C расщепляет цитрат аммония, а при 37° C — нет.
К термическим и химическим воздействиям устойчивость слабая. Кипячение в воде убивает микроб в течение одной-двух минут, при нагревании до 58—60° C — в течение 30 минут.
Этиология. Микроб поражает пчёл и ос. Весной, после выставки семей из зимних помещений, гафниоз распространяется от больных семей к здоровым при перестановке сотов, блуждании пчёл, при пользовании общей поилкой.
Клинические признаки. Инкубационный период болезни длится 3—14 дней, смертность достигает 50— 60%. Болезнь протекает обычно в конце зимы или весной, редко — летом после похолоданий и дождей. Развитию болезни зимой способствуют закисший жидкий мёд и сырость в ульях. Чаще болеют рабочие пчёлы.
Гафниоз не имеет характерных внешних признаков. Скованность в движениях больных пчёл, паралич крыльев, слабость и понос представляют собой признаки, встречающиеся и при других заболеваниях. Больные пчёлы слабеют, ползают с раздутым брюшком у летка или на дне улья, теряют способность летать. Появляются понос, ослабление дыхательных движений, иногда паралич ножек.
В острой форме заболевание протекает с большим отходом пчёл. При весеннем облете пчёлы выделяют много зловонных, очень клейких или полужидких каловых масс тёмно-бурого цвета. Весенний облёт не дружный. При осмотре ульев обычно находят достаточные запасы корма, но все соты испачканы экскрементами в виде бурых клейких или жидких масс. При вскрытии больных пчёл кишечник вздут и имеет грязно-белый или светло — серый цвет.
Диагноз. Его ставят на основании бактериологического и серологического исследований чистых культур в лабораторных условиях.
Меры борьбы. Пчёлам необходимо создать максимально комфортные условия, что ведёт к прекращению болезни. При значительной гибели пчёл их кормят троекратно с недельным интервалом 50%-ным сахарным сиропом с добавлением на 1 литр сиропа одного из следующих антибиотиков: левомицетина 0,2 гр., стрептомицина 200 тыс. ЕД или биомицина 100 тыс. ЕД.
Семейство Enterobacteriaceae. Часть 1
Автор: врач – клинический фармаколог Трубачева Е.С.
.jpg)
Автор: врач – клинический фармаколог Трубачева Е.С.
Morganella spp. и Proteus spp.
Особо выдающихся представителей семейства Enterobacteriaceae мы уже разбирали в отдельных статьях, а именно представительницу рода Esherichia — кишечную палочку E.coli, а также одну из представительниц клебсиелл — Klebsiella pneumonia. В ближайших статьях мы постараемся осветить все оставшееся семейство, как, во-первых, одно из самых проблемных в плане развития резистентности к антимикробным препаратам, а во-вторых — как возбудителей, наиболее часто являющихся причиной внутрибольничных инфекций.
Микробиологические аспекты
Основными клинически значимыми представителями родов семейства Enterobacteriaceae, вызывающими заболевания у человека, являются:
Естественно совсем уж экзотику мы рассматривать не станем, но по наиболее часто встречающимся представителям обязательно пробежимся.
Клинические аспекты
Почему данное семейство так актуально? Наверное, потому, что почти ни одна нозология не обходится без его представителей. В самом широком смысле семейство Enterobacteriaceae является причиной следующих заболеваний:
Как мы видим, наши знакомые отметились практически везде. Но надо обязательно помнить, что выявление вышеуказанных представителей у здоровых людей из респираторного тракта, урогенитального и уж тем более желудочно-кишечного ни в коем случае не говорит о том, что человек чем-то болен, так как в большинстве своем эти микробы являются представителями нормальной микрофлоры, а не все люди умеют мыть руки, особенно летом.
Когда можно думать о наличии бактериальной патологии? Во-первых, когда имеется четкая клиника, во-вторых, когда микробы выделены из стерильных в норме сред, таких как кровь и ликвор, брюшная или плевральная полость, точнее, экссудат оттуда и, в-третьих, когда микроорганизмы выделены в клинически значимых концентрациях (тут в помощь будет ваша бак. лаборатория).
Стоит отметить еще один немаловажный момент — не все представители семейства Enterobacteriaceae умеют жить вне организма человека, и поэтому не размножаются во внешней среде, а потому обнаружение оных на пищевых продуктах и всевозможных поверхностях в лечебных учреждениях говорит о фекальном загрязнении, проще говоря, о неумении обрабатывать руки после посещения туалетной комнаты. Одним из таких микробов-детекторов является кишечная палочка, и стоит ее поймать даже не на руках персонала, а, например, на компьютерной мышке, как дальше можно уже ничего не искать, а начинать очередной этап избиения младенцев, пардон, обучения правилам асептики и антисептики, в частности, обработки рук.
Но давайте перейдем к частностям — и первым микроорганизмом, который будем сегодня рассматривать, станет:
Morganella spp.
Зверюшка названа так в честь своего первооткрывателя Гарри Р. Моргана.
Начнем традиционно с микробиологических аспектов
Семейство морганелл включает единственный вид M. morganii, включающий два подвида M. morganii и M. sibonii, которые различаются только ферментацией трегалозы.
Морганеллы являются представителями нормальной микрофлоры как человека, так и животных, а потому могут присутствовать в качестве сапрофитов в окружающей (внебольничной!) среде.
Морганеллы имеют довольно сложные отношения с антибактериальными препаратами и обладают природной резистентностью к:
Проявляют высокую чувствительность к:
Клинические аспекты
Как говорилось выше, морганеллы являются частью нормальной микрофлоры человека, крайне редко вызывая инфекционные заболевания. Чаще всего они являются возбудителями осложненных инфекций мочевыводящих путей.
Факторами риска развития инфекции являются:
В качестве механизмов резистентности морганеллы способны продуцировать бета-лактамазы, чем и объясняется их природная устойчивость к пенициллинам и цефалоспоринам 1-2 поколений. При нерациональном использовании антибиотиков они начинают вырабатывать бета-лактамазы расширенного спектра и факторы устойчивости к фторхинолонам, которыми довольно бодро делятся с соседями по семейству Enterobacteriaceae. Отдельно стоит отметить способность отдельных штаммов морганелл к резистентности к имипенему.
Какие заболевания вызывают чаще всего:
Терапевтические аспекты
Антибактериальная терапия будет полностью зависеть от результата из микробиологической лаборатории. Повторимся еще раз, микроб изначально умеет вырабатывать бета-лактамазы, а потому в случае развития осложненных инфекции мочевыводящих путей, которые чаще всего уже не связанны с кишечной палочкой, препаратами выбора становятся карбопенемы (имипенем, если штамм к нему чувствителен, или меропенем), дозирование которых проводится с учетом клиренса креатинина. Длительность лечения должна быть не менее 7 дней. В качестве альтернативы можно использовать цефалоспорин 4-го поколения Цефипим каждые 8 часов или фторхинолоны.
Аминогликозиды, несмотря на чувствительность к оным, при лечении заболеваний мочевыводящих путей лучше не применять в виду их нефро- и отоксичности, и по этой же причине их невозможно будет использовать около трех месяцев после проведенной терапии, например, в лечении синегнойной инфекции. Цефалоспорины третьего поколения тоже применять не стоит, так как морганеллы довольно быстро обзаводятся бета-лактамазами расширенного спектра, которые, как мы помним, эту генерацию препаратов быстро инактивируют.
Proteus spp.
Микробиологические аспекты
Протей долгое время был практически родным отцом морганеллы, так как последняя рассматривалась как один из видов рода протей. Этот род примечателен тем, что занимает почетное второе место по выявляемости после кишечной палочки в семействе Enterobacteriaceae.
В данный момент представителями рода протей являются P. mirabilis, вызывающий порядка 90% инфекционных заболеваний, а также P. vulgaris и P. penneri.
Клинические аспекты
Протеи выступают возбудителями порядка 10% неосложненных инфекций мочевыводящих путей, с чем могут быть связаны неудачи в лечении последних с использованием аминопенициллинов.
Как и все клинически значимые возбудители семейства Enterobacteriaceae, протей является возбудителем нозокомиальных инфекций, таких как пневмония, вплоть до сепсиса. Кроме того выступает возбудителем интраабдоминальных, а также хирургических инфекций кожи и мягких тканей, сепсиса, связанного с медицинскими вмешательствами как последствий нозокомиальной пневмонии в результате недостаточной дезинфекции, например, бронхоскопов.
Таким образом, мы видим, что, как и в предыдущем случае, проще правильно помыть руки и обработать инструменты, чем лечить это все с учетом природной и приобретенной резистентности.
Терапевтические аспекты
Как и в случае с морганеллой, нам просто необходим результат микробиологического исследования с определением чувствительности по МПК возбудителя либо результаты микробиологического мониторинга, которые помогут предположить зверей в случае неудачи ранее проводимого лечения.
В случае ампициллин-чувствительного P.mirabilis именно ампициллин может выступать препаратом первой линии. Кроме того, возможно использование цефуроксима и фторхинолонов. Обязательным аспектом лечения является его длительность. В случае неосложненных инфекций мочевыводящих путей (цистита) — не менее 3 дней, пиелонефрита — 10–14 дней, осложненных инфекций — 10–21 день. Сепсис является состоянием, требующим индивидуального подхода, но лечим не менее 14 дней.
На этом на сегодня мы закончим, но повторим одну базовую и, чего уж, наиважнейшую истину: в лечении инфекций, связанных с любым представителем семейства Enterobacteriaceae, самым главным будет являться профилактика. А именно правильное и тщательное мытье рук. Обеспечим мытье рук, не будет большинства проблем с инфекциями, вызванными указанным семейством.
Нейссерии
Автор: врач – клинический фармаколог Трубачева Е.С.
Автор: врач – клинический фармаколог Трубачева Е.С.
В роду нейссерий присутствуют всего два вида патогенных микроорганизмов — N. meningitidis, он же менингококк, и N. gonorrhoeae, он же гонококк. Все остальные нейссерии являются представителями нормальной микрофлоры человека, обитающей на слизистых оболочках верхних дыхательных путей и урогенитального тракта. Кроме того, носительство этих микроорганизмов распространено и среди теплокровных животных.
Микробиологические аспекты
Основными представителями рода нейссерий являются:
Все нейссерии являются типичными аэробными грамотрицательными кокками, неподвижными, образующими пары или тетрады. Не обладают свойством спорообразования, но менингококк, например, умеет образовывать капсулу. Малоустойчивы во внешней среде, быстро гибнут при высыхании, убиваются практически любым дезинфектантом, и хотя бы с этими микробами у нас почти отсутствует проблема внутрибольничного инфицирования. Правда, ключевое слово «все-таки», «почти», ибо люди остаются людьми, и пациенты не исключение. Но все это, конечно, не касается менингококка, который, в прямом смысле, умеет летать от человека к человеку, передаваясь воздушно-капельным путем, а также через общую вентиляцию, и еще пару лет назад был одним из очень немногих микроорганизмов, которые заставляли надевать СИЗ и сидеть в карантине. О менингококке мы будем говорить отдельно, а сейчас продолжим об общих свойствах всего рода нейссерий.
Практически все представители рода обладают природной чувствительностью к:
бета-лактамам (пенициллинам и цефалоспоринам)
И проявляют природную устойчивость к:
Клинические аспекты:
Зачем вообще стоит знать о непатогенных нейссериях?
Во-первых, мы не знаем, что еще принесет доставший всех до печенок ковид и схемы антибактериальной терапии, которые используются в его лечении, в том числе при отсутствии вторичных бактериальных осложнений (автор в очередной раз изобразил двойной фейспалм, но понимает, почему все это происходит — начиная с пресловутых «временных клинических рекомендаций», которые все-таки стали требовать подтверждения присоединения бактериальной инфекции, и заканчивая внутрибольничными инфекциями, которые никуда не делись, потому что к их распространению есть вполне объективные причины, первой и главной из которых автор видит банальную вымотанность до степени проф. выгорания, и тут хоть обвизжись на тему чистоты рук — без нормально выстроенного режима, в том числе отдыха, эпиднадзор в больничных отделениях просто физически недостижим).
Во-вторых, для нейссерий характерна колонизация слизистых, особенно в детском возрасте, когда в зеве ребенка может определяться до двух видов одномоментно, а при детских тонзиллитах нейссерия вырастет практически в 100% случаев, естественно, в ассоциации с другими патогенами, например, со стрептококком. С возрастом носительство снижается, и к совершеннолетию эти микробы будут выделяться не чаще чем в 2% случаев.
В-третьих, у иммунокомпрометированных пациентов (ВИЧ, онкогематология, ковид, точнее, последствия его лечения и т. п.) нейссерии могут вызывать сепсис, пневмонии, менингиты и т. д., и сбрасывать их со счетов сразу, как возможный контаминат, у такой категории пациентов все-таки не стоит.
Теперь приступим к подробному рассмотрению патогенных представителей нейссерий и начнем с гонококка, он же
Neisseria gonorrhoeae
Гонококк является одним из наиболее проблемных микробов в мире и в плане распространенности, и в плане антибиотикорезистентности. Тому есть очень много причин, в том числе и связанных с медицинской помощью, когда однодневные схемы применения антибиотиков, порочные по своей сути, но используемые в странах, имеющих большие проблемы с доступностью медицинской помощи, потащили их туда, где этих проблем нет. Странно, что те же люди, кто прославлял однодневное применение цефтриаксона, практикуемое в странах экваториальной Африки, отказываются пить профильтрованную через салфетку воду из лужи, что практикуется там же.
Микробиологические аспекты
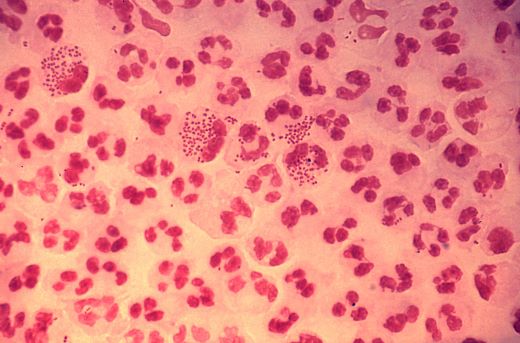
Гонококк относится к грамотрицательным диплококкам, требовательным к своему культивированию, а именно к таким факторам, как температура и pH среды, и лучше всего растущим на кровяных и шоколадных агарах, так как на обычных средах расти не способен. Умеет образовывать капсулоподобные структуры. Является абсолютным паразитом, так как использует для своей жизнедеятельности вещества из организма человека. При этом неустойчив во внешней среде и, например, при кипячении погибает мгновенно. Любой дезинфектант убивает его также очень быстро.
Клинические аспекты
Гонококки могут инфицировать конъюнктиву, ротоглотку, уретру, цервикальный канал, сначала прикрепляясь к эпителиальным клеткам, а затем проникая внутрь. В месте внедрения образуется острый воспалительный процесс в классическом случае (которого вы можете и не увидеть, так как пациент успел наесться «таблеток из Интернета»), сопровождающийся большим количеством гнойного отделяемого. Далее процесс распространяется как в глубину, так и по поверхности пораженных слизистых оболочек, и без адекватного лечения переходит в хроническую форму. Кроме того, часть гонококков умеет поражать и выживать внутри фагоцитирующих клеток и, таким образом мигрируя внутри организма, забирается в самые отдаленные его отделы, то есть диссеминирует и маскируется вообще подо что угодно.
Что поражается чаще всего:
Уретра, вызывая уретриты
Цервикальный канал, вызывая цервициты
Эндометрий, вызывая эндометриты
Глиссонову капсулу печени
Диссеминированные формы — поражение кожи, суставов, септические артриты, миокардиты, менингиты и т. д.
Существуют бессимптомная и манифестирующая формы гонококковой инфекции, расшифровка коих особого смыла не имеет, так как все понятно по названию.
У мужчин обычно появляется симптоматика уретрита, но до четверти случаев течет совершенно бессимптомно, а эпидидимит является наиболее частым осложнением гонорейной инфекции. Более редкими осложнениями являются стриктуры уретры и простатит.
У женщин в половине случаев гонорейная инфекция носит бессимптомный характер, особенно при инфицировании ротоглотки и прямой кишки. При клинически выраженной (манифестированной) форме она проявляется уретритами, цервицитами, проктитами, вульвовагинитами, циститами, фарингитами и конъюнктивитами, протекающими с обильным гноетечением.
Инкубационный период у мужчин может составлять 3–7 дней, у женщин — до 10.
Терапевтические аспекты
Прежде чем начинать лечить, надо выяснить, насколько дикий и симпатичный гонококк достался вашему пациенту, но в современных условиях на это можно сразу не рассчитывать и считать, что очень сильно повезло, если чувствительность утеряна только к пенициллинам. Для качественной диагностики необходимы количественные, то есть с определением MIC, методики микробиологической диагностики, а не качественный диско-диффузионный метод.
В случае неосложненного цервицита, уретрита или поражения прямой кишки необходимо назначать два препарата с активностью как против гонококка, так и против хламидии в виду высокой их ассоциации. При этом фторхинолоны из-за высокой резистентности к ним у N. gonorrhoeae не могут быть препаратами выбора. Поэтому смотрим в сторону комбинации цефалоспоринов с макролидами при условии ОБЯЗАТЕЛЬНОЙ чувствительности к оным. И никаких одноразовых дозировок — только курсовое применение, иначе хронизация процесса будет обеспечена. О том, как работаю дозо- и времязависимые антибактериальные препараты, автор сотрясала воздух тут. И никаких субклинических дозировок! Не смешите гонококк, у него все равно нет чувства юмора.
Во всех остальных случаях мы ориентируемся в лечении только и исключительно на антибиотикограмму. К чему будет зверье чувствительно, то и назначаем в нормальных, то есть бактерицидных дозах. А пациенту убедительно объясняем, почему терапия носит комбинированный характер и почему речи быть не может «об одном единственном уколе». Да не убьется гонококк, учитывая, как он зарывается в эпителий, а далее под него, и уж тем более плавая в фагоцитах по всему организму. Не нужны нам «африканские» схемы, мы же все-таки в более развитом обществе живем и нормальное, надеюсь, медицинское образование получаем, а потому способны объяснить, что раз пневмония или ангина за день не лечатся, то и с гонококком ровно та же история. Автор умышленно не будет писать никаких терапевтических схем, так как в базовых ситуациях они являются справочным материалом, а во всех остальных, коих большинство, персонифицированной медициной, опирающейся на результаты бактериологических исследований.
В заключение хотелось бы сказать, что хотя на улице и ковид, и иной раз даже у врачей создается впечатление, что ничем другим люди уже не болеют, но мы же понимаем, что это не так. И маски не носят, и точно так же барьерными методами защиты при половых актах не пользуются. Бессмертных Маклаудов оказалось намного больше, чем, например, автор еще совсем недавно подозревала, а потому гонококковые инфекции отнюдь не только проблема дерматовенерологов, с ней и к кардиологу, и к травматологу, да даже к клиническому фармакологу могут придти в любой момент, и основным и главным становится посыл пациента в правильном направлении, то есть в бак. лабораторию и к профильному специалисту. А в следующей статье будем вспоминать менингококк.
Нейссерии: возбудители гонореи и менингита
Также у человека выделяют непатогенные виды нейссерий, обитающих на слизистых оболочках: Neisseria sicca, Neisseria mucosa, Neisseria perflava.
Гонококковая инфекция (гонорея)
Гонорея относится к инфекциям, передаваемым половым путем (ИППП).
Возбудитель гонореи, как и возбудитель урогенитального хламидиоза (Chlamydia trachomatis), имеет высокую тропность к цилиндрическому эпителию, поэтому поражает цервикальный канал, эндометрий, маточные трубы, уретру.
Неосложненная гонорея у мужчин протекает чаще всего в форме острого гнойного или гнойно-слизистого уретрита. Признаками гонореи у женщин является цервицит с гнойно-слизистыми выделениями. При аногенитальных и орогенитальных контактах возможно развитие проктита или фарингита.
Симптомы и проявления гонококковой инфекции, за небольшим исключением, неспецифичны, для постановки диагноза необходимы лабораторные исследования для выявления возбудителя гонореи.
У мужчин до 15% случаев гонококковой инфекции может протекать без клинической симптоматики, а у 5-10% не сопровождается и лабораторными признаками уретрита. У женщин доля бессимптомных форм гонореи может достигать 45-55%.
Своевременно проведенное лабораторное исследование позволяет вовремя поставить диагноз и предотвратить развитие осложнений.
Менингококковая инфекция (менингит)
Возбудителем менингококковой инфекции (менингита) является Neisseria meningitidis (менингококк).
Менингококковая инфекция – острое инфекционное заболевание, протекающее в виде острого назофарингита, гнойного менингита и менингококкцемии.
Штаммы менингококка в зависимости от химического строения капсулы делятся на группы: А, В, С, X, Y, Z, W-135, 29-E, H, I, K, L. Более чем 90% случаев генерализованных форм менингококковой инфекции обусловлены штаммами групп А, В и С, значительно реже – штаммами групп X, Y и W-135, остальные группы не представляют эпидемиологического интереса.
Менингококковая инфекция поражает лиц всех возрастов, но чаще (70%) болеют дети. Показатель летальности при менингите составляет в среднем 10%, что определяет высокую социальную значимость заболевания.
Колонизируя заднюю стенку носоглотки человека, менингококк может долгое время не вызывать заболевание. В этом случае, при отсутствии симптомов, его обнаружение возможно только в результате лабораторного обследования. Часто назофарингит предшествует развитию менингита.
Менингит – воспаление оболочки головного и/или спинного мозга. Говоря «менингит» обычно подразумевают воспаление именно мягкой мозговой оболочки, так как эта патология встречается чаще других. К симптомам менингита относят:
При менингите, обусловленном именно Neisseria meningitidis, показательным симптомом является сыпь. Она носит геморрагических характер и «звёздчатую» форму. Начинается с бедер и ягодиц, распространяется по телу. Появление сыпи на лице – неблагоприятный признак.
Лабораторная диагностика генерализованной формы менингококковой инфекции (менингита) включает микроскопию биологического материала, посев биоматериала с дальнейшей культуральной и биохимической идентификацией возбудителя, определением чувствительности к антибиотикам; обнаружение специфических антител методом РПГА.