Консервативное лечение болезни Грейвса: принципы, маркеры рецидива и ремиссии
Полный текст:
Аннотация
Болезнь Грейвса (диффузный токсический зоб) — системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреотропного гормона (АТ-рТТГ), клинически проявляющееся поражением щитовидной железы (ЩЖ) с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией (эндокринная офтальмопатия, претибиальная микседема, акропатия). Впервые заболевание описал С. Ивес в 1722 г., затем Пери в 1786 г. и Флаяни в 1802 г. В 1835 г. Р. Грейвс связал возникновение описанного симптомокомплекса, известного в наше время как синдром тиреотоксикоза, с патологией ЩЖ. В 1840 г. К. Базедов выделил в клинической картине триаду: зоб, пучеглазие, тахикардию.
Ключевые слова
Для цитирования:
Абрамова Н.А., Фадеев В.В. Консервативное лечение болезни Грейвса: принципы, маркеры рецидива и ремиссии. Проблемы Эндокринологии. 2005;51(6):44-49. https://doi.org/10.14341/probl200551644-49
For citation:
Abramova N.A., Fadeyev V.V. Medical treatment for Graves’ disease: principles, markers of a relapse and remission. Problems of Endocrinology. 2005;51(6):44-49. (In Russ.) https://doi.org/10.14341/probl200551644-49
Болезнь Грейвса (БГ, диффузный токсический зоб) — системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреотропного гормона (АТ-рТТГ), клинически проявляющееся поражением щитовидной железы (ЩЖ) с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией (эндокринная офтальмопатия, претибиальная микседема, акропатия). Впервые заболевание описал С. Ивес в 1722 г., затем Пери в 1786 г. и Флаяни в 1802 г. В 1835 г. Р. Грейвс связал возникновение описанного симптомокомплекса, известного в наше время как синдром тиреотоксикоза, с патологией ЩЖ. В 1840 г. К. Базедов выделил в клинической картине триаду: зоб, пучеглазие, тахикардию [2].
В России и странах СНГ в качестве синонима термина «болезнь Грейвса» (болезнь Базедова) традиционно используют термин «диффузный токсический зоб», который не лишен ряда существенных недостатков. Во-первых, он характеризует лишь макроскопическое (диффузный зоб) и функциональное (токсический зоб) изменение ЩЖ, которое не является облигатным для БГ: с одной стороны, увеличения железы может не быть, с другой — оно может быть недиффузным. Кроме того, диффузное увеличение ЩЖ в сочетании с тиреотоксикозом может иметь место при других заболеваниях, в частности при так называемой диффузной функциональной автономии. Использование более широкого термина «болезнь» (а не просто токсический зоб) применительно к обсуждаемому заболеванию, скорее всего, более оправданно, поскольку он в большей мере подчеркивает системность аутоиммунного процесса. Кроме того, во всем мире традиционно наиболее часто используют и, таким образом, узнают именно термин «болезнь Грейвса», а в немецкоговорящих странах — термин «болезнь Базедова».
В регионах с нормальным потреблением йода среди всех пациентов с тиреотоксикозом 60—80% составляют больные с БГ. В целом БГ относится к наиболее распространенным аутоиммунным заболеваниям. Так, частота новых случаев БГ в США составляет 13,9 на 100 000 населения [27]. В йодде- фицитных регионах в этиологической структуре токсического зоба БГ конкурирует с функциональной автономией ЩЖ (узловой и многоузловой токсический зоб) [32].
Как показал ряд исследований, в большинстве стран, за исключением североамериканских, в качестве начального лечения при БГ наиболее принята консервативная терапия тиреостатическими препаратами [17]. Основным недостатком этого варианта лечения является высокий риск развития рецидива тиреотоксикоза после его окончания. В связи с этим наиболее актуальной проблемой лечения БГ является выделение группы пациентов, у которых вероятность развития стойкой ремиссии заболевания будет наибольшей. Этому были посвящены многие проспективные исследования, которые имели различный дизайн и продолжительность и были выполнены в странах с разным уровнем потребления йода.
1. Этиология и патогенез
. пируют захват ЩЖ йода, синтез и высвобожде- те тиреоидных гормонов, а также пролиферацию ■цроцитов. В результате развивается тиреотоксикоз.
2. Генетические факторы
3. Выбор лечебной модели
На сегодняшний день, к сожалению, не существует метода лечения БГ, который бы обеспечивал норрекцию аутоиммунных нарушений, восстанавливая нормальную функцию ЩЖ. Выбор между имеющимися методами лечения (терапия тирео- статиками, операция, применение 131 1) определяется многими факторами, такими как тяжесть заболевания, размер зоба, предпочтения больного, а также сложившейся практикой в различных странах. Так, в США в абсолютном большинстве случаев независимо от размеров зоба, длительности заболевания и других факторов осуществляют терапию радиоактивным 131 1 [58]. Европейские и японские врачи предпочитают проводить лечение зпервые заболевшего пациента с помощью тирео- статиков. В России более 3/4 врачей предпочитают длительное лечение тиреостатиками, 6% — оперативное лечение и 3% — терапию радиоактивным йодом [1].
Если в отношении вариантов консервативной терапии и показаний к ней существует много разногласий, то в отношении целей оперативного лечения и терапии радиоактивным 13! 1 они уже практически отсутствуют. На сегодняшний день подавляющее большинство руководств и клинических рекомендаций выдвигают в качестве цели этих вариантов лечения развитие стойкого гипотиреоза, который достигается тиреоидэктомией или предельно субтотальной резекцией ЩЖ или назначением достаточной для этого активности 131 1 [9, 39]. В связи с этим указанные методы лечения обозначают как радикальные. Указанная концепция возникла после того, как был выяснен патогенез БГ (аутоиммунное заболевание, при котором ЩЖ — мишень для антител), и стала осуществима после внедрения в клиническую практику современных препаратов левотироксина (L-T4) и принципов заместительной терапии гипотиреоза, обеспечивающих высокое качество жизни пациентов, мало отличающееся от обычного [41].
4. Консервативное лечение
Тиреостатические препараты
Консервативное лечение направлено на снижение продукции тиреоидных гормонов путем торможения их синтеза и высвобождения, а также на подавление продукции тиреостимулирующих антител. Для тиреостатической терапии применяют производные имидазола и тиоурацила. В клинической практике используют 2 представителя группы имидазолов: 1-метил-2-меркаптоимидазол (тиама- зол) и 1-метил-2-тио-3-карбетокси-имидазол (кар- бимазол). В связи с тем что карбимазол в организме превращается в тиамазол, их эффекты сопоставимы. Из группы тиоурацила применяют 6-пропил- 2-тиоурацил (ПТУ).
Тиамазол и ПТУ быстро адсорбируются в кишечнике. Содержание препарата в сыворотке крови зависит от его дозы. Как тиамазол, так и ПТУ не блокируют транспорт йода и не тормозят высвобождение гормонов из депо ЩЖ, поэтому компенсация тиреотоксикоза происходит через 2—6 нед после начала приема препарата. Интратиреоидная концентрация препарата через 8 ч после приема 10 мг тиамазола и 100 мг ПТУ составляет 0,74 и 12,5 мг на 1 г тиреоидной ткани соответственно. Тионамиды выводятся из организма в основном с мочой и 3% с калом. Учитывая различия в скорости метаболизма в организме, ПТУ следует назначать в дозе в 10 раз выше, чем тиамазол. Кроме того, тиамазол можно назначать 1—2 раза в сутки, в то время как ПТУ — 3—4 раза [38]. ПТУ обладает ограниченной липофильностью, что затрудняет его прохождение через биологические мембраны (плацента, эпителий молочной железы), поэтому во время беременности и лактации препаратом выбора считается именно ПТУ [6].
Тионамиды, попадая в ЩЖ, оказывают свое действие посредством влияния на тиреоидную пероксидазу, ингибируя окисление йода, йодирование тиреоглобулина и конденсацию йодтирозинов. Препараты конкурируют в тиреоглобулине с тирозильными группами за йод и выводят его из процесса биосинтеза тиреоидных гормонов [12, 13]. Кроме того, тионамиды способны связывать тиреоглобулин и, изменяя его конформацию, переводить его в более устойчивую к последующему гидролизу форму [16]. ПТУ также способен блокировать конверсию Т4 в Т3 в периферических тканях посредством угнетения активности 5-дейодиназы 1-го типа и тем самым тормозить синтез Т3 [44].
Иммуносупрессивное действие тионамидов
Вопрос о том, оказывают ли тиреостатики специфическое действие на иммунную систему, т. е. является ли терапия этими препаратами не только симптоматической (ликвидация тиреотоксикоза), но и патогенетической, остается открытым. Выдвигаются несколько гипотез иммуносупрессивного действия тионамидов [57]: снижение продукции тиреоидных гормонов, изменяющее активность и количество субпопуляций лимфоцитов и растворимых рецепторов интерлейкина-2 (sIL-2); снижение йодирования тиреоглобулина, приводящее к снижению его иммуногенности; снижение экспрессии тироцитов класса 1; снижение продукции простагландинов Е2, IL-1 и IL-6; отсутствие влияния на экспрессию HLA-DR, вызванную интерфероном- у; снижение продукции тироцитами белков теплового шока.
Согласно одной из теорий, тионамиды снижают образование АТ-рТТГ и других антител к ЩЖ. Скорее всего, это действие тионамидов связано с тем, что они снижают образование различных сигнальных молекул тироцитами. В своих исследованиях A. Gamstedt и соавт. сравнивали влияние фармакологических доз тиамазола и бетаметазона на увеличение уровня АТ-рТТГ при БГ после проведения терапии 131 1. Бетаметазон в отличие от тиамазола не препятствовал повышению уровня АТ- рТТГ. Был сделан вывод, что тиамазол, вероятно, оказывает прямое иммуносупрессивное действие на функции В- и Т-лимфоцитов [19].
В качестве доказательства иммуносупрессивного действия тионамидов рассматривается тот факт, что после курса тиреостатической терапии повышаются количество и активность CD8-клеток. Следует отметить, что изменения в этой популяции клеток происходят обратно пропорционально уровню Т3 в крови, который является одним из показателей тяжести тиреотоксикоза [57].
Поскольку тиреостатические препараты влияют на многие функции тироцитов, они могут также нарушать продукцию цитокинов. A. Weetman и соавт. [60] обнаружили, что тироцит обладает способностью продуцировать простагландин Е2, IL-1 и IL-6. Тиреостатические препараты снижают выработку этих цитокинов. Поскольку комплемент участвует в иммунном ответе, снижение продукции цитокинов, в частности IL-6, может нарушать пролиферацию и дифференцировку интратиреоидных В-лимфоцитов. Следует добавить, что тиреостатические препараты также снижают продукцию белка теплового шока (hsp-72) [24].
Тем не менее серьезным аргументом против того, что тиреостатики оказывают клинически значимое иммуномодулирующее действие, является тот факт, что стойкая ремиссия БГ развивается лишь у небольшого количества пациентов (по данным разных авторов), около 15—40%) [60].
Показания к консервативной терапии Б Г
Наиболее часто показания к проведению длительной тиреостатической терапии формулируются следующим образом: впервые выявленный диффузный зоб небольшого размера (до 40 мл), отсутствие клинически значимых узловых образований и тяжелых осложнений тиреотоксикоза, достаточная комплаентность пациента. Кроме того, выбор метода лечения может определяться рядом дополнительных факторов, таких как возможность квалифицированного контроля за лечением, планирование беременности, развитие побочных эффектов тиреостатиков, предпочтения пациента, которые необходимо оценивать комплексно.
4. Риск рецидива после курса тиреостатической терапии
Основной проблемой консервативной тиреостатической терапии, как указывалось, является высокий риск рецидива БГ после 1—2-годичного курса лечения. В связи с этим использующиеся в настоящее время критерии отбора пациентов для такого варианта лечения остаются неудовлетворительными. Многим пациентам с БГ уже после первичной постановки диагноза показано радикальное лечение (операция, терапия 131 1), что существенно сократит период активного наблюдения у эндокринолога и затраты на лечение, а также предотвратит возможные осложнения. К факторам, повышающим риск рецидива БГ после курса тиреостатической терапии, относят [39] мужской пол, молодой возраст, увеличение объема ЩЖ, курение, гиперваскуляризацию ЩЖ, значительное повышение уровня Т3 и Т4 и соотношения Т3/Т4, выраженную эндокринную офтальмопатию (?), высокий уровень АТ-рТТГ (?).
Эти факторы можно разделить на 3 группы: к 1-й относят факторы, связанные с пациентом (возраст, пол, курение), ко 2-й — особенности клинической картины заболевания (размер зоба, уровни Т3, Т4, АТ-рТТГ), к 3-й — тиреостатики (выбор препарата, режим дозирования, присоединение к терапии L-T4).
Факторы, связанные с пациентом
Особенности клинической картины
С целью определения оптимальной продолжительности курса тиреостатической терапии у больных с БГ G. Edan и соавт. [15] исследовали динамику уровня АТ-рТТГ. Исследование было проспективным и продолжалось 24 мес после окончания курса терапии. Все пациенты (« = 64) получали 40 мг карбимазола в сутки; при достижении эу- тиреоза дозу препарата снижали. У 44 пациентов (1-я группа) АТ-рТТГ в ходе терапии перестали определяться и лечение было прекращено (продолжительность терапии составила 9—18 мес). Контрольную группу составили пациенты (п = 12), у которых антитела продолжали определяться на протяжении 18 мес тиреостатической терапии. Исходные уровни антител в 1-й группе были ниже, чем в контрольной, как и частота рецидивов (41% против 92%; р <0,001). Следует отметить, что интервал времени, через который развился рецидив, у пациентов 1-й группы был больше по сравнению с пациентами контрольной группы (12 мес против 1 мес; р <0,001). Таким образом, мониторирование уровня стимулирующих АТ-рТТГ позволяет уменьшить продолжительность тиреостатической терапии без снижения ее эффективности [15].
Как указывалось, D. Glinoer и соавт. показали, что риск развития рецидива БГ составляет 100%, если к концу курса тиреостатической терапии уровень АТ-рТТГ не снижается и пациент курит [21]. В исследовании участвовали 82 пациента (70 женщин и 12 мужчин в возрасте 36 лет). Все пациенты заболели БГ впервые. В течение 15 мес проводили тиреостатическую терапию. После достижения эу- тиреоза присоединяли терапию Ь-Т4 (как минимум 12 мес) с целью поддержания уровня ТТГ ниже 2,5 мЕд/л. После прекращения тиреостатической терапии все пациенты были рандомизированы и получали или Ь-Т4 (100 мкг/сут), или плацебо в течение 1 года. В результате было показано, что дополнительное применение Ь-Т4 не влияет на вероятность рецидива БГ, а сохранение повышенного уровня АТ-рТТГ к концу лечения и курение являются определяющими факторами риска рецидива БГ.
Наряду с исследованием уровня стимулирующих АТ-рТТГ определенное значение может иметь уровень блокирующих антител. Так, V. Michelangeli и соавт. [37] определяли стимулирующие и блокирующие АТ-рТТГ у 85 больных с БГ, которым до этого не проводили тиреостатической терапии. АТ- рТТГ исследовали перед началом лечения и затем с интервалами 6 мес на протяжении всего курса терапии. Курс тиреостатической терапии продолжался не менее 12 мес. Ретроспективно были выделены 2 группы: основная, в которую вошли больные с рецидивом БГ, и контрольная — больные с ремиссией заболевания на протяжении как минимум 15 мес после окончания терапии. Изначально уровни как стимулирующих, так и блокирующих АТ-рТТГ были выше у больных с рецидивом БГ по сравнению с лицами контрольной группы (р <0,001). Через 6 мес после начала терапии скорость снижения уровня блокирующих АТ-рТТГ была одинакова в обеих группах, однако если в контрольной группе уровень этих антител продолжал снижаться при продолжении терапии, в основной группе этого не происходило. В результате исследования было установлено, что изменение уровня блокирующих АТ-рТТГ с 6-го по 12-й месяц тиреостатической терапии определяет возможность рецидива заболевания. Так, если уровень блокирующих АТ-рТТГ снижается до контрольных значений через 12 мес терапии, в 70% случаев следует ожидать ремиссии заболевания [37].
В последние годы стали появляться исследования, в которых уровень АТ-рТТГ определяли с помощью человеческого антигена. К сожалению, многоцентровых и проспективных исследований значения этих антител как предикторов рецидива БГ пока не проводили.
Особенности тиреостатической терапии
Тем не менее у монотерапии тиреостатиками есть один важный недостаток: на ее фоне необходим более частый контроль уровня Т4 и ТТГ в связи с тем, что у многих пациентов с БГ гиперфункция ЩЖ характеризуется некоторой динамикой, которая определяется варьирующим уровнем продукции стимулирующих и блокирующих АТ-рТТГ. В этой ситуации даже при аккуратном приеме одной и той же подобранной дозы тиреостатика тиреотоксикоз может периодически декомпенсироваться либо, наоборот, развиваться медикаментозный гипотиреоз. Эта проблема может быть решена при использовании схемы «блокируй и замещай», когда железа надежно блокируется большой дозой тиамазола.
Заключение
Как и большинство других системных аутоиммунных заболеваний, БГ характеризуется склонностью к постоянному прогрессированию, а стойкая ремиссия после курса тиреостатической терапии развивается у меньшинства пациентов (15—30%). Не вполне понятно, индуцируется ли эта ремиссия специфическими иммуномодулирующими эффектами тиреостатиков или же иммунологическая ремиссия в этом небольшом проценте случаев развивается самопроизвольно, а тиреостатики оказывают лишь симптоматическое действие, блокируя синтез тиреоидных гормонов и предотвращая тиреотоксикоз. К доказанным факторам риска рецидива БГ относятся большой размер зоба и отсутствие его редукции либо увеличение на фоне терапии, тяжелый тиреотоксикоз, высокий уровень АТ-рТТГ к концу курса тиреостатической терапии, курение и мужской пол.
Болезнь Грейвса
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ММА имени И.М. Сеченова
Б олезнь Грейвса (болезнь Базедова, диффузный токсический зоб, БГ) – системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреоторопного гормона (ТТГ), клинически проявляющееся поражением щитовидной железы (ЩЖ) с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией (эндокринная офтальмопатия, претибиальная микседема, акропатия). Одновременное сочетание всех компонентов системного аутоиммунного процесса встречается относительно редко и не является облигатным для постановки диагноза. В большинстве случаев наибольшее клиническое значение при БГ имеет поражение ЩЖ.
В США и Англии частота новых случаев БГ варьирует от 30 до 200 случае на 100 тысяч населения в год. Женщины заболевают БГ в 10–20 раз чаще. В регионах с нормальным йодным обеспечением болезнь Грейвса является наиболее частой причиной стойкого тиреотоксикоза, а в йододефицитных регионах в этиологической структуре токсического зоба БГ конкурирует с функциональной автономией ЩЖ (узловой и многоузловой токсический зоб). В России в качестве синонима термина болезнь Грейвса (болезнь Базедова) традиционно используется термин диффузный токсический зоб, который не лишен ряда существенных недостатков. Во–первых, он характеризует лишь макроскопическое (диффузный зоб) и функциональное (токсический) изменение ЩЖ, которое не является облигатным для болезни Грейвса: с одной стороны, увеличения железы может не быть, с другой – он может быть не диффузным. Вместе с тем, диффузное увеличение ЩЖ в сочетании с тиреотоксикозом может иметь место при других заболеваниях, в частности, при так называемой диффузной функциональной автономии. Использование более широкого термина «болезнь» (а не просто токсический зоб) применительно к обсуждаемому заболеванию, скорее всего, более оправдано, поскольку он в большей мере подчеркивает системность аутоиммунного процесса. Кроме того, во всем мире традиционно наиболее часто используется и, таким образом, узнается именно термин болезнь Грейвса, а в немецко–говорящих странах – болезнь Базедова.
БГ является мультифакториальным заболеванием, при котором генетические особенности иммунного реагирования реализуются на фоне действия факторов окружающей среды. Наряду с этнически ассоциированной генетической предрасположенностью (носительство гаплотипов HLA–B8, –DR3 и –DQA1*0501 у европейцев) в патогенезе БГ определенное значение придается психосоциальным и средовым факторам. Так, уже достаточно давно обсуждается значение инфекционных и стрессорных факторов, в частности, ряд работ выдвигает теорию «молекулярной мимикрии» между антигенами ЩЖ, ретробульбарной клетчатки и рядом стресс–протеинов и антигенов бактерий (Yersinia enterocolitica). Эмоциональные стрессорные и экзогенные факторы, такие как курение, могут способствовать реализации генетической предрасположенности к БГ. Так, была обнаружена временная взаимосвязь между манифестацией БГ и потерей супруга (партнера). Курение повышает риск развития БГ в 1,9 раз.
БГ в ряде случаев сочетается с другими аутоиммунными эндокринными заболеваниями (сахарный диабет 1 типа, первичный гипокортицизм); такое сочетание принято обозначать, как аутоиммунный полигландулярный синдром II типа.
В результате нарушения иммунологической толерантности, аутореактивные лимфоциты (CD4 + – и CD8 + –T–лимфоциты, B–лимфоциты) опосредованно адгезивными молекулами (ICAM–1, ICAM–2, E–селектин, VCAM–1, LFA–1, LFA–3, CD44) инфильтрируют паренхиму ЩЖ, где распознают ряд антигенов, которые презентируются дендридными клетками, макрофагами, В–лимфоцитами и HLA–DR–экспримирующими фолликулярными клеткам. В дальнейшем цитокины и сигнальные молекулы инициируют антигенспецифическую стимуляцию В–лимфоцитов, в результате чего начинается продукция специфических иммуноглобулинов против различных компонентов тироцитов. В патогенезе БГ основное значение придается образованию стимулирующих антител к рецептору ТТГ (АТ–рТТГ). Эти антитела связываются с рецептором ТТГ, приводят его в активное состояние, запуская внутриклеточные системы (каскады цАМФ и фосфоинозитолов), которые стимулируют захват ЩЖ йода, синтез и высвобождение тиреоидных гормонов, а также пролиферацию тироцитов. В результате развивается синдром тиреотоксикоза, доминирующий в клинической картине БГ.
Классическая мерзебургская триада (зоб, тахикардия, экзофтальм), описанная еще Карлом Базедовым, встречается примерно у 50% пациентов. Примерно в 2/3 случаев БГ развивается в возрасте после 30 лет, не менее, чем в 5 раз чаще – у женщин. В отдельных популяциях (Япония, Швеция) БГ почти в половине случаев манифестирует на протяжении первого года после родов.
Как указывалось, клиническая картина БГ определяется синдромом тиреотоксикоза, для которого характерны: похудение (часто на фоне повышенного аппетита), потливость, тахикардия и ощущение сердцебиения, внутреннее беспокойство, нервозность, дрожь рук (а порой, всего тела), общая и мышечная слабость, быстрая утомляемость и ряд других симптомов, подробно описанных в литературе. В отличие от многоузлового токсического зоба, который связан с функциональной автономией ЩЖ, при БГ, как правило, имеет место короткий анамнез: симптомы развиваются и прогрессируют быстро и в большинстве случаев приводят пациента к врачу в пределах 6–12 месяцев. У пожилых пациентов тиреотоксикоз любого генеза часто протекает олиго– или моносимптомно (вечерний субфебрилитет, аритмии) или даже атипично (анорексия, неврологическая симптоматика). При пальпаторном исследовании примерно у 80% пациентов удается выявить увеличение ЩЖ, порой весьма значительное: пальпаторно железа плотноватая, безболезненная.
В ряде случаев, при БГ на первое место могут выходить проявления эндокринной офтальмопатии (выраженный экзофтальм, нередко имеющий несимметричный характер, диплопия при взгляде в одну из сторон или вверх, слезотечение, ощущение «песка в глазах», отечность век). Здесь следует оговориться, что наличие у пациента выраженной эндокринной офтальмопатии (ЭОП) позволяет практически безошибочно установить пациенту этиологический диагноз уже по клинической картине, поскольку среди заболеваний, протекающих с тиреотоксикозом, ЭОП сочетается только с БГ.
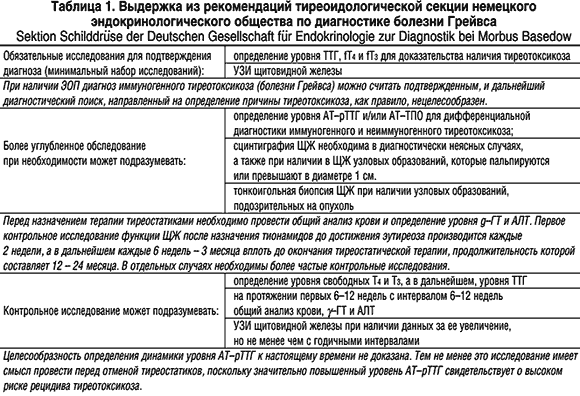
Диагностика в типичных случаях не вызывает существенных трудностей (табл. 1). При подозрении на наличие у пациента тиреотоксикоза ему показано определение уровня ТТГ высокочувствительным методом (функциональная чувствительность не менее 0,01 мЕд/л). При обнаружении пониженного уровня ТТГ пациенту проводится определение уровня свободных Т4 и Т3: если хотя бы один из них повышен – речь идет о манифестном тиреотоксикоза, если они оба в норме – о субклиническом.
После подтверждения наличия у пациента тиреотоксикоза проводится этиологическая диагностика, направленная на выявление конкретного заболевания, которое его обусловило. При УЗИ примерно в 80% случаев БГ обнаруживается диффузное увеличение ЩЖ; кроме того, этот метод может выявить характерную для большинства аутоиммунных заболевания гипоэхогенность ЩЖ. По данным сцинтиграфии при БГ выявляется диффузное усиление захвата изотопа железой. Как и при всех других аутоиммунных заболеваниях ЩЖ, при БГ могут определяться высокие уровни классических антител к ЩЖ (антитела к тиреоидной пероксидазе – АТ–ТПО и антитела к тиреоглобулину – АТ–ТГ). Это наблюдается не менее чем в 70–80% случаев БГ. Таким образом, обнаружение классических антител не позволяет отличить БГ от хронического аутоиммунного, послеродового и «безболевого» («молчащего») тиреоидита, но может, в сумме с другими признаками, существенно помочь в дифференциальной диагностике БГ и функциональной автономии ЩЖ. Следует помнить о том, что классические антитела могут обнаруживаться у здоровых людей без каких–либо заболеваний ЩЖ. Большее диагностическое значение имеет определение уровня антител к рецептору ТТГ (АТ–рТТГ), которое, увы, пока не абсолютно из–за несовершенства имеющихся тестсистем. В таблице 2 представлена краткая характеристика других заболеваний, протекающих с тиреотоксикозом, с которыми необходимо дифференцировать БГ.
Прежде всего, планируя лечение, нужно отчетливо понимать, что при БГ речь идет об аутоиммунном заболевании, причиной которого является выработка антител к ЩЖ иммунной системой. Вопреки этому, к сожалению, очень часто приходится сталкиваться с представлением о том, что хирургическое удаление части ЩЖ само по себе способно вызвать ремиссию заболевания (т.е., по сути, аутоиммунного процесса), хотя как хирургия БГ, так и терапия радиоактивным йодом–131 идеологически должна восприниматься, лишь как удаление из организма «органа–мишени» для антител, ликвидирующее тиреотоксикоз. В настоящее время существует 3 метода лечения БГ, каждый из которых не лишен существенных недостатков.
Прежде всего, планируя лечение, нужно отчетливо понимать, что при БГ речь идет об аутоиммунном заболевании, причиной которого является выработка антител к ЩЖ иммунной системой. Вопреки этому, к сожалению, очень часто приходится сталкиваться с представлением о том, что хирургическое удаление части ЩЖ само по себе способно вызвать ремиссию заболевания (т.е., по сути, аутоиммунного процесса), хотя как хирургия БГ, так и терапия радиоактивным йодом–131 идеологически должна восприниматься, лишь как удаление из организма «органа–мишени» для антител, ликвидирующее тиреотоксикоз. В настоящее время существует 3 метода лечения БГ, каждый из которых не лишен существенных недостатков.
Консервативное лечение болезни Грейвса
Назначается для достижения эутиреоза перед оперативным лечением, а также в отдельных группах пациентов в качестве базового длительного курса лечения, который в некоторых случаях приводит к стойкой ремиссии. Длительную консервативную терапию имеет смысл планировать далеко не у всех пациентов. В первую очередь, речь идет о пациентах с умеренным увеличением объема ЩЖ (до 40 мл); при зобе больших размеров после отмены тиреостатиков неминуемо разовьется тиреотоксикоз. Кроме того, консервативную терапию нецелесообразно планировать у пациентов с крупными (более 1–1,5 см) узловыми образованиями в ЩЖ и при наличии выраженных осложнений тиреотоксикоза (мерцательная аритмия, выраженный остеопороз и др.). Практически бессмысленно (и главное – небезопасно для пациента) назначение повторных курсов лечения при развитии рецидива тиреотоксикоза спустя 12–24 месяца тиреостатической терапии. Важным условием планирования длительной тиростатической терапии является готовность пациента следовать рекомендациям врача (комплаентность) и доступность квалифицированной эндокринологической помощи.
В качестве основных тиреостатиков на протяжении многих десятилетий в клинической практике во всем мире используются препараты из группы тионамидов: тиамазол (Метизол) и пропилтиоурацил. Ключевой механизм действия тионамидов заключается в том, что, попадая в ЩЖ, они подавляют действие тиреоидной пероксидазы, ингибируют окисление йода, йодирование тиреоглобулина и конденсацию йодтирозинов. В результате прекращается синтез тиреоидных гормонов и купируется тиреотоксикоз. Наряду с этим выдвигается не всеми поддерживаемая гипотеза о том, что тионамиды, в первую очередь, тиамазол, обладают эффектами на иммунологические изменения, развивающиеся при БГ. В частности, предполагается, что тионамиды влияют на активность и количество некоторых субпопуляций лимфоцитов, снижают иммуногенность тиреоглобулина за счет уменьшения его йодирования, снижают продукцию простагландинов Е2, IL–1, IL–6 и продукцию тироцитами белков теплового шока. Именно с этим связывается тот факт, что в правильно отобранной группе пациентов с БГ, на фоне подержания тионамидами эутироза в течение 12–24 месяцев примерно в 30% случаев можно ожидать развития стойкой ремиссии заболевания.
После нормализации уровня свободного Т4 пациенту начинают снижать дозу тиреостатика и примерно через 2–3 недели переходят на прием поддерживающей дозы (10–15 мг в день). Параллельно, начиная от момента нормализации уровня Т4 или несколько позже, пациенту назначается левотироксин в дозе 50–100 мкг в день. Такая схема получила название «блокируй и замещай»: один препарат блокирует железу, другой замещает формирующийся дефицит тиреоидных гормонов. Схема «блокируй и замещай» проста в использовании, поскольку позволяет полностью заблокировать продукцию тиреоидных гормонов, что исключает возможность возвращений тиреотоксикоза. Критерием адекватности терапии является стойкое поддержание нормального уровня Т4 и ТТГ (последний может приходить в норму на протяжении нескольких месяцев от начала лечения). Вопреки бытующим представлениям тиамазол и пропилтиоурацил сами по себе не обладают так называемым «зобогенным» эффектом. Увеличение размера ЩЖ на фоне их приема закономерно развивается лишь при развитии медикаментозного гипотиреоза, которого можно легко избежать, назначив левотироксин в рамках схемы «блокируй и замещай».
Поддерживающая терапия «блокируй и замещай» (10–15 мг тиамазола и 50–100 мкг левотироксина) продолжается от 12 до максимум 24 месяцев (табл. 1). Дальнейшее увеличение объема ЩЖ на фоне проводимой терапии даже при условии стойкого поддержания эутиреоза (это закономерно произойдет при медикаментозном гипотиреозе или, наоборот, при недостаточной блокаде ЩЖ) существенно снижает шансы на успех лечения. На протяжении всего лечения у пациента с интервалом не менее чем 1 раз в месяц необходимо проводить определение уровня лейкоцитов и тромбоцитов. Редким (0,06%), но грозным осложнением тионамидов (как тиамазола, так, с практически одинаковой частотой пропилтиоурацила) является агранулоцитоз, казуистически редко – изолированная тромбоцитопения. После окончания курса лечения препараты отменяются; наиболее часто рецидив развивается в течение первого года после прекращения терапии.
По современным представлениям, целью оперативного лечения, равно как и обсуждаемой ниже терапии йодом–131, является удаление большей части ЩЖ, с одной стороны, обеспечивающее развитие послеоперационного гипотиреоза, а с другой (что наиболее принципиально) – исключающее любую возможность рецидива тиреотоксикоза. С этой целью рекомендуется проведение предельно субтотальной резекции ЩЖ с оставлением тиреоидного остатка не более 2–3 мл. Проведение субтотальных резекций, с одной стороны, несет высокий риск сохранения или отдаленного рецидива тиреотоксикоза, а с другой, отнюдь не исключает развития гипотиреоза. При выполнении так называемых «экономных резекций», объем которых во всем мире расцениваются, как неадекватный, следует понимать, что оставляя во время операции достаточную для продукции тиреоидных гормонов часть ЩЖ, в организме, по сути дела, остается «мишень» для антитиреоидных антител, продуцирующихся клетками иммунной системы.
Таким образом, полеоперационный гипотиреоз в настоящее время перестал рассматриваться, как осложнение оперативного лечения БГ, и является его целью. Предпосылкой для этого стало внедрение в широкую клиническую практику современных препаратов левотироксина, на фоне адекватного приема которых у пациента сохраняется стойкий эутиреоз и качество жизни, не отличающееся от обычного. На сегодняшний день можно без преувеличения сказать, что не существует такого гипотиреоза, компенсация которого при грамотном использовании современных препаратов тиреоидных гормонов была бы невозможна. Неудачи в лечении послеоперационного и любого другого гипотиреоза следует искать либо в недостаточной квалификации проводящего заместительную терапию, либо в несоблюдении пациентом достаточно простых рекомендаций по приему препарата.
Терапия радиоактивным йодом
Можно без преувеличения сказать, что во всем мире большая часть пациентов с БГ, равно как и с другими формами токсического зоба, в качестве лечения получает именно терапию радиоактивным йодом–131. Это связано с тем, что метод эффективен, неинвазивен, относительно дешев, лишен тех осложнений, которые могут развиться во время операции на ЩЖ. Единственными противопоказаниями к лечению йодом–131 являются беременность и грудное вскармливание.
Если в нашей стране по сей день продолжает бытовать мнение о том, что терапия йодом–131 показана лишь пожилым пациентам, которым по тем или иным причинам невозможно провести операцию, то на самом деле, уже не существует нижней возрастной границы для назначения йода–131, и во многих странах йод–131 с успехом используется для лечения БГ у детей. Было доказано, что независимо от возраста риск терапии йодом–131 существенно ниже такового при оперативном лечении.
Серьезной проблемой отечественной эндокринологии является фактическое отсутствие в распоряжении эндокринологов такого прекрасного способа лечения БГ, как терапия йодом–131.
БГ является одним из самых частых аутоиммунных заболеваний человека. Его клиническая картина и прогноз в большинстве случаев определяются стойким тиреотоксикозом, который при отсутствии адекватного лечения может привести к тяжелой инвалидизации пациента. Существующие на сегодняшний день принципы лечения БГ, хотя и не лишены недостатков, но позволяют полностью избавить пациента от тиреотоксикоза и обеспечить приемлемое качество жизни.