Granulicatella adiacens
Granulicatella adiacens представляет собой привередливые грамположительные кокки (пары, цепочки) и является частью питательных стрептококков (NVS). [2] [3] [4] Как и другие составляющие NVS, он может вызывать бактериемию и инфекционный эндокардит (ИЭ) со значительной заболеваемостью и смертностью. [4] [2] NVS реже участвует в ряде других инфекций, включая инфекции глазницы, носослезного протока и грудных имплантатов. [5] Это комменсал ротовой полости, половых органов и кишечника человека, хотя он редко вызывает инфекции, [5] [2] отчасти из-за того, что он привередлив и редко идентифицируется в лабораторных условиях. [5] Однако его идентификация стала более частой с использованием коммерческих средств массовой информации и автоматизированных систем идентификации. [5] Поскольку его трудно идентифицировать, он считается одной из причин ИЭ с отрицательной культурой. [2] Идентификация G. adiacens может позволить более подходящий выбор антибиотиков, особенно когда тестирование на чувствительность недоступно. [4]
| Антибиотик | Восприимчивый (%) |
|---|---|
| Пенициллин | 38,9 |
| Цефотаксим | 18,9 |
| Цефтриаксон | 43,3 |
| Эритромицин | 52,2 |
| Левофлоксацин | 84,5 |
| Клиндамицин | 91,9 |
| Меропенем | 100 |
| Ванкомицин | 100 |
Инфекционный эндокардит
Лечение антибиотиками
Род Granulicatella более устойчив к антибиотикам, чем стрептококки viridans (еще одна частая причина ИЭ), хотя по-прежнему часто чувствителен к клиндамицину, эритромицину, рифампицину и ванкомицину. [2]
Зловонное дыхание
Лучше всего растет на средах, содержащих тиол или пиридоксаль. [5] Фенотипическая идентификация этого рода трудна, но выполнима с помощью автоматизированных систем идентификации. [5] Секвенирование гена 16S рРНК является подтверждающим. [5]
Давайте целоваться, это не только приятно
Александр Суворов,
член-корреспондент РАН, доктор медицинских наук
«Природа» №4, 2019
Нельзя не признать, что человек оказался на вершине эволюции благодаря хорошо развившемуся головному мозгу. Но это не единственное, что делает Homo sapiens самым успешным, хотя и довольно уязвимым видом млекопитающих.
Наш организм «спроектирован» очень сложно, при этом его жизнедеятельность контролируется разными взаимосвязанными механизмами — нейрональными и гормональными, метаболическими и иммунологическими. Он как бы следит за нашим поведением, действуя по хорошо известному принципу кнута и пряника. В качестве наказания за необдуманные поступки мы чувствуем боль, отдергивая, например, руку от огня, а предостережением служит страх, который мы ощущаем, оказавшись на краю пропасти или рядом с опасным животным (в том числе и своего вида). Точно также работают и механизмы поощрения: мы испытываем наслаждение, сытно пообедав и хорошо выспавшись, или умиление, глядя на маленьких детей (которых, к слову, делаем обычно тоже с удовольствием). Таким образом наш собственный организм нас же поощряет за биологически оправданное поведение, такое как продолжение рода, получение пищи, приводящее к снабжению необходимой энергии и содержание своего тела в хорошей форме.
Как происходит «награждение», изучено уже неплохо. В качестве бонуса за хорошее поведение у нас вырабатываются нейромедиаторы (норадреналин, дофамин, эндорфины), которые стимулируют центры головного мозга, отвечающие за позитивные эмоции. Существует даже специальный белок — кисспептин (от англ. kiss — ‘поцелуй’ и peptid — ‘белок’), который может управлять активностью лимбических структур головного мозга, отвечающих за эмоции, в том числе и сексуальные. Как это работает, проверено в двойном слепом исследовании: в эксперименте участвовали добровольцы (29 здоровых мужчин), которым внутривенно вводили либо кисспептин, либо плацебо (рис. 1) [1]. Во время проведения магнитно-резонансной томографии всем участникам эксперимента предлагали рассматривать фотографии с эротическими, нейтральными или негативными сценами. Кисспептин усиливал реакцию лимбических структур мозга, связанных с сексуальным возбуждением, только при просмотре эротических снимков. Без гормона «поцелуев» таких изменений не наблюдалось.
Рис. 1. Реакция (BOLD-ответ) различных отделов головного мозга на демонстрацию фотографий с эротическими сценами у людей, которым внутривенно ввели кисспептин или плацебо [1]. МТ — миндалевидные тело (ЛМТ — левое, ПМТ — правое), Г — гиппокамп, Т — таламус, ППК — передняя поясная кора, ЗПК — задняя поясная кора, БШ — бледный шар, П — путамен (скорлупа). В исследовании участвовали добровольцы (29 здоровых мужчин), которые во время проведения магнитно-резонансной томографии рассматривали изображения (фотографии с эротическими, нейтральными или негативными сценами). Кисспептин усиливал реакцию лимбических структур мозга, связанных с сексуальным возбуждением, только при просмотре эротических снимков. Без гормона «поцелуев» таких изменений не наблюдалось
Однако почему нам должно быть приятно целоваться? Казалось бы, поцелуй любимой женщины или мужчины и тем более родственника или друга не грозит продолжением рода и не улучшает пищеварение. Зачем же тратить ресурс поощрения на бесполезные поступки? Склонен думать, что объяснение тут кроется в микробиоме ротовой полости.
Рис 2. Схема состава микробиоты двух человек в разных участках тела [3]. У каждого человека она разнообразна и уникальна. Цвет сектора соответствует определенному типу бактерий
Оральная микробиота, которая включает популяции бактерий не только полости рта, но и глотки, носовых ходов и пищевода, — второй (после желудочно-кишечного тракта) по численности микробиом человека. В расширенной базе данных орального микробиома человека, eHOMD (от англ. expanded Human Oral Microbiome Database), уже содержится информация о приблизительно 700 видах микроорганизмов, 70% из которых пригодны для культивирования, и большинству (57%) из них уже присвоены названия [4].
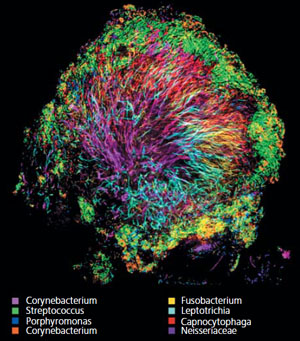
Рис. 3. Биогеография микробиоты в зубном налете [6]. Анаэробные бактерии живут внутри, а аэробные — снаружи
В полости рта взрослого человека обитает от 50 до 100 млрд бактерий около 96% видов от общего числа оральных бактерий, которые относятся к шести условным типам — Firmicutes, Actinobacteria, Proteobacteria, Fusobacteria, Bacteroidetes и Spirocheetes [5]. С этими, казалось бы, незаметными обитателями связано состояние здоровья нашего организма: они влияют на многие протекающие в нем процессы — от метаболизма до иммунных реакций. Микробиом полости рта не только уникален, но и легкодоступен: ротовая полость служит воротами, через которые микроорганизмы проникают внутрь и находят подходящее место для колонизации в пищеварительном тракте и дыхательных путях. Существует обширная литература, описывающая роль орального микробиома в жизни здорового человека и при развитии различных патологий (диабета, бактериемии, эндокардита, преждевременных родов, онкологических, аутоиммунных и других заболеваний). Американские микробиологи выпустили специальное руководство, в котором собраны все сведения о микробиоме полости рта [6]. Давно известно, что бактерии ротовой полости очень привередливы к тому, где и с кем им жить: выбирая соседей или место колонизации, они связываются с помощью своих адгезинов с рецепторами, расположенными на других бактериях или эпителиальных клетках. Таким образом, они не случайно накапливаются на поверхности зубов, языка или десен, а в результате специфического взаимодействия с ними. Несколько лет назад была разработана технология, которая позволяет визуализировать in situ пространственную организацию (биогеографию) бактериальных таксонов определенного микробиоценоза на основе известной информации о функциональных признаках конкретных его членов (рис. 3).
На основе информации о микробиомах, полученной благодаря современным достижениям метагеномики и техники секвенирования, можно будет разрабатывать биомаркеры для ранней диагностики заболеваний. Таким биомаркерами могут служить, например, оральные бактерии, обнаруженные в новообразованиях поджелудочной железы [7]. В результате анализа микробиомов по 16S рРНК выяснилось, что в доброкачественных (с низкой степенью дисплазии) кистах поджелудочной железы преобладают протеобактерии (Proteobacteria), а при высокой дисплазии и при раке они конкурируют с фирмикутами (Firmicutes). Из 38 выявленных оральных видов бактерий с тяжестью онкогенеза оказались связаны Fusobacterium nucleatum и Granulicatella adiacens. Аналогичные результаты получены при изучении некоторых бактерий, живущих в полости рта и способствующих развитию пародонтоза: выяснилось, что два вида — Tannerella forsythia и Porphyromonas gingivalis — связаны с повышенным риском рака пищевода [8]. Хотя о способности некоторых оральных бактерий подавлять работу иммунной системы в опухолевой среде было уже известно, столь явная его связь с развитием онкологических заболеваний показана впервые. Эти результаты полезно учитывать при разработках профилактики, ранней диагностики и терапии рака.
Состав микробиоты полости рта зависит от наследственности, возраста, местожительства, образа жизни, пищевых пристрастий и даже выбора сексуального партнера. Голландские ученые провели метагеномный анализ состава микробиоты полости рта 21 пары сексуальных партнеров (среди них были две гомосексуальные пары мужчин и женщин) [9]. Авторы пришли к следующим выводам: сходство микробиоты на поверхности языка партнеров не коррелирует с частотой поцелуев и, скорее, связано с наследственностью, общими условиями и образом жизни; а вот похожий микробный состав слюны проявлялся у пар, целующихся не менее девяти раз в день (рис. 4).
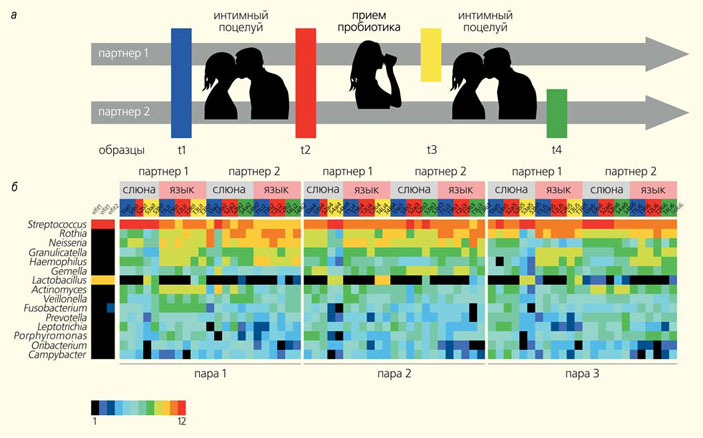
Рис. 4. Дизайн исследования микробиоты целующихся партнеров (а) и карта данных метагеномного анализа состава их микробиоты (б) [8]. У всех испытуемых брали образцы с поверхности языка и слюны до (синий цвет) и в течение 10 с после (красный) интимного поцелуя. Количество бактерий, которыми обмениваются партнеры во время интимного поцелуя, оценивалось с помощью маркерных бактерий: одного из партнеров просили выпить 50 мл пробиотического йогуртового напитка и вновь собирали образцы до (желтый) и после (зеленый) второго поцелуя. Относительная распространенность 15 самых доминирующих родов ротовой микробиоты и пробиотического йогурта нанесена на преобразованную цветную шкалу от 0 (черный цвет) до 12 (красный). Идентификаторы образцов (vifit), пары и тип образца указаны одним цветом
В процессе эволюции у нас сформировались механизмы для оценки партнера, с которым можно жить долго и безопасно. Это функцию, вероятно, выполняет первый поцелуй, во время которого передаются вкусовые сигналы, зависящие от качества продуктов метаболизма бактерий в полости рта. Если все хорошо, возникают чувства, которые побуждают нас целоваться, чтобы обменяться микробиотой. Так что, если вы влюблены, не отказывайте себе в удовольствии горячего поцелуя.
Литература
1. Comninos A. N., Wall M. B., Demetriou L. et al. Kisspeptin modulates sexual and emotional brain processing in humans // J. Clin. Invest. 2017; 127(2): 709–719. DOI: 10.1172/JCI89519.
2. Gomez A., Nelson K. E. The oral microbiome of children: development, disease and implications beyond oral health // Microb. Ecol. 2017; 73(2): 492–503. DOI: 10.1007/s00248-016-0854-1.
3. Gilbert J. A., Blaser M. J., Caporaso J. G. et al. Current understanding of the human microbiome // Nat. Med. 2018; 24(4): 392–400. DOI: 10.1038/nm.4517.
4. Escapa I. F., Chen T., Huang Y. et al. New insights into human nostril microbiome from the expanded Human Oral Microbiome Database (eHOMD): a resource for the microbiome of the human aerodigestive tract // mSystems. 2018; 3(6): e00187-18. DOI: 10.1128/mSystems.00187-18.
5. Verma D., Garg P. K., Dubey A. K. Insights into the human oral microbiome // Arch. Microbiol. 2018; 200(4): 525–540. DOI: 10.1007/s00203-018-1505-3.
6. Krishnan K., Chen T., Paster B. J. A practical guide to the oral microbiome and its relation to health and disease // Oral Dis. 2017; 23(3): 276–286. DOI: 10.1111/odi.12509.
7. Gaiser R. A., Halimi A., Alkharaan H. et al. Enrichment of oral microbiota in early cystic precursors to invasive pancreatic cancer // Gut. 2019. DOI: 10.1136/gutjnl-2018-317458.
8. Peters B. A., Wu J., Pei Z. et al. Oral microbiome composition reflects prospective risk for esophageal cancers // Cancer Res. 2017; 77(23): 6777–6787. DOI: 10.1158/0008-5472.CAN-17-1296.
9. Kort R., Caspers M., van de Graaf A. et al. Shaping the oral microbiota through intimate kissing // Microbiome. 2014; 2: 41. DOI: 10.1186/2049-2618-2-41.
* Подробнее см. статьи А. Н. Суворова в «Природе»: Полезные микробы — кто они? (2009. № 7. С. 21–30); Микробиота детей (2011. № 8. С. 14–21); Мир микробов и человек (2015. № 5. С. 11–19); Микробиота пожилых: истоки долголетия (2017. № 1. С. 22–29.) и др. — Примеч. ред.
Влияние препарата циклоферон на флору миндалин у часто болеющих детей
Опубликовано в журнале:
« Экспериментальная и клиническая фармакология » № 3, 2013 С.А. Ляликов, П.Г. Бедин, СЮ. Ермак, Р.В. Янович
УО «Гродненский государственный медицинский университет». Кафедра клинической лабораторной диагностики и иммунологии (заведующий кафедрой профессор С.А. Ляликов). Беларусь, г. Гродно.
Резюме. Для оценки способности препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей (ЧБД) была изучена микрофлора миндалин до и после стандартного курса этого препарата у 68 дошкольников, относящихся к категории ЧБД. Установлено, что микробный пейзаж поверхности миндалин детей после курса циклоферона характеризовался уменьшением разнообразия микрофлоры и снижением титра бактерий, в том числе и золотистого стафилококка, а также уменьшением количества штаммов, резистентных к бензилпенициллину, клиндамицину и ванкомицину. Таким образом, препарат циклоферон можно рекомендовать для реабилитации ЧБД.
Ключевые слова: часто болеющие дети, циклоферон, микрофлора миндалин.
Введение.
По современным литературным данным в группу часто болеющих детей (ЧБД) входят на том или ином возрастном этапе от 15 до 65% детской популяции [10], в связи с этим частые респираторные заболевания является актуальной проблемой педиатрии [4, 9]. В 1986 году В.Ю. Альбицким и А.А. Барановым была предложены критерии включения детей в группу часто болеющих. К (ЧБД) относят детей, страдающих острыми респираторными заболеваниями (ОРЗ) свыше 4-х раз в год в возрасте до 1 года, 6-и раз – в 1-3 года, 5-и раз – в 4-5 лет и 4-х раз – после 5 лет [1].
Система иммунитета в детском возрасте характеризуется относительно пониженным уровнем нейтрофилов – основных эффекторных клеток врожденного звена иммунного ответа, а также низкой продукцией иммуноглобулинов на фоне повышенного числа Т- и В-лимфоцитов, что свидетельствует о неполноценности адаптивного звена [8]. Это в совокупности с анатомо-физиологическими особенностями органов дыхания [6], недостаточными гигиеническими навыками и расширением контактов с окружающим миром делает детей дошкольного возраста особенно уязвимыми для инфекций.
Несмотря на то, что вирусы являются этиологическими агентами более чем в 80% случаев ОРЗ [2], по данным литературы в практической медицине для их лечения в большинстве случаев, даже при неосложнённом течении, используются антибактериальные (АБ) препараты [13, 14], что способствует развитию дисбиоза. Показано, что после перенесенного эпизода ОРЗ дисбиотические изменения микрофлоры зева сохраняются до 1,5 месяцев [11]. Гибель резидентной микрофлоры приводит к заселению биотопа условно-патогенными микроорганизмами. Существуют данные, что 35% детей, относящихся к группе ЧБД, имеют хроническую ЛОР патологию [10]. Не менее, чем в 30% случаев, ЧБД являются носителями β-гемолитического стрептококка группы А [3, 7]. Не менее 50% детей являются носителями золотистого стафилококка [7, 9].
Приведенное выше факты определили цель нашего исследования: оценить способность индуктора эндогенного интерферона – препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей.
Материалы и методы.
Было обследовано 68 детей (32 девочки и 36 мальчиков) в возрасте от 4 до 7 лет, медиана (Ме) – 5,1 лет, нижняя квартиль (Q25) – 4,5 года, верхняя квартиль (Q75) – 5,8 лет. Все дети посещали специализированные детские сады (№94 и №95) г. Гродно для ЧБД. Критериями включения в исследование были добровольное информированное согласие законных представителей детей, возраст 4-7 лет, отсутствие острых инфекционных заболеваний на момент обследования, наличие в анамнезе 6-и и более эпизодов ОРЗ за предшествующие 12 месяцев. Обследование включало клинический осмотр детей, анкетирование родителей и выкопировку данных из амбулаторной карты (форма №112-у).
Двукратно, до начала приема препарата циклоферон и через 2 недели после окончания приема детям выполнили посев микрофлоры с поверхности миндалин. Материал – слизь с поверхности миндалин – брали стерильными ватными тампонами натощак и помещали в универсальную гелевую транспортную среду Стюарта фирмы Copan (Италия). В течение 2 часов полученный материал доставлялся в лабораторию. Для идентификации микрофлоры и определения её чувствительности к антибактериальным препаратам была использована автоматизированная система VITEC-2 фирмы BioMerieux (Франция). Тестирование чувствительности к антибактериальным препаратам осуществлялось методом минимальных ингибирующих концентраций.
Препарат циклоферон (таблетки по 0,15) назначался двумя курсами (с перерывом в 1 месяц) по схеме, указанной в аннотации: на курс по 1 таблетке 1 раз в день за полчаса до еды в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23 дни.
Статистический анализ проводился с использованием стандартного пакета прикладных программ Statistica версия 6.0. При сравнении двух независимых групп изучаемой переменной использовали тест Манна-Уитни (U), в случае зависимости групп – тест Вилкоксона (Z). При сравнении долей (процентов) использовался метод Фишера (Fisher exact test). Нулевая гипотеза об отсутствии различий между переменными отвергалась на уровне значимости α=0,05 (p ≤0,05) для каждого из использованных тестов. Для представления результатов статистической обработки использовали величины медианы (Me), верхней (Q75) и нижней квартилей (Q25) в формате Me (Q25-Q75).
Результаты и обсуждение.
Таблица 1.
Микрофлора с поверхности миндалин ЧБД, выделенная при первом обследовании
| Название | Количество культур | % носителей |
|---|---|---|
| Aerococcus viridans | 1 | 1,47 |
| Candida famata | 3 | 4,41 |
| Dermococcus nishinomiyaensis | 1 | 1,47 |
| Erisipelotrix rusiopathiae | 4 | 5,88 |
| Fackmalia hominis | 1 | 1,47 |
| Granulicatella adiacens | 3 | 4,41 |
| Granulicatella elegans | 1 | 1,47 |
| Kocuria kristinae | 1 | 1,47 |
| Kocuria rosea | 4 | 5,88 |
| Leuconostoc mesenterioides | 1 | 1,47 |
| Leuconostoc mesenteroides cremosis | 3 | 4,41 |
| Rothia mucilaginosa | 1 | 1,47 |
| S. aureus | 33 | 48,53 |
| S. epidermidis | 1 | 1,47 |
| S. haemolyticus | 1 | 1,47 |
| S. hominis | 7 | 10,29 |
| S. ludgunensis | 3 | 4,41 |
| S. vitulinus | 1 | 1,47 |
| Serratia marcescens | 1 | 1,47 |
| Sphingomonas thalpophilium | 1 | 1,47 |
| Str. oralis | 12 | 17,65 |
| Str. parasanguinis | 2 | 2,94 |
| Str. pneumoniae | 11 | 16,18 |
| Str. salivarius | 2 | 2,94 |
| Str. spp. | 4 | 5,88 |
| Всего | 103 |
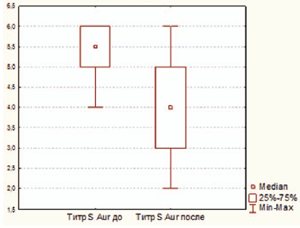
При повторном обследовании спектр микроорганизмов значительно сузился. В мазках с поверхности миндалин у детей были обнаружены представители только 16 семейств, родов и видов микроорганизмов (таблица 2). Как и при первом исследовании, золотистый стафилококк выявлялся практически у половины обследованных, но в более низких титрах (по сравнению с исходными р=0,04) (рисунок 1). У 11 детей (25,58%) рост бактерий отсутствовал, у 24 детей (55,81%) была идентифицирована 1 культура, у 6 (13,96%) – 2, у 2 (13,96%) – 3 культуры бактерий.
Таблица 2.
Микрофлора с поверхности миндалин ЧБД, выделенная при повторном обследовании
| Название | Количество культур | % носителей |
|---|---|---|
| Нет роста | 11 | 25,58 |
| Acinetobacter ursingii | 1 | 2,32 |
| Candida | 3 | 6,98 |
| E.coli | 1 | 2,32 |
| Enterobacter cloacae | 2 | 4,65 |
| Kocuria roseae | 1 | 2,32 |
| Micrococcus luteus | 1 | 2,32 |
| Pantoteae spp. | 1 | 2,32 |
| Ps.aeruginosa | 1 | 2,32 |
| S.aureus | 19 | 44,19 |
| S.epidermidis | 1 | 2,32 |
| S.warneri | 1 | 2,32 |
| Stenotrophomonas maltophyla | 1 | 2,32 |
| Str.oralis | 3 | 6,98 |
| Str.parasanguinis | 1 | 2,32 |
| Str.sanguinis | 2 | 4,65 |
| Str.spp. | 3 | 6,98 |
| Всего | 42 | 100,0 |
Рисунок 1. Динамика титра S. aureus у ЧБД, принимавших циклоферон
При анализе чувствительности к антибиотикам золотистого стафилококка, высеянного с поверхности миндалин ЧБД, при повторном исследовании было установлено несущественное уменьшение доли метициллин-, рифампицин-, эритромицин-, тетрациклин резистентных штаммов и достоверное снижение процента штаммов устойчивых к бензилпенициллину, ванкомицину и клиндамицину по сравнению с исходными показателями (таблица 3).
Таблица 3.
Доля (%) S. aureus, резистентных к антибиотикам до и после лечения
| Антибиотики | До приема циклоферона | После приема циклоферона | Р |
|---|---|---|---|
| MRSA | 10,00 | 5,26 | — |
| Бензилпенициллин | 84,09 | 63,64 | 0,05 |
| Ванкомицин | 26,67 | 4,55 | 0,03 |
| Клиндамицин | 20,93 | 0,0 | 0,02 |
| Линезолид | 0,0 | 0,0 | — |
| Моксифлоксацин | 0,0 | 0,0 | — |
| Оксациллин | 15,56 | 4,55 | — |
| Рифампицин | 4,44 | 0,0 | — |
| Эритромицин | 11,11 | 9,09 | — |
| Гентамицин | 0,0 | 0,0 | — |
| Ципрофлоксацин | 0,0 | 0,0 | — |
| Левофлоксацин | 0,0 | 0,0 | — |
| Тетрациклин | 6,67 | 0,0 | — |
| Нитрфурантоин | 0,0 | 0,0 | — |
| Бисептол | 0,0 | 0,0 | — |
| Дальфопристин | 0,0 | 0,0 | — |
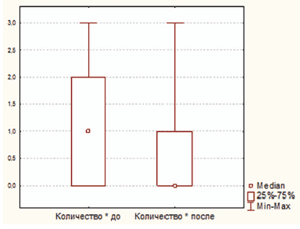
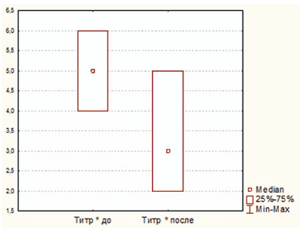
На фоне приема циклоферона изменилась не только обсемененность поверхности миндалин золотистым стафилококком, но и непатогенной микрофлорой. При повторном обследовании среднее количество обнаруженных непатогенных видов бактерий и их титры были достоверно ниже (в обоих случаях p
Рисунок 2. Количество непатогенных видов микроорганиз
Рисунок 3. Динамика титра непатогенной микрофлоры у ЧБД, принимавших циклоферон
Поскольку циклоферон не обладает прямой антибактериальной активностью, можно предположить, что снижение обсемененности и видового разнообразия микроорганизмов поверхности миндалин обусловлено иммунокоррегирующими свойствами этого препарата.
Уменьшение количества устойчивых к антибиотикам штаммов на фоне приема циклоферона, несомненно, представляется весьма интересным и важным эффектом ввиду всеобщей тенденции к развитию резистентности к используемым в повседневной практике антибактериальным препаратам. Таким образом, препарат циклоферон можно рекомендовать к применению в составе комплексной терапии и для реабилитации ЧБД.
Выводы
Прием двух курсов препарата циклоферон (с перерывом в 1 месяц) по схеме, указанной в аннотации снижает у ЧБД видовое разнообразие микрофлоры поверхности миндалин, достоверно уменьшает обсеменённость поверхности миндалин микрофлорой, в том числе золотистым стафилококком.
Приём препарата циклоферон приводит к значимому снижению количества штаммов золотистого стафилококка устойчивых к бензилпенициллину, ванкомицину и клиндамицину.