Сертификат GMP: подтверждение качества лекарственных средств
Сертификат GMP — это соблюдение изготовителем лекарственных препаратов требований надлежащей производственной практики. В России они сформулированы в национальном стандарте ГОСТ Р 52249-2009, который идентичен правилам, действующим в Европейском Союзе.
К каким производствам применима эта процедура?
В настоящее время в странах, которые контролируют соответствие стандарту GMP на своих территориях, его правила применяются для проверки качества следующих категорий продукции:
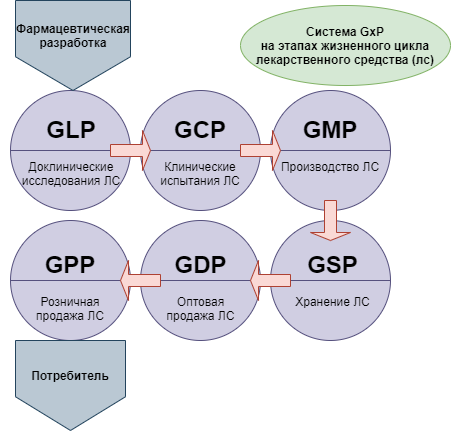
При этом для понимания ситуации следует принимать во внимание, что новая версия сертификации GMP — это не единственная система требований, которые в международной практике применяются в целях стандартизации медицинского обслуживания населения. Кроме них, производителям, работающим в такой сфере как фармация, необходимо соответствовать требованиям комплекса правил, объединенных под общим наименованием GxP:
Нормативная база
В Российской Федерации получение сертификата GMP осуществляется на основании действующей нормативной базы, включающей следующие основные правовые акты:
При этом необходимо принимать во внимание, что в настоящий момент наша страна вместе с другими государствами, входящими в состав Евразийского экономического союза, находится на этапе становления общего рынка, объединяющего фармацевтическое и косметическое производство в границах Союза. Это предполагает в том числе введение в действие единых требований к качеству и безопасности таких продуктов. В соответствии с принятым в мире порядком они реализуются в форме внедрения стандартов надлежащей производственной практики. Применение таких стандартов регулируется следующими нормативными документами:
Обратите внимание!
Для полноценного применения разработанного административного регламента необходимо решение Правительства о порядке реализации некоторых процедур, связанных с проведением фармацевтических инспекций. Приказ № 2945 вступит в силу только после принятия соответствующего постановления: пока этого не произошло.
Преимущества обладания сертификатом
Несмотря на необходимость проведения достаточно сложной и дорогостоящей процедуры, производители знают, что сертификация по стандартам GMP является весьма важной для представителей фармацевтической отрасли. В частности, оно обеспечивает продукции и производству следующие серьезные преимущества:
КОММЕНТАРИЙ ЭКСПЕРТА АТТЭК
Каков срок действия сертификата?
Срок действия российских сертификатов составляет 3 года. При этом срок действия иностранного сертификата GMP составляет от 1 до 3 лет. По истечении этого периода сертификацию потребуется проходить заново. Кроме того, это означает, что на протяжении всего этого срока компании необходимо обеспечить соответствие своего производства и продукции требованиям комплекса правил GMP.
Кто в России занимается сертификацией по стандартам GMP?
Сейчас сертификация контролируется департаментом развития медицинской и фармацевтической промышленности Министерства промышленности и торговли РФ. Он является организацией, ответственной за обеспечение надлежащего контроля за качеством, безопасностью и эффективностью лекарственных средств. Осуществлением требуемых сертификационных процедур занимается Государственный институт лекарственных средств и надлежащих практик (ФГБУ «ГИЛС и НП»).
Стандарт GMP в международной практике
Процесс сертификации на соответствие лекарственного препарата стандартам GMP в международной практике имеет комплексный характер, а ее основной целью является подтверждение безопасности и действенности продукции. В этой связи для достижения поставленной цели специалисты аккредитованных сертификационных организаций не ограничиваются оценкой ряда выборочных образцов лекарственных препаратов, как это часто предусматривается другими стандартами. В процедуру установления требуемого уровня качества лекарств любой международный центр сертификации лекарственных средств включает оценку предприятия, занимающегося его выпуском. В результате эксперты, занимающиеся проведением сертификации, анализируют конкретный препарат и процесс его выпуска в следующих областях:
Правила GMP в России
Порядок и сроки проведения всех операций в рамках этой процедуры, список лиц и организаций, ответственных за их осуществление, размер платы за проведение экспертной оценки и другие аспекты выполнения сертификации определены постановлением Правительства № 1314.
Процедура получения сертификата в России
Первым шагом для производителя, который желает пройти сертификацию, является подача соответствующего заявления в Минпромторг. В течение 10 рабочих дней специалисты ведомства проводят проверку корректности представленных в заявлении сведений и определяют возможность проведения сертификации.
В случае необходимости они вправе запросить у заявителя дополнительные документы, которые он обязан предоставить в течение 20 рабочих дней. В случае, если в отношении данного препарата принято положительное решение о проведении процедуры сертификации, необходимые данные направляются в ФГБУ «ГИЛС и НП», который в течение 20 рабочих дней с момента их получения обязан определить дату проведения сертификационных мероприятий и внести ее в график. Такая дата должна наступить не позднее 160 рабочих дней со дня, когда специалисты Минпромторга приняли положительное решение о сертификации, а сама экспертиза и расшифровка ее результатов должны занимать не более 10 рабочих дней.
На подготовку итогового отчета по результатам ее проведения исполнителю отводится 30 рабочих дней, а на его направление заявителю — 3 рабочих дня. Копия такого отчета также направляется в Минпромторг. На основании отчета формируется окончательное заключение, которое в случае положительного характера сопровождается выдачей сертификата производителю лекарственного препарата.
Документы для сертификации
Чтобы получить сертификат GMP в России, производитель обращается в уполномоченный орган с заявлением, к которому прилагает пакет документов, включающий:
Важнейшие документы предоставляются заявителем в копиях, поскольку при утере их восстановить невозможно или очень сложно. Правила регламентируют, что если заявление подает иностранный производитель, и некоторые документы в составе пакета представлены на другом языке, они должны быть переведены на русский язык и заверены в установленном порядке.
Сроки сертификации
Общая продолжительность процедуры сертификации складывается из следующих сроков.
Этап сертификационной процедуры
Максимальная допустимая продолжительность
Проверка полноты пакета документации, представленной с заявлением о сертификации, и правильности ее оформления, назначение инспекции
Направление информации о назначении инспектирования в уполномоченное учреждение, которое проводит проверку
Инспектирование и анализ лекарственного средства
Принятие решения о выдаче заключения по результатам инспекционного отчета
160-дневный период инспектирования включает внесение производителя в график инспекций, ожидание процедуры и проведение самой инспекции. Она должна занимать не более 10 рабочих дней.
Такой порядок действует, если в документации, поданной производителем, не обнаружат ошибок и недочетов, из-за которых ее могут направить на доработку. В этом случае вся процедура займет немногим более 180 рабочих дней, то есть свыше 8 месяцев.
Стоимость получения сертификата
Обязательной для всех производителей лекарственных средств, претендующих на получение сертификата, подтверждающего соответствие их продукции стандартам GMP, является оплата государственной пошлины за рассмотрение соответствующего заявления в Министерстве промышленности и торговли. Ее размер составляет 7500 рублей. Оплатить данную сумму необходимо еще до подачи заявления в ведомство, а ее размер никак не зависит от результатов рассмотрения документа.
Однако данная пошлина — это далеко не единственный и не самый крупный платеж, который потребуется осуществить производителю лекарств. Другой значительной статьей расходов станет плата за проведение экспертной оценки производства и продукции заявителя. Такая процедура выполняется специалистами ФГБУ «ГИЛС и НП»: для каждого из них предварительно проводится аттестация эксперта по GMP в России.
При этом размер платы за проведение оценки не является строго установленным, а определяется в зависимости от объема, характера и сложности необходимых процедур в соответствии с положениями приказа Министерства промышленности и торговли Российской Федерации от 11.01.2016 № 9 «Об утверждении методики определения размера платы за оказание услуги по инспектированию GMP». В случае, если проверка потребует проведения значительного объема работы и привлечения большого количества высококвалифицированных экспертов, размер платы за ее проведение может превышать 2,5 миллиона рублей.
Разбор Что такое сертификат GMP и зачем он нужен кормовым компаниям
Корма составляют до 70% в структуре себестоимости производства молока, именно поэтому аграриям очень важно качество готового продукта. От того, насколько эффективны и безопасны корма и кормовые добавки, напрямую зависит прибыль молочного хозяйства. Сегодня на рынке представлено множество предприятий, которые заявляют о высоком качестве продукта, но часто, кроме громких заявлений, за этим ничего не стоит. Как разобраться в большом разнообразии компаний на рынке? Для этого существуют международная система сертификации кормовых компаний GMP+, которая гарантирует, что все производственные процессы компании соответствуют высоким требованиям стандарта. Наличие такого сертификата говорит о том, что выпускаемые компанией продукты полностью безопасны и качественны. Вместе с обладателем такого сертификата — компанией «Мустанг Технологии Кормления» — Milknews разобрался, что такое GMP+ и как его получить. Также предлагаем читателям пройти опрос о сертификате GMP+.
Что это такое?
Сертификат GMP (Good Manufacturing Practice) – официальный документ, который говорит о том, что на данном предприятии соблюдаются «надлежащие производственные практики». Этот международный стандарт определяет требования к организации и контролю качества кормов, кормовых добавок и премиксов.
Первые принципы надлежащей производственной практики были сформулированы в США в 1963 году для фармацевтической промышленности. Правила GMP официально внедрены на государственном уровне в Евросоюзе и США для производителей лекарственных препаратов, в том числе для животных, а также пищевых добавок. В России правила GMP для фармацевтической отрасли включены в ГОСТ Р 52249 «Правила производства и контроля качества лекарственных средств» и ГОСТ Р 53699 «Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP». Фактически во многих странах нормы GMP обеспечивают товарам доступ на рынок и являются своеобразной лицензией на работу.
Для компаний по производству кормов требования GMP в России не считаются обязательными, но некоторые прогрессивные участники рынка в России успешно внедряют их. Для кормовых компаний действует сертификат GMP FSA, который состоит из нескольких стандартов: одного общего GMP+ B1 «Производство, торговля и услуги» и трех для более конкретных видов деятельности GMP+B2 «Производство кормовых ингредиентов», GMP+B3 «Торговля, сбор, хранение и перевалка», GMP+ B4 «Перевозка».
Чем GMP отличается от других?
Сегодня на многих предприятиях действуют серьезные системы контроля качества и безопасности. Однако зачастую на заводах контролируются только выборочные образцы продукции, которые по сути гарантируют качество только этих образцов и партий. Стандарт GMP+ представляет собой целостный подход и регулирует все принципы производства. Таким образом, правила надлежащей производственной практики снижают риск ошибки и производства некачественного или опасного товара до минимума.
Какие требования предъявляются к качеству и безопасности?
GMP+ устанавливает четкие и прозрачные требования к производству. В основу GMP+ входят нормы HACCP и требования ISO 9001, а также специальные требования к продукции и всем производственным процессам. Нормы по продукции основаны на европейских стандартах качества и безопасности. GMP+ определяют требования к персоналу, помещениям, документации, контролю качества.
Правила предписывают регистрировать все этапы производства и отклонения. Любое действие на предприятии должно быть задокументировано. В случае необходимости, сотрудники завода могут поднять запись по любому этапу производственного процесса, узнать результаты лабораторных исследований или имена сотрудников, которые их проводили.
Сложно ли получить сертификат?
Для того, чтобы получить сертификат, компании нужно обратиться в специальный сертификационный орган, уполномоченный проводить подобный аудит. По словам представителя компании «СЖС Восток Лимитед», которая проводит аудиты, перед подачей заявки, компании стоит убедиться, что в компании грамотно выстроена система менеджмента безопасности и качества кормов.
Какие кормовые компании получили такой сертификат в России?
В компании строго следят за качеством продукции: для производства используются только натуральные ингредиенты, качественные витаминные и минеральные комплексы и добавки, проверенное сырье. Основной портфель компании составляют продукты собственного производства. С 2010 года “Мустанг” регулярно подтверждает соответствие стандарту ISO 9001. Соблюдение международных норм безопасности — дополнительный инструмент контроля качества на всех этапах производства.
Через расстояния

FDA США приостановило все очные инспекции и сосредоточилось на проведении инспекций в удаленном и документальном формате, используя уже внедренную в стране риск-ориентированную модель оценки производства в тесной ее взаимосвязи с другими регуляторными данными, а также данными по контролю качества и фармаконадзору.
В период пандемии как никогда стала актуальной тема эффективного использования ресурсов регуляторов и отрасли, международного сотрудничества и «регуляторного доверия» (regulatory reliance), принятие во внимание отчетов других регуляторных органов мира о проведенных инспекциях и экспертизах, признание оценок, выполненных другими компетентными регуляторными органами. Страны, имеющие в своей системе инспектирования подходы, основанные на риск-ориентированной модели, смогли наилучшим образом адаптироваться к условиям пандемии и распределить ограниченные ресурсы. Все это позволяет не дублировать инспекции, сфокусировав работу на приоритетных производствах и новых функциях.
Внедрение формата дистанционных инспекций потребовало от регуляторных агентств и отрасли активного использования цифровых технологий: видеотуров по производству, предоставления большого объема документации по закрытым каналам связи, использования облачных хранилищ, работы с конфиденциальными данными и обеспечения информационной безопасности. А также проведения совещаний по теле- и видео-конференц-связи, работа в разных временных зонах, привлечение переводчиков и многое другое.
Несмотря на новизну этого опыта и порой экстремальность условий в пандемию первые результаты можно оценить как положительные. Отрасль работала в тесной взаимосвязи с регуляторами, внедряя новые для обеих сторон форматы работы. Благодаря своевременным и правильным управленческим решениям регуляторных органов РФ, оперативной перестройке системы инспектората Минпромторга РФ и ГИЛСиНП, а также конструктивному партнерству с индустрией российская система инспектирования продемонстрировала новое качество своего функционала, достойно справилась с задачами и успешно встроилась в международный формат.
По прошествии времени очень важно оценить этот опыт и опыт агентств других стран, и внедрять инструменты риск-ориентированной модели инспектирования, признания оценок других регуляторных органов, информационные технологии, дистанционное инспектирование производств с низким риском или результаты прежних инспекций в рутинную регуляторную практику. Это позволит всем эффективно перераспределить ресурсы и сфокусировать внимание на проблемных зонах, повышая качество продукции и производственных процессов.
Хайнц Шмидт, директор компании Merck Life Science в России и странах СНГ:
Наталья Моргунова, директор отдела клинических исследований, регистрации продукции и медицинских программ в России и Белоруссии компании «Ново Нордиск»:
— Сейчас мы наблюдаем новый уровень взаимодействия между фарминдустрией и регуляторными органами, ориентированный на совместный поиск решений. Продление действующих сертификатов GMP на год, гибкие подходы к GMP-инспекциям и другие меры позволяют повысить доступность инновационных препаратов.
Дмитрий Овчинников, директор по регуляторным вопросам компании AbbVie по России и СНГ:
— В условиях пандемии AbbVie, как и другим фармацевтическим компаниям, пришлось преодолеть многие препятствия и оперативно перестраиваться для сохранения бесперебойности поставок. В конце мая проведена первая дистанционная инспекция нашей производственной площадки в Италии (AbbVieS.r.L.) на соответствие правилам российского GMP. В ходе инспекции было задано много вопросов, связанных с производственными процессами, организацией системы качества и безопасности, а также взаимоотношениями участников производственного процесса. Успешное проведение дистанционной инспекции площадки позволило продолжить процесс регистрации нового препарата.
Наталия Назарова, руководитель отдела регистрации и обеспечения качества лекарственных препаратов компании «Рош»:
— В мае «Рош» стала первой международной компанией, которая в условиях пандемии прошла российскую дистанционную GMP-инспекцию своей зарубежной производственной площадки. Ее проведение потребовало тщательной оценки технических средств и подготовки всех сторон. Но с учетом ограничений, связанных с эпидемической ситуацией, это позволило максимально приблизиться к формату выездной инспекции на площадке.
Наталья Чукреева, директор по фармацевтической деятельности по странам ЕАЭС компании Сервье»:
— Гибкий подход к поддержанию регистрационного статуса препаратов позволяет обеспечивать как их наличие, так и пациентоцентричность действий фармкомпаний. В период пандемии предприятия работали в напряженном режиме, восполняя срочные потребности здравоохранения. В мае и июне вступили в действие документы правительства и минпромторга, конкретизирующие правоприменение постановления № 440. В июне минпромторг продлил заключения для предприятий, в том числе и зарубежных. Считаем, что это способствует полноценному восстановлению отрасли.
Олег Прокофьев, директор по регистрации компании «Такеда»:
— Пандемия создала условия, в которых всем игрокам фармрынка нужно было принять срочные меры для обеспечения пациентов качественными лекарствами. Ряд инициатив фармотрасли был учтен, также были внедрены дистанционные GMP-инспектирования. Эти меры позволили сохранить контроль за качеством лекарств и способствовали продолжению регистрационной деятельности в отношении новых препаратов.
Сертификация GMP
Для реализации зарубежного медицинского препарата в России важно получить разрешение – сертификат GMP (Good Practice Manufacturing) российского образца. Выдается документ Министерством промышленности и торговли РФ. Для этого проверяется зарубежная площадка, где выпускается продукция. На всех этапах процедуры важна поддержка специалистов, обеспечить которых готова компания GlobalPharma.
Этапы подготовки к
инспекции Минпромторга РФ
Наша команда профессионалов
Соглашаюсь с политикой конфиденциальности
и даю согласие на обработку персональных данных.
Подготовительные этапы
Обратившись в GlobalPharma, клиенты могут рассчитывать на профессиональную помощь. Сотрудничество состоит из таких этапов:
Специалисты помогут пройти сертификацию, получить положительное решение Минпромторга и ФГБУ «ГИЛС и НП».
Экспертная помощь
Обратившись в GlobalPharma, клиенты могут рассчитывать на экспертную помощь, а именно:
В результате продукция пройдет успешную сертификацию GMP, что позволит реализовывать продукт в РФ.
Требуемые документы
Для получения разрешения реализовывать продукт в России, важно подготовить ряд бумаг:
Если по продукции были выявлены несоответствия, не подтверждено качество, эту информацию также нужно предоставить. Производитель должен в письменной форме дать согласие на произведение инспекции.
Как проходит процедура
Первоначально подается заявление и готовится документация. После Минпромторг проводит инспектирование (на инспекцию выделятся 10 рабочих дней). Потом принимается решение. Если у представителей Министерства промышленности и торговли РФ возникнут вопросы, они могут подать запрос, к примеру, запрос на подтверждение сведений о предъявленных бумагах. Для предоставления ответа заявителю дается 20 рабочих дней. Если за это время ответ не поступит, сертификат GMP получить не удастся. Полученный сертификат действителен 3 года.
Выполненные работы
Кейс Сертификация по GMP: Проведение инспекции и получение сертификата GMP Минпромторга РФ за 8 месяцев.
Компания «ПП» обратилась в Глобалфарма с целью проведения инспекции GMP Минпромторга РФ. Данная компания не имеет своего представительства в РФ и делегировала нам свои полномочия по организации инспекции своей производственной площадки.
22.02.2017 подписали договор на проведение и сопровождение инспекции GMP Минпромторга РФ производственной площадки, расположенной в одной из европейских стран.
Мы провели анализ имеющихся документов площадки и разработали пакет документов в соответствии с требованиями Минпромторга РФ. Это заняло у нас 2 недели.
03.03.2017 подали заявление и пакет документов в Минпромторг РФ на проведение инспекции.
Около 3-х недель документы были на рассмотрении в Минпромторге и в апреле регулятор нас проинформировал, что документы были переданы в сертификационный орган РФ.
25.04.2017 мы получили письмо о назначении дат инспекции (18-23.09.2017) и подтверждение о внесении данной площадки в график инспекций Минпромторга РФ: http://minpromtorg.gov.ru/activities/services/licensing/ (раздел Лекарственные средства/Выдача заключений GMP).
С апреля по сентябрь 2017 нами были согласованы организационные моменты по трансферам, проживанию и присутствию инспекторов и переводчиков на производственной площадке.
В запланированные сроки 18.09.2017 инспекторы Минпромторга РФ прибыли на производственную площадку для проведения инспекции.
По завершении инспекции 23.09.2017 мы получили письмо 06.10.2017 от Минпромторга РФ по незначительным замечаниям, которые были исправлены производственной площадкой незамедлительно.
11.10.2017 подготовили письмо по внедренным изменениям, которое было направлено в Минпромторг РФ.
27.10.2017 компанией «ПП» был получен сертификат о соответствии нормам российского GMP.
Общее время на получение сертификата GMP Минпромторга РФ производственной площадки заняло 8 месяцев, из них 5 месяцев были в очереди на проведение инспекции.
P.S. Название компании и иные конфиденциальные данные были намеренно скрыты с целью соблюдения соглашения о конфиденциальности между нашими компаниями.
Соглашаюсь с политикой конфиденциальности
и даю согласие на обработку персональных данных.
Кейс регистрация БАД. Регистрация 10 наименований БАД за 10 месяцев на территории РФ и таможенного союза.
Компания ЛК обратилась к нам с целью регистрации 10-ти наименований БАД (различного состава и формы выпуска) на территории РФ и Таможенного союза.
В августе 2016 г. подписали соглашение о конфиденциальности и договор. А также был заключен договор иностранного производителя с юридическим лицом на территории РФ (так как заявителем может быть только юридическое лицо на территории РФ или Таможенного союза).
В конце августа 2016 нами были проанализированы документы по рецептуре на их соответствие нормам ТР ТС 021/2011.
По итогам проведенного анализа документов у заказчика были запрошены дополнительные документы на каждый БАД (схема производства, диплом переводчика и т.д.), а также нами были даны рекомендации по обновлению имеющейся документации в соответствии с требованиями аккредитованного органа инспекции.
10.2016 Собранное досье на основании заявки подали в аккредитованный орган инспекции для проведения экспертизы.
10.2016 Было получено от эксперта направление на лабораторные исследования 10 БАДов. Нами были подобраны лаборатории и отданы образцы БАДов на проведение исследований.
11.2016 По определенным лабораторным показателям некоторые БАДы не соответствовали заявленным критериям и образцы были отправлены на повторное исследование в другую лабораторию. На основании лабораторных исследований и полученных показателей экспертами аккредитованного органа инспекции было подготовлено и выдано экспертное заключение о соответствии заявленных 10-ти БАДов нормам ТР ТС 021/2011, ТР ТС 022/2011, ТР ТС 029/2012 и СанПин 2.3.2.1290-03.
12.2016 По полученному экспертному заключению было сформировано досье для подачи в регуляторный орган с целью получения свидетельства о государственной регистрации.
01.2017 Подали заявление на регистрацию вместе с досье в регуляторный орган.
02.2017 Получены замечания от эксперта регуляторного органа на внесение дополнительной информации, которые были разрешены должным образом.
05.2017 Получено свидетельство о государственной регистрации.
Общий срок регистрации 10 БАДов различного состава и форм выпуска и получения свидетельства о государственной регистрации составил 10 месяцев.
P.S. Название компании и иные конфиденциальные данные были намеренно скрыты с целью соблюдения соглашения о конфиденциальности между нашими компаниями.
Соглашаюсь с политикой конфиденциальности
и даю согласие на обработку персональных данных.