Зеленящие стрептококки
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику. Под наименованием «Зеленящие стрептококки или S.viridans» прячется целая группа микроорганизмов, относящихся к альфа-зеленящим стрептококкам семейства Streptococcaceae.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Под наименованием «Зеленящие стрептококки или S.viridans» прячется целая группа микроорганизмов, относящихся к альфа-зеленящим стрептококкам семейства Streptococcaceae. Эта группа является очень важным компонентом в составе нормально микрофлоры полости рта, слизистых оболочек дыхательных путей, пищеварительного тракта и половых органов. Поэтому обнаружив следующих ее представителей (S.gordonii, S.oralis, S. mutants, S.sanguis и S.salivarius) в посеве из полости рта, не надо немедленно начинать это лечить – этим вы только навредите организму, выбив из его состава важный компонент его нормальной микрофлоры.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
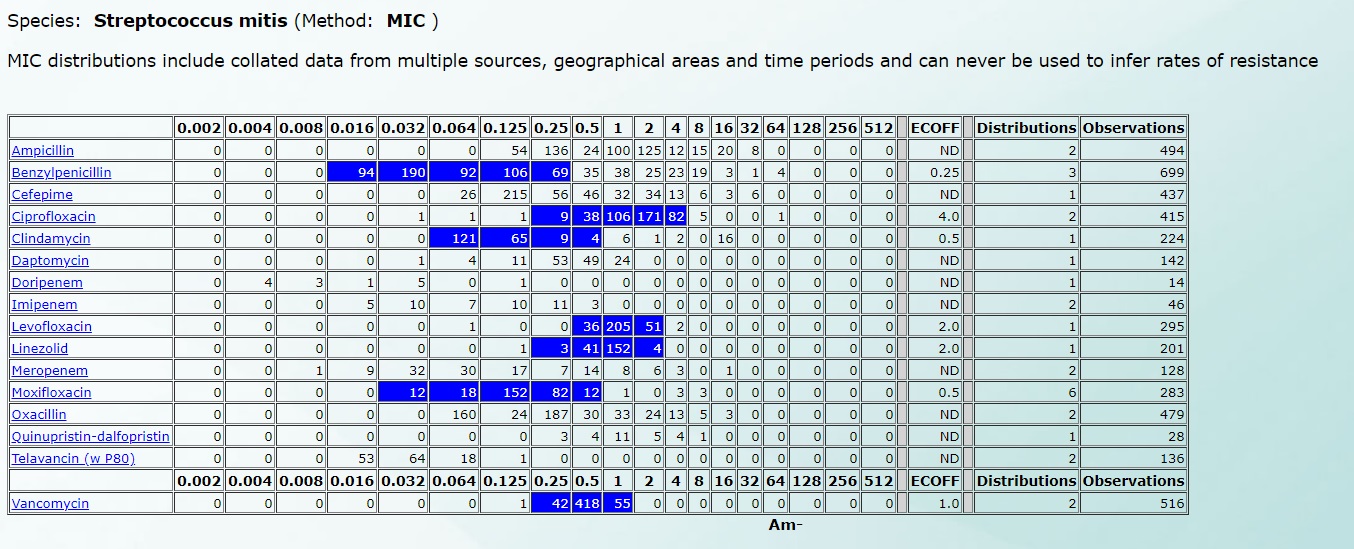
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
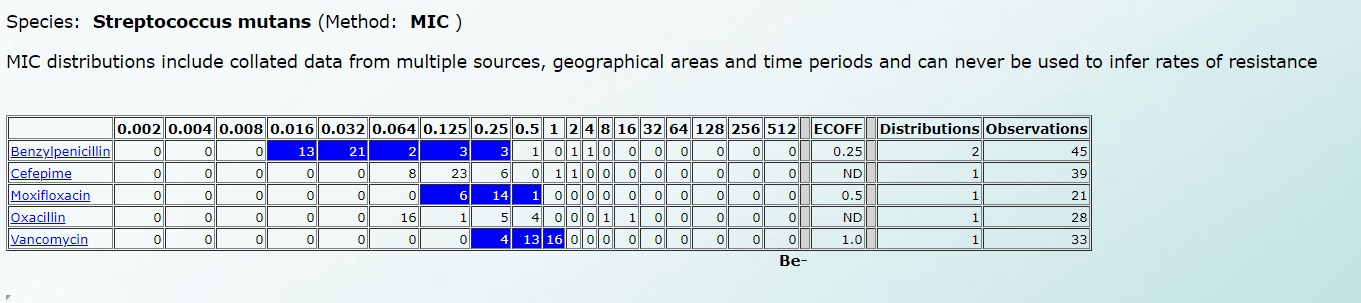
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
Gemella (гемелла)
Гемелла (Gemella) – неподвижные грамвариабельные аспорогенные бактерии. Чаще всего они колонизируют в ротовой полости, в верхних отделах ЖКТ. Вид гемелла впервые выявили в 1938 г., а спустя почти 30 лет, его выделили в отдельный род. Название «Gemella» было предложено из-за особенности строения микроорганизма: их относят к диплококкам.
Систематика грамвариабельной бактерии гемеллы
Раньше гемелла входила в род стрептококков, но после тщательного изучения, ее вывели в Bacillales Family XI. Incertae Sedis.
Бактерии анаэробны, способны давать отрицательную реакцию на разные виды окрашиваний. Гемеллы обладают способностью ферментировать, производить кислоты.
К роду гемелла относят следующие микроорганизмы:
Гемелла встречается в ротовой полости, в верхних отделах пищеварительной системы у людей и у животных. Разновидность haemolysans способна вызывать легочные патологии у людей, страдающих пороками сердца, после стоматологических вмешательств. Для подавления колоний бактерий, применяют гентамицин и пенициллиновый ряд антибактериальных препаратов. При обнаружении гемеллы во влагалище, велика вероятность заражения ВИЧ-инфекции.
В некоторых случаях гемелла обнаруживается в желудке, но только при условии отсутствия большого количества хеликобактери пиллори.
Строение и размножение бактерии гемелла
Бактерии Gemella попадают во внешнюю среду с дыханием человека, животного. Этот вид имеет продолговатый сферический вид. Чаще всего они располагаются в парах. Соприкасающиеся стороны имеют уплощение. Как правило, в паре одна гамелла крупнее другой.
Стенка бактерии дает грамположительный окрас, а по Граму — вариабельна. Бактерии можно культивировать на кровяном агаре, МПА, где образуется росинчатые маленькие колонии. На молочном и капустном субстрате растут медленно. Бактерии способны вызывать гемолиз.
Некоторые представители рода колонизируют на растениях. Они могут сбраживать молоко, из-за чего применяются в пищевой промышленности совместно с другими видами микроорганизмов (например, для получения сыров, квашенной капусты). Микробактерии размером до 1.2 мкм окружены капсулой. При средней температуре 25 градусов хорошо размножаются.
При выявлении гемеллы в организме человека, применяют антибактериальные препараты пенициллинового ряда.
Особенности антибактериальной терапии неспецифических анаэробных инфекций
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ГКБ № 23 им. «Медсантруд», Москва
А наэробные бактерии представляют собой разные группы микроорганизмов (рис. 1), способных удовлетворять энергетические потребности при отсутствии кислорода (не более 0,5% для строгих анаэробов и от 2 до 8% для умеренно облигатных анаэробов [1]).
Рис. 1. Рабочая классификация клинически значимых анаэробов
Анаэробы формируют нормальную микрофлору человека и в отдельных локусах (прямая кишка, ротовая полость) превышают на несколько порядков число аэробных (Pseudomonas aeruginosa, Acinetobacter spp. и др.) и факультативно анаэробных (семейство Enterobacteriaceae, Staphylococcus spp., Streptococcus spp., Enterococcus spp. и др.) микроорганизмов (табл. 1). С практической точки зрения важно знать, какие группы анаэробов колонизируют разные участки тела, так как большинство анаэробных инфекций эндогенного происхождения и анаэробы распространяются из места своего обитания в прилежащие стерильные ткани, где развивается инфекционный процесс. Например, анаэробы группы Bacteroides fragilis колонизируют толстый кишечник и наиболее часто связаны с развитием интраабдоминальных инфекций. Prevotella spp., Porphiromonas spp. и Fusobacterium spp. обитают в верхнем отделе дыхательного тракта и поэтому чаще встречаются среди возбудителей плевролегочных инфекций. Actinomyces spp. колонизируют верхние дыхательные пути и ЖКТ, в связи с чем способны вызывать актиномикозы шейно-лицевой, торакальной и абдоминальной локализации.
Экзогенные анаэробные моноинфекции встречаются относительно редко и в основном связаны с клостридиями. Обычно это пищевые отравления, ботулизм, столбняк, гастроэнтерит и некротический энтерит, мионекроз.
Клостридии. Газовая гангрена (мионекроз) является классической раневой анаэробной инфекцией, вызываемой гистотоксическими клостридиями. Среди них ведущую роль играет C. perfringens (80%), в меньшей степени C. novyi (40%), C. septicum (20%), далее следуют C. histolyticum и C. bifermentans [3]. Гемокультура выделяется у 15% больных [4]. При скальпированных ранах с вовлечением мышечной и других мягких тканей при участии C. perfringens возникает анаэробный целлюлит, также сопровождающийся газообразованием, но в отличие от мионекроза мышцы сохраняют жизнеспособность [5]. К развитию инфекции часто подключаются E. coli, Peptostreptococcus spp, Bacteroides spp. и другие бактерии. Неклостридиальный крепитирующий целлюлит отличается по клинике и более широким спектром ассоциаций возбудителей: Peptostreptococcus spp, Streptococcus spp., S. aureus, E. coli, Klebsiella spp, Proteus spp., Prevotella spp., Porphiromonas spp., группа Bacteroides fragilis. При обеих формах целлюлита в пораженных тканях скапливаются нерастворимые в воде водород и азот, что создает условия для реализации анаэробного пути метаболизма бактерий [6].
У больных с обструктивными или перфоративными повреждениями терминальных отделов подвздошной и толстой кишки клостридии (в первую очередь C. perfringens и C. septicum [7]) участвуют в развитии перитонита, интраабдоминального абсцесса, септицемии. Бактериемия, обусловленная C. septicum, наблюдается у 70-85% больных с карциномой толстой кишки, лейкемией или лимфомой [7]. C. perfringens выделяется из вагины у 1-9% здоровых беременных и небеременных женщин, поэтому возможно возникновение инфекции, чаще после криминального аборта [8]. Токсигенные штаммы C. difficile, колонизирующие толстый кишечник, вызывают псевдомембранозный колит, который лечится приемом внутрь метронидазола или ванкомицина.
Неспороносные грамположительные анаэробы очень чувствительны к действию кислорода даже при использовании транспортных сред и в отличие от других анаэробов при посеве растут более 48 ч, в связи с чем, их значение в патологии часто недооценивается. Среди палочковидных бактерий актиномицеты являются наиболее наглядными условными патогенами, вызывающими актиномикозы разной локализации (в основном экзогенного происхождения). Mobiluncus curtisii и M. mulieris имеют отношение к возникновению бактериального вагиноза (в ассоциации с Gardnerella vaginalis). Eubacterium spp. входят в состав фекальной флоры и иногда вызывают раневую инфекцию и эндокардит. Бифидобактерии и лактобациллы колонизируют толстый кишечник, где снижение их пороговой концентрации сопровождается явлениями дисбактериоза, и вегетируют в ротовой полости; в редких случаях, выходя за пределы своей экологической ниши, они могут вызвать плевропневмонию. Пропионобактерии обитают на коже, а Propionobacterium acnes служит причиной появления угревой сыпи и может вызывать катетерную инфекцию.
Большинство палочковидных анаэробов чувствительны к карбокси- и уреидопенициллинам, цефокситину, карбапенемам и хлорамфениколу. Mobiluncus curtisii и M. mulieris чувствительны к ампициллину, цефалоспоринам, клиндамицину, эритромицину, ванкомицину и резистентны к метронидазолу (МИК90=256 мкг/мл) [11]. Метронидазол не активен против Actinomyces spp. и Propionobacterium spp. (МИК90 варьирует от 25 до >125 мкг/мл), но 92% культур Eubacterium spp. сохраняют к нему чувствительность [12].
Пептострептококки наиболее широко представлены в качестве возбудителей анаэробных инфекций. С ними тесно связана этиология послеродового эндометрита: Peptostreptococcus magnus (41%), P. tetradius (26%), P. asaccharoliticus (20%), P. anaerobius (19%), P. prevotii (15%), P. niger (4%) [13]. Они часто выделяются при тубоовариальных абсцессах, воспалительных заболеваниях органов малого таза, септическом аборте, амнионите и хориоамнионите [14], нередко в ассоциациях с Prevotella spp., Porphiromonas spp., E. coli, Streptococcus spp., а также при периодонтитах, хроническом среднем отите, хроническом синусите, абсцессе мозга. При их аспирации из ротовой полости возникают пневмониты, некротизирующая пневмония, легочные абсцессы, эмпиема плевры (часты ассоциации со стрептококками и кишечной палочкой). Перечисленные заболевания нередко сопровождаются бактериемией. При перитонитах пептострептококки участвуют в смешанных инфекциях. P. magnus играет важную роль при инфекциях костей и суставов, катетерной инфекции.
Грамотрицательные анаэробы выделяются более чем у 50% больных при неспецифических инфекциях. Среди них ведущее положение занимает группа Bacteroides fragilis, включающая разные виды, из которых наибольшее клиническое значение имеют B. fragilis и B. thetaiotaomicron, прежде всего при абдоминальных инфекциях, а также инфекциях других локализаций. Бактероиды группы fragilis превалируют среди нормальной микрофлоры ЖКТ, в незначительном количестве встречаются в нижних отделах генитального тракта и практически отсутствуют в ротовой полости и среди микрофлоры верхних дыхательных путей (ВДП). Они продуцируют бета-лактамазы, что определяет профиль их антибиотикоустойчивости.
Fusobacterium nucleatum обычно встречаются во рту, генитальном тракте, ЖКТ, ВДП и могут вызывать абсцессы мозга, легких, септический артрит и другие инфекции соответствующей локализации. Fusobacterium necroforum отличается высокой вирулентностью и является возбудителем тяжелого тонзиллофарингита у детей и лиц молодого возраста (ангина Венсана), вплоть до образования метастатических абсцессов в легких, плевральной полости, печени, крупных суставах, сопровождающихся бактериемией [17].
Рис. 2. Влияние сроков транспортировки биоматериалов на высеваемость разных групп бактерий
Показания к обследованию на анаэробы ограничиваются следующими патологическими состояниями:
— сепсис неясной этиологии;
— гангрена, абсцессы, флегмона;
— нагноения ран с подозрением на анаэробную инфекцию.
Анаэробную инфекцию можно заподозрить по ряду косвенных признаков. Это прежде всего наличие заболевания, прочно ассоциируемого с анаэробной этиологией (периодонтит, аспирационная пневмония, интраабдоминальная инфекция, раны после укусов животных и человека), и клинических условий, связанных с деструкцией тканей и бедным их кровоснабжением (при травме, злокачественных новообразованиях). Существенную роль играет близкая локализация инфекции к поверхности слизистых оболочек, газообразование в ткани, формирование абсцесса, гнилостный запах отделяемого. И, наконец, обнаружение гранул серы в содержимом гайморовых пазух наводит на мысль об актиномикозе. Однако ни один из перечисленных признаков не является специфичным, и для объективного подтверждения анаэробной инфекции требуется посев соответствующих биоматериалов. Материалами для исследования служат:
— кровь, ликвор (особенно, если он мутный), плевральная, перитонеальная, синовиальная жидкости;
— гной из абсцессов и других закрытых полостей (транспортируют в шприце с полностью вытесненным воздухом и согнутой у основания иглой). Если объем гноя превышает 2 мл, то в пробирке под резиновой пробкой сохраняются относительно анаэробные условия в течение нескольких часов;
— материалы из глубоких отделов свища (после очистки и асептической обработки наружного отверстия) и ран. Если нет возможности использовать метод аспирации шприцом, материал берут стерильным ватным тампоном, который помещают в анаэробную среду сохранения и до транспортировки в лабораторию содержат при комнатной температуре;
— фрагменты костной и мышечной ткани размером 1х1 см, взятые из глубокого очага воспаления во время операции. Если сроки доставки материалов в лабораторию превышают 15-20 мин, фрагменты тканей погружают в небольшой объем стерильной смеси, состоящей из цитратной донорской крови и 90% стерильного изотонического раствора хлористого натрия.
Не подлежат исследованию на анаэробы:
— отделяемое поверхностных ран, язв;
— мазки из зева, носа, ротовой полости;
— мазки из влагалища, цервикального канала;
— мокрота, бронхиальные смывы;
— моча (кроме мочи, полученной надлобковой пункцией мочевого пузыря);
— содержимое желудка, тонкого и толстого кишечника;
Основы антибактериальной терапии анаэробных инфекций. Учитывая трудоемкость и длительность получения результатов, определение чувствительности анаэробов к антибиотикам, согласно Международным рекомендациям [23] показано при выделении:
— анаэробных гемокультур и штаммов из ликвора;
— изолятов в чистой культуре и от больных, неподдающихся антибиотикотерапии;
— штаммов при инфекциях, требующих длительного лечения (особенно, когда мониторинг затруднен, как при остеомиелитах).
Обычно используют метод разведений в агаре, микро- (на плашках) и макро- (в пробирках) разведений в бульоне.
Поскольку антианаэробная терапия чаще всего проводится эмпирически, важно знать тенденции формирования резистентности клинических изолятов к антимикробным препаратам (табл. 3).
Европейские данные по группе Bacteroides fragilis, как и результаты отечественных исследователей, свидетельствуют о неэффективности ампициллина и снижении активности цефокситина (антибиотик из группы цефамицинов, отличающихся антианаэробным спектром), более выраженной в Российском регионе, несмотря на то, что этот препарат не применяется в отечественной практике. Обращает внимание рост устойчивости бактероидов к клиндамицину, единичные штаммы резистентны к имипенему. Метронидазол (Метрогил) сохраняет свою активность против разных групп анаэробов (как указывалось выше, исключение составляют актиномицеты и пропионобактерии) и имеет целый ряд преимуществ по сравнению с другими антианаэробными препаратами.
Имеется широкий перечень показаний для его применения: некротические инфекции мягких тканей; хронические остеомиелиты и септический артрит; интраабдоминальные инфекции (перитонит, внутрибрюшинный абсцесс, абсцесс печени, инфекция желчного пузыря); инфекции в области малого таза (эндометрит, пельвиоперитонит, инфицированный аборт и др.); анаэробные эндокардиты; инфекции дыхательных путей (абсцесс легкого, эмпиема плевры); инфекции полости рта и околозубных тканей; профилактика анаэробной инфекции при хирургических вмешательствах в колоректальной области, на желчном пузыре, в области малого таза, в ротовой полости. Метронидазол применяют для лечения псевдомембранозного колита (C. difficile) и некротического колита, вызванного C. perfringens, а также неспецифического язвенного колита и болезни Крона, при которых возможна активация анаэробной флоры.
При многоцентровом рандомизированном двойном слепом исследовании эффективности лечения тяжелых интраабдоминальных инфекций комбинацией метронидазола с ципрофлоксацином при инфузионной и ступенчатой терапии в сравнении с имипенемом были получены одинаковые показатели исходов заболеваний в группах сравнения (82-84% излечения) [29], но фармакоэкономические преимущества были на стороне комбинированной ступенчатой терапии метронидазолом и ципрофлоксацином [30].
При лечении инфекций полимикробной этиологии подбор антибактериальных препаратов осуществляют с таким расчетом, чтобы по возможности максимально перекрыть спектр наиболее значимых предполагаемых возбудителей. Это особенно важно для анаэробов, поскольку чаще всего, в отсутствие микробиологических возможностей, ни подтвердить, ни опровергнуть их наличие в биоматериалах в ранние сроки не представляется возможным. Обычная практика применения метронидазола при тяжелых смешанных инфекциях подразумевает его комбинацию с ципрофлоксацином, либо с цефалоспоринами III-IV поколений (цефотаксим, цефтриаксон, цефтазидим, цефоперазон, цефепим) или с аминогликозидами (амикацин, нетилмицин). Из других лекарственных средств, обладающих антианаэробной активностью, часто используют ингибиторзащищенные аминопенициллины (ампициллин/сульбактам и амоксициллин/клавуланат, например, при хроническом синусите, хроническом среднем отите), пиперациллин/тазобактам (в основном при интраабдоминальных инфекциях и гнойно-воспалительных процессах в малом тазу), линкозамиды (клиндамицин и гораздо чаще применяемый в России линкомицин) в комбинации с антибиотиками широкого спектра, карбапенемы (имипенем или меропенем) при проведении монотерапии. Перспективными препаратами в лечении анаэробных инфекций за счет широкого антимикробного спектра являются цефоперазон/сульбактам и моксифлоксацин.
Выбор схемы лечения во многом зависит от локализации первичного очага и характера инфекции, тяжести состояния больного, средней продолжительности лечения соответствующей нозологической формы заболевания, медико-экономических возможностей лечебного учреждения. Имеющиеся отечественные руководства последнего периода по антибактериальной терапии [31,32] содержат конкретные рекомендации по применению современных средств в лечении широкого круга неспецифических гнойно-воспалительных заболеваний, в том числе анаэробных инфекций.
Globicatella sanguinis что это
|
Old synonym: Globicatella sanguis Collins et al. 1995.
Positive results for alanine phenylalanine proline arylamidase, alpha-galactosidase, beta-glucosidase, esculin hydrolysis, hippurate
hydrolysis, pyroglutamic acid arylamidase, starch hydrolysis, acid production from glucose (without gas production), glycogen,
mannitol, melibiose, raffinose, ribose, sucrose & trehalose.
Negative results for arginine dihydolase, alkaline phosphatase, catalase, H 2 S production, beta-glucuronidase (most strains), glycyl
tryptophan arylamidase, N-acetyl-beta-glucosaminidase, urease, Voges–Proskauer reaction, acid production from: D-arabitol,
cyclodextrin, inulin, melezitose & D-tagatose.
Variable results for beta-galactosidase, pyrrolidonyl arylamidase, acid production from lactose, methyl beta-D-glucopyranoside,
pullulan & sorbitol.