ДИАГНОСТИКА И ВАКЦИНОПРОФИЛАКТИКА ИНФЕКЦИОННОГО РИНИТА ПТИЦ. АНАЛИЗ ДАННЫХ ПО РАСПРЕДЕЛЕНИЮ ЗАБОЛЕВАНИЯ НА ТЕРРИТОРИИ РОССИЙСКОЙ ФЕДЕРАЦИИ.
Т. Б. Манин, кандидат ветеринарных наук, руководитель научно-технического отдела препаратов для птицеводства, ООО «Берингер Ингельхайм», Россия, Москва
А. В. Чернышов, кандидат ветеринарных наук, ООО «ВКНТИТ», Россия, Санкт-Петербург
Респираторные заболевания занимают ведущее место в структуре инфекционных патологий птиц. Этиологическими агентами данных заболеваний могут выступать как вирусы (ньюкаслская болезнь, грипп птиц, инфекционный бронхит кур, инфекционный ларинготрахеит, метапневмовирусная инфекция), так и бактерии (респираторный микоплазмоз, бордетеллиоз, орнитоактериоз и др.). Также к респираторным болезням относится инфекционный ринит, вызываемый бактериями вида Avibacterium paragallinarum, ранее известными как Haemophilus paragallinarum.
Инфекционный ринит (гемофилез птиц) — острое энзоотическое высококонтагиозное заболевание верхних дыхательных путей домашней птицы, в первую очередь цыплят и кур, характеризующееся катаральным воспалением слизистых оболочек носовой полости, конъюнктивы и воздухоносных пазух, а также подкожным отеком головы и в редких случаях — пневмонией. Распространение данного заболевания происходит горизонтальным путем. Источником инфекционного ринита является больная и переболевшая птица, в организме которой бактерии могут сохраняться в течение 6-12 месяцев. Опубликована информация о бактерионосительстве A. paragallinarum дикими птицами, что делает их потенциальным резервуаром инфекции. Существует мнение, что инфекционный ринит не является системной инфекцией и не способен вызвать высокую смертность восприимчивой птицы, однако при острых вспышках отход поголовья может достигать 10 %. Экономический ущерб наносится также отставанием в росте молодняка и снижением яйценоскости кур до 40 %, особенно на пике продуктивности. По антигенным свойствам штаммы A. paragallinarum классифицируют по двум основным схемам, предложенным L. A. Page и К. Кише. Наибольшее распространение получила схема Пейджа, в которой все штаммы возбудителя инфекционного ринита делятся на три серотипа: А, В и С. Данные серотипы не обладают перекрестной защитой при иммунизации птицы.
К инфекционному риниту восприимчивы птицы всех возрастов, но особенно — цыплята старше 4-недельного возраста. У молодой птицы заболевание, как правило, начинается с неспецифических клинических признаков, таких как угнетение, отставание в росте, сонливость (симптом «спящей птицы»). У кур более старшего возраста наблюдается синусит, геморрагический конъюнктивит, серозный и/или серозно-фибринозный ринит.
При прогрессировании болезни возникает синдром, схожий с часто наблюдаемым клиническим признаком при метапневмовирусной инфекции птиц, более известном как «SHS» (или синдром опухшей головы), вызывающий слепоту.
Также инфекционный ринит ассоциируется с такими патолого-анатомическими изменениями, как фибринозные поражения подчелюстного пространства, одно- или двухсторонние аэросаккулиты, септические поражения печени и почек и в редких случаях, как указывалось выше, с пневмониями.
Лабораторная диагностика.
Лабораторную диагностику инфекционного ринита птиц осуществляют классическими бактериологическими методами выделения чистых культур бактерий, а также посредством молекулярно-биологических исследований.
Для бактериологического исследования на наличие возбудителя инфекционного ринита стерильным способом отбирают кусочки легких, смывы с трахеи и инфраорбитальных синусов от вынужденно убитой с диагностической целью птицы с признаками респираторной инфекции.
Бактерии A. paragallinarum — это грамотрицательные, плеоморфные, неподвижные палочки или коккобациллы, которые растут при наличии 5-10 % углекислого газа (СО2). Для культивирования микроорганизма обязательным условием является наличие в питательной среде факторов роста гемина (X) и никотинамида-дениндинуклеотида ( NAD )( F ). Есть сведения о существовании NAD — независимых штаммов возбудителя. Рост бактерий A. paragallinarum отмечают через 24 часа культивирования в термостате при 37 °С. По морфологии колоний и культуральным свойствам их достаточно просто отдифференцировать от возбудителей других бактериальных инфекций птиц, таких как Ornithobacterium rhinotracheale, Pasteurella multocida,
Серологическая диагностика инфекционного ринита птиц — не менее важный инструмент контроля данного заболевания. Как известно, одним из самых главных преимуществ этого вида исследований является возможность контроля поствакцинального иммунитета. Для выявления специфических антител против A. paragallinarum используют иммуноферментный анализ (ИФА) и реакцию торможения гемагглютинации (РТГА). В настоящее время сертифицированных коммерческих наборов ИФА для диагностики инфекционного ринита не существует. Некоторые компании предлагают наборы ИФА для научных целей без гарантии воспроизводимости полученных результатов. РТГА, широко применяющуюся для серологической диагностики многих гемагглютинирующих вирусов и бактерий, таких как вирусы ньюкаслской болезни, гриппа птиц или возбудителя респираторного микоплазмоза, также используют для выявления антител к A. paragallinarum. С помощью РТГА достоверно определяют специфические антитела к серотипам А и С с использованием как нативного антигена, так и антигена, обработанного тиоцианатом калия. Чувствительность реакции к выявлению постинфекционных антител к серотипу С низкая. Также существует третий тип РТГА для обнаружения антител к A. paragallinarum, где для постановки реакции используют антиген, обработанный гиалуронидазой, и эритроциты, обработанные формальдегидом. Этот вариант реакции позволяет с высокой достоверностью выявлять специфические антитела к серотипам А и С. При этом ни одна из предложенных модификаций РТГА не обладает достаточной чувствительностью для выявления специфических антител к серотипу В.
Вакцинопрофилактика.
Наиболее популярной и эффективной является вакцинация против инфекционного ринита кур-несушек и племенной птицы непосредственно перед началом яичной продуктивности. Чаще вакцинация совпадает с плановым перемещением птицы из корпусов доращивания ремонтного молодняка в помещения для содержания промышленного стада. Такой тип вакцинации позволяет избежать самых значительных потерь, обусловленных развитием инфекционного ринита в период пика продуктивности. Однако в более сложных случаях, когда бактерионосительство выявляется у цыплят раннего возраста, рекомендуется проводить как минимум две вакцинации против данной болезни с интервалом между иммунизациями не менее 6 недель (в случае крайней необходимости птица может быть вакцинирована в возрасте 5 недель).
Анализ распространения инфекционного ринита на территории Российской Федерации.
Несмотря на заметный прогресс в диагностике и вакцинопрофилактике инфекционных болезней птиц в Российской Федерации, проблема борьбы с бактериальными инфекциями, в частности с инфекционным ринитом, является не решенной. Отсутствие нормативных документов по диагностике болезни и эффективных отечественных препаратов для профилактики, а также недостаток знаний в области оценки эффективности используемых вакцин привели к тому, что любая практическая информация об A. paragallinarum является актуальной для российских специалистов.
Анализ опубликованных научных данных показал, что в течение 2009-2010 гг. изоляты A. paragallinarum были выделены в 7 регионах страны. При этом возраст птиц с положительным диагнозом варьировался от 29 до 276 суток. Полевые штаммы инфекционного ринита были выявлены как от кур-несушек, так и от племенных кур мясного направления. В большинстве случаев патогенные бактерии A. paragallinarum были выделены из инфраорбитальных синусов клинически больных птиц, в меньшей степени — из других органов респираторной системы. В целом доля положительных проб составила 12 %.
В заключение стоит добавить, что существует множество неопубликованных данных о выделении чистых культур бактерий и выявлении генома A. paragallinarum из проб патологического материала в ПЦР, проведенных независимыми лабораториями, не имеющими аккредитации в Российской Федерации.
Источник: журнал «БИО» №5, 2013 г.
Вопросы борьбы с антибиотикорезистентными микроорганизмами на птицефабриках РФ
Инфекционные заболевания и заболевания, связанные с бактериями, являются причиной довольно значительной части смертей сельскохозяйственных птиц и животных. Некоторые из бактерий патогенны и для человека, их присутствие в продуктах питания может представлять опасность для его здоровья, а иногда – и жизни.
К актуальным для нашей страны возбудителям бактериальных инфекций птиц можно отнести Y. enterocolitica, Salmonella enterica, Avibacterium spp., Pasteurella spp., Listeria monocitogenes, Gallibacterium anatis, Lactobacillus salivarius (патогенные формы), Enterococcus cecorum, E.coli, Mycoplasma spp., Pseudomonas aeruginosa, Clostridium perfringens и многие другие [2, 5, 7]. Следует отметить, что большая часть перечисленных микроорганизмов не культивируется в лабораториях птицефабрик. Выделение и подтитровка на антибиотики культур кишечной палочки или стафилококков никак не могут заменить изоляцию всего многообразия этиологических агентов бактериальных инфекций.
С одной стороны, использование антибиотиков в животноводстве повышает риск попадания антибиотикоустойчивых микроорганизмов в организм человека с продуктами питания, а с другой – встает вопрос, не приведет ли ограничение потребления антибиотиков в животноводстве к росту заражения людей патогенными бактериями и повышению вероятности появления антибиотикоустойчивых штаммов. В этом случае возрастет потребление антибиотиков населением.
Из нашего опыта следует, что работа бактериологических лабораторий птицефабрик порой приносит больше вреда, чем пользы. Выделение не основной причины гибели птицы, а наиболее легко культивируемых микроорганизмов дезориентирует врача и приводит к назначению неактуальных антибиотиков. Кроме того, многие бактерии могут быть выделены только от живой птицы, и доставка проб биоматериала в посторонние лаборатории часто сопровождается гибелью притязательных микроорганизмов (пастерелл, возбудителей гемофилеза и орнитобактериоза). Из данных наблюдений вытекают два вывода:
Проблема развития антибиотикорезистентности по-прежнему стоит остро: мы регулярно выделяем полирезистентные, т. е. устойчивые к широкому спектру антибиотиков культуры E. coli и Salmonella spp., и ряду птицефабрик уже нельзя предложить антибиотик, обладающий достаточной активностью в отношении сальмонелл или кишечной палочки. Решение данной проблемы следует разбить на две части:
Наибольший риск развития антибиотикорезистентности обеспечивает повторное применение антибактериального препарата одной группы в пределах одного тура в одном и том же птичнике. Вторым по значимости фактором является использование комплексных антибиотиков (нередко это провоцирует бактериальные клетки вырабатывать столь же «комплексный» ответ, например эффлюкс).
Необоснованное применение антибиотиков и низкая их эффективность – повод для увеличения курсовых доз и кратности курсов лечения, а это, в свою очередь, ускоряет формирование устойчивых штаммов бактерий.
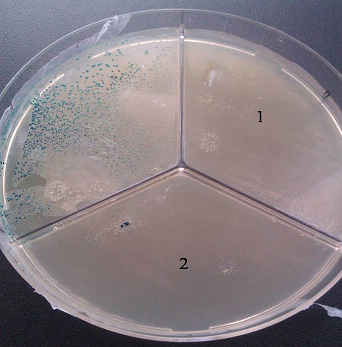
Мероприятия санитарного характера и биозащита предприятия – мощный фактор профилактики антибиотикорезистентности. Однако следует учитывать, что уничтожение устойчивых к антибиотикам микроорганизмов путем дезинфекции может быть недостаточным, важно разрушить и генетический материал, потенциально содержащий гены антибиотикорезистентности. К наиболее эффективным дезинфектантам, разрушающим ДНК, можно отнести персульфаты (Экоцид) (рис. 1.), хлорсодержащие антисептики и кислоты. Альдегиды, гуанидины и четвертичные аммонийные соединения не способны подавлять горизонтальный перенос генетических факторов устойчивости к антибиотикам [3].
Рис. 1. Подавление устойчивости к ампициллину путем разрушения плазмид с геном лактамазы. Результаты трансформации плазмиды pBlueskript, подвергнутой воздействию препаратов Экоцид (1) и HPPI (2), культуры E.coli XL Blue
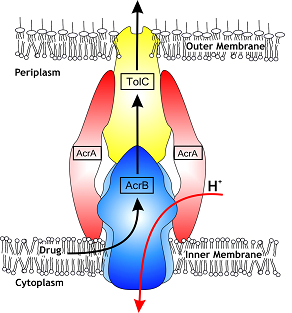
На протяжении последних лет в секторе молекулярной биологии СФНЦА РАН часто выделяются культуры кишечной палочки и сальмонелл, устойчивые к широкому спектру антибиотиков (фторхинолонам, лактамам, аминогликозидам) именно на птицефабриках, предпринявших попытку тотального отказа от данных препаратов. Резистентность к антибиотикам у этих микроорганизмов реализуется с помощью эффлюкса – системы активного выброса токсичных ксенобиотиков (рис. 2, 3), к которым относятся и многие антибиотики (энрофлоксацин, гентамицин, хлорамфеникол, флорфеникол и др.).
Для активного выброса используется система насосов, запускаемых с использованием сложной системы регуляции в ответ на оксидативный стресс, действие некоторых дезинфектантов и положительно заряженных молекул. Так, например, микотоксин цитринин, продуцируемый микроскопическими грибами родов Penicillium и Aspergillus, обладает антибактериальной активностью, вызывает дисбиоз кишечника и, в отличие от антибиотиков, попадает в организм с кормом ежедневно. Наши исследования показали наличие активации эффлюкса у сальмонелл под действием цитринина.
Таким образом, качество кормов может оказаться даже более значимым фактором, влияющим на устойчивость микробиоты птиц к антибактериальным препаратам, так как нередко птицы потребляют микотоксины непрерывно и в существенно больших концентрациях, чем антибиотики.
Что касается терапии и профилактики заболеваний, вызванных антибиотикорезистентными бактериями, картина здесь следующая.
Во-первых, далеко не всегда мы видим корреляцию результатов подтитровки на антибиотики и клинической эффективностью последних. Размеры отечественных птицефабрик велики, уровень биозащиты и высокая культура производства способствуют ограничению спектра возбудителей бактериальных инфекций. Именно поэтому результаты ограниченных экспериментов с лекарственными препаратами можно смело экстраполировать на птичники.
Во-вторых, механизмы действия многих антибиотиков до конца еще не изучены [4]. Например, некоторые антибиотики способны активировать лизогенные бактериофаги (многие бактериальные клетки содержат в своем составе неактивные бактериофаги в виде профагов). Как следует из наших исследований, наиболее часто наблюдается активизация бактериофагов под действием сульфаниламидных антибиотиков, доксициклина, флорфеникола [4]. Возможно, необъяснимо высокая клиническая эффективность сульфаниламидных препаратов обусловлена именно этим фактором. В итоге представляется перспективным использовать препараты бактериофагов в качестве дополнительного фактора для борьбы с антибиотикорезистентными формами бактерий [6].
Высокую клиническую эффективность показали челночные схемы антибиотикотерапии. Например, 2–3 дня квестигин и 2–3 дня гентамицин или 3 дня флорон и 2 дня гиракса. Преимуществом таких схем является дополнительное подавление вторым антибиотиком бактерий, приобретших устойчивость к первому. При терапии кишечных инфекций нередко развивается постантибиотический дисбиоз. В такой ситуации дополнительное введение колистина обеспечивает пребиотический эффект и минимизирует риски реинфекции.
В подавляющем большинстве случаев массовые бактериальные инфекции развиваются на фоне инфекций вирусных. Из наших наблюдений следует, что разные вирусные агенты провоцируют разные вторичные бактериальные инфекции. Например, метапневмовирусная инфекция часто влечет за собой орнитобактериозы и пастереллезы. Эшерихиозы чаще возникают на фоне всплеска ИБК, ИЛТ, болезни Гамборо и НБ. Флавивирусная инфекция кур обычно провоцирует иерсиниозы [1].
Синдром везикулярного энтерита резко повышает риск развития кормовых бактериальных токсикоинфекций, энтерококковых инфекций и бактериального эндокардита, ассоциируемого с L. salivarius [7]. Наблюдаемый последние два года парвовирусный энтерит цыплят обычно ассоциируется с широким спектром вторичных бактериальных инфекций, плохо поддающихся антибиотикотерапии. Как правило, противодействие первичным вирусным инфекциям позволяет добиться лучшего клинического эффекта.
Однако птицефабрики с высоким уровнем сохранности часто отличаются от птицефабрик с меньшим уровнем сохранности эффективной биозащитой и высокой антагонистической активностью у птиц кишечной микробиоты, а не интенсивным потреблением ими антибиотиков.
Рис. 4. Кутикулиты вызванные флавивирусной инфекцией и очаговые поражения печени ассоциируемые с иерсиниозом
Заключение
Комплекс мероприятий, нацеленных на борьбу с антибиотикорезистентными формами микроорганизмов, в первую очередь должен обеспечивать на птицефабрике биозащиту и минимизацию рисков развития устойчивости бактерий к антибиотикам при неправильном использовании данных препаратов.
Авторы:
В. Н. Афонюшкин, кандидат биологических наук, зав. сектором молекулярной биологии, Сибирский федеральный научный центр агробиотехнологий РАН и Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск
А. Н. Аксенов, руководитель отдела, ООО «КРКА Фарма», Москва
И. Н. Гусева, продакт-менеджер, ООО «КРКА Фарма», Москва
Библиографические ссылки:
1. Афонюшкин В. Н., Аксенов А. Н., Филипенко М. Л. Обнаружение антител к флавивирусам у бройлеров с пониженной продуктивностью // Ветеринария. 2015. № 12. С. 24–27.
2. Афонюшкин В. Н. Изучение видового разнообразия микрофлоры зерна // Птицеводство. 2010. № 10. С. 47–49.
3. Влияние дезинфицирующих средств на генетический материал патогенов, специфичных для мясоперерабатывающей промышленности / В. Н. Афонюшкин, К. А. Табанюхов, В. С. Черепушкина, Ю. С. Хоменко, О. П. Татарчук // Российский ветеринарный журнал. Сельскохозяйственные животные. 2016. № 1. С. 17–19.
4. Изменение устойчивости Salmonella enterica и Pseudomonas aeruginosa к антибактериальной и иммобилизационной активности хлорамфеникола / В. Н. Афонюшкин, И. Н. Троменшлегер, М. Л. Филиппенко, М. А. Титова // Сибирский вестник сельскохозяйственной науки. 2013. № 5. С. 66–74.
5. Обнаружение генов патогенности и антибиотикорезистентности S. enterica у некоторых микроорганизмов сем. Enterobacteriaceae / В. Н. Афонюшкин, Ю. Г. Юшков, А. С. Донченко, Т. В. Сподырева, М. Л. Филипенко // Вестник Российской академии сельскохозяйственных наук. 2012. № 2. С. 67.
6. Перспективы использования бактериофагов в качестве альтернативы антибиотиков / В. Н. Афонюшкин, Е. В. Дударева, В. С. Черепушкина, М. Л. Филипенко, Ю. Н. Козлова, С. М. Березин // Ветеринария. 2017. № 7. С. 14–17.
7. Эпизоотии бактериальных эндокардитов / В. Н. Афонюшкин, Л. И. Малахеева, Е. В. Дударева, М. Л. Филипенко // Птицеводство. 2012. № 9. С. 41–44.
Bordetella avium
Bordetella avium forms two types of colonies on blood agar (6).
Related terms:
Bordetella and Alcaligenes
Publisher Summary
Poultry and Avian Diseases
Other Bacterial Diseases
Yersinia pseudotuberculosis (Yersiniosis)
Yersinia pseudotuberculosis (Yersiniosis) is a Gram-negative coccobacillus that causes severe enteritis, splenomegaly, hepatomegaly, and lung lesions in young turkeys. In chronic cases it is possible to observe caseous tubercle-like lesions in the liver, spleen, and lungs ( Lister et al., 2008 ).
Avibacterium paragallinarum
Avibacterium paragallinarum is a Gram-negative, non-spore-forming, capsulated rod-shaped bacterium that causes coryza in chickens. The lesions consist of catarrhal and fibrinopurulent inflammation of the nasal passages, infraorbital sinuses, and conjunctivae in old birds ( Blackall, 1999 ).
Gallibacterium anatis
Gallibacterium anatis is a Gram-negative, rod-shaped, or pleomorphic bacterium that is a normal inhabitant of the upper respiratory tract and the lower genital tract. Gallibacterium anatis produces purulent salpingitis and oophoritis in chickens, turkeys, geese, ducks, pheasants, partridges, cage bird, and wild birds. In chronic cases purulent peritonitis may be found ( Paudel et al., 2013 ).
Bordetella avium
Bordetella avium is a Gram-negative, rod-shaped bacterium. Bordetella avium causes turkey coryza, which is an acute respiratory tract disease in young turkeys. Lesions consist of mucopurulent pneumonia and respiratory stress syndrome. Bordetella avium also infects young Muscovy ducks, quail chicks, and cockatiels (Nymphicus hollandicus) ( Jackwood and Saif, 2013 ).
Erysipelothrix rhusiopathiae
Erysipelothrix rhusiopathiae is a Gram-positive, rod-shaped bacterium. There are 26 serovars of E. rhusopathiae, but only the serovars 1, 2, and 5 produce outbreaks. Erysipelothrix rhusiopathiae is found in pigs, rodents, fish, and birds, and rarely in sheep. In birds, E. rhusopathiae infects turkeys, chickens, ducks, geese, emus, pigeons, and game birds. Birds acutely affected show lesions indicative of septicemia, such as petechial hemorrhages in the myocardium, epicardium, gizzard serosa, mesentery, liver, and pleura. In chronic cases, there is vegetative endocarditis and fibrinopurulent arthritis ( Bricker and Saif, 2013 ). Erysipelothrix rhusiopathiae in humans may cause erysipeloid (localized infection of the fingers and hands), generalized cutaneous infections and septicemias ( Wang et al., 2010 ).
Staphylococci, Streptococci, and enterococci
Staphylococci consist of Gram-positive cocci belonging to the family Micrococcaceae and genus Staphylococcus. The genus includes 40 species, of which Staphylococcus aureus is the most important and common one in poultry. Staphylococcus aureus may cause septicemia, fibrinous arthritis and tenosinovitis, chondronecrosis, and osteomyelitis (also called femoral head necrosis) in chickens, turkeys, ducks, and geese ( Andreasen, 2013 ).
Streptococci and Enterococci of importance in poultry include Streptococcus gallinaceus, S. gallolyticus, S. equi subsp. zooepidemicus, Enterococcus hirae, E. durans, and E. faecalis. Lesions associated with infections by Streptococci and Enterococci consist of septicemia (common in chickens, ducks, and pigeons), caseous cellulitis (caused by S. dysgalactia in chickens and turkeys), encephalomalacia (associated with E. durans and E. hirae), vegetative endocarditis (caused by E. hirae in young birds and E. faecalis in older birds), and amyloid arthropathy (observed in chickens infected with E. faecalis) ( Thayer and Waltman, 2013 ).
Infective Endocarditis
Etiologic Agents
Bartonella spp. have emerged as an important cause of culture-negative IE in people and in dogs and was the cause of IE in 28% of dogs living in Northern California, including 45% of dogs with negative blood cultures. 4,13 This may be an unusually high prevalence of IE caused by Bartonella spp. compared with other parts of the country but highlights the importance of testing for bartonellosis in dogs with IE. Bartonella vinsonii ssp. berkhoffii is the most important species of Bartonella causing IE in dogs. 4,14 Other, less common Bartonella species that cause IE in dogs include B. clarridgeiae, B. washoensis, B. quintana, B. rochalimae, B. clarridgeiae-like, and B. koehlerae. 15,16 In dogs, Bartonella spp. affect primarily the aortic valve and less commonly affect the mitral valve. The clinical characteristics of dogs with IE resulting from Bartonella spp. are not different than dogs with IE resulting from traditional bacteria. In the author’s experience, dogs with IE resulting from traditional bacteria do not have coinfections with Bartonella spp. 4,17 Several epidemiologic studies have suggested that ticks and fleas may be vectors for Bartonella spp. Concurrent seroreactivity to Anaplasma phagocytophilum, Ehrlichia canis, or Rickettsia rickettsii is common in dogs with IE resulting from Bartonella spp., and titers should be submitted for tick-borne diseases in any dog that is seroreactive to Bartonella spp. antigens. 4,13
Alcaligenes
Detection Methods
The genera Alcaligenes and Bordetella have been shown to be closely related on the basis of 16S rRNA sequence, fatty acid composition, and biochemical properties. Bordetella pertussis and Bordetella parapertussis, the causative agents of whooping cough, are isolated from human samples, whereas Bordetella bronchiseptica and Bordetella avium are animal and bird pathogens, respectively. Recently, two new species, Bordetella hinzii and Bordetella holmesii, have been isolated from human blood and are the only members of the genus not associated with respiratory infections. Alcaligenes faecalis and both subspecies of A. xylosoxidans can be found as saprophytic inhabitants of human and animal intestinal tracts and are sources of nosocomial infection. Although not usually pathogenic, they may be opportunistic invaders in a compromised host. Therefore, it is critical to be able to distinguish confidently between the two genera when dealing with veterinary or clinical isolates.
| Growth on MacConkey agar | Motility | Citrate utilization | Nitrate reduction | Oxidase | Urease | |
|---|---|---|---|---|---|---|
| B. pertussis | − | − | − | − | + | − |
| B. parapertussis | + | − | v | − | − | + |
| B. avium | + | + | v | − | + | − |
| B. bronchiseptica | + | + | + | + | + | + |
| B. hinzii | + | + | + | − | + | v |
| B. holmesii | + | − | − | − | − | − |
| A. faecalis | + | + | + | − | + | − |
| A. xylosoxidans subsp. xylosoxidans | + | + | + | + | + | − |
| A. xylosoxidans subsp. denitrificans | + | + | + | + | + | v |
V, some strains positive, some negative.
Information from Collier, L., Balows, A., Sussman, M., 1998. Topley and Wilson’s Microbiology and Microbial Infections, nineth ed. Oxford University Press, London; Lennette, E.H., Balows, A., Hausler Jr., W.J., Shadomy, H.J., 1985. Manual of Clinical Microbiology, fourth ed. American Society for Microbiology Press, Washington DC; Roop, R.M., 1990. Bordetella and Alcaligenes. In: Carter, G.R., Cole, J.R. (Eds.), Diagnostic Procedures in Veterinary Bacteriology and Mycology, fifth ed. Academic Press, New York.
Multidrug resistance is common in many bacterial genera, and these organisms can rapidly spread throughout the world, primarily due to the ease of travel. Therefore, it is urgent that diagnostic tools be developed for epidemiological typing. Advances in PCR, gel electrophoresis, and automated ribotyping of organisms have resulted in the ability to classify species and variants within species to a degree not previously possible. Alcaligenes xylosoxidans subsp. xylosoxidans has become more prominent as an opportunistic pathogen, particularly in the hospital environment. Many isolates are resistant to the common classes of β-lactam, aminoglycoside, and quinolone antibiotics. A combination of antibiotic selectivity and pulsed-field gel electrophoresis of digested chromosomal DNA has been developed as an effective method for distinguishing variants of this strain.
Trauma-Related Medical Conditions
Conjunctivitis, Keratoconjunctivitis, and Keratitis
Conjunctivitis can be classified clinically into three groups. The first group is caused by strictly local factors, such as localized conjunctival infection or foreign bodies. The second group is caused when conjunctivitis is a manifestation of periorbital or orbital disease, which is mainly related to sinusitis. In the third group conjunctival hyperemia is caused by septicemia. Almost any organism causing systemic infection can result in conjunctivitis. A careful examination of the bird for upper respiratory disease is mandatory in determining the causes of ocular discharge or conjunctival hyperemia. Exposure to cigarette smoke, chemical fumes, and other airborne environmental toxins should always be considered in the differential diagnostics of conjunctivitis, with or without signs of upper respiratory disease ( Williams, 1994 ).
The most frequent parasites are spirurids (Ceratospira and Oxyspirura) in psittacines and mynahs and trematodes (Philophthalmus gralli), nematodes (Thelazia in Senegal parrot; Poicephalus senegalus), and Setaria in passerines. Conjunctivitis can also be secondary to poor hygienic sanitary conditions from ammonia in feces ( Kern, 1989 ; Williams, 1994 ).
Treatment of conjunctivitis consists of the administration of topical antibiotics (bacitracin-polymixin B, neomycin, tetracycline, and chloramphenicol) for 14 days. When respiratory signs also exist an antibiotic should be administered parenterally. If there are parasites, they can be removed with forceps under topical anesthesia. If this is impossible, the use of ivermectin must be considered.
Keratoconjunctivitis, a frequent ocular disease in psittacines, can be caused by chlamydiosis, trauma in the cage, and vitamin A deficiency. Corneal crystalline deposits of unknown etiology have been found in 8.7% of nymphs, parakeets, and Amazons on necropsy and observed in Amazon parrots with poxvirus. Bilateral deposits of cholesterol have been observed in the corneal stroma in falcons. Punctate keratitis associated with sinusitis has been described in Amazons in which the lesions were bilateral and the most common presenting signs were blepharospasm and clear ocular discharge ( Kern, 1989 ; Williams, 1994 ). Keratitis can be difficult to resolve, but, as a rule, topical antibiotics and corneal bandaging techniques provide a sterile environment and time for the corneal epithelium to heal. By extrapolation from other species, anticollagenases should be used in deep ulcers, especially in hotter climates, where corneal melting may cause rupture of the globe ( Bayón et al., 2007 ). Also, antibiotic treatment and the use of topical nonsteroidal antiinflammatories can be useful in punctate keratitis ( Kern, 1989 ).
Galliformes
Bacterial Diseases
Avian tuberculosis is caused by the bacterium Mycobacterium avium. In zoologic settings, avian tuberculosis has been reported in other bird species in aviary collections. Galliformes species are susceptible to infection by M. avium. Avian tuberculosis tends to be a chronic condition, and affected birds often do not demonstrate any clinical signs until death. 40 On physical examination, emaciation and a prominent keel bone are seen. Transmission is via ingestion of contaminated feed, water, and exposure to contaminated feces from infected birds. Wild birds such as sparrows, starlings, and pigeons may disseminate the bacteria to exotic Galliformes. Necropsy often reveals granulomatous lesions in the intestines, liver, and spleen. Treatment is not recommended unless endangered species are affected. 64
Avian cholera affects a wide range of avian species, including many Galliformes species. Sulfadimethoxine is the drug of choice.Sulfaquinoxaline and sulfamethazine have been very effective in treating affected birds. Rodent control is an effective measure to reduce the incidence of avian cholera, as this disease has been associated with rodents for other zoo-housed aviary species. 33,38 This disease should be considered if free-ranging passerine and waterfowl are present and if facilities house children’s zoo or barnyard exhibits with domestic chickens. Chickens may serve as reservoirs and not demonstrate any clinical signs. However, turkeys, peafowl, and pheasants are often affected with unilateral or bilateral infraorbital sinusitis.
Infectious coryza is caused by the bacterium Hemophilus paragallinarium. This is a disease primarily reported in chickens, but pheasant, guinea fowl, and turkeys have also been reported to have this disease. 64 It should be noted that recovered birds may serve as carriers. Transmission is from infected aerosols from direct contact of infected birds or by ingestion of contaminated water and feed. This bacterium may also be transferred from contaminated clothing and fomites. Affected birds have upper respiratory infection, often with swelling of the infraorbital sinuses. 33,40 This disease should be considered if domestic chickens are housed on site with exotic Galliformes. Sulfa drugs, tetracycline, and erythromycin have been effective. 64
The general terminology of mycoplasmosis refers to disease caused by species belonging to the Mycoplasma genus of bacteria. This disease is transmitted via horizontal as well as vertical transmission. Free-living passerines have been reported with Mycoplasma. 2 In exotic Galliformes, vertical transmission may disseminate this disease among aviary and zoologic collections. Birds infected with Mycoplasma often do not display any clinical signs of disease. This bacterium does not cause any problems unless a concurrent respiratory infection exists, in which case clinical signs could become more severe. This organism has been reported in pheasants, partridges, pea fowl, guinea fowl, and quail. 64 In some aviary collections of exotic peafowl, up to 100% of the birds may be infected, with initial clinical signs reported as bilateral or unilateral swollen infraorbital sinuses (Morishita, unpublished data). Treatment of affected birds has been effective with tylosin, erythromycin, baytril, lincomycin, and spectinomycin. 64 Tylosin in water has been effective in bringing the infection under control. 64 All incoming exotic Galliformes species entering zoologic facilities and in captive breeding facilities during the quarantine period should be monitored for this disease through serologic examinations.
Necrotic enteritis is caused by the bacterium Clostridium perfringens and is often associated with intestinal injury initiated by coccidia. Chukar partridges and pheasants have been known to be infected with this disease. 64 Affected birds have mucoid and often bloody diarrhea. A number of antibiotics may be used to treat the infection and include bacitracin, lincomycin, streptomycin, and tetracycline. 64 This is a soil-borne disease and is usually prevalent in high-density captive breeding conditions. It is usually not a problem in zoologic aviaries, but it may occur when birds are temporarily crowded during maintenance of pens.
Ulcerative enteritis is also known as quail disease and is caused by the bacterium Clostridium colinum. It has been reported in quails and pheasants. 64 Affected quails have a white watery diarrhea that is characteristic of this disease. Affected birds become depressed and are often found dead. Typical lesions at necropsy include ulcers in the small intestines and cecum. The liver may have tan or yellow focal lesions. Neomycin may be provided in the water. 64
Paratyphoid Salmonella infections have been reported in exotic Galliformes species. Over 2000 species of Salmonella exist, and they have a wide host range. Many Galliformes species do not show any signs and yet shed the bacteria. Culture of feces when birds are in quarantine is recommended to determine prevalence, but this needs to occur for several successive collections, as shedding may be sporadic. 35 Maintaining Salmonella-free conditions may be impracticable, as the large variety of host species would be difficult to control. Moreover, free-living waterfowl and passerines have been documented to carry Salmonella species in their feces. 15,57
Reasons for antimicrobial treatment failures and predictive value of in-vitro susceptibility testing in veterinary practice: An overview
3 Uncertainties in antimicrobial susceptibility testing and evaluation of the results
3.1 Antimicrobial susceptility testing of bacteria from animals
Incorrect data on antimicrobial susceptibility testing (AST) can be misleading for the choice of antibacterial drugs with negative consequences on the clinical outcome. To obtain reliable results of antimicrobial susceptibility testing (AST) of a bacterial pathogen, the use of appropriate methods in microbiological routine diagnostics is of outstanding importance ( Schwarz et al., 2003 ; Schwarz et al., 2010 ). The most frequently used AST methods are agar disc diffusion and broth dilution methods. Nowadays, laboratories commonly measure minimal inhibitory concentrations (MICs) by using an antimicrobial broth microdilution test. As known, the more susceptible the isolate is to the antibacterial agent under in vitro conditions, the lower is its MIC, defined as the lowest concentration of an antimicrobial that prevents visible growth of a bacterium ( CLSI, 2018b ).
A systematic review of cumulative susceptibility data derived from hospital laboratories in the USA for the year 2005 revealed that about 19% of prepared antibiograms were incorrect ( Boehme et al., 2010 ). The authors concluded that automated instrumentation cannot replace the need for well-trained, experienced microbiologists. As shown by an interlaboratory trial for the broth microdilution method in Germany ( Wallmann et al., 2006 ), reliable results could be obtained by specialized laboratories using standardized methods, e.g. those from the CLSI. Agar disc diffusion is still reliable if MIC determination cannot be performed and many laboratories still use this method due to cost reasons ( Badger et al., 2019 ). The CLSI document VET01 5 th edition ( CLSI, 2018b ) provides a detailed description of how to do AST of fast growing aerobic and microaerophilic bacteria from animals. Moreover, the CLSI document VET06 ( CLSI, 2017 ) contains AST methods for infrequent or fastidious bacteria isolated from animals. In addition, the CLSI documents VET03 ( CLSI, 2006 ) and VET04-A2 ( CLSI, 2014a ) describe methods for antimicrobial disc susceptibility testing or broth dilution susceptibility of bacteria isolated from aquatic animals, respectively. Thus, CLSI-approved and harmonized methods for a large number of bacteria from animals are available.
However, there are still validated AST methods for certain veterinary pathogens missing. This includes in particular poultry pathogens, such as Ornithobacterium rhinotracheale, Riemerella anatipestifer, Bordetella avium and Avibacterium paragallinarum. Furthermore, there are no harmonized methods for AST of Mycoplasma spp. from any animal species currently available. Harmonized AST protocols are also urgently needed for Brachyspira spp. and related organisms, but also for obligatory intracellular bacterial pathogens, such as Lawsonia intracellularis and Chlamydophila psittaci. In cases, when AST is conducted for bacteria for which no approved and harmonized methods are available, methods from the published literature or in-house methods are commonly applied. The use of such methods bears the risk of non-reliable AST results, which then may lead to false recommendations for antimicrobial therapy, thereby abetting treatment failures.
3.2 Evaluation of AST results
Incorrect interpretation of AST results can initiate the wrong choice of antimicrobials, leading to insufficient clinical efficacy. As known, clinical breakpoints are used for the categorization of a bacterial strain as susceptible (the pathogen will most likely respond to therapy with the respective antimicrobial agent), intermediate (implies an uncertain response at standard dosing, but a possible positive outcome at an increased dose) or resistant (the pathogen will most likely not respond). Criteria to set clinical breakpoints include the distribution of MICs within the target bacteria species, pharmacokinetic data in the target animal species, data from clinical efficacy studies, and pharmacokinetic-pharmacodynamic (PK/PD) analysis using Monte Carlo simulations ( Schwarz et al., 2008 ; Papich, 2013 ). In veterinary medicine, the correct evaluation of AST results requires veterinary-specific clinical breakpoints (VSCBs) and quality control ranges. VSCBs are usually specific for a combination of antimicrobial agent, target bacteria, infected organ system, and animal species. That means a VSCB for tulathromycin–Pasteurella multocida–respiratory tract infections–swine is different from that for pirlimycin–Staphylococcus aureus–mastitis–cattle ( Table 2 ). It is important that AST results obtained from veterinary bacterial pathogens are evaluated by using VSCBs. Although the CLSI documents VET08 ( CLSI, 2018a ) and VET03/04-S2 ( CLSI, 2014b ) contain numerous VSCBs for disk diffusion and broth microdilution tests, there are still VSCBs missing for a number of the aforementioned combinations. As VSCBs are specific for the different bacteria, a false bacteriological diagnosis may result in the application of the wrong VSCBs, which can lead to false treatment recommendations and eventually results in treatment failures.
| Animal species | Indication | Antimicrobial agent | Organism | Disk content | Interpretive categories and zone diameter breakpoints, nearest whole mm | Interpretive categories and MIC breakpoints, μg/mL | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| S | I | R | S | I | R | |||||
| Dog | Urinary tract infection | Cefovecin | Escherichia coli, Proteus mirabilis | 30 μg | ≥ 24 | 21 – 23 | ≤ 20 | ≤ 2 | 4 | ≥ 8 |
| Cattle | Mastitis | Pirlimycin | Staphylococcus aureus | 2 μg | ≥ 13 | — | ≤ 12 | ≤ 2 | — | ≥ 4 |
| Horse | Skin, soft tissue, respiratory tract infection | Enrofloxacin | Escherichia coli | 5 μg | ≥ 23 | 17 – 22 | ≤ 16 | ≤ 0.25 | 0.5 – 1 | ≥ 2 |
| Cat | Skin, soft tissue, urinary tract infection | Ampicillin | Staphylococcus spp. | – | – | – | – | ≤ 0.25 | 0.5 | ≥ 1 |
| Pig | Respiratory tract infection | Tulathromycin | Pasteurella multocida | 30 μg | ≥ 19 | 15 – 18 | ≤ 14 | ≤ 16 | 32 | ≥ 64 |
MIC = minimal inhibitory concentration; S: susceptible, I: intermediate, R: resistant.
In the cases of non-existing VSCBs, diagnosticians often try to extrapolate from one animal species to another, e.g. using the approved VSCB for enrofloxacin–Pseudomonas aeruginosa–skin/soft tissue infections–cat for evaluation of the AST results for enrofloxacin–P. aeruginosa–skin/soft tissue infections–dog, for which such a VSCB currently does not exist. It is important to understand that VSCBs for antimicrobials have been developed on the basis of an approved dosage regimen (dose, frequency of administration, administration route, and duration of therapy) which results in a defined drug concentration at the infection site of a defined animal species ( Papich, 2013 ). If e.g. feline-specific VSCBs are applied to either (i) different bacteria, (ii) different sites of infection, or (iii) different animal species than listed for the approved VSCB, the interpretation of the AST results should be made with distinctly lower confidence and treatment failures cannot be excluded. In this regard, the recently published CLSI document VET09 1 st edition ( CLSI, 2019b ) provides a lot of helpful information. The use of human-specific clinical breakpoints (HSCBs) ( CLSI, 2019a ) for the interpretation of AST data commonly does not produce reliable results since the PK/PD in humans and the different animal species are usually not comparable. The CLSI document VET09 ( CLSI, 2019b ) provides numerous examples for considerations and precautions for or against using antimicrobial agents with HSCBs for interpreting AST results of bacteria of animal origin. The use of antimicrobial agents approved for human use in veterinary medicine for monetary reasons should be avoided. For example, experience from the USA has shown that veterinarians often use ciprofloxacin to treat infections in small animals as ciprofloxacin is distinctly cheaper than the fluoroquinolones approved for use in dogs and cats ( Papich, 2017 ). However, in contrast to the veterinary fluoroquinolones ( CLSI, 2018a ), neither VSCBs nor dosage regimens for the treatment of dogs and cats have been established for ciprofloxacin.
Whenever AST is performed, quality control (QC) strains must be tested side-by-side. The QC strains are defined bacterial strains that are commercially available from the national strain collections. If the results obtained with the QC strains are out of range, the AST results cannot be regarded as valid and must be repeated. The CLSI document VET01 ( CLSI, 2018b ) contains a QC protocol for daily and weekly testing that must be applied when results are in/out of range.
In summary, valid AST results will help the veterinary practitioner to (i) select the potentially most effective antimicrobial agent to which the causative bacterial pathogen is susceptible under in-vitro conditions and (ii) to sort out all those antimicrobial compounds to which it shows resistance. Valid VSCBs are still limited in veterinary medicine, leading to uncertainties in the categorization of bacterial pathogens as susceptible, intermediate or resistant in some cases.