3 964 смерти, 162 610 пострадавших: Европейская база данных о побочных явлениях на «вакцины» от COVID-19
Европейская база данных сообщений о реакциях на принимаемые лекарства – EudraVigilance – начала учитывать сообщения о травмах и смертях после введения экспериментальных «вакцин» от COVID-19.
Веб-сайт был запущен Европейским агентством по лекарственным средствам (ЕМА) в 2012 году для обеспечения открытого доступа к сообщениям о предполагаемых побочных эффектах (также известных как предполагаемые побочные реакции на лекарства). Эти отчеты отправляются в EudraVigilance в электронном виде национальными регулирующими органами в области лекарственных средств и фармацевтическими компаниями, имеющими регистрационные удостоверения (лицензии) на эти лекарства.
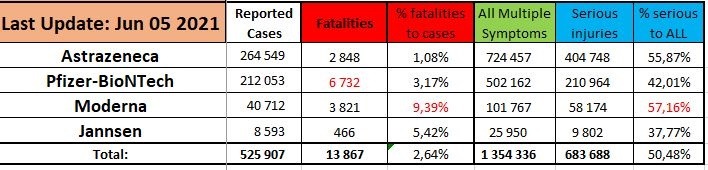
В отчете EudraVigilance по состоянию на 13 марта 2021г. приведено 3 964 случая смерти и 162 610 побочных реакций после введения трех экспериментальных прививок от COVID-19: COVID-19 MRNA VACCINE MODERNA (CX-024414), COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) и COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19).
Сводные данные на 13 марта 2021 года:
Всего реакций на экспериментальную мРНК-вакцину от BioNTech / Pfizer: 2 540 смертей и 102 100 травм:
7 604 заболевания крови и лимфатической системы, в т.ч. 15 смертей
4 636 сердечных заболеваний, в т.ч. 276 смертей
22 врожденные, семейные и генетические нарушения, в т.ч. 2 смерти
72 072 общие расстройства и местные осложнения в области введения препарата, вкл. 957 смертей
6 020 инфекции и заражения, включая 275 случаев смерти
44 993 расстройства нервной системы, включая 185 смертей
8 788 респираторных, грудных и медиастинальных расстройств, включая 294 случая смерти
4 820 сосудистых заболеваний, вкл. 74 смертельных случая
и т.д.
Всего реакций на экспериментальную мРНК-вакцину от Moderna: 973 смертельных случая и 5 939 травм:
330 заболевания крови и лимфатической системы, в т.ч. 9 смертей
501 сердечных заболеваний, вкл. 96 смертей
4 198 общие расстройства и местные осложнения в области введения препарата, вкл. 393 смертей
2 324 расстройства нервной системы, включая 111 случаев смерти
17 респираторные, грудные и медиастинальные расстройства, включая 93 случая смерти
368 сосудистых расстройств, в том числе 32 смертей
и т.д.
1 180 заболевания крови и лимфатической системы, в т.ч. 11 смертей
2 080 сердечных заболеваний, в т.ч. 63 смерти
42 367 общие расстройства и местные осложнения в области введения препарата, вкл. 198 смертей
4 293 респираторных, торакальных и медиастинальных расстройств, включая 33 случая смерти
1 656 сосудистых расстройств, включая 11 случаев смерти
и т.д.
Эта информация, финансируемая Европейским агентством по лекарственным средствам (EMA), предназначена для широкой общественности, но она, по всей видимости, подвергается цензуре со стороны корпоративных средств массовой информации.
EudraVigilance
Исследования и разработки в области лекарственных средств
Содержание
Введение
EudraVigilance — это информационная онлайн-система Европейского союза для управления данными о безопасности, созданная Европейским агентством по лекарственным средствам (EMA) и содержащая сведения о нежелательных реакциях на медицинские препараты, разрешенные в ЕС. Сведения о нежелательных реакциях вносятся в базу данных EudraVigilance. Хотя база данных Eudravigilance не является открытым источником информации, существует интернет-сайт, на котором представители общественности могут получить аналогичные данные: Европейская база данных со сведениями о возможных нежелательных реакциях на медицинские препараты.
Очень важно организовать бесперебойное распространение сведений о возможных нежелательных реакциях на территории Европейского экономического сообщества (ЕЭС). Это позволяет отслеживать преимущества и риски применения медицинских препаратов и обнаружить первые сигналы об опасности. Сигнал об опасности можно определить как новую информацию, относящуюся к известным возможным нежелательным реакциям или любым другим признакам, будь то отрицательные или положительные признаки, которые потенциально связаны с использованием медицинского продукта и требуют дальнейшего изучения.
Сигналы об опасности распознаются в системе EudraVigilance благодаря регулярно осуществляемому анализу сведений об этих сигналах.
Введение информации в базу данных EudraVigilance.
Сведения о нежелательных реакциях поступают от национальных компетентных органов, владельцев регистрационных свидетельств, спонсоров клинических испытаний, пациентов и медицинских специалистов. В EudraVigilance хранятся сведения о нежелательных реакциях на исследуемые и утвержденные медицинские препараты как на территории ЕС, так и за его пределами. В систему EudraVigilance также включен «Медицинский словарь регулирующей деятельности» (Medical Dictionary for Regulatory Activities, MedDRA), который содержит международную медицинскую терминологию.
Для внесения сведений в базу данных EudraVigilance используются два модуля.
В модуль для предварительного утверждения вносятся
В пострегистрационный модуль вносятся данные
С июля 2012 г. Европейское агентство по лекарственным средствам использует процедуру распознавания сигналов для медицинских препаратов, утвержденных на территории всего ЕС, и оказывает содействие всем странам-членам ЕС в организации процедур распознавания сигналов для медицинских препаратов, утвержденных внутри этих стран. База данных EudraVigilance — основной источник сигналов, которые могут послужить основанием для введения мер со стороны контрольно-надзорных органов.
Отчеты о возможных нежелательных реакциях на медицинские препараты
Адрес Европейской базы данных со сведениями о возможных нежелательных реакциях на медицинские препараты в интернете: http://www.adrreports.eu. В базе данных уже содержатся данные о миллионах возможных нежелательных реакций на медицинские препараты. Доступ в базу данных открыт спонсорам и научно-исследовательским организациям, владельцам регистрационных свидетельств в ЕЭС, медицинским работникам и широкой общественности.
Данные о нежелательных реакциях классифицированы таким образом, чтобы пользователи могли осуществлять поиск по указанным параметрам (ими могут быть продукция (медицинские препараты), активное вещество, реакция, возрастная группа, пол, период времени). Результаты поиска можно сохранить на компьютере пользователя или распечатать. Материал может представлять собой подборку отдельных отчетов, основанных на отдельных элементах данных, что обеспечивает соответствие законодательству о защите личных данных. Пользователям предоставляются четкие инструкции относительно толкования данных. Доступ предоставляется примерно на 25% от приблизительно 220 элементов, которые в среднем содержатся в отчете.
Интерпретация информации, содержащейся в европейских базах данных
Информация в базах данных относится к возможным нежелательным реакциям — например, действие медицинского препарата, отмеченное в ходе введения его в организм или лечения с его помощью. При этом такие возможные нежелательные реакции могут быть не связаны с медицинским препаратом и вызваны не им.
Необходимо понимать, что информацию на этом сайте нельзя использовать для того, чтобы определять, имеется ли у пациента нежелательная реакция.
При толковании данных необходимо также учитывать, насколько велико количество людей, принимающих медицинский препарат, и как давно этот препарат присутствует на рынке.
EudraVigilance: electronic reporting
Table of contents
Marketing authorisation holders and sponsors of clinical trials must report and evaluate suspected adverse drug reactions during the development and following the marketing authorisation of medicinal products in the European Economic Area (EEA). Marketing authorisation holders must also electronically submit information on medicinal products authorised in the European Union (EU).
Reporting obligations are defined in the EU pharmacovigilance legislation and the clinical trials legislation and guidance, and apply to the electronic submission and exchange of:
Guidance is available for marketing authorisation holders on submitting COVID-19-related ICSRs to EudraVigilance, including on the correct use of COVID-19-related terms of version 23.0 of the Medical Dictionary for Regulatory Activities (MedDRA): For more information, see:
Who needs to report what?
Spontaneous reports and non-interventional clinical trials
Preparing for the electronic exchange of safety reports
EudraVigilance supports the electronic transmission of ICSRs between electronic data interchange (EDI) partners: EMA, national competent authorities (NCAs), marketing authorisation holders (MAHs) and sponsors of clinical trials in the European Economic Area (EEA).
Organisations are required to perform testing before they can initiate the electronic transmission with the EudraVigilance production environment. This is to ensure that their local safety/pharmacovigilance database is compatible with the EudraVigilance system and compliant with messaging format and terminology requirements.
At least one user per organisation should be trained using EudraVigilance, who can subsequently train other in-house staff as necessary. For details on the training offerings see EudraVigilance training and support. Following successful completion of the training, users can register with EudraVigilance.
Type of organisation
Testing applies to organisations that electronically report ICSRs to EudraVigilance for the first time (“new organisations”) or organisations that introduce a major change to their local safety/pharmacovigilance database which might impact the electronic reporting of ICSRs (“major changes”).
In addition, EMA supports initial testing of software/system solutions by IT vendors and third party service providers (“third party service providers”).
Below is an overview of the steps users should follow for the electronic transmission of ICSRs depending on their type of organisation and technical infrastructure:
| Type of organisation | Steps |
|---|---|