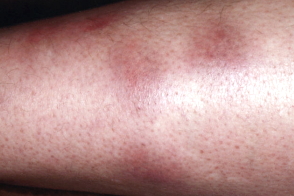
Мигрирующая эритема
Мигрирующая эритема (хроническая мигрирующая эритема Афцелиуса-Липшютца) – кожное проявление первой стадии боррелиозной инфекции. Возникает в месте укуса заражённого боррелиозом клеща при проникновении возбудителя болезни в кожу со слюной насекомого. Отличительной особенностью эритемы является её постоянное увеличение в размерах с одновременным разрешением гиперемии в центре. Патология диагностируется после консультации врача-инфекциониста с учетом данных иммуноферментного анализа венозной крови на антитела к возбудителю. Лечение – антибиотикотерапия, иногда глюкокортикоиды и антигистаминные средства.
Общие сведения
Мигрирующая эритема – инфекционный дерматоз, возникающий при укусе клеща, который является передатчиком боррелиоза. Характеризуется высокой скоростью распространения и быстрым изменением границ патологического очага, что обуславливает использование слова «мигрирующая» в названии заболевания. Патология не имеет возрастных, расовых и гендерных особенностей. Природные очаги боррелиоза постоянно расширяются. Совсем недавно эндемичными территориями считались США, Австралия, островная Европа, Приморье и Сибирь, в настоящее время клещ встречается практически повсеместно. 80% случаев заболевания регистрируются летом.
Впервые «мигрирующий дерматит» неясной этиологии был описан А. Афцелиусом в 1908 году. Мигрирующей эритемой заболевание назвал Б. Липшютц в 1913 году. В качестве аллергической реакции кожи при болезни Лайма дерматологи рассматривают мигрирующую эритему, начиная с 70-80х годов прошлого века, после открытия боррелии и составления описания боррелиоза. В настоящее время связь между мигрирующей эритемой и боррелиозом практически не дискутируется, дерматоз считается ранним кожным маркером болезни Лайма. Актуальность проблемы связана с миграцией клещей, большим количеством заражённых боррелиозом особей в популяции, длительным периодом их активного существования (с мая по сентябрь), обитанием в лесных массивах, городских садах, парках и скверах.
Причины мигрирующей эритемы
Возбудитель мигрирующей эритемы – боррелия, переносчиком которой является заражённый иксодовый клещ. Существуют природные очаги его обитания, клещ встречается в лесах, прибрежных зонах и парках, где насекомое обитает на стеблях цветов и трав. Заражение человека происходит в момент укуса, когда со слюной клещ впрыскивает в кровь боррелию. Продолжительность пребывания переносчика на коже не имеет значения, инфекционно-аллергический процесс начинает развиваться сразу после проникновения слюны с возбудителем в кровь пациента. Хозяевами боррелий являются домашние или дикие животные, клещ выступает только в роли пожизненного носителя, становясь переносчиком инфекции после укуса заражённого животного.
Укус клеща нарушает целостность кожных покровов. Часть боррелий остаётся в месте внедрения, остальные с током крови и лимфы разносятся ко всем органам и тканям, оседают в лимфатических узлах. Инфекционно-аллергическая эритема является патогномоничным проявлением дебюта болезни Лайма и образуется на коже в первые часы с момента заражения. Вслед за ней через месяц появляется полиорганная симптоматика. Следует отметить тот факт, что в 25% случаев мигрирующая эритема не развивается. Вероятно, это связано с особенностями функционирования иммунной системы организма, силой ответной реакции, количеством проникшего в кожу возбудителя и его вирулентностью.
Боррелия внедряется в кожу, по лимфатическим сосудам проникает в глубокие слои и вызывает воспаление, одновременно сенсибилизируя дерму. В процессе альтерации, экссудации и пролиферации участвуют клетки иммунной и гистиоцитарной системы кожи, лимфоциты и макрофаги. Они связывают боррелии, воспринимая их как чужеродные антигены. Одновременно происходит стимуляция клеточной пролиферации с замещением дефекта ткани в месте укуса клеща.
Сама эритема возникает в результате извращённой реакции расширения сосудов кожи, замедления кровотока и увеличения давления плазмы на стенки капилляров. В результате перечисленных процессов «выдавленная» из сосудов часть плазмы пропитывает дерму, которая отекает, приподнимая пятно над окружающей кожей. Вслед за плазмой в дерму мигрируют Т-лимфоциты сосудистого русла, которые контролируют чужеродное внедрение, ликвидируя оставшиеся боррелии. Эритема начинает разрешаться с центра. В зоне первичного повреждения воспаление стихает, а по краям продолжает расти эритематозный вал из Т-лимфоцитов и дермальных клеток. Именно так, центробежно, увеличиваются размеры эритемы.
Симптомы мигрирующей эритемы
Мигрирующая эритема является ключевым признаком, позволяющим установить наличие боррелиоза, поэтому ранняя диагностика этого заболевания чрезвычайно важна. Патологический процесс при возникновении мигрирующей эритемы имеет инкубационный период продолжительностью 32 дня и включает 3 клинические стадии развития: раннюю, диссеминированную и позднюю.
На ранней (местной, локализованной) стадии мигрирующей эритемы на коже появляется ярко-розовое или красное пятно с папулой или макулой в центре (в месте укуса). Пятно немного выпуклое, горячее на ощупь, имеет чёткие границы и быстро растёт. После увеличения до 5 сантиметров начинается разрешение элемента в центральной части, пятно приобретает кольцевидную форму. Возможны неприятные ощущения, реже – зуд, жжение и боль в зоне поражения. Иногда наблюдаются продромальные явления, безжелтушный гепатит и признаки поражения мозговых оболочек. Пятна сохраняются в течение 3-30 дней, а затем начинают шелушиться и «растворяются», оставляя небольшую гиперпигментацию по контуру. При подключении антибактериальной терапии на этом патологический процесс останавливается. При отсутствии лечения или недостаточной терапии наступает вторая стадия.
В диссеминированной стадии мигрирующей эритемы боррелии в большом количестве поступают в кровь из лимфоузлов. Эритема увеличивается в размерах. Происходит дополнительная сенсибилизация организма, отмечается снижение иммунитета. Появляются новые множественные уртикарные высыпания и вторичные кольцевидные элементы, возможна доброкачественная лимфоцитома кожи. Присоединяются температура и головная боль, нарастают слабость и бессонница, выявляются неврологические и кардиальные симптомы. Вторая стадия длится от 6 месяцев до 2 лет. При недостаточном иммунном ответе, некорректно рассчитанной дозе лекарственного препарата, высокой вирулентности и большом количестве боррелий заболевание переходит в третью стадию.
Хроническая (поздняя) стадия мигрирующей эритемы характеризуется развитием акродерматита и хронического Лайм-артрита. Наблюдается симметричное поражение суставов, сопровождающееся отеком, ограничением движений, локальной гиперемией и гипертермией. Мигрирующая эритема приобретает фиолетовый оттенок, истончается и атрофируется в центре, через кожу начинают просвечивать сосуды и подлежащие ткани. При этом пятно по-прежнему растёт, увеличиваясь в размерах, но локализуется уже не в месте укуса клеща, а рядом с суставами или на разгибательной поверхности конечностей. Стадия длится годами.
Диагностика мигрирующей эритемы
Быстрота и точность диагностики при мигрирующей эритеме важны для своевременного купирования процесса. Диагноз выставляется коллегиально врачом-дерматологом и врачом-инфекционистом на основании клинической картины и данных анамнеза. Для подтверждения проводят иммуноферментный анализ венозной крови, взятой через 21 день после укуса клеща (раньше антитела не различимы), на антитела к боррелиям. Применяют метод непрямой иммунофлуоресценции (РНИФ), иммуноблоттинг (сочетание электрофореза и ИФА или РИА). Реже используют иммунофлюорометрию и реакцию непрямой агглютинации.
Для исключения менингита и сочетанной инфекции проводят люмбальную пункцию с исследованием спинномозговой жидкости методом ПЦР и ИФА. Патоморфологическая картина неспецифична. Мигрирующую эритему дифференцируют с укусами пчёл и других насекомых, дерматитом, трихофитией, сифилитической розеолой, склеродермией, эритемой Дарье, мигрирующим миазом.
Лечение мигрирующей эритемы
Самолечение исключается. Лечение мигрирующей эритемы патогенетическое, проводится врачом-инфекционистом. Необходимость в местной терапии отсутствует. Во время инкубационного периода превентивно в амбулаторных условиях назначают цефалоспорины, антибиотики тетрациклинового и пенициллинового ряда. Аналогичную терапию продолжают на ранней стадии заболевания. Индивидуальную схему приёма антибактериальных препаратов рассчитывают для каждого пациента на килограмм веса. При возникновении осложнений или резистентности к проводимой терапии осуществляют инъекционное введение антибиотиков в сочетании с антигистаминными средствами. В тяжёлых случаях применяют глюкокортикоиды.
После купирования мигрирующей эритемы пациент обязан находиться на диспансерном наблюдении у врача инфекциониста в течение 1,5-3 лет (в зависимости от тяжести патологического процесса), периодически сдавая анализ крови на титр антител к боррелиям.
Профилактика и пргноз мигрирующей эритемы
Специфической профилактики боррелиоза не существует. Летом, в фазу активной жизнедеятельности клещей, нужно минимизировать риск попадания насекомых на кожу: помнить, что клещи живут в траве, использовать репелленты при выезде на природу, одеваться в светлые одежды, максимально закрывающие кожу от насекомых (длинные рукава, брюки с резинками, высокие сапоги, головные уборы), осматривать кожу по возвращении домой.
При укусе клеща не следует дожидаться развития мигрирующей эритемы. Необходимо снять насекомое с кожи, поместить в герметичный сосуд и сдать на анализ в СЭС. Нужно обратиться к инфекционисту, который может сделать инъекцию интерферона или (реже) назначить профилактический курс антибактериальной терапии. После получения результатов анализа решение о дальнейшем ведении пациента принимает специалист. Прогноз при своевременной диагностике и лечении благоприятный.
Некролитическая мигрирующая эритема как диагностический маркер рака поджелудочной железы

К паранеопластическим синдромам относят заболевания, возникающие вследствие развития злокачественного новообразования и проявляющиеся симптомами, отдаленными от локализации самой опухоли и ее метастазов.
Abstract. Paraneoplastic syndromes include diseases that arise as a result of the development of a malignant neoplasm, manifested by symptoms that are remote from the localization of the tumor itself and its metastases. Paraneoplastic dermatoses are a large group of various skin manifestations that indicate the possibility of the presence of a tumor, including at an early asymptomatic stage of development. One of these dermatoses is necrolytic migrating erythema, a skin pathology associated with glucagonoma, an alpha – cell tumor of the pancreas that produces glucagon. The description of the clinical case presented in the article will help to improve the understanding of the common pathogenetic aspects between neoplasm and dermatosis, increase the oncological alertness of related specialists and organize effective interdisciplinary interaction, as a result, improving the quality of life of patients with tumor-associated dermatoses. For citation: Tlish M. M., Naatyzh Zh. Yu., Kuznetsova T. G., Masko D. I., Kozyr Ya. V. Necrolytic migrating erythema as a diagnostic marker of pancreatic cancer // Lechaschy Vrach. 2021; 8 (24): 45-47. DOI: 10.51793/OS.2021.24.8.007
Резюме. К паранеопластическим синдромам относят заболевания, возникающие вследствие развития злокачественного новообразования и проявляющиеся симптомами, отдаленными от локализации самой опухоли и ее метастазов. Паранеопластические дерматозы – это многочисленная группа различных кожных проявлений, указывающих на возможность наличия опухоли, в том числе на ранней бессимптомной стадии развития. Одним из таких дерматозов является некролитическая мигрирующая эритема – патология кожи, имеющая ассоциацию с глюкагономой – альфа-клеточной опухолью поджелудочной железы, продуцирующей глюкагон. Представленное в статье описание клинического случая поможет улучшить понимание общности патогенетических аспектов между новообразованием и дерматозом, повысить онкологическую настороженность смежных специалистов и организовать эффективное междисциплинарное взаимодействие, улучшив качество жизни больных с опухоль-ассоциированными дерматозами.
Паранеопластические синдромы (ПС) рассматриваются как результат опосредованного воздействия злокачественного новообразования на регуляторные системы организма, проявляющегося отдаленными симптомами, не связанными с локализацией и метастазированием опухолевых клеток [1]. Обширную группу среди ПС представляют паранеопластические дерматозы – кожные заболевания, являющиеся первыми и часто единственными маркерами бессимптомного опухолевого роста, ранняя диагностика которых имеет колоссальную прогностическую значимость для жизни пациентов [2, 3].
Одним из таких дерматозов является некролитическая мигрирующая эритема (НМЭ) – патология кожи, имеющая ассоциацию с глюкагономой – альфа-клеточной опухолью поджелудочной железы, продуцирующей глюкагон [4]. Предполагается, что именно устойчивый высокий уровень глюкагона вызывает гликогенолитические и глюконеогенные эффекты, приводящие к истощению эпидермального белка и увеличению концентрации арахидоновой кислоты, вызывающие дальнейшее воспаление и некролиз [5]. НМЭ является распространенной (до 70% случаев) дерматологической находкой при глюкагономе [6]. Дерматологическая картина представлена эритематозными шелушащимися очагами, быстро растущими по периферии, располагающимися преимущественно в естественных складках кожи, на коже туловища, конечностей, а также в местах постоянного трения, давления и травматизации [4]. Кожные проявления сопровождаются мучительным зудом и болезненностью, за счет присоединения вторичной инфекции возможно возникновение глоссита и хейлита [6]. Другими клиническими проявлениями, указывающими на наличие альфа-клеточной опухоли, наряду с НМЭ могут быть психоневрологические расстройства, рецидивирующий тромбоз глубоких вен, нормохромная нормоцитарная анемия, сахарный диабет (СД) [5].
Важным аспектом диагностического поиска является тот факт, что НМЭ как проявление ПС может формироваться параллельно с развитием опухоли или задолго до ее клинического дебюта [3]. Раннее установление верного диагноза и своевременное хирургическое лечение до начала метастазирования опухоли являются важнейшими факторами благоприятного прогноза для пациента [1]. Коморбидный статус пациента с ПС требует интегральной тактики ведения [7]. В связи с трудностью дифференциальной диагностики и частыми ошибками дерматологов при постановке диагнозов приводим описание собственного клинического наблюдения.
Клиническое наблюдение
Пациентка Л., 49 лет, считает себя больной с июля 2018 г., когда впервые появились высыпания на коже нижних конечностей, которые связывает с перенесенным стрессом. Обратилась к дерматологу по месту жительства, выставлен диагноз «дерматит неуточненный», назначена терапия топическими глюкокортикостероидами, после которой пациентка отмечала незначительное улучшение. Спустя 2 недели отметила появление новых высыпаний в складках под молочными железами. Вновь обратилась к дерматологу по месту жительства, выставлен диагноз «микоз гладкой кожи», после проведения курсового лечения высыпания не регрессировали, а имели тенденцию к распространению на кожу рук и ног. С января 2019 г. неоднократно обращалась к различным специалистам – дерматологу, терапевту, аллергологу. Выставлялись различные диагнозы: «микоз гладкой кожи», «токсикодермия», «микотическая экзема, аллергиды распространенные». Проводилась дезинтоксикационная, гипосенсибилизирующая, седативная и другая симптоматическая терапия, без видимого эффекта.
В январе 2019 г. пациентка обратилась на кафедру дерматовенерологии ФГБОУ ВО КубГМУ Минздрава России.
На момент осмотра пациентка предъявляла жалобы на высыпания, периодический зуд в течение дня, жжение в очагах, ноющие боли в тазобедренных суставах. Также отмечала повышенную утомляемость, подавленность настрое-ния, снижение массы тела на 12 кг за последние 6 месяцев. Со стороны других органов и систем жалоб не предъявляла.
Из представленной медицинской документации стало известно: 1) пациентка неоднократно обращалась к психотерапевту по поводу депрессивного расстройства, однако прием медикаментов отрицает; 2) состоит на диспансерном учете у эндокринолога по месту жительства: «СД 2 типа. Целевой уровень гликозилированного гемоглобина менее 6,5%».
Объективно: на коже туловища (в области живота, спины, с переходом на крестец и ягодицы), коже рук (в области разгибательных поверхностей плеч, предплечий, тыльной стороне кисти) и ног (передняя и задняя поверхность бедер и голеней) визуализируются множественные единичные и сгруппированные милиарные папулы ярко-розового цвета, четко отграниченные, возвышающиеся над поверхностью кожи. На коже в складках под молочными железами, паховых складках, межъягодичной области располагаются пятна ярко-красного цвета, с четкими границами, с участками экзематизации и мокнутия (рис. 1-3).
При общем осмотре: периферические лимфатические узлы не увеличены. Сердечные тоны приглушены, ритм правильный. Артериальное давление
Результаты лабораторно-инструментальных исследований:
Рентгенограмма легких без патологии.
Заключение УЗИ гепатобилиарной зоны: «Признаки гепатомегалии, аномалия формы желчного пузыря – загиб тела; выраженные диффузно-неоднородные изменения эхоструктуры поджелудочной железы, солидное образование (Tumor?) тела поджелудочной железы».
Консультация терапевта: «Объемное образование поджелудочной железы? Анемия неясного генеза».
На основании данных анамнеза, лабораторных исследований, а также имеющейся клинической картины выставлен предварительный диагноз: «Некролитическая мигрирующая эритема? Кандидоз крупных складок».
С целью установления окончательного клинического диагноза назначен дополнительный метод исследования – компьютерная томограмма (КТ) органов брюшной полости.
Описание: на серии КТ-срезов получено изображение органов брюшной полости, забрюшинного пространства в нативном виде и после болюсного контрастного усиления Ультравист 370.
Печень имеет четкие ровные контуры, не увеличена, паренхима однородная, ее плотностные характеристики в пределах нормы – 55 ед. Н. Признаков портальной и билиарной гипертензии не выявлено. Краниокаудальный размер правой доли – 169 мм, левой – 54 мм. Желчный пузырь грушевидный, патологических образований не содержит. Холедох и внутрипеченочные протоки не расширены.
Поджелудочная железа нерезко увеличена в размерах. На уровне головки толщина – 26 мм, тело – 24 мм, хвост – 19 мм. В паренхиме на границе тела и хвоста железы определяется очаг пониженной плотности в нативном виде до 25 ед. Н, с размытыми контурами, размером 12 × 9 × 7 мм. После контрастного усиления определяется повышение плотности в очаговом образовании до 52 ед. Н. Вирсунгов проток не расширен.
Селезенка с продольным размером 86 мм, толщина – 44 мм, паренхима однородная. Почки не увеличены, контрастирование паренхимы адекватное. Чашечно-лоханочная система не расширена.
Увеличенных лимфоузлов на исследованном уровне не выявлено. После контрастного усиления зон патологического повышения плотности в паренхиматозных органах не определяется.
Заключение КТ органов брюшной полости: «КТ-признаки очагового образования поджелудочной железы (не исключен c-r)» (рис. 4, а-в).
После получения результатов обследования и на основании кожного патологического процесса выставлен окончательной клинический диагноз: «Некролитическая мигрирующая эритема. Кандидоз крупных складок», назначена топическая терапия комбинированными ГКС, анилиновые красители. Для определения дальнейшей тактики ведения пациентка переведена в Клинический онкологический диспансер № 1.
Таким образом, представленный нами клинический случай демонстрирует, что своевременная диагностика НМЭ является определяющим фактором раннего выявления рака поджелудочной железы. Понимание общности патогенетических аспектов между новообразованием и дерматозом, онкологическая настороженность смежных специалистов и полноценный комплекс диагностических мероприятий позволят организовать эффективное междисциплинарное взаимодействие и оказать своевременное лечение, повысив качество жизни больных с опухоль-ассоциированными дерматозами.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
* ФГБОУ ВО КубГМУ Минздрава России, Краснодар, Россия
** ГБУЗ ДККБ Минздрава Краснодарского края, Краснодар, Россия
Некролитическая мигрирующая эритема как диагностический маркер рака поджелудочной железы/ М. М. Тлиш, Ж. Ю. Наатыж, Т. Г. Кузнецова, Д. И. Масько, Я. В. Козырь
Для цитирования: Тлиш М. М., Наатыж Ж. Ю., Кузнецова Т. Г., Масько Д. И., Козырь Я. В. Некролитическая мигрирующая эритема как диагностический маркер рака поджелудочной железы // Лечащий Врач. 2021; 8 (24): 45-47. DOI: 10.51793/OS.2021.24.8.007
Теги: кожа, дерматоз, эритема, опухоль, метастазы
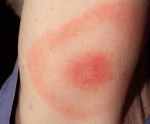
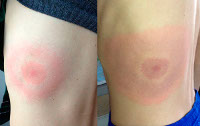
Erythema migrans что такое
Часто основным заболеванием при этом является иерсиниозная инфекция. Типичный патогенетический механизм в этом случае представляет собой иммунный ответ организма-хозяина на циркулирующие иммунные тела. При этом могут возникать иммунные комплексы, которые способствуют развитию болезни. При воспалительных заболеваниях кишечника узловатая эритема является результатом повышенной проницаемости кишечника для эндо- и экзогенных антигенов.
Заболевание может быть и результатом нарушенной функции клеточного иммунитета. Недавние исследования показали разницу в использовании p-цепи вариабельного домена молекул Т-клеточного рецептора при узловатой эритеме, ассоциированной с воспалительным заболеванием кишечника, что предполагает потенциальную роль суперантигенов.
Узловатая эритема может также вызываться лучевой терапией. Продукты распада раковых клеток, разрушенных облучением, могут активировать циркулирующие антитела и комплемент, что способствует образованию иммунных комплексов и, следовательно, запуску соответствующей реакции.Лучевая терапия, как известно, активизирует еще некоторые реактивные дерматозы.
Заболевание представляет собой септальный гранулематозный панникулит.
Острая узловатая эритема
Хроническая узловатая эритема
Мигрирующая узловатая эритема (болезнь Вилановы)
Выделяют также поверхностно-инфильтративную форму мигрирующей узловатой эритемы, характеризующуюся плоскими поверхностными склеродермоподобными инфильтратами, склонными к периферическому увеличению.
Лепрозная узловатая эритема
(Реактивные состояния II типа). Возникает у половины больных лепроматозной проказой, как правило, в первые 2 года после начала лечения. На коже появляются множественные воспаленные подкожные узлы.
Для постановки диагноза, как правило, достаточно клинических данных. Биопсия кожи показывает септальный панникулит и помогает исключить лобулярный панникулит, узловатый васкулит и узелковый периартериит. Биоптат берут из центрального участка очага и достаточно глубоко, чтобы захватить подкожную жировую ткань.
Общие терапевтические рекомендации
Лечение острой формы
Йодид калия (препарат, состоящий из 76% йода и 23% калия) является лечением выбора.После попадания внутрь йодид калия быстро всасывается в пищеварительном тракте и распределяется по межклеточному пространству. Йод концентрируется в щитовидной железе, а также в других тканях, таких как слюнные железы, слизистая оболочка желудка и молочная железа.Йодид калия может оказывать свое действие достаточно быстро, так что бывает легко оценить эффективность лечения. Препарат назначают внутрь по 300 мг 3 раза в день. Полная ремиссия очагов происходит за 10-14 дней после назначения лекарства, особенно если препарат начинают принимать сразу после начала заболевания. Самый лучший ответ наблюдают у пациентов с ЭУ, которая ассоциируется с системными симптомами, такими как лихорадка, боли в суставах и присутствие С-реактивного белка. Иногда бывают тошнота и рвота, но обычно при этом нет необходимости прекращать лечение. Нежелательные кожные реакции могут включать эритематозные, пурпуроподобные, уртикарные, акнеформные, узловатые, пустулезные и вегетативные очаги. Кроме этих довольно незначительных побочных эффектов, могут быть более существенные побочные реакции у беременных женщин и у пациентов с заболеваниями почек и щитовидной железы в анамнезе. Сообщалось о развитии выраженного гипотиреоидизма вторично к экзогенному приему йодида. Блокировка органического его связывания в щитовидной железе при избытке йодида, результатом которой является прекращение синтеза тиреоидных гормонов, известна как эффект Вольфа-Чайкоффа (Wolf- Chaikoff).
Механизм, посредством которого йодид калия оказывает свое действие не выяснен. Одна из гипотез предполагает, что йодид калия может вызывать высвобождение гепарина из тучных клеток, а гепарин, в свою очередь, подавляет клеточный иммунитет. Лекарство может также модулировать функцию нейтрофилов, подавляя производство перекиси водорода и гидроксильных радикалов. Эти промежуточные продукты кислорода являются до такой степени реактивными, что могут повреждать ткань. Йодид калия, препятствуя производству промежуточных продуктов кислорода, осуществляет защиту ткани от повреждения вследствие самоокисления.
Лечение хронической формы
Узловатая эритема является изнурительным хроническим заболеванием, для которого было предложено много вариантов лечения, но ни один из них не является универсально эффективным. Хотя пациенты быстро реагируют на кортикостероиды, риск их хронического применения вынуждает к поискам альтернативного подхода.
В хронических случаях часто не реагирует на большие дозы аспирина, но может драматически отвечать на противовоспалительное действие индометацина в дозах 100-150 мг/день. Подавление процесса индометацином связано с блокировкой активности синтеза простагландина в подкожной жировой ткани, что влияет как на клеточный, так и на гуморальный иммунный ответ.
Хроническую форму можно также успешно лечить напроксеном. Однако индометацин превосходит системные кортикостероиды и, возможно, имеет также преимущества над другими, менее мощными нестероидными противовоспалительными препаратами.
Гидроксихлорохин является эффективной и безопасной альтернативной терапией для некоторых пациентов в дозе 200 мг 2 раза в день, которую затем снижают до 200 мг 1 раз в день в течение 4 мес.
Лечение лепрозной узловатой эритемы
_575x.png)
.png)