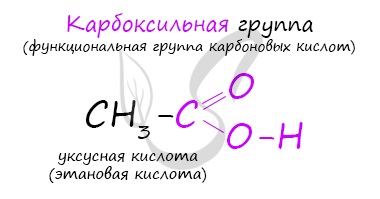
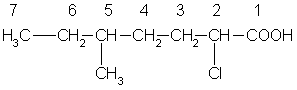Карбоновые кислоты
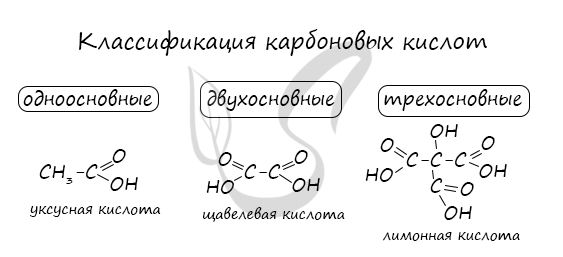
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
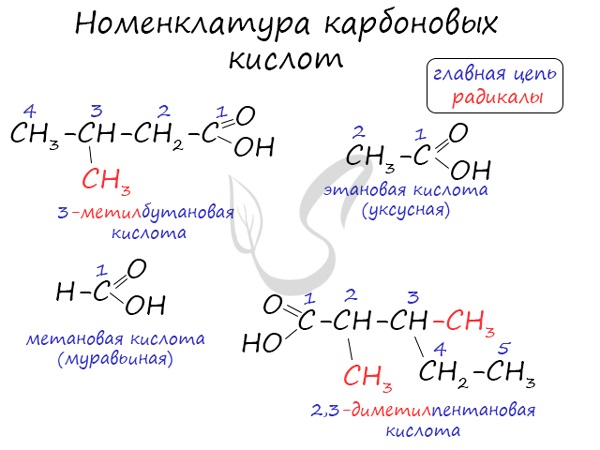
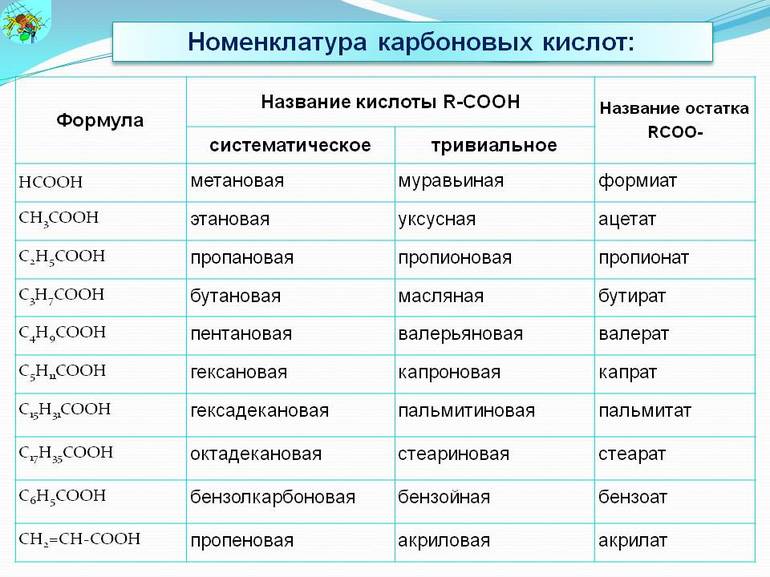
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
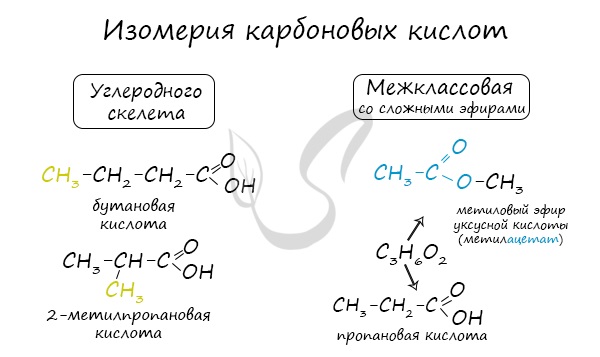
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
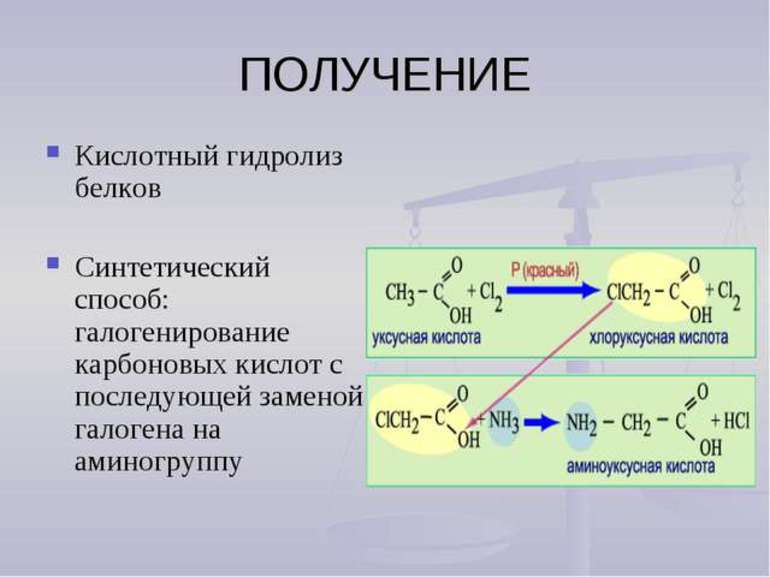
Получение карбоновых кислот
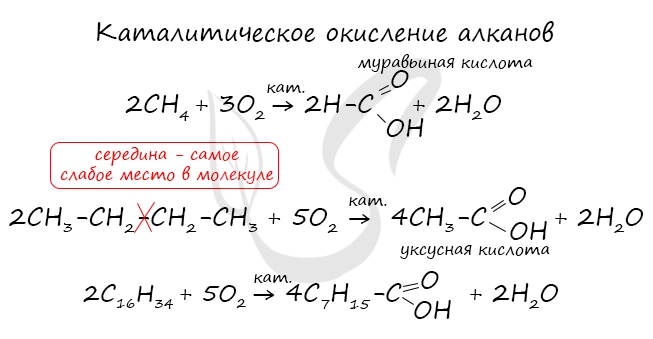
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
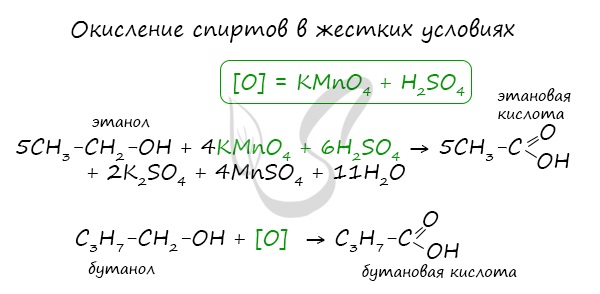
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
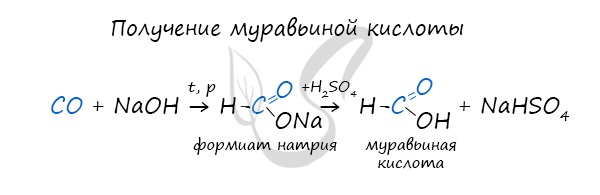
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
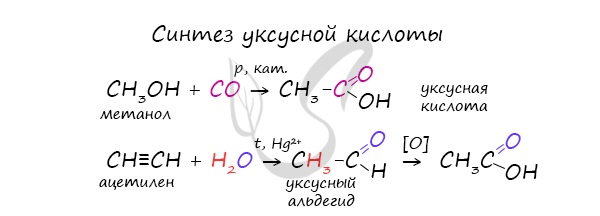
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
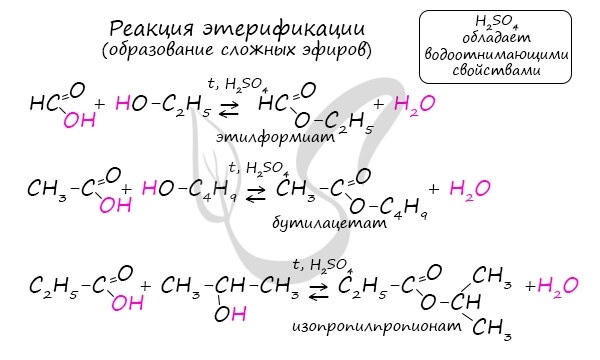
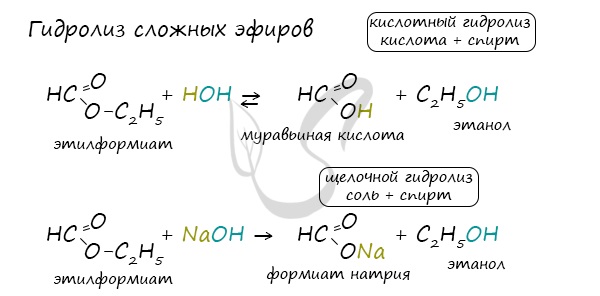
Сложные эфиры
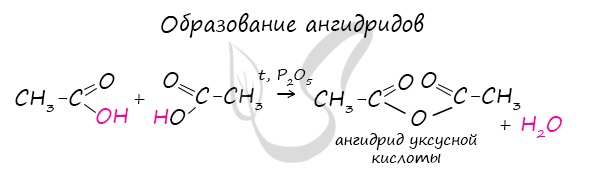
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
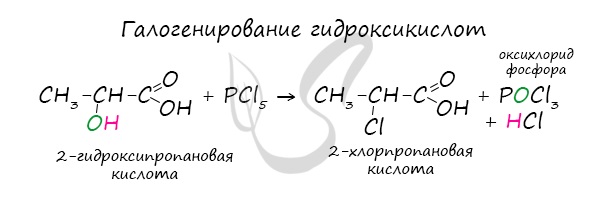
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
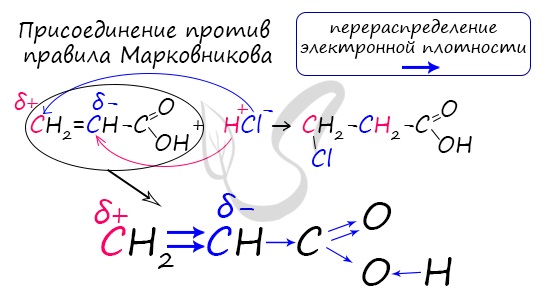
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Двухосновные предельные карбоновые кислоты
Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH, где n = 0, 1, 2, …
Номенклатура
Систематические названия двухосновных предельных карбоновых кислот даются по названию соответствующего алкана с добавлением суффикса -диовая и слова кислота.
Изомерия
Изомерия скелета в углеводородном радикале проявляется, начиная с бутандиовой кислоты, которая имеет два изомера:
Гомологический ряд
| Тривиальное название | Название по ИЮПАК | Формула | Название солей |
|---|---|---|---|
| Щавелевая кислота | Этандиовая кислота | HOOCCOOH | оксалаты |
| Малоновая кислота | Пропандиовая кислота | HOOCСH2COOH | малонаты |
| Янтарная кислота | Бутандиовая кислота | HOOC(СH2)2COOH | сукцинаты |
| Глутаровая кислота | Пентандиовая кислота | HOOC(СH2)3COOH | глутараты |
| Адипиновая кислота | Гександиовая кислота | HOOC(СH2)4COOH | адипинаты |
| Пимелиновая кислота | Гептандиовая кислота | HOOC(СH2)5COOH | пимелинаты |
| Пробковая кислота | Октандиовая кислота | HOOC(СH2)6COOH | субераты |
| Азелаиновая кислота | Нонандиовая кислота | HOOC(СH2)7COOH | азелаинаты |
| Себациновая кислота | Декандиовая кислота | HOOC(СH2)8COOH | себацинаты |
| — | Ундекандиовая кислота | HOOC(СH2)9COOH | |
| — | Додекандиовая кислота | HOOC(СH2)10COOH | |
| Брассиловая кислота | Тридекандиовая кислота | HOOC(СH2)11COOH | |
| — | Тетрадекандиовая кислота | HOOC(СH2)12COOH | |
| — | Пентадекандиовая кислота | HOOC(СH2)13COOH | |
| Тапсиевая кислота | Гексадекандиовая кислота | HOOC(СH2)14COOH | |
| — | Гептадекандиовая кислота | HOOC(СH2)15COOH | |
| — | Октадекандиовая кислота | HOOC(СH2)16COOH | |
| — | Нонадекандиовая кислота | HOOC(СH2)17COOH | |
| — | Эйкозандиовая кислота | HOOC(СH2)18COOH | |
| Японовая кислота | Генэйкозандиовая кислота | HOOC(СH2)19COOH |
Полезное
Смотреть что такое «Двухосновные предельные карбоновые кислоты» в других словарях:
Двухосновные насыщенные карбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Двухосновные карбоновые кислоты — (или дикарбоновые кислоты) это карбоновые кислоты, содержащие две карбоксильные группы COOH, с общей формулой HOOC R COOH, где R любой двухвалентный органический радикал. Содержание 1 Химические свойства 2 Примеры … Википедия
Предельные дикарбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Дикарбоновые кислоты — Двухосновные карбоновые кислоты (дикарбоновые кислоты) – это карбоновые кислоты, содержащие две карбоксильные группы –COOH. Общей формулой HOOC R–COOH, где R любой двухвалентный органический радикал. Содержание 1 Химические свойства 2 Примеры … Википедия
Насыщенные дикарбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
Азелаиновая кислота — Азелаиновая кислота … Википедия
Адипиновая кислота — Адипиновая кислота … Википедия
Малоновая кислота — Общие … Википедия
Себациновая кислота — Номенклатура Тривиальное название себациновая кислота Систематическое название декандиовая кислота … Википедия
Одноосновные предельные карбоновые кислоты
Номенклатура
Систематические названия одноосновных предельных карбоновых кислот даются по названию соответствующего алкана с добавлением суффикса -овая и слова кислота.
Изомерия
Изомерия скелета в углеводородном радикале проявляется, начиная с бутановой кислоты, которая имеет два изомера:
Межклассовая изомерия проявляется, начиная с уксусной кислоты:
Гомологический ряд
| Тривиальное название | Название по ИЮПАК | Формула | Название солей |
|---|---|---|---|
| Муравьиная кислота | Метановая кислота | HCOOH | формиаты |
| Уксусная кислота | Этановая кислота | CH3COOH | ацетаты |
| Пропионовая кислота | Пропановая кислота | C2H5COOH | пропионаты |
| Масляная кислота | Бутановая кислота | C3H7COOH | бутираты |
| Валериановая кислота | Пентановая кислота | C4H9COOH | валераты |
| Капроновая кислота | Гексановая кислота | C5H11COOH | капраты |
| Энантовая кислота | Гептановая кислота | C6H13COOH | энантоаты |
| Каприловая кислота | Октановая кислота | C7H15COOH | каприлаты |
| Пеларгоновая кислота | Нонановая кислота | C8H17COOH | пеларогоаты |
| Каприновая кислота | Декановая кислота | C9H19COOH | капринаты |
| Ундециловая кислота | Ундекановая кислота | C10H21COOH | ундеканоаты |
| Лауриновая кислота | Додекановая кислота | C11H23COOH | лаураты |
| — | Тридекановая кислота | C12H25COOH | тридеканоаты |
| Миристиновая кислота | Тетрадекановая кислота | C13H27COOH | миристиаты |
| — | Пентадекановая кислота | C14H29COOH | пентадеканоат |
| Пальмитиновая кислота | Гексадекановая кислота | C15H31COOH | пальмитаты |
| Маргариновая кислота | Гептадекановая кислота | C16H33COOH | маргараты |
| Стеариновая кислота | Октадекановая кислота | C17H35COOH | стеараты |
| — | Нонадекановая кислота | C18H37COOH | нонадеканоаты |
| Арахиновая кислота | Эйкозановая кислота | C19H39COOH | арахаты |
| — | Генэйкозановая кислота | C20H41COOH | генэйкозаноаты |
| Бегеновая кислота | Докозановая кислота | C21H43COOH | бегенаты |
| — | Трикозановая кислота | C22H45COOH | трикозаноаты |
| Лигноцериновая кислота | Тетракозановая кислота | C23H47COOH | лигноцераты |
| — | Пентакозановая кислота | C24H49COOH | пентакозаноаты |
| Церотиновая кислота | Гексакозановая кислота | C25H51COOH | церотитаты |
| — | Гептакозановая кислота | C26H53COOH | гептакозаноаты |
| Монтановая кислота | Октакозановая кислота | C27H55COOH | монтаноаты |
| — | Нонакозановая кислота | C28H57COOH | нонакозаноаты |
| Мелиссовая кислота | Триаконтановая кислота | C29H59COOH | мелиссаты |
| — | Гентриаконтановая кислота | C30H61COOH | Гентриаконтаноаты |
| — | Дотриаконтановая кислота | C31H63COOH | Дотриаконтаноаты |
| Псилластеариловая кислота | Тритриаконтановая кислота | C32H65COOH | псилластеарилаты |
Полезное
Смотреть что такое «Одноосновные предельные карбоновые кислоты» в других словарях:
Одноосновные насыщенные карбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Предельные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Насыщенные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Валериановые кислоты — н пентановая (валериановая) кислота Валериановая кислота (пентановая кислота) С4Н9COOH – одноосновная предельная карбоновая кислота, бесцветная жидкость с неприятым запахом. Соли и эфиры валериановой кислоты называют валератами. Валериановая… … Википедия
Тридекановая кислота — Общие … Википедия
Уксусная кислота — Уксусная кислота … Википедия
Муравьиная кислота — Муравьиная кислота … Википедия
Пропионовая кислота — Пропионовая кислота … Википедия
Стеариновая кислота — Стеариновая кислота … Википедия
Валериановая кислота — Валериановая кислота … Википедия
Cooh ch2 cooh что это
Если в углеводородном радикале карбоновых кислот атом (атомы) водорода замещен на другие функциональные группы, то такие кислоты называются гетерофункционапьными. Среди них различают галогенкарбоновые (например, CH2Cl—COOH), нитро-кислоты (например, NO2—С6Н4СООН), аминокислоты, оксикислоты (например, молочная СН3—СН(ОН)—СООН) и др.
Карбоновые кислоты с числом атомов углерода выше 6 называют высшими (жирными) кислотами. Название «жирные» эти кислоты получили потому, что большинство из них могут быть выделены из жиров.
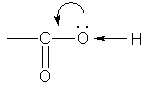
В свою очередь, группа ОН «гасит» положительный заряд на группе СО, которая из-за этого теряет способность к реакциям присоединения, характерным для карбонильных соединений.
Углеводородную цепь нумеруют начиная с атома углерода карбоксильной группы, например:
Часто карбоксильную группу рассматривают как заместитель в молекуле углеводорода. При этом в названии употребляют словосочетание «карбоновая кислота» и в нумерацию атомов углерода цепи атом углерода карбоксильной группы не включают:
Гептадецен-8-карбоновая (олеиновая) кислота
Названия дикарбоновых кислот производят от названия соответствующего углеводорода с добавлением суффикса «диовая» и слова «кислота». Например, этандиовая (щавелевая) кислота (НООС-СООН).
При рассмотрении карбоксильной группы как заместителя, название двухосновной кислоты производят от названия углеводородного радикала с добавлением словосочетания «дикарбоновая кислота». Например, малоновую кислоту (НООС-СН2-СООН) называют метандикарбоновой кислотой.
1. Изомерия углеродной цепи. Она начинается с бутановой кислоты (С3Н7СООН), которая существует в виде двух изомеров:
2. Изомерия положения кратной связи, например:
СН2=СН—СН2—СООН СН3—СН=СН—СООН
Бутен-3-овая кислота Бутен-2-овая кислота
(винилуксусная кислота) (кретоновая кислота)
3. Цис-транс- изомерия, например:
4. Межклассовая изомерия: например, масляной кислоте (СН3—СН2—СН2—СООН) изомерны метиловый эфир пропановой кислоты (СН3—СН2—СО—О—СН3) и этиловый эфир уксусной кислоты (СН3—СО—О—СН2—СН3).
5. У гетерофункциональных кислот имеется изомерия, связанная с положением функциональных групп, например, существуют три изомера хлормасляной кислоты:
СН3—СН2—СНСl—СООН СН3—СНСl—СН2—СООН
2-хлорбутановая кислота 3-хлорбутановая кислота
Для гетерофункциональных кислот возможна также оптическая изомерия.
Кислоты, содержащие 1-3 углеродных атома, неограниченно смешиваются с водой. С дальнейшим ростом углеводородного радикала растворимость монокарбоновых кислот уменьшается, твердые высшие жирные кислоты в воде не растворяются.
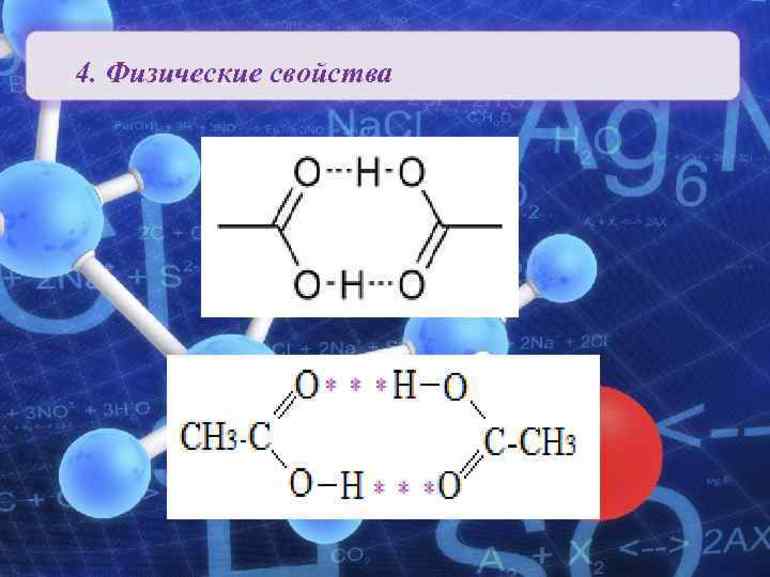
В жидком состоянии и в неводных растворах молекулы монокарбоновых кислот димеризуются в результате образования между ними водородных связей. Это объясняет гораздо более высокие температуры кипения карбоновых кислот по сравнению со спиртами и альдегидами с тем же числом атомов углерода; температуры плавления и кипения с ростом молекулярной массы возрастают.
Описание вещества и параметры
Общая формула карбоновых кислот (не путать с карбонатной или угольной кислотой) — CH2 + COOH; в нормальных условиях имеют маслянистую жидкую форму с характерным неприятным запахом, однако начиная с C10-углеродов кислота представляет собой твёрдое вещество, нерастворимое в воде. Однако при количестве атомов углерода свыше 3, вещество неограниченно смешивается с водой. Так как кислотные свойства этого вещества являются относительно слабыми (за исключением муравьиной и уксусной кислоты), их соли подвергаются обратимому гидролизу.
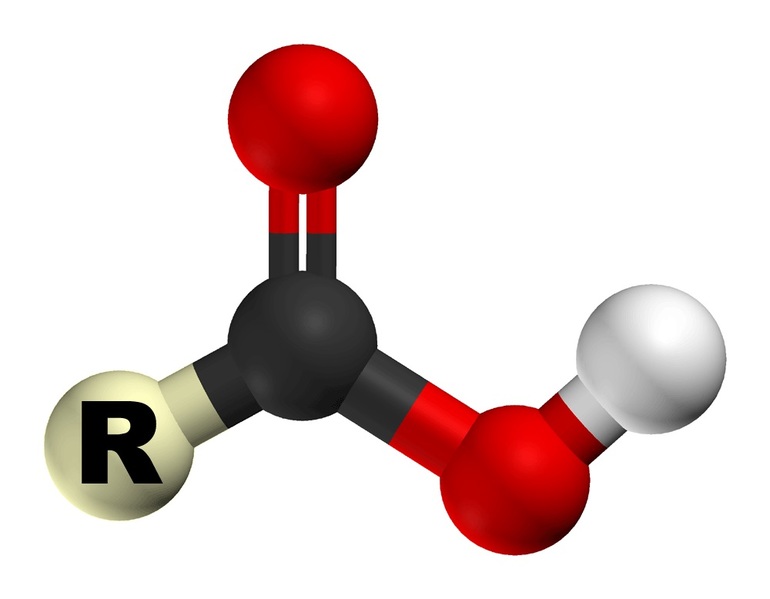
Электронное строение карбоксильной группы сочетает в себе наличие двух функциональных групп — гидроксил (-OH) и карбонил (>C=0). Длина водородной связи в димере равна 0,26 нм, длина связи C=O в различных соединениях составляет около 0,122 нм. При диссоциации образуется стабилизированный сопряжением отрицательно заряженный анион.
Систематическая номенклатура
В названии этих химических соединений в первую очередь нумеруют атом углерода группы COOH. Образованные в процессе реакции соли получают наименования при помощи добавления суффикса «ат» или «оат» к названию углеводорода (к примеру, этандиоат калия). Гомологический ряд предельных и непредельных карбоновых растворов имеет следующий вид:
Помимо этого, в таблицу классификации карбоновых кислот подобного типа также включают бутановую, линолевую, бензойную и щавелевую кислотную основу. Карбоновым соединениям свойственна структурная межклассовая и пространственная изомерия (начиная с С2), положение кратной связи, а также изомерия скелета в углеводородном радикале.
Физические свойства
Физические особенности и свойства веществ карбоксильной группы зависят от числа атомов углерода в их соединениях. Те соединения, в состав которых входят не более 3 атомов С, относятся к низшему классу. Они легко растворимы в воде, имеют резкий запах и не имеют цвета. Кислотные растворы, содержащие в своём составе свыше 9 атомов являются высшими; они относятся к твёрдым веществам, нерастворимым в воде.
Плотность уксусной и муравьиной кислоты больше единицы, у всех остальных видов плотность меньше. Кипение карбоновых соединений происходит при более высоких температур, чем у спиртов. Связи молекул кислорода и водорода (O — H) сильно поляризованы. Также химические соединения этого типа могут реагировать посредством образования водородных связей с кислородом карбонильного диполя, который обладает значительной электроотрицательностью.
Кислоты в твёрдом виде существуют в качестве циклических димеров; в жидком виде может происходить линейная ассоциация.
Химические реакции и особенности
При реакции с металлами, оксидами либо с некоторыми из их гидроксидов, карбоновые растворы проявляют типичные свойства всех слабых кислот — образование солей соответствующих металлов, вытеснение более слабого кислотного раствора из её соли, а также вытеснение самого карбонового соединения. В воде соли карбоновых соединений имеют щелочную реакцию и подвергаются гидролизу. Лакмусовую бумажку раствор окрашивает в красный цвет. В качестве примера можно привести следующие химические формулы:
Высокая полярность связи O — H приводит к значительной диссоциации карбоновой кислоты в водном растворе. Все соединения являются слабыми электролитами. Реакция горения выглядит таким образом: CH3COOH + 2O2 => 2CO2 + 2H2O. К химическим свойствам карбоновых кислот также относят этерификацию (так называется химическое взаимодействие со спиртами, которая приводит к образованию сложных эфиров).
Этерификация может происходить и многоатомные спирты типа глицерина. В результате реакции образовываются сложные жиры (смеси триглицеридов); пальмитиновая кислота и некоторые другие предельные жирные кислотные растворы образуют твёрдые жиры животного происхождения.
Свойства кислотных растворов обуславливаются наличием изомерного углеводородного радикала. В случае когда реакция протекает в присутствии красного фосфора, происходит образование продукта: CH3-CH2-COOH + Br2 =>CH3-CHBr-COOH + HBr. Карбоновые соединения окисляются хлором: HCOOH + Cl2 => CO2 + 2HCl.
Способы получения
На сегодняшний день существует несколько основных способов получения этого химического вещества. Соединения этой группы можно получить посредством окисления спиртов. Спирты взаимодействуют с разбавленной серной кислотой и оксидом хрома с добавлением марганцовки или ацетона: RCH2OH + [O] => RCOOH. Также необходимо выделить и другие, не менее распространённые способы:
Следует знать, что в промышленных масштабах получение карбоновых кислот происходит, как правило, посредством окисления парафиновых углеводородов техническим кислородом при высокой температуре и давлении (как в присутствии катализаторов, так и без таковых). В качестве катализаторов служат соли и оксиды металлов.
Применение в жизни
Карбоновые соединения применяются во многих отраслях промышленности. Помимо этого, кислотная основа является важным элементом для получения промежуточных продуктов органического синтеза, к которым относятся кетены, галогенкислоты, виниловые эфиры и галогенангидриды. Наиболее широкое применение эти кислотные растворы получили в химической промышленности, в медицине и в сельском хозяйстве.
Бытовая химия
Различные виды солей, получаемых в процессе реакции, используются в качестве сырья для органического синтеза. К примеру, для производства мыла, шампуней, моющих средств, а также для изготовления лакокрасочных материалов, смазочных масел, эмульгаторов, растворителей и клеёв.
Уксусная кислотная основа (в частности, её ацетаты) необходима для производства ацетатного шёлка, пальмитиновая кислота добавляется в качестве загустителя при изготовлении технических масел для смазки, а также для производства различных пластификаторов. Акриловая кислота незаменима при изготовлении эмульсий для лакокрасочных материалов, для пропитки кожи, акриловых каучуков, а также для создания полиакрилонитрильных волокон.
Медицина и косметика
Уникальный молекулярный состав муравьиной кислоты позволяет её использовать во многих отраслях науки, в том числе и в медицине. Эту кислоту часто используют для дезинфекции кожного покрова и как наружное обезболивающее средство при ушибах и травмах, так как она обладает согревающим, бактерицидным и противовоспалительным действием. Смесь муравьиной кислоты с водой (муравьиный спирт) нередко используется при ревматических и неврологических болях.
Для лечения отдельных заболеваний желудочно-кишечного тракта используется масляная кислота — её соли создают в кишечнике благоприятную среду для развития полезных микроорганизмов, препятствуя при этом размножению патогенных бактерий. Помимо этого, эта разновидность карбоновой кислоты регулирует водно-электролитный баланс в организме. Линоленовая кислота снижает уровень холестерина и предотвращает развитие сосудистых заболеваний. В косметических целях могут использоваться следующие виды кислот:
Лимонная кислота (как и щавелевая) хорошо очищает пятна на коже; помимо этого, она добавляется в состав многих лаков для ногтей, придавая им блеск и свежесть (при умеренном использовании). Молочная кислота добавляется в состав шампуней, делая волосы объёмными, густыми и шелковистыми.
Сельское хозяйство
При помощи различных карбоновых соединений производится обработка корма, сена и силоса, что позволяет значительно замедлить процессы гниения и распада, увеличивая их срок хранения. Помимо этого, кислоты используются для изготовления инсектицидов и фунгицидов (та же уксусная кислота является средством для борьбы с паразитами в пчеловодстве).
Отдельные разновидности кислотного раствора применяются для консервирования продуктов (пищевая добавка Е260), овощей и приправ. Соли маслянистого кислотного раствора используются в животноводстве — их добавляют в корм для укрепления иммунитета и усвояемости пищи.