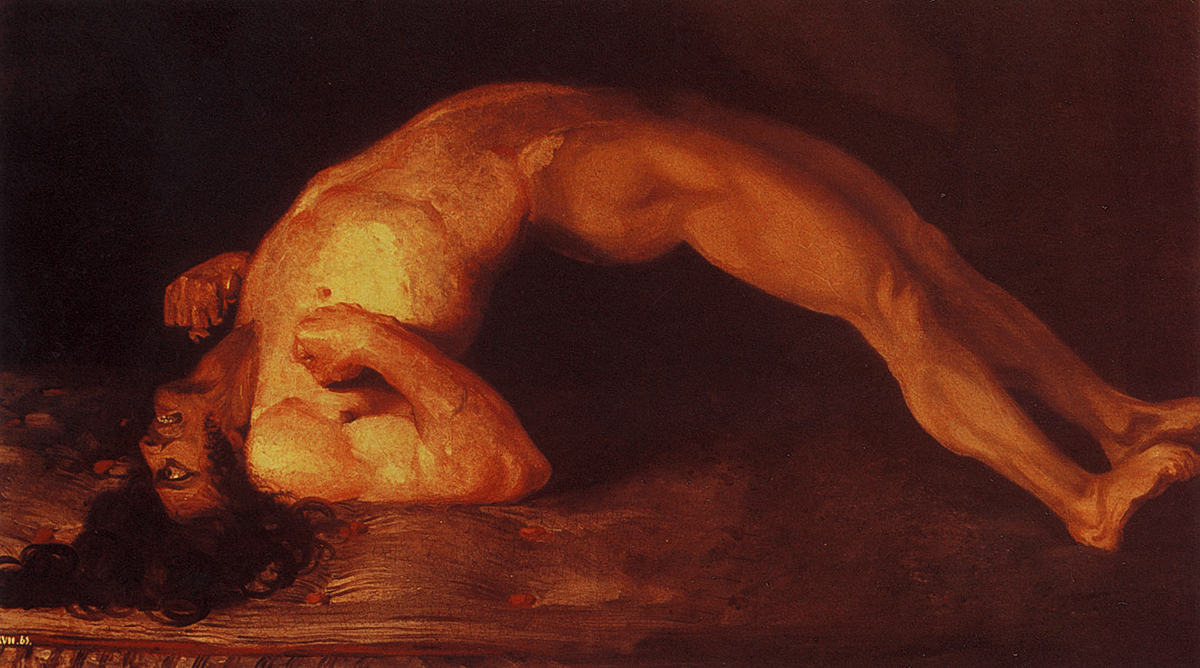Клостридии вызывают острые кишечные инфекции.
Бактерии рода Клостридий вырабатывают наиболее сильные из известных ядов – ботулотоксин, тетаноспазмин и другие.
Клостридии – бактерии в составе постоянной собсвтенной микрофлоры кишечника. Растут строго без доступа воздуха и их очень трудно идентифицировать.
В организме человека клостридии являются стимуляторами Т-регуляторных клеток, которые снижают аллергическую настроенность организма. Один из клостридиальных метаболитов – бутират –защищает нас через интерлейкин 10. к
Кроме того, клостридии учавствуют в обмене липидов, в обмене желчных кислот и их частичном выведении из организма, подавляют рост и развитие в ЖКТ болезнетворных бактерий, расщепляют до молекулярного состояния белки.
В кишечнике новорожденных детей клостридии появляются к 6-7 дню жизни.
У детей на грудном вскармливании уровень клостридий держится в норме.
У детей при раннем введении смешанного или искусственного вскармливании клостридий превышает норму.
Анализ на дисбактериоз
Количество клостридий у взрослых:
Повышенное содержание клостридий часто наблюдается у людей старшего возраста на фоне физиологического снижения бифидобактерий.
Также повышенное содержание мясных продуктов в диете может спровоцировать рост клостридий с превышением естественной нормы.
При дисбактериозах надо регулировать эубактерии, клостридии, бифидо- и лактобактерии.
Лечшими препаратами для коррекции микрофлоры в сторону нормы являются жидкие синбиотики бифидум баг и трилакт. В них запредельное количество живых бактерий плюс жидкая среда в качестве пребиотика.
Живые культуры бифидо- и лактобактерий вместе с частью культуральной среды работают как биокатализаторы, стимулирующие восстановление кишечного гомеостаза в сторону нормы.
Людям старшего возраста необходимо 2 раза в год проводить профилактические курсы бифидум баг+трилакт для восстановления бифидобактерий, латофлоры, клостридий и др. А также регулярно употреблять в пищу кисломолочные продукты.
Трилакт и Бифидум БАГ – это безопасная микробиологическая профилактика и терапия дисбиотических нарушений ЖКТ.
Clostridium ramosum чем лечить
Рис.2. Сопоставление распределения ключевых маркеров клостридий C . ramosum с их соотношением в моче ребенка. Приведена общепринятая аббревиатура жирных кислот и альдегидов. Последние отмечены буквой а в конце символа. В профиле липидных компонент стрептококков и метилотрофов сем. Methylomonadaceae альдегиды отсутствуют
Такого рода идентификация клостридий известна в клинической практике:
Allen S.D., Siders J.A., Riddell M.J., Fill J.A. and Wegener W.S. (1995). Cellular
fatty acid analysis in the differentiation of Clostridium species in the clinical
Местообитание и клиническая значимость
Clostridium ramosum – вид бактерий рода Clostridium ; один из возбудителей газовой гангрены. Вызывает газовую гангрену в ассоциации с другими анаэробами. Выделен из фекалий детей и взрослых, из шейки матки. C . ramosum – полиморфные неподвижные грамположительные или грамотрицательные палочки размером 0,5-0,9 х 2-12,8 мкм, образуют круглые, чаще – терминальные споры. Облигатные анаэробы:
Атлас по медицинской микробиологии, вирусологии и иммунологии. Под ред А.А. Воробьева и А.С. Быкова. – М., Медицинское информационное агентство, 2003. – 236 с.: ил.
Brook, I. Bacterial studies of peritoneal cavity and postoperative surgical wound drainage following perforated appendix in children. Annals of Surgery. 1980; 192: 208–12.
С. ramosum обладает близкой к C . perfringens активностью, в том числе также может вызывать газовую гангрену, язвенный и некротизирующий колиты. Они известны как агенты септицемии, нефропатии, бактериемии и менингита.
Известны в рутинной клинической практике выделение и идентификация культурально-биохимическим методом клостридий из вагинального содержимого женщин с хроническими вагинитами и цервицитами в Центре акушерства, гинекологии и перинатологии:
Муравьева В.В., кандидатская диссертация
Г.Р.Байрамова, Гинекология, Том 3/N 2/2001
Franklin R. Cockerill III, John G. Hughes, Emily A. Vetter, Roger A. Mueller, Amy L. Weaver,
Клостридиозы у детей
Клостридиозы — острые инфекционные заболевания человека и животных, которые вызваны клостридиями.
Клостридиозы классифицируют по механизму возникновения на травматические и энтеральные. К энтеральным относят: клостридиоз диффициле, клостридиоз перфрингенс, ботулизм. К травматическим относят газовую гангрену и столбняк. Ниже будут рассмотрены клостридиоз диффициле и клостридиоз перфрингенс.
Клостридиоз перфрингенс – острое заболевание инфекционной природы с энтеральным путем заражения, которое проявляется синдромом гастроэнтерита или энтероколита и инфекционным токсикозом, а в более редких случаях и некротическим энтеритом или сепсисом.
Клостридиоз диффициле – острое заболевание инфекционной природы (путь заражения также энтеральный), которое вызывается антибиотикоиндуцированными штаммами клостридий диффициле и проявляется диарейным синдромом с развитием псевдомембранозного колита и инфекционным токсикозом.
Что провоцирует / Причины Клостридиозов у детей:
Человек может заразиться только некоторыми представителями клостридий 2-й и 4-й групп, которые приводят к энтеральным клостридиозам, а также возбудителем столбняка и возбудителями газовой гангрены. Данные бактерии вырабатывают специфические активные экзотоксины.
Клостридии «проживают» в естественной среде в кишечниках животных и человека. Они могут там находиться длительное время и размножаться, но при этом к болезням не приводят. С каловыми массами клостридии попадают во внешнюю среду, в основном в землю. Там они могут «жить» долгий срок в виде спор.
Клостридии перфрингенс длительное время считали возбудителем лишь газовой гангрены. Но в середине прошлого столетия наши связь между данными бактериями и пищевыми токсикоинфекциями.
Клостридии перфрингенс представляю собой короткие полиморфные палочки, которые не имеют жгутиков. Могут образовывать субтерминально расположенные споры. Относятся к строгим анаэробам. Их делят на шесть типов в зависимости от способности производить экзотоксины и ферменты: А, В, С, D, Е, F.
Чаще всего детский кишечный клостридиоз спровоцирован клостридиями перфрингенс типа А, в более редких случаях – типами С и F.
Патогенез (что происходит?) во время Клостридиозов у детей:
Клостридиоз перфрингенс попадает в организме в ЖКТ (желудочно-кишечный тракт) вместе с зараженной едой. Далее они следуют в тонкий кишечник, там размножаются, приводя к развитию воспалительного процесса. Через эпителиальный слой кишечника ребенка они попадают в близлежащие ткани и кровь. Так заболевание переходит в тяжелую септическую форму (но не во всех случаях).
Клостридии перфрингенс продуцируют экзоэнтеротоксины, имеющие цитолитические и некротические свойства, что и определяет основные симптомы, которые проявляются в ходе заболевания.
В кишечнике, многих органах и системах (даже в ЦНС) экзотоксины клостридии перфрингенс приводят к функциональным и структурным изменениям. Может развиться токсикоз и эксикоз. К диарее приводит местный воспалительный процесс в кишечнике ребенка.
Патоморфология клостридиоза перфрингенс. Во время болезни максимальные структурные изменения случаются в тонкой или толстой (реже) кишке. У умерших фиксируют отечность слизистой оболочки кишечника, ее гиперемированность, множественные кровоизлияния, стазы, в более редких случаях и некрозы.
Клостридиоз диффициле начинается лишь во время или по окончанию применения антибиотиков широкого спектра действия, в особенности цефамизина, ампициллина, линкомицина и клиндамицина. Это происходит по причине подавления антибиотиками естественной флоры кишечника, вследствие чего клостридии диффициле могут колонизировать кишечник, размножаясь там и образовывая токсины.
Некоторые антибиотики приводят к энтеротоксинообразованию у бактерий. Помимо этого, нормальная кишечная флора у детей и взрослых производит бета-лактамазу — фермент, разрушающий бета-лактамное кольцо бета-лактамов, чем инактивируется действие антибиотика в кишечнике.
Симптомы Клостридиозов у детей:
Инкубационный период клостридиоза перфрингенс составляет от 6 до 24 часов. Это довольно короткий срок. Болезнь имеет острое начало. Проявляются такие симптомы:
С самого начала клостридиоза перфрингенс стул становится жидкой консистенции, частота дефекации повышается. Стул энтеритный или энтероколитный. Болезнь протекает относительно легко, выздоровление наступает на 3-4 сутки после начала.
Кишечный клостридиоза перфрингенс протекает иногда в тяжелых формах – по типу некротического энтероколита или энтерита. Такой форме болезни подвержены ослабленные дети с длительными дисфункциями желудочно-кишечного тракта; дети, которые пролечили антибиотиками широкого спектра действия; дети с кишечным дисбактериозом. Болезнь начинается по типу острого гастроэнтерита. Появляются боли в животе, частая рвота с наличием крови, стул обильный водянистый или пенистый (дефекация от 15 до 20 раз за сутки). В стуле может наблюдаться примесь крови или слизи. От старших детей поступают жалобы на разбитость и общую слабость, головокружения, боли в животе (могут быть постоянными или схваткообразными). Далее начинается обезвоживание организма ребенка, «падает» артериальное давление. Фиксируют увеличение печени и селезенки, парез кишечника (резкое вздутие живота).
Если болезнь прогрессирует и не вылечена вовремя, может случиться летальный исход вследствие нарушения сердечно-сосудистой деятельности. У ослабленных детей и грудничков инфекция может генерализироваться, развивается сепсис.
Кишечный клостридиоз диффициле в большинстве случаев по симптомам аналогичен псевдомембранозному колиту, в более редких случаях – некротическому энтероколиту или диарейному синдрому. Заболевания псевдомембранозным колитом характерны для грудничков, новорожденных и дошкольников.
Псевдомембранозиый колит появляется, как правило, через неделю-10 дней после начала приема антибиотиков. Болезнь начинается остро – поднимается температура, появляются срыгивания или повторная рвота, боли в животе и диарея. Малыши отказываются от еды, родители могут заметить вздутие живота и снижение массы тела.
Кожа приобретает бледно-серый оттенок, на коже живота часто видна сеть застойных вен. Стул становится жидким, водянистым, наблюдаются примеси слизи и крови (не всегда). В некоторых случаях большая часть стула представляет собой густую белесоватую слизь и обрывки фибринозных наложений. Иногда стул гнойный, с кровянистыми примесями. Для некоторых случаев характерно кишечное кровотечение, что часто приводит к летальному исходу.
Болезнь протекает у новорожденных (в особенности – у недоношенных) тяжело. Наблюдают профузный понос, обезвоживание, расстройство периферического кровообращения или расстройство кровообращения по типу коллапса без диареи.
Если есть изъязвление пораженных участков слизистой оболочки кишечника, могут фиксировать перформацию кишечника и каловый перитонит. При этом состояние ребенка тяжелые, кожа окрашивается в серый оттенок, дыхание поверхностное, резко выражен парез кишечника, наблюдаются гиподинамия и гипорефлексия, заостренность черт лица больного ребенка. Не исключена отечность гениталий. Если лечение не начато вовремя, есть вероятность летального исхода.
Клостридии диффициле, помимо некротических энтероколитов, псевдомембранозных колитов и кишечного сепсиса могут приводить к более легким болезням ЖКТ, которые протекают схоже с энтеритами и энтероколитами, особенностей не имеют.
Диагностика Клостридиозов у детей:
Кишечный клостридиоз перфрингенс диагностируют при помощи эпидемиологических и клинико-лабораторных данных в сумме. Для заболевания характерны острое начало, быстро развитие клинических проявлений – диареи, рвоты, повышения температуры, интоксикации или нейротоксикоза и т. д. Симптомы ярче всего выражены на 1-2 день после начала заболевания. Так же быстро «сходят на нет», как и появляются.
Такие симптомы характерны не только для данного заболевания, потому проводят лабораторную диагностику. Используют экспресс-методы (РНГА и ИФА) для обнаружения в фекалиях больного ребенка энтеротоксина. У выделенных штаммов клостридий определяют энтеротоксигенность.
В крови у больных с кишечным клостридиозом перфрингенс наблюдают умеренный лейкоцитоз и палочко-ядерный сдвиг.
Для диагностики кишечного клостридиоза диффициле необходимы сведения анамнеза о терапии антибиотиками, а также инструментальные и клинические показатели. Проводится комплекс лабораторных исследований для обнаружения в фекалиях больного ребенка специфических токсинов (энтеро- и цитотоксина) и возбудителя.
Селективное выделение клостридии диффициле проводят с помощью циклосерин-цефокситин-фруктозного агара. В последнее время диагностику энтероклостридиоза диффициле проводят с помощью высокочувствительных методов ИФА и РЛА.
Доказать клостридиоз диффициле с помощью только обнаружения возбудителя и его токсинов в кале или другом биоматериале от больного нельзя. Потому что данные микроорганизмы и токсины могут быть и у здорового человека, в основном у недавно рожденных и детей до 6 месяцев.
Лечение Клостридиозов у детей:
Лечебные мероприятия при кишечном клостридиозе перфрингенс аналогичны таковым при других бактериальных диареях. Назначают этиотропную терапию, учитывая чувствительность обнаруженных штаммов клостридий к антибиотикам. Врачи рекомендуют использовать для лечения энтеральные формы антибиотиков, к примеру, азитромицин, амоксиклав, цефалоспорины 3-го поколения и т. д.
Комплексная терапия включает бактерийные препараты, такие как бификол или бифидумбактерин, а также другие препараты для нормализации биоценоза кишечника. Бактерийные препараты служат для прекращения колонизации кишечника клостридиями. При особо тяжелых формах заболевания, если установлен тип возбудителя, для лечения могут применять антитоксическую сыворотку в дозе 5000—10000 АЕ внутримышечно по методу Безредки или энтерально.
Под этиотропной терапией антибиотикоиндуцированного кишечного клостридиоза диффициле подразумевают введение парентеральных аминогликозидов, метронидазола, цефалоспоринов.
После окончания приема антибиотиков следует назначить ребенку прием бактерийных препаратов (к примеру, линекса, бифидумбактерина, лактобактерина и пр). Это поможет нормализовать биоценоз в кишечнике.
Лечат клостридий диффициле также ферментными препаратами, например, фесталом, креоном и т. д., витаминами (в особенности – группой В). Необходима симптоматическая и патогенетическая терапия. Если есть соответствующие показания, применяют инфузионную терапию, чтобы нормализовать баланс жидкости в организме ребенка, провести дезинтоксикацию и парентеральное питание. Применяют антигистаминные препараты, а при тяжелых формах кортикостероиды и специфические антитоксические сыворотки.
Профилактика Клостридиозов у детей:
Самые важные профилактические меры заключаются в:
— строгом соблюдении санитарно-гигиенических норм приготовления, хранения и сбыта пищевых продуктов;
— активном выявлении носителей клостридий среди работников пищеблоков и детских учреждений;
— своевременной изоляции и лечении зараженных клостридиями детей и взрослых;
— санитарно-просветительной работе среди населения о правильном уходе за детьми и их кормлении;
— кратновременном хранении продуктов и термической обработке.
Профилактические меры при кишечном клостридиозе диффициле должны быть направлены, прежде всего, на предупреждение антибиотикоиндуцированности как важнейшего фактора заболевания этим клостридиозом.
Не следует использовать как профилактическое или лечебное средство антибактериальные лекарства широкого спектра действия длительными курсами.
Чтобы избежать колонизации кишечника клостридиями, необходимо вовремя лечить кишечный дисбактериоз и проводить его профилактику. В стационарах, особенно в отделениях для новорожденных, следует обеспечивать необходимый санитарно-гигиенический режим, правильную дезинфекцию инструментария, посуды, белья и т. д.
Обработка предметов проводится с помощью хлориндиоксида или его аналогов, имеющих бактерицидные и спороцидные свойства, влияющие на клостридий.
К каким докторам следует обращаться если у Вас Клостридиозы у детей:
Клостридии. Всегда рядом, всегда начеку
Ботулизм, столбняк, газовая гангрена… Об этих заболеваниях наслышаны если не все, то очень многие люди. Но если от столбняка существуют вакцины, например АКДС (адсорбированная коклюшно-дифтерийно-столбнячная сыворотка), то от псевдомембранозного колита, некротического энтерита, ботулизма или газовой гангрены таких вакцин нет. А вызываются все эти заболевания бактериями рода Clostridium.
Одним из наиболее распространенных видов клостридий является Clostridium difficile. Ее высевают из почвы, воды (в том числе и морской). Благодаря возможности образовывать эндоспоры (покрываться оболочкой и переживать неблагоприятный период в состоянии своеобразной «спячки») этот вид может длительно, до двух месяцев, сохраняться во внешней среде. Более того, в состоянии эндоспоры клостридия диффициле выдерживает даже кипячение. Чувствительность к антибиотикам у Clostridium difficile от природы очень низкая, поэтому лечение посредством антибиотикотерапии зачастую терпит фиаско.
Clostridium difficile входит в нормофлору (является представителем нормального микробного состава) желудочно-кишечного тракта, обитая преимущественно в толстом кишечнике. Хотя отдельные его представители встречаются и во рту, и в тонком отделе кишечника, и во влагалище у женщин. Чаще всего Clostridium difficile обнаруживается в кишечнике новорожденных (около половины младенцев), а из детей старше 2 лет и взрослых каждый 10 является обладателем этой бактерии.
Clostridium difficile вызывает такие заболевания как псевдомембранозный колит и антибиотикоассоциированные диареи. Патогенные (болезнетворные) свойства этой клостридии обусловлены выделением токсинов А и В, а также белка, угнетающего перистальтику (сократительную функцию) кишечника.
Антибиотикодиссоциированные диареи (сокращенно – ААД) могут вызываться не только клостридией дифициле, а и множеством других микроорганизмов (сальмонеллами, кандидами, клостридией перфрингенс, золотистым стафилококком, клебсиеллой). Этот вид диарей является наиболее частой внутрибольничной инфекцией и связана такая тенденция с тем, что в больницах, во-первых, концентрируется большая масса больных и здоровых людей. А во-вторых, здесь используется множество антибиотиков и дезинфицирующих средств, которые способствуют образованию генераций (поколений) микроорганизмов, устойчивых к антибиотикам. Поэтому в мире ежегодно регистрируется около миллиона случаев ААД. Возникновение антибиотикоассоциированных диарей связано с тем, что антимикробные препараты подавляют как патогенную, так и нормальную микрофлору. Даже однократный прием антибиотиков широкого спектра действия может послужить причиной развития ААД.

Несмотря на это, дети младенческого возраста практически не болеют антибиотикоассоциированными диареями, вызываемыми клостридией диффициле. Связано это с тем, что дети получают с материнским молоком достаточно иммунных факторов, которые могут сдерживать размножение Clostridium difficile. Более того, в младенческом организме нет такого количества сопутствующей условно-патогенной микрофлоры, которая ослабляет иммунитет.
Антибиотикозависимые диареи могут иметь разную симптоматику и течение: от легкой диареи до тяжелейшего псевдомембранозного энтероколита (ПМК). Последний чаще всего вызывается именно клостридией диффициле.
В процессе течения заболевания отмечаются следующие симптомы:
При отсутствии лечения количество смертельных случаев составляет до 30 %.
Характерная особенность болезней, вызванных Clostridium difficile, является то, что около четверти случаев через время повторяются (рецидив заболевания). Причиной этого явления становятся споры клостридий, которые переживают период лечения, либо повторное заражение. Как правило, после лечения больные выздоравливают, или чувствуют себя значительно лучше, но спустя несколько дней (от 3 до 7) развивается рецидив.
Еще одна клостридия, которая может вызывать такие болезни желудочно-кишечного тракта, как пищевые токсикоинфекции и некротический энтерит, — Clostridium perfringens.
Некротический энтерит характеризуется формированием язв и эрозий и деструктивными (разрушающими) изменениями в слизистой оболочке. Первым симптомом заболевания является возникновение участков геморрагического некроза в начальных отделах тощей кишки. Эти участки имеют красный цвет. Наблюдается также сужение просвета кишечника в месте воспаления, за счет отечности стенки. Происходит тромбоз (закупорка) мелких кровеносных сосудов (артериол). У больного отмечаются озноб и лихорадка, рвота и кровавый пенистый понос.
Clostridium perfringens производит ферменты, расщепляющие белки (протеиназа), коллаген (коллагеназа), гиалуроновую кислоту (гиалуронидаза).

Профилактика заболеваний, причиной которых являются клостридии, в первую очередь заключается в соблюдении санитарно-гигиенических норм и правил: мытье и ошпаривание овощей и фруктов; длительная термическая обработка. Но немаловажным является также нормализация микрофлоры и укрепление иммунитета. Причем, как в процессе лечения, так и в процессе предупреждения этих болезней. Ограниченное и строго подконтрольное врачам применение антибиотиков, отказ от самолечения также очень важны для профилактики возникновения АДД и других болезней, связанных с клостридиями.
Столбнячная палочка: токсична и смертельно опасна
Столбнячная палочка: токсична и смертельно опасна
Столбнячная палочка присутствует в почве, пыли и даже в кишечнике человека. В целом она безобидна, но попав в рану с бескислородной средой, становится смертельно опасна. Защититься помогает вакцинация.
Автор
Редакторы
В этой статье спецпроекта, посвященного вакцинации, мы поговорим о столбняке. Он отличается от большинства инфекций, против которых массово делают прививки: им нельзя заразиться, побывав рядом с больным человеком. Возбудители столбняка окружают каждого из нас в повседневной жизни и, вероятно, их никогда не получится полностью ликвидировать. Поэтому так важно проводить вакцинацию: она — важнейший метод защиты от смертельно опасной болезни.
Вакцинация
Генеральный партнер спецпроекта — Zimin Foundation.
Изобретение вакцин кардинально изменило жизнь человечества. Многие болезни, уносившие тысячи, а то и миллионы жизней ежегодно, теперь практически не встречаются. В этом спецпроекте мы не только рассказываем об истории возникновения вакцин, общих принципах их разработки и роли вакцинопрофилактики в современном здравоохранении (этому посвящены первые три статьи), но и подробно говорим о каждой вакцине, включенной в Национальный календарь прививок, а также вакцинах против гриппа и вируса папилломы человека. Вы узнаете о том, что собой представляет каждый из возбудителей болезней, какие существуют варианты вакцин и чем они различаются между собой, затронем тему поствакцинальных осложнений и эффективности вакцин.
Для соблюдения объективности мы пригласили стать кураторами спецпроекта Александра Соломоновича Апта — доктора биологических наук, профессора МГУ, заведующего лабораторией иммуногенетики Института туберкулеза (Москва), — Сусанну Михайловну Харит — доктора медицинских наук, профессора, руководителя отдела профилактики НИИ детских инфекций (Санкт-Петербург), — а также Сергея Александровича Бутрия — педиатра, автора блога «Заметки детского врача».
Бактерия, которая не любит кислород
Возбудитель столбняка — столбнячная палочка (по-латыни — Clostridium tetani). Она относится к роду Clostridium, который включает, как минимум, 209 разных видов и 5 подвидов анаэробных сапрофитных (использующих для питания разлагающиеся ткани или продукты жизнедеятельности животных и растений) грамположительных бактерий [1]. Столбнячная палочка — один из четырех наиболее изученных видов патогенных микроорганизмов из рода Clostridium. Другие три:
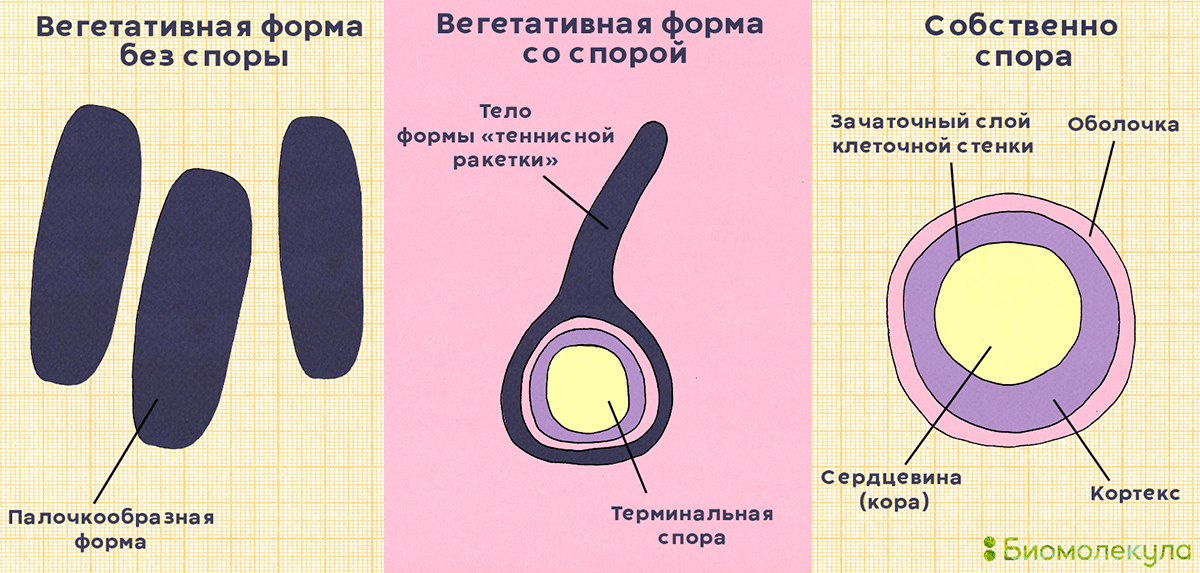
Столбнячная палочка может существовать только там, где нет кислорода (в науке такие организмы называются облигатными анаэробами) [1]. Несмотря на такую привередливость, она распространена повсеместно, и полностью ее ликвидировать, видимо, никогда не удастся. Секрет живучести прост: помимо вегетативной («взрослой», активно размножающейся) формы, она может существовать в виде спор. Под микроскопом вегетативная форма бактерии выглядит как палочка, имеет длину 2–2,5 и ширину 0,3–0,5 микрометра. Она подвижна за счет расположенных по всей поверхности клетки жгутиков. В процессе образования спор бактерия теряет жгутики и приобретает характерную форму, напоминающую барабанную палочку или теннисную ракетку (рис. 1) [1–4].
Рисунок 1. Внешний вид вегетативной формы Clostridium tetani (без споры и со спорой) и споры. Вегетативная форма привередлива, быстро погибает под действием негативных факторов, чувствительна к некоторым антибиотикам. Споры, напротив, очень живучие и могут годами сохраняться в почве и домашней пыли.
Споры столбнячной палочки устойчивы к высушиванию, они выживают при кипячении и обработке дезинфицирующими средствами. Вегетативные формы, напротив, быстро погибают в неблагоприятных условиях и чувствительны к некоторым антибиотикам, таким как метронидазол и бензилпенициллин. Споры сохраняются в почве и домашней пыли от нескольких месяцев до нескольких лет, они присутствуют в пищеварительном тракте животных, навозе. Clostridium tetani может обитать даже в кишечнике человека, не причиняя вреда и не вызывая каких-либо симптомов [2], [5].
Оптимальная температура для культивирования возбудителя в лаборатории — 33–37 °C. Столбнячную палочку выращивают на различных анаэробных (лишенных кислорода) питательных средах, таких как тиогликолят и гидролизат казеина. На кровяном агаре микроорганизм образует характерные колонии в виде сеточек из тонких нитей (рис. 2). Во время роста колоний выделяется газ и возникает характерный неприятный запах [3].
Рисунок 2. Колонии Clostridium tetani на кровяном агаре
Для того чтобы инактивировать споры, нужно опустить их на 15–24 часа в дезинфицирующие растворы, например, фенола (5%), формалина (3%), хлорамина (1%), перекиси водорода (6%). Водный раствор йода и 2% глутаровый альдегид при рН 7,5–8,5 убивают споры в течение трех часов. Автоклавирование при 120 °С и 100 кПа уничтожает их в течение 15–20 минут [3].
Конечно же, самая важная особенность Clostridium tetani, из-за которой против этого возбудителя нужна вакцинация, — это способность вырабатывать опасный для человека токсин.
Историческая справка
Столбняк известен человечеству с древних времен: впервые его симптомы были описаны более 3000 лет назад в Древнем Египте [6]. В древнеегипетском папирусе Эдвина Смита (1550 г. до н. э., рис. 3) рассказывается о 33 случаях травм черепа, лица, челюсти и спинного мозга. Особенно интересен случай №7 — лечение зияющей раны на голове. Судя по описанию, развилось осложнение, которое вполне могло быть столбняком. Древний врач обработал рану обезболивающим средством и наложил чистую повязку. Он считал, что у пациента есть все возможности выздороветь. Но со временем рана начала неприятно пахнуть, и больной перестал открывать рот из-за спазма мышц.
Рисунок 3. Фрагмент папируса Эдвина Смита — первого в истории документа, в котором можно найти описание клинической картины столбняка и выводы о бесполезности его лечения.
Папирус так описывает эту ситуацию [7]:
Вы обнаружите у этого пациента, что его плоть под раной стала теплой. Его стала беспокоить зубная боль на стороне поражения. Вы кладете руку на его лицо и обнаруживаете, что его лоб мокрый от пота. Мышцы его шеи напряжены, его лицо красное. Запах, который исходит от его черепа, похож на запах экскрементов овец/коз. Он не может открыть рот, его брови приподняты, лицо выглядит так, как будто он плачет. Вы скажете об этом больном: “У него зияющая рана на голове, распространяющаяся до кости и проникающая в полость черепа”. У него возникла зубная боль, его рот не может открыться, мышцы шеи напряжены. Этот недуг не стоит лечить.
А вот как описал случай столбняка древнегреческий врач Гиппократ:
Капитан корабля поранил якорем указательный палец правой руки. Через семь дней появилось некоторое количество отвратительных выделений, а затем проблемы с речью — он пожаловался, что не может должным образом разговаривать. Был диагностирован столбняк, его челюсти сжались, зубы сжались, появилось напряжение мышц на шее, на третий день появились опистотонус и потливость. Через шесть дней с момента установления диагноза он умер.
Шли столетия, а в отношениях между людьми и столбнячной палочкой практически ничего не менялось. Люди по-прежнему заражались, некоторые погибали, а врачи по-прежнему могли лишь разводить руками и всякий раз надеяться, что болезнь пройдет, не погубив очередную жертву.
Ситуация стала меняться в конце XIX века. Впервые предположение о том, что столбняк — инфекционное заболевание, вызванное неким микроорганизмом, высказал русский хирург Нестор Дмитриевич Монастырский (рис. 4). В 1883 году он обнаружил бактерию в выделениях из раны больного столбняком спустя восемь дней после заражения. Возбудителя удалось выделить из раны как прижизненно, так и посмертно. Но Монастырский не успел получить лавры первооткрывателя столбнячной палочки из-за того, что опубликовал результаты своих наблюдений с большой задержкой — только в 1885 году [8].
Независимо от Монастырского, в 1884 году возбудителя столбняка обнаружил 22-летний немецкий медик Артур Николаер (рис. 5). Его и считают во всем мире первооткрывателем Clostridium tetani. В Англии и Франции эту бактерию зачастую так и называют — бацилла Николаера [9].
Рисунок 4. Нестор Дмитриевич Монастырский (1847–1888 гг.) — русский хирург, первым установивший микробную природу столбняка и выделивший бактерию из раны больного. Результаты своих наблюдений он изложил в сочинении «Наблюдения и исследования о травматическом столбняке», опубликованном в Санкт-Петербурге в 1885 году.
Ядовитый микроб: почему столбнячная палочка опасна для человека?
Столбнячная палочка выделяет два токсина: тетанолизин и тетаноспазмин.
Тетанолизин — это кислородочувствительный гемолизин, который может играть роль в развитии местной инфекции, но не имеет никакого другого известного значения в развитии столбняка [3].
Минута научного занудства: о токсинах клостридии для профессионалов
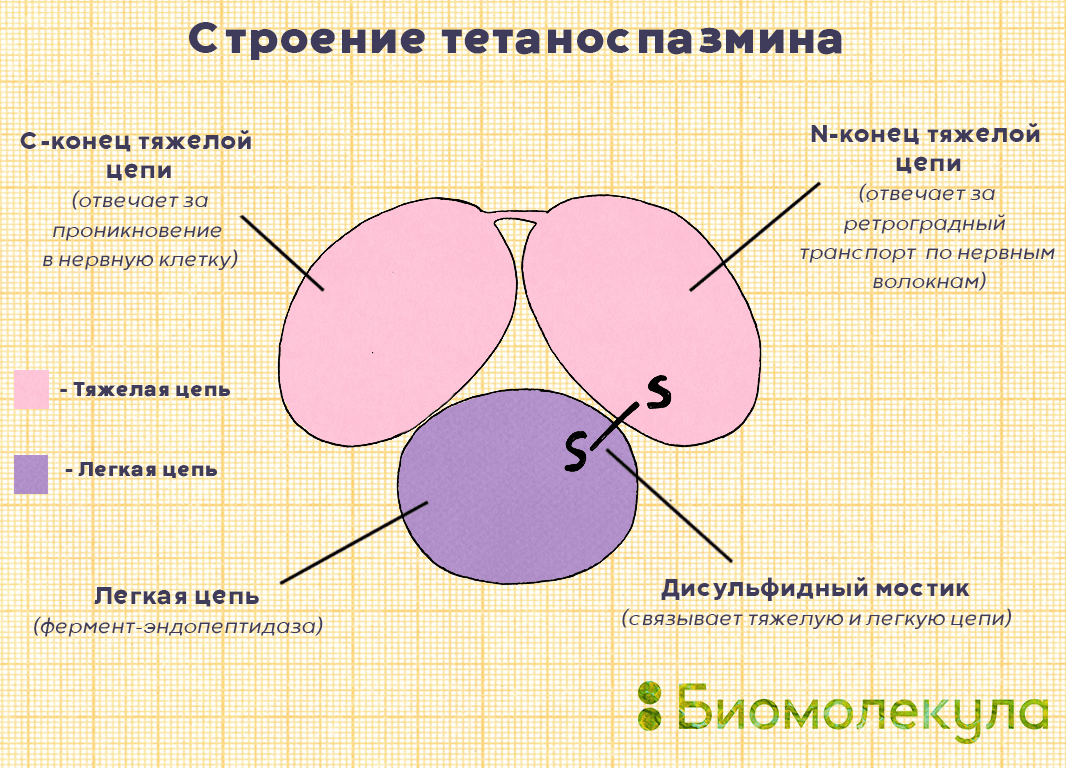
Тетаноспазмин выделяется в ткани после разрушения бактериальных клеток в виде протоксина (неактивного предшественника). Оказавшись вовне, он расщепляется тканевыми или бактериальными ферментами протеазами и переходит в активную форму. Она имеет молекулярную массу 150 000 кДа и состоит из двух цепей: легкой (50 000 кДа) и тяжелой (100 000 кДа) (рис. 6) [3].
Рисунок 6. Строение тетаноспазмина. Токсин состоит из тяжелой цепи с двумя доменами и легкой цепи, которые соединены между собой дисульфидной связью.
Молекула токсина имеет три домена, каждый из которых выполняет свою роль на определенном этапе [3]:
В общих чертах путь тетаноспазмина в организме зараженного человека выглядит следующим образом [3]:
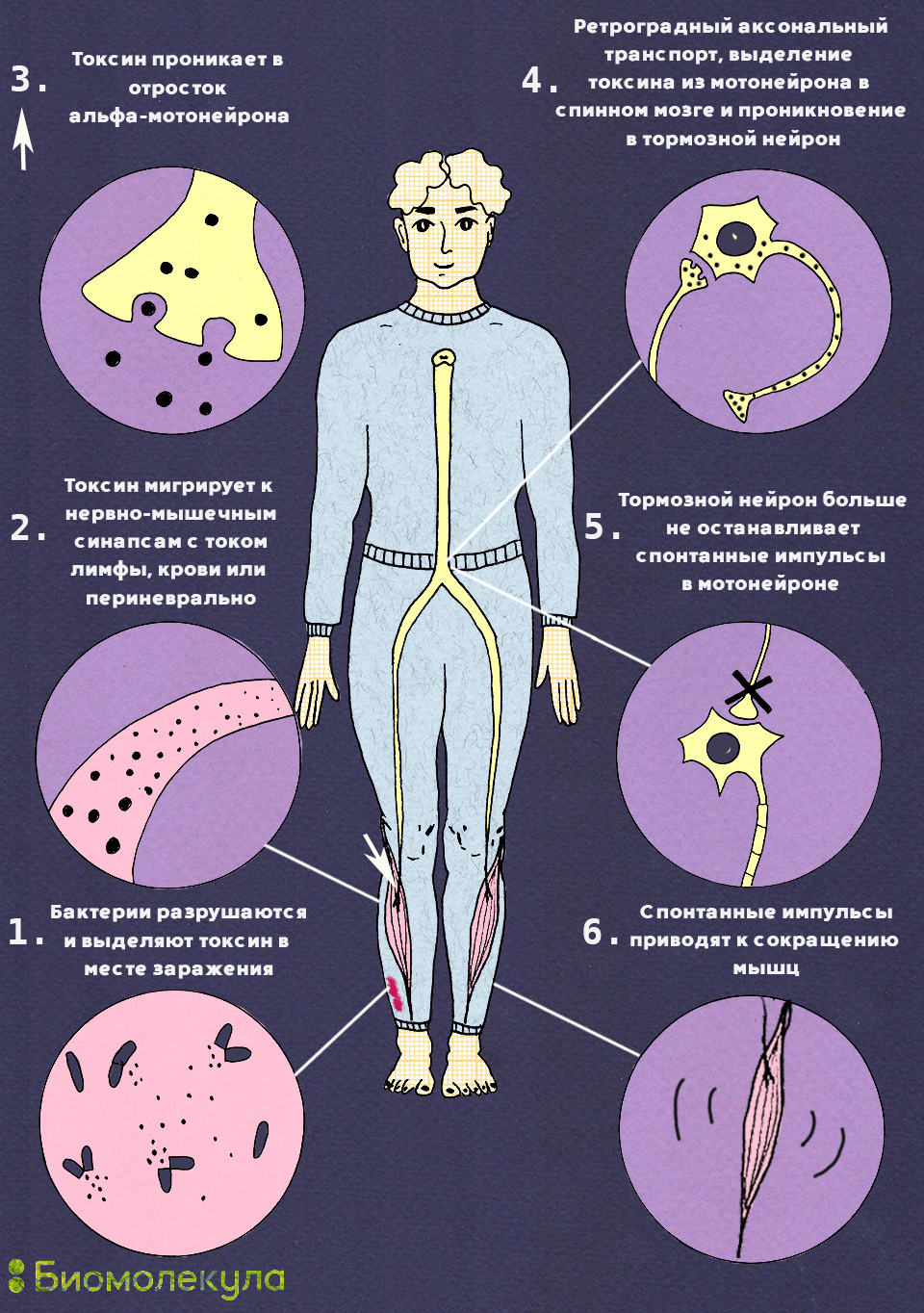
Путь токсина в нервной системе и патогенез заболевания показаны на рисунке 7.
Рисунок 7. Путь столбнячного токсина в теле человека
Пути заражения
Наиболее распространенный способ заражения столбняком — через рану. Это может произойти как на улице, так и в помещении. Так как вегетативная форма возбудителя не может жить в присутствии кислорода, рана должна быть особенной: небольшой, но глубокой. За счет этого внутри создаются бескислородные условия, которые способствуют выживанию бактерий. Чаще всего столбняк развивается у людей, которые получили колотые, рваные раны, ссадины. Примерно в трети случаев колотая рана, через которую произошло заражение, находилась в области ногтя. Это происходит из-за того, что ноги и руки часто контактируют с землей, часто происходит повреждение в области ногтей на руках острыми предметами (например иглами) во время работы. В то же время, за счет того, что ноготь прикрывает кожу, в этих местах легко возникает «бескислородный мешок» [2], [3].
Риск заражения столбняком повышается при дополнительном повреждении кожи, например, абсцессах, гангрене, ожогах, обморожениях, трофических язвах (как при сахарном диабете). Известны случаи, когда заболевание развивалось как осложнение среднего отита, повреждений роговицы, абсцесса пародонта, инородных тел носа, после абортов, различных хирургических вмешательств, стоматологических процедур (например, удаления зубов, лечения корневых каналов). Возбудителя можно занести в организм, если делать инъекции грязными шприцами, в тату-салонах и салонах пирсинга, где не соблюдаются правила стерилизации инструментов [2].
Столбнячная палочка проникает в организм человека только из окружающей среды в виде спор, которые затем, в бескислородных условиях, могут перейти в вегетативную форму.
Больной человек не опасен для окружающих, от него нельзя заразиться.
Симптомы
В зависимости от проявлений, принято выделять четыре типа столбняка:
Рассмотрим течение и основные симптомы заболевания на примере классической формы — генерализованного столбняка.
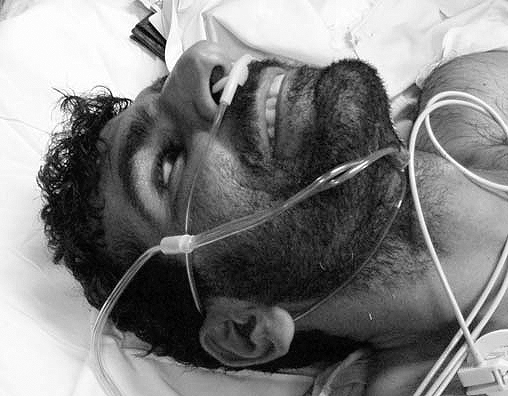
Инкубационный период заболевания составляет в среднем 8–14 дней, может продолжаться от 3 до 21 дня. У новорожденных он обычно короче. Поначалу беспокоит боль в области раны, возникают подергивания в окружающих мышцах, болезненность по ходу нерва в пораженной конечности. Иногда основным симптомам предшествуют раздражительность, беспокойство, учащенное сердцебиение, потливость [1], [13].
Далее возникает напряжение в мышцах нижней челюсти (тризм), из-за этого больному становится сложно открывать рот, а затем это становится и вовсе невозможным. Появляется характерное выражение лица: челюсти сильно сжаты, брови приподняты, крылья носа «раздуты», углы рта оттянуты в стороны и вниз. Лицо больного как будто одновременно выражает улыбку и гримасу страдания, поэтому такая картина получила образное название «сардоническая гримаса» — risus sardonicus (рис. 8) [1], [13].
Рисунок 8. Risus sardonicus — характерное выражение лица при столбняке. Рот больного как будто растянут в страдальческой улыбке, брови и крылья носа приподняты.
Постепенно напряжение распространяется ниже, на другие группы мышц. Возникает ригидность (напряжение и жесткость) мышц затылка. В зависимости от того, какие группы мышц затрагивает тоническое напряжение, больной принимает одну из характерных поз:
Рисунок 9. Опистотонус — характерное проявление генерализованной формы столбняка. Больной выгибается в виде дуги и фиксируется на голове и пятках. Эту картину написал в 1809 году сэр Чарльз Белл — шотландский анатом и физиолог. На ней изображен человек, который заразился столбняком после огнестрельного ранения.
Периодически тоническое напряжение сменяется клоническими судорогами — короткими сокращениями, подергиваниями мышц. Они причиняют сильную боль, могут возникать часто и сохраняться очень долго, изнуряют больного.
Почему столбняк — опасное заболевание?
Прогноз сильно зависит от того, был ли человек ранее привит. Так, согласно статистике США, смертность от заболевания среди непривитых на данный момент составляет 15%, а среди привитых — всего 6% [2].
Самая распространенная причина смерти от столбняка — аритмия и остановка сердца в результате поражения ствола головного мозга [1], [2]. Но заболевание может приводить и к другим серьезным осложнениям:
Если у человека возникли симптомы, напоминающие столбняк, его нужно немедленно доставить в больницу. Врач устанавливает диагноз после осмотра на основании характерной клинической картины. Лабораторные исследования, направленные на обнаружение возбудителя, не требуются [1], [15].
Неонатальный столбняк: бич новорожденных
Столбняк у новорожденных выделен в особую категорию, потому что он протекает очень тяжело и нередко приводит к смерти. Наиболее высока заболеваемость и смертность в странах с низким уровнем доходов населения, в сельской местности, где роды зачастую происходят на дому, в антисанитарных условиях.
Заражение неонатальным столбняком происходит через пуповину. Симптомы появляются на 3–24 день жизни. Ребенок отказывается от кормления, потому что не может нормально сосать из-за спазма жевательных мышц, у него возникает risus sardonicus, спазм мышц рук и ног — сначала от воздействия раздражителей (яркого света, прикосновений, громких звуков), затем спонтанно. В финале развивается опистотонус.
Помимо неонатального, актуальна проблема материнского столбняка. Этим термином обозначают заболевание, которое развивается в течение беременности или шести недель после родов (аборта). Оно также отличается более тяжелым течением и высокой смертностью по сравнению с «обычным» столбняком.
В качестве мер профилактики неонатального и материнского столбняка эксперты рекомендуют: вакцинацию женщин репродуктивного возраста и во время беременности, роды в условиях родильных домов с соблюдением правил асептики и антисептики, тщательный эпиднадзор [16].
Лечение
Как только пациент доставлен в клинику, его сразу помещают в палату интенсивной терапии и начинают лечение:
Как работает иммунитет против столбняка?
О том, как работает противоинфекционный иммунитет, можно узнать из нашей статьи «Иммунитет: борьба с чужими и… своими» [17]. В случае со столбняком важную роль играют антитела. Они умеют специфически «распознавать» разные белки столбнячной палочки. Наиболее важны те, что нацелены на тетаноспазмин.
Иммунная система нейтрализует тетаноспазмин с помощью особых антител — антитоксинов, которые представляют собой иммуноглобулины класса G. Они вырабатываются в организме при двух условиях: во время болезни и после прививки [15], [18].
Человек может получить защиту против столбняка путем активной (прививка анатоксином, который заставляет организм вырабатывать собственные антитела) или пассивной (после введения иммуноглобулина) иммунизации. Во время беременности будущего ребенка защищают антитела матери, которые проникают через плаценту [15], [18].
Раньше велись споры о том, возможна ли естественная иммунизация: может ли иммунитет сохраняться после перенесенного столбняка и защищать человека еще в течение некоторого времени? На данный момент ученые уверены, что ответ на этот вопрос — «нет». После перенесенного заболевания человек вполне может заболеть повторно. Единственный эффективный способ защиты — вакцина [3].
История создания противостолбнячной вакцины
Рисунок 10. Китасато Шибасабуро (1853–1931 гг.) — японский ученый, впервые в истории получивший чистую культуру Clostridium tetani.
В 1889 году японский врач и бактериолог Китасато Шибасабуро (рис. 10) впервые получил чистую культуру столбнячных палочек [19]. Вместе с Эмилем Адольфом фон Берингом [20] они продемонстрировали, что сыворотка кроликов, подвергшихся воздействию столбнячного токсина, будучи введенной неиммунизированным животным, помогает предотвратить у них заболевание [21]. Этим было положено начало развитию пассивной иммунизации.
В 1893 году французский ветеринар и микробиолог Эдмонд Нокар (рис. 11) успешно применял сыворотку для пассивной иммунизации лошадей против столбняка [22].
Рисунок 11. Эдмонд Нокар (1850–1903 гг.) — французский ученый, внесший большой вклад в развитие пассивной иммунизации против столбняка.
Вся последующая история развития вакцин против столбняка сильно связана с историей войн (рис. 14). Ведь поле боя — это место, где люди постоянно получают ранения, и тут клостридии не упускают своих возможностей. Усилия врачей и ученых были направлены на решение этой проблемы.
Спустя пару десятилетий нашелся повод для первого массового применения лошадиного противостолбнячного антитоксина на людях: началась Первая мировая война. Из-за того что препарат был плохо очищен, у многих пациентов развивались анафилактические реакции, сывороточная болезнь и другие серьезные осложнения [23], [24].
С 1960-х годов стали доступны человеческие противостолбнячные антитела. Сегодня от лошадиной сыворотки в развитых странах отказались из-за аллергических реакций.
Рисунок 12. Рамон Гастон (1886–1963 гг.) — создатель столбнячного анатоксина. Он первым обнаружил, что формалин инактивирует дифтерийные и столбнячные токсины, сохраняя их способность вызывать иммунный ответ.
Эпоха активной иммунизации против столбнячной палочки началась в 1923 году, когда французский ветеринар Рамон Гастон (рис. 12) сначала открыл феномен флокуляции, позволяющий титровать столбнячный и дифтерийный токсины in vitro («в пробирке»), а затем заметил, что после обработки небольшим количеством формалина токсин больше не может нанести вреда человеку, но сохраняет антигенность, то есть способность вызывать иммунный ответ. Так были изобретены анатоксины (токсоиды) — «обезоруженные» токсины, которые и являются основным работающим компонентом вакцины [25], [26].
На основе анатоксинов, полученных Гастоном, создали вакцину, которая спустя 20 лет помогла спасти множество жизней. Вакцинация от столбняка, которая на тот момент уже была широко внедрена, принесла неоценимую пользу армиям союзников во время Второй мировой войны.
Рисунок 13. Павел Феликсович Здродовский (1890–1976 гг.) — микробиолог, иммунолог, д. м. н., профессор, академик АН СССР. Под его руководством были разработаны методы вакцинации против столбняка в Советском Союзе.
Бойцам советской армии вводили анатоксин, поливакцины, содержавшие смесь антигенов микробов брюшного тифа, паратифа А и В, холеры, дизентерий Григорьева—Шиги и Флекснера и столбняка, — они помогали быстро и относительно эффективно создавать иммунитет. Методы вакцинации против столбняка и некоторых других инфекций в СССР были разработаны под руководством микробиолога и иммунолога Павла Феликсовича Здродовского (рис. 13) [27], [28].
В 1944 году, в ходе кровопролитных сражений, британская, французская и американская армии практически не пострадали от столбняка, в то время как от него погибли многие немецкие солдаты. Вакцинация стала обязательной во французской армии еще с 1936 года, а в 1939 году союзные войска решили привить всех своих бойцов [26].
К 60-м годам прошлого столетия столбнячный анатоксин уже довольно широко применяли для активной иммунизации во многих странах. В 1974 году Всемирная организация здравоохранения (ВОЗ) приняла «Расширенную программу по иммунизации», в которую вошла комбинация дифтерийного и столбнячного анатоксинов [29]. С тех пор охват населения мира вакцинацией постоянно рос. Так, в 1980 году в странах за пределами Европы, Северной и Южной Америк три дозы вакцины АКДС [30] получило лишь 20% населения. К 2013 году средний показатель составил 86%, минимальный — 75% [31].
Рисунок 14. История столбняка: от первого упоминания до разработки АКДС.
Как изменилась ситуация со столбняком после появления вакцины?
После введения массовой вакцинации люди стали болеть столбняком намного реже. Это хорошо видно по динамике заболеваемости в США. Если в 1947 году, когда активная иммунизация, можно сказать, делала первые шаги, заболеваемость составляла 4 случая на 1 миллион населения, то в период с 2008 по 2011 год в США было зарегистрировано всего 233 случая, то есть на 95% меньше [29]. За тот же промежуток времени ежегодное количество смертей от столбняка уменьшилось на 99%. Конечно же, снижение показателей смертности — это заслуга не только активной иммунизации. Большую роль играют пассивная иммунизация и своевременное, правильное лечение [2].
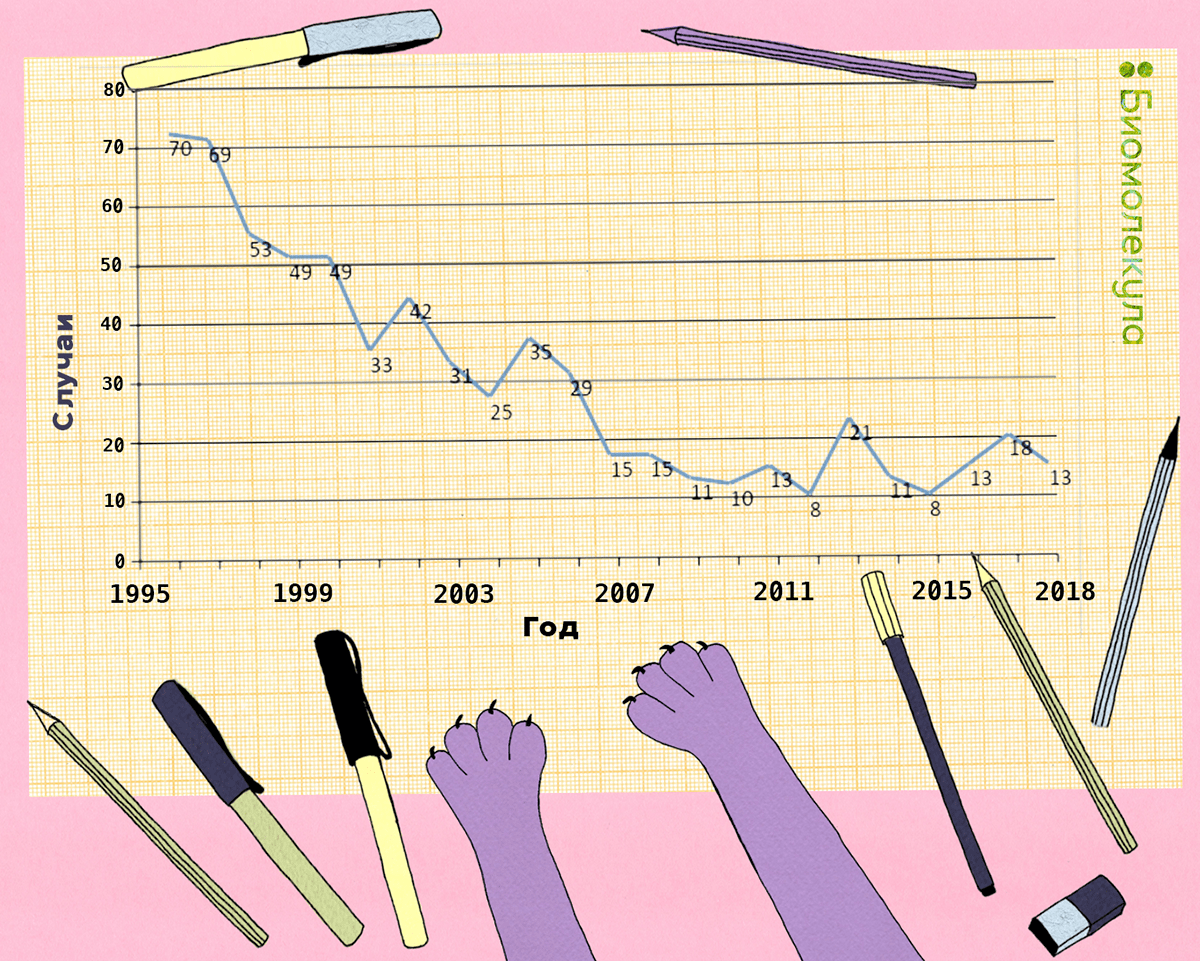
Последняя статистика по смертности от неонатального столбняка доступна за 2015 год на сайте ВОЗ. Инфекция унесла жизни 34 019 новорожденных, что на 96% меньше, чем в 1980 году [32]. На рисунке 15 представлена динамика заболеваемости столбняком в России в 1997–2018 гг.
Рисунок 15. Заболеваемость столбняком на территории России с 1997 по 2018 годы
Тем не менее, столбняк остается актуальной проблемой современного здравоохранения. Он все еще убивает людей, хотя и далеко не так часто, как раньше. Чаще всего такие случаи встречаются в развивающихся странах, где есть проблемы с доступностью медицинской помощи, особенно в тропической зоне. Риски повышены у пожилых людей, так как многие из них получали последнюю дозу вакцины давно, а иммунитет с возрастом снижается [2], [29].
В ряде стран большую проблему представляет распространение столбняка среди детей, подростков и молодежи. По данным ВОЗ, в 2004 году 27 миллионов детей не получили третью дозу вакцины — решение этой проблемы помогло бы предотвратить многие случаи заболевания [29].
Современные вакцины
Все противостолбнячные вакцины для активной иммунизации производятся из анатоксина. На современном рынке представлены разные препараты, которые различаются по составу и в зависимости от этого имеют те или иные сокращенные обозначения:
Об истории разработки АКДС, ее составе, а также противопоказаниях и риске осложнений рассказано в статье «Коклюш: кашель, который убивает» [30]. Поэтому, прежде чем читать далее, очень советуем сначала ознакомиться с этим материалом! — Ред.
Требования к производству, свойствам и составу столбнячного анатоксина в России прописаны в Фармакопейной статье Министерства Здравоохранения Российской Федерации «Анатоксин столбнячный адсорбированный (АС-анатоксин)» ФС.3.3.1.0007.15.
Порядок вакцинации
Эксперты ВОЗ утверждают, что в идеале каждый человек должен получить 5 доз вакцины в детстве и еще одну — бустерную — в раннем зрелом возрасте. Первичный курс, состоящий из трех доз, рекомендуется проводить в течение первого года жизни. Затем в идеале ревакцинацию нужно провести в 4–7 лет и 12–15 лет. Шестую дозу женщинам обычно вводят во время первой беременности, а мужчинам — во время военной службы. Такая схема обеспечивает длительную защиту, возможно, в течение всей жизни. Схемы вакцинаций для разных групп людей, предложенные ВОЗ, представлены в таблице 3.
| Схема вакцинации с рождения | DTP | DTP | DTP | dT | dT | dT |
| Вакцинацию начинают до 1 месяца или после 6 недель, как можно раньше. Промежутки между введениями вакцин должны быть не менее 4 недель. | Идеально в 4–7 лет. | Идеально в 12–15 лет. | В раннем зрелом возрасте. | |||
| Взрослые и подростки, которые ранее не прививались | dT | dT | dT | dT | dT | |
| Как можно раньше. | Не менее чем через 4 недели после введения первой дозы. | Не менее чем через 6 месяцев. | Не менее чем через год. | Не менее чем через год. | ||
| Беременные женщины, которые не прививались, либо у них отсутствуют данные о предшествовавших прививках | dT | dT | dT | dT | dT | |
| Как можно раньше в течение первой беременности. | Не менее чем через 4 недели после введения первой дозы. | Не менее чем через 6 месяцев или во время второй беременности. | Не менее чем через год или во время второй беременности. | Не менее чем через год или во время второй беременности | ||
| Беременные женщины, которым в детстве были введены три дозы вакцины | dT | dT | dT | |||
| Как можно раньше в течение первой беременности. | Не менее чем через 4 недели после введения первой дозы. | Не менее чем через год. | ||||
| Беременные женщины, которым в детстве были введены четыре дозы вакцины | dT | dT | ||||
| Как можно раньше в течение первой беременности. | Не менее чем через год. | |||||
| Дополнительная иммунизация при повышенном риске заражения у женщин репродуктивного возраста | dT | dT | dT | dT | dT | |
| В течение 1 курса. | Не менее чем через 4 недели после первого курса, в течение 2 курса. | Не менее чем через 6 месяцев после второго курса, в течение третьего курса. | Не менее чем через год, во время второй беременности. | Не менее чем через год, во время второй беременности. | ||
Российские рекомендации
В России вакцинация против столбняка входит в национальный календарь профилактических прививок, который регламентирован Приказом Министерства здравоохранения РФ от 21 марта 2014 г. N 125н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям». В нем установлены следующие сроки иммунизации:
Дополнительную информацию содержат Методические указания МУ 3.1.2436-09 «Эпидемиологический надзор за столбняком», которые определяют не только возраст вакцинации, но и интервал между введениями и объем вводимой дозы (табл. 4, 5).
| Возраст ребенка на момент начала вакцинации | 3 месяца — 4 года, не имеют противопоказаний | 3 месяца — 7 лет, если есть противопоказания к введению АКДС, либо ребенок переболел коклюшем* | 7 лет и старше, если ребенок ранее не был привит против столбняка и дифтерии |
| Вакцинации | |||
| Первая прививка | АКДС (0,5 мл) | АДС (0,5 мл) | АДС-М (0,5 мл) |
| Промежуток между первой и второй вакцинациями | 1,5 месяца | ||
| Вторая прививка | АКДС (0,5 мл) | АДС (0,5 мл) | АДС-М (0,5 мл) |
| Интервал между второй и третьей вакцинациями | 1,5 месяца | — | — |
| Третья прививка | АКДС (0,5 мл) | Не проводят | Не проводят |
| Интервал между последней вакцинацией и первой ревакцинацией | 12 месяцев | 9–12 месяцев | 6–9 месяцев |
| Ревакцинации | |||
| Первая ревакцинация | АКДС (0,5 мл) | АДС (0,5 мл) | АДС (0,5 мл) |
| Вторая ревакцинация | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) |
| Третья ревакцинация | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) |
| Последующие ревакцинации через каждые 10 лет | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) | АДС-М (0, 5 мл) |
| * — Сейчас в развитых странах перенесенный коклюш не является противопоказанием для вакцинации. Даже если ребенок переболел, его все равно прививают по календарю, потому что иммунитет после болезни нестойкий и ненадежный [30]. | |||
| Сведения о предшествовавших вакцинациях | Не были привиты против столбняка | Не были привиты против дифтерии и столбняка | |
| Препараты | АС | АС | АДС-М |
| Вакцинация | |||
| Схема | Обычная | Сокращенная | Обычная |
| Первая прививка | 0,5 мл | 1 мл | 0,5 мл |
| Промежуток между первой и второй вакцинациями | 1 месяц | — | 30–40 дней |
| Вторая прививка | 0,5 мл | — | 0,5 мл |
| Промежуток между последней вакцинацией и первой ревакцинацией | 6–24 месяцев | 6–24 месяцев | 9–12 месяцев |
| Ревакцинация | |||
| Первая ревакцинация | 0,5 мл | 0,5 мл | 0,5 мл |
| Последующие ревакцинации через каждые 10 лет | 0,5 мл | 0,5 мл (АС или АДС-М) | 0,5 мл |
Экстренная профилактика столбняка
Если есть подозрение, что человек уже мог заразиться столбняком, проводят экстренную профилактику. Для нее применяют четыре препарата:
Высокий риск заражения возникает, когда человек получил травму кожи или слизистой оболочки (в том числе ожог, обморожение, лучевое повреждение), при проникающих ранениях желудка и кишечника, при их прободении (когда в стенке органа образуется отверстие), после абортов и родов, произошедших вне стен медицинского учреждения, укусов животных, при гангрене, длительно текущих гнойных процессах.
Врач определяет, нужна ли человеку профилактика столбняка, и какие препараты вводить, в зависимости от того, как он прививался ранее. Данные представлены в таблице 6.
Если человека покусало животное, важно провести иммунизацию не только против столбняка, но и против бешенства [33].
Возможные осложнения противостолбнячных вакцин
Противостолбнячная вакцина довольно безопасна. Согласно позиции ВОЗ, ее можно вводить женщинам во время беременности, людям, имеющим иммунодефицит (в том числе вызванный ВИЧ-инфекцией) [29]. Возможные реакции и осложнения после введения вакцины представлены в таблице 7.
Насколько эффективна прививка?
Установлено, что у многих людей концентрации антител, которые способны защитить от столбняка, достигаются после второй вакцинации. После введения третьей вакцины иммунитет вырабатывается практически у всех привитых. В большинстве исследований была обнаружена эффективность прививки от 80 до 100%. Люди с иммунодефицитом (ВИЧ-инфекция, СПИД) слабее реагируют на введение анатоксина, но в целом у них тоже вырабатывается защитный иммунитет.
Защита после прививки может сохраняться разное время, в зависимости от того, в каком возрасте человек был вакцинирован, сколько доз ему было введено, какие между ними были промежутки времени. Три первые дозы вакцины, введенные в детстве, обеспечивают защиту на 3–5 лет. Потом еще одна ревакцинация в детстве защищает до юношеского возраста. Затем еще две дозы вакцины помогают защититься от столбняка предположительно на 20–30 лет (всего получается 6 доз, в соответствии с рекомендациями ВОЗ; в соответствии с Российским прививочным календарем вводят минимум 7 доз) [29].
Можно ли ликвидировать столбняк?
В медицине существует такое понятие, как коллективный иммунитет: когда большой процент населения вакцинирован, возбудителю становится намного сложнее распространяться. Таким образом, невакцинированные люди тоже в какой-то степени находятся под защитой. Привитые создают своего рода подушку безопасности для маленьких детей, больных с иммунодефицитными состояниями и других людей, у кого повышен риск заражения [36]. Особенность столбняка в том, что он не передается от человека к человеку. Заражение происходит только из окружающей среды. Поэтому и коллективный иммунитет не формируется: даже если вокруг вас все привиты, ваши риски от этого не снижаются. Поэтому вакцинироваться должен каждый [18].
Заключение
Прививка столбнячным анатоксином — единственный надежный способ защититься от заболевания. Эффективные вакцины существуют, и задача, с которой предстоит справиться врачам и специалистам в области здравоохранения — обеспечить максимальный охват населения планеты вакцинацией. Мешают два фактора: низкая доступность препаратов в некоторых развивающихся странах и то и дело громко заявляющие о себе антипрививочные движения.
В настоящее время эксперты Всемирной организации здравоохранения (ВОЗ) заявляют в отношении столбняка две основные цели: