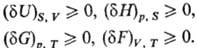Термодинамическое равновесие
Термодинамическое равновесие — состояние системы, при котором остаются неизменными по времени макроскопические величины этой системы (температура, давление, объём, энтропия) в условиях изолированности от окружающей среды. В общем, эти величины не являются постоянными, они лишь флуктуируют (колеблются) возле своих средних значений. Если равновесной системе соответствует несколько состояний, в каждом из которых система может находиться неопределенно долго, то о системе говорят, что она находится в метастабильном равновесии. В состоянии равновесия в системе отсутствуют потоки материи или энергии, неравновесные потенциалы (или движущие силы), изменения количества присутствующих фаз. Отличают тепловое, механическое, радиационное (лучистое) и химическое равновесия. На практике условие изолированности означает, что процессы установления равновесия протекают гораздо быстрее, чем происходят изменения на границах системы (то есть изменения внешних по отношению к системе условий), и осуществляется обмен системы с окружением веществом и энергией. Иными словами, термодинамическое равновесие достигается, если скорость релаксационных процессов достаточно велика (как правило, это характерно для высокотемпературных процессов) либо велико время для достижения равновесия (этот случай имеет место в геологических процессах).
В реальных процессах часто реализуется неполное равновесие, однако степень этой неполноты может быть существенной и несущественной. При этом возможны три варианта:
В неравновесных системах происходят изменения потоков материи или энергии, или, например, фаз.
Устойчивость термодинамического равновесия
Состояние термодинамического равновесия называется устойчивым, если в этом состоянии не происходит изменения макроскопических параметров системы.
Критерии термодинамической устойчивости различных систем:
Термодинамика
Лекция 1. Предмет технической термодинамики и ее методы
1. Предмет термодинамики
2. Основные параметры состояния тела
3. Понятие о термодинамическом процессе
4. Гомогенные и гетерогенные термодинамические системы
5. Термодинамическое равновесие
1. Предмет термодинамики
Термодинамика наука о превращениях различных видов энергии из одного в другой, и о наиболее общих макроскопических свойствах материи. Она изучает различные как физические, так и химические явления, обусловленные превращениями энергии. Применение закономерностей термодинамики позволяет анализировать свойства веществ, предсказывать их поведение в различных условиях. Термодинамика дает возможность исследовать различные процессы от простых в однородных средах до сложных с физическими и химическими превращениями, биологических и др.
Слово «термодинамика» происходит от греч. «therme» – тепло и «dynamis» – сила. Название науки возникло в период ее основания – в начале XIX в. В настоящее время слово «термодинамика» трактуют так: наука «о силах, связанных с теплотой».
Термодинамика основана на двух, экспериментально установленных законах (началах).
Первый закон (начало) является по существу законом преобразования и сохранения энергии применительно к процессам, изучаемым в термодинамике; невозможен процесс возникновения или исчезновения энергии.
Второй закон (начало) – определяет направление течения реальных (неравновесных) процессов; невозможен процесс, имеющий единственным своим результатом превращение теплоты в работу.
Термодинамический метод исследования основан на законах (началах) термодинамики и представляет собой их логическое и математическое развитие.
Объект исследования в термодинамике называют термодинамической системой или, в простом случае, термодинамическим телом. Одна из особенностей метода термодинамики состоит в том, что система (тело) противопоставляется всем другим телам, которые называют окружающей средой. Термодинамика построена дедуктивно: частные выводы получены из общих законов (начал).
Принято разделять термодинамику на физическую, или общую, химическую и техническую.
Физическая термодинамика разрабатывает метод термодинамики и применяет его для изучения фазовых превращений термоэлектрических и магнитных явлений, излучения, поверхностных явлений и т. п.
Химическая термодинамика изучает процессы с физическими и химическими превращениями с помощью метода термодинамики.
Техническая термодинамика устанавливает закономерности взаимного преобразования теплоты и работы, для чего изучает свойства газов и паров (рабочих тел) и процессы изменения их состояния; устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, протекающими в тепловых двигателях и холодильных установках. Одна из основных ее задач – отыскание наиболее рациональных способов взаимного превращения теплоты, и работы.
термодинамическое равновесие
ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ
состояние термодинамич. системы, не изменяющееся во времени и не сопровождающееся переносом через систему вещества или энергии. Если состояние системы не изменяется во времени, но есть поток вещества или энергии через систему, состояние системы наз. стационарным. Изолированная система, не обменивающаяся со средой веществом и энергией, со временем всегда приходит к Т. р. и не может самопроизвольно из него выйти. Постепенный переход системы из неравновесного состояния, вызванного внеш. воздействием, в состояние Т. р. наз. релаксацией.
Т. р. включает: термич. равновесие — постоянство температуры в объеме системы, отсутствие градиентов температуры; мех. равновесие, при котором невозможны никакие макроскопич. перемещения частей системы, т. е. имеется равенство давления в объеме системы; допустимы, однако, движения системы как целого-поступат. движение в поле действия внеш. сил и вращение. В случае гетерог. системы сосуществование термодинамически равновесных фаз наз. фазовым равновесием. Если между компонентами системы происходят хим. реакции, в состоянии Т. р. скорости прямых и обратных процессов равны между собой ( см. химическое равновесие). При Т. р. в системе прекращаются все необратимые переноса процессы (теплопроводность, диффузия, вязкое течение и т. п.). В системе не наблюдается изменение концентраций реагирующих веществ, для закрытой системы характерно равновесное распределение компонентов между составляющими систему фазами. Параметры состояния, определяющие Т. р., строго говоря, не являются постоянными, а флуктуируют около некоторых статистич. средних значений; обычно эти флуктуации пренебрежимо малы.
Буква d означает бесконечно малую вариацию величины, в т. ч. флуктуацию, в отличие от знака дифференциала, означающего действительно малое изменение величины в реальном процессе. Знак равенства имеет место при протекании в системе обратимых процессов, знак неравенства-необратимых (в случае изолир. системы). Принцип равновесия можно выразить также через термодинамические потен-циалы-внутр. энергию U, энтальпию H, энергию Гиббса G, энергию Гельмгольца F — при условиях, характеризуемых постоянством соответствующих параметров состояния. Т. р. отвечает условный минимум термодинамич. потенциалов:
Переход системы из одного состояния Т. р. в другое может происходить через последовательность состояний, каждое из которых является также состоянием Т. р. Это означает, что параметры состояния в течение всего процесса перехода бесконечно мало отличаются от своих значений при Т.р. Это-равновесный (квазистатический) процесс. Реальные процессы перехода всегда неравновесны; они изучаются химической термодинамикой.
Наряду с основным (глобальным) максимумом энтропии и минимумами термодинамич. потенциалов, отвечающими стабильному Т.р., в пространстве параметров состояния возможны локальные максимумы энтропии и минимумы термодинамич. потенциалов. Соответствующие им состояния системы наз. метастабильными равновесиями. Такие состояния, как и состояние стабильного Т. р., локально устойчивы, т. е. устойчивы к бесконечно малым изменениям параметров состояния. Но метастабильные состояния Т.р. могут быть неустойчивыми при некоторых конечных изменениях параметров.
Под локальным Т.р. в термодинамике неравновесных процессов подразумевается равновесие в очень малых (элементарных) объемах среды, содержащих все же достаточное число частиц (атомов, молекул, ионов), чтобы состояние этих объемов можно было характеризовать температурой, давлением, хим. потенциалом и др. термодинамич. потенциалами, но не постоянными, а зависящими от координат и времени. При локальном Т. р. элементарных объемов состояние системы в целом неравновесное.
ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ
ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ, состояние термодинамич. системы, не изменяющееся во времени и не сопровождающееся переносом через систему в-ва или энергии. Если состояние системы не изменяется во времени, но есть поток в-ва или энергии через систему, состояние системы наз. стационарным. Изолированная система, не обменивающаяся со средой в-вом и энергией, со временем всегда приходит к термодинамическому равновесию и не может самопроизвольно из него выйти. Постепенный переход системы из неравновесного состояния, вызванного внеш. воздействием, в состояние термодинамического равновесия наз. релаксацией.
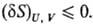
Буква d означает бесконечно малую вариацию величины, в т.ч. флуктуацию, в отличие от знака дифференциала, означающего действительно малое изменение величины в реальном процессе. Знак равенства имеет место при протекании в системе обратимых процессов, знак неравенства-необратимых (в случае изолир. системы). Принцип равновесия можно выразить также через термодинамические потен-циалы-внутр. энергию U, энтальпию H, энергию Гиббса G, энергию Гельмгольца F-при условиях, характеризуемых постоянством соответствующих параметров состояния. Термодинамическому равновесию отвечает условный минимум термодинамич. потенциалов:
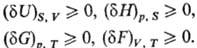
Переход системы из одного состояния термодинамического равновесия в другое может происходить через последовательность состояний, каждое из к-рых является также состоянием термодинамического равновесия. Это означает, что параметры состояния в течение всего процесса перехода бесконечно мало отличаются от своих значений при термодинамическом равновесии. Это-равновесный (квазистатический) процесс. Реальные процессы перехода всегда неравновесны; они изучаются химической термодинамикой.
Наряду с основным (глобальным) максимумом энтропии и минимумами термодинамич. потенциалов, отвечающими стабильному термодинамическому равновесию, в пространстве параметров состояния возможны локальные максимумы энтропии и минимумы термодинамич. потенциалов. Соответствующие им состояния системы наз. метастабильными равновесиями. Такие состояния, как и состояние стабильного термодинамического равновесия, локально устойчивы, т.е. устойчивы к бесконечно малым изменениям параметров состояния. Но метастабильные состояния термодинамического равновесия могут быть неустойчивыми при нек-рых конечных изменениях параметров.
Под локальным термодинамическим равновесием в термодинамике неравновесных процессов подразумевается равновесие в очень малых (элементарных) объемах среды, содержащих все же достаточное число частиц (атомов, молекул, ионов), чтобы состояние этих объемов можно было характеризовать т-рой, давлением, хим. потенциалом и др. термодинамич. потенциалами, но не постоянными, а зависящими от координат и времени. При локальном термодинамическом равновесии элементарных объемов состояние системы в целом неравновесное.
Термодинамическое равновесие
Термодинамическое равновесие — состояние изолированной термодинамической системы, при котором в каждой точке для всех химических, диффузионных, ядерных, и других процессов скорость прямой реакции равна скорости обратной.
Термодинамическое равновесие можно делить на термическое, механическое и химическое равновесие, выделяя различные типы физических процессов, на которых достигнуто состояние равновесия.
Согласно нулевому началу термодинамики к термодинамическому равновесию стремится термодинамическая система, изолированная от внешних воздействий.
На практике условие изолированности означает, что процессы внутри системы протекают гораздо быстрее, чем обменные процессы с внешней средой.
В реальных процессах часто реализуется неполное равновесие, однако степень этой неполноты может быть существенной и несущественной. При этом возможны три варианта:
Содержание
Устойчивость термодинамического равновесия
Из нулевого начала термодинамики следует устойчивость состояния термодинамического равновесия. В этом состоянии не меняются интегральные параметры системы (макропараметры) — температура, давление, плотность. Собственно, эти и другие макропараметры строго определяются только для систем, которые находятся в состоянии термодинамического равновесия.
В состоянии термодинамического равновесия не меняются также и различные вероятностные величины, например, функции распределения по энергиям и скоростям для всех составляющих системы (молекул, атомов, электронов, ионов). Для идеального газа, распределение частиц по энергиям в равновесном состоянии описывается функцией распределения Максвелла.
Достижимость термодинамического равновесия
В природе не существуют полного термодинамического равновесия. Всякая система в реальном мире изолирована лишь отчасти, и в каждой системе химические, ядерные процессы или процессы передачи энергии уравновешены лишь с определённой точностью. Невозможно достичь постоянства граничных условий вокруг какой-либо замкнутой области, также как невозможно бесконечно долго ждать момента наступления полного термодинамического равновесия в этой замкнутой области.
Но при этом в жизни есть множество примеров систем, достаточно близких к термодинамическому равновесию, чтобы получать полезные выводы из расчетов, проведённых в предположении термодинамического равновесия.
Примеры
Для герметического сосуда произвольной формы (это может быть закрытая стеклянная бутылка или, камера от велосипеда), наполненного любым газом или жидкостью и помещённым в другой сосуд, наполненный газом или жидкостью с постоянной температурой условия теплового равновесия выполняются.