Структурная функция белков
Структурная функция белков заключается в том, что белки
Содержание
Белки межклеточного вещества
В теле человека белков межклеточного вещества больше, чем всех остальных белков. Основными структурными белками межклеточного вещества являются фибриллярные белки.
Коллагены
Коллагены — семейство белков, в теле человека составляют до 25 — 30 % общей массы всех белков. Кроме структурной функции коллаген выполняет также механическую, защитную, питательную и репаративную функции.
Молекула коллагена представляет собой правозакрученную спираль из трёх α-цепей.
Всего у человека имеется 28 типов коллагена. Все они сходны по структуре.
Эластин
Эластин широко распространён в соединительной ткани, особенно в коже, легких и кровеносных сосудах. Общими характеристиками для эластина и коллагена являются большое содержание глицина и пролина. В эластине значительно больше валина и аланина и меньше глутаминовой кислоты и аргинина, чем в коллагене. В эластине содержатся десмозин и изодесмозин. эти соединения можно обнаружить только в эластине. Эластин нерастворим в водных растворах (как и коллаген), в растворах солей, кислот и щелочей даже при нагревании. В эластине большое количество аминокислотных остатков с неполярными боковыми группами, что, по-видимому, обусловливает высокую эластичность его волокон.
Другие белки внеклеточного матрикса
Другие белки внеклеточного матрикса — ламинины, фибронектин и др. — выполняют как структурную, так и сигнальную функцию. Взаимодействуя с мембранными рецепторами, они воздействуют на миграции клеток и другие стороны их поведения.
Белки цитоскелета
Кератин
Один из основных структурных белков — кератин. В основном из кератина состоят мертвые клетки ороговевающего эпителия и их производные (волосы млекопитющих, рога, копыта, когти, перья птиц, чешуя рептилий и др.). В живых клетках эпителиальных тканей кератины образуют промежуточные филаменты.
Кератины разделяются на две группы: α-кератины и β-кератины. Прочность кератина уступает, пожалуй, только хитину. Характерной особенностью кератинов является их полная нерастворимость в воде при pH 7,0. Содержат в молекуле остатки всех аминокислот. Отличаются от других фибриллярных структурных белков (например, коллагена) в первую очередь повышенным содержанием остатков цистеина. Первичная структура полипептидных цепей a-кератинов не имеет периодичности.
Другие белки промежуточных филаментов
Тубулин
Тубулин относится к филаментозным белкам. Димеры тубулина после полимеризации превращаются в нити (протофиламенты). Из них собираются микротрубочки, образующие цитоскелет, который помогает клетке поддерживать форму, обеспечивает связь между органеллами и выполняет ряд других функций.
Актин
Актин — тоже филаментозный белок. Из его мономеров при полимеризации образуются тонкие филаменты мышц и микрофиламенты немышечных клеток.
Миозин
Хотя миозин обычно относят к моторным белкам, в мышечных клетках он входит в состав постоянных структур. В скелетных и сердечной мышцах миозин входит в состав саркомеров, образуя толстые филаменты.
Вспомогательные белки цитоскелета
К структурным относятся и многие вспомогательные белки, входящие в состав цитоскелета. Так, в образовании саркомеров участвуют белки титин, тропомиозин и др.
Структурные белки органелл
Белки создают и определяют форму (структуру) многих клеточных органелл. В основном из белков состоят такие органеллы, как рибосомы, протеасомы, ядерные поры и др. Гистоны необходимы для сборки и упаковки нитей ДНК в хромосомы. Из белков состоят клеточные стенки некоторых протистов (например,хламидомонады); в составе оболочки клеток многих бактерий и архей присутствует белковый слой (S-слой), который крепится у грамположительных видов к клеточной стенке, а у грамотрицательных — к наружной мембране. Из белка флагеллина состоят прокариотические жгутики.
Полезное
Смотреть что такое «Структурная функция белков» в других словарях:
Третичная структура белков — Разные способы изображения трёхмерной структуры белка на примере фермента триозофосфатизомеразы. Слева «палочковая» модель, с изображением всех атомов и связей между ними; цветами показаны элементы. В середине изображены структурные мотивы … Википедия
НЕЙТРОНОГРАФИЯ СТРУКТУРНАЯ — исследования атомной структуры конденсир. сред методом дифракции нейтронов низких энергий на атомных ядрах (упругого когерентного рассеяния). В H. с. используются нейтроны с длиной волны де Бройля l >= 0,3 Рассеяние нейтронной волны на… … Физическая энциклопедия
Белки — У этого термина существуют и другие значения, см. Белки (значения). Белки (протеины, полипептиды[1]) высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа аминокислот. В живых организмах… … Википедия
Биополимеры — высокомолекулярные природные соединения, являющиеся структурной, основой всех живых организмов и играющие определяющую роль в процессах жизнедеятельности. К Б. относятся белки, нуклеиновые кислоты и полисахариды; известны также смешанные… … Большая советская энциклопедия
Протеин — Кристаллы различных белков, выращенные на космической станции «Мир» и во время полётов шаттлов НАСА. Высокоочищенные белки при низкой температуре образуют кристаллы, которые используют для получения модели данного белка. Белки (протеины,… … Википедия
Протеины — Кристаллы различных белков, выращенные на космической станции «Мир» и во время полётов шаттлов НАСА. Высокоочищенные белки при низкой температуре образуют кристаллы, которые используют для получения модели данного белка. Белки (протеины,… … Википедия
Факторы транскрипции — (транскрипционные факторы) белки, контролирующие процесс синтеза мРНК на матрице ДНК (транскрипцию) путём связывания со специфичными участками ДНК[1][2]. Транскрипционные факторы выполняют свою функцию либо самостоятельно, либо в комплексе… … Википедия
Фактор транскрипции — Факторы транскрипции (транскрипционные факторы) белки, контролирующие перенос информации с молекулы ДНК в структуру мРНК (транскрипцию) путем связывания со специфичными участками ДНК.[1][2] Транскрипционные факторы выполняют свою функцию… … Википедия
ЖИЗНЬ — особое качественное состояние мира, возможно, необходимая ступень в развитии Вселенной. Естественно научный подход к сущности Ж. сосредоточен на проблеме ее происхождения, ее материальных носителей, на отличии живого от неживого, на эволюции… … Философская энциклопедия
Химическая связь — взаимное притяжение атомов, приводящее к образованию молекул и кристаллов. Принято говорить, что в молекуле или в кристалле между соседними атомами существуют Х. с. Валентность атома (о чём подробнее сказано ниже) показывает число связей … Большая советская энциклопедия
Основные функции белков в клетке
Благодаря сложности, разнообразию форм и состава, белки играют важную роль в жизнедеятельности клетки и организма в целом.
Белок — это отдельный полипептид или агрегат нескольких полипептидов, выполняющий биологическую функцию.
Полипептид — понятие химическое. Белок — понятие биологическое.
В биологии функции белков можно разделить на следующие виды:
1. Строительная функция
Белки участвуют в образовании клеточных и внеклеточных структур. Например:
2. Транспортная функция
Некоторые белки способны присоединять различные вещества и переносить их к различным тканям и органам тела, из одного места клетки в другое. Например:
Белки транспортируют в крови катионы кальция, магния, железа, меди и другие ионы.
3. Регуляторная функция
Большая группа белков организма принимает участие в регуляции процессов обмена веществ. Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например:
4. Защитная функция
5. Двигательная функция
6. Сигнальная функция
7. Запасающая функция
8. Энергетическая функция
9. Каталитическая (ферментативная) функция
Ферменты, или энзимы, — особый класс белков, являющихся биологическими катализаторами. Благодаря ферментам биохимические реакции протекают с огромной скоростью. Вещество, на которое оказывает свое действие фермент, называют субстратом.
Ферменты можно разделить на две группы:
10. Функция антифириза
11. Питательная (резервная) функция.
Решай задания и варианты по биологии с ответами
Биология. 11 класс
§ 4-1. Функции белков
Белки выполняют разнообразные биологические функции — структурную, транспортную, регуляторную и многие другие. При этом одной из самых важных функций белков в живых организмах является каталитическая (ферментативная).
Ферменты. Из курса химии вы знаете, что вещества, повышающие скорость химических реакций, называются катализаторами. Ферменты *(энзимы)* — это белки, которые выполняют функции биологических катализаторов, т. е. ускоряют протекание химических реакций в живых организмах. Без их участия биохимические процессы происходили бы слишком медленно или не происходили бы вообще. Ферменты осуществляют расщепление и синтез различных соединений, обеспечивая протекание обмена веществ. Практически все процессы жизнедеятельности обусловлены ферментативными реакциями.

Присоединение субстрата вызывает небольшие изменения конфигурации активного центра — такие, чтобы максимально соответствовать субстрату. Функционально активные группы фермента, за счет которых будет протекать реакция, наиболее благоприятным образом располагаются в пространстве. Образно говоря, активный центр подстраивается под субстрат как перчатка, которую надевают на руку.
В результате присоединения к активному центру молекула субстрата особым образом располагается в пространстве, и в ее структуре ослабляются определенные химические связи. Реакционная способность субстрата возрастает. Поэтому, по сравнению с некатализируемой реакцией, ферментативное превращение субстрата в продукт (или продукты) происходит с меньшими затратами энергии и гораздо большей скоростью. Образовавшиеся продукты отделяются от активного центра. После этого он может принимать новые молекулы субстрата.
Сходство ферментов с обычными химическими катализаторами проявляется в том, что и те и другие увеличивают скорость реакции, но при этом не расходуются и могут использоваться многократно.
В ходе некоторых окислительно-восстановительных процессов, протекающих в живых организмах, образуется токсичное для клеток соединение — пероксид водорода (Н2О2). Без участия катализаторов его расщепление идет очень медленно: 2H2O2 → 2H2O + O2. Вы знаете, что в лаборатории при проведении этой реакции обычно используют неорганический катализатор, например оксид марганца (MnO2). В его присутствии разложение Н2О2 происходит значительно быстрее. В живых организмах под действием фермента каталазы этот процесс протекает с удивительно высокой скоростью: одна молекула каталазы расщепляет за 1 с около 200 000 молекул H2O2!
Ферменты являются белками, поэтому активно работают лишь в определенном диапазоне рН, температуры и других факторов. Например, фермент желудочного сока пепсин активен только в кислой среде, а ферменты слюны амилаза и мальтаза — в слабощелочной. В диапазоне 0—40 °С повышение температуры приводит к ускорению ферментативных реакций. Но при дальнейшем увеличении температуры реакции, катализируемые большинством ферментов, замедляются, а затем вовсе прекращаются. Значительное повышение температуры, изменение кислотности среды и других факторов приводит к денатурации ферментов, в результате чего они теряют способность связываться со своими субстратами.
*Существуют ферменты, которые, кроме активного центра, имеют один или несколько регуляторных (аллостерических) центров. С активным или регуляторным центром, либо с другими участками молекулы фермента могут связываться определенные вещества, влияющие на его активность. Вещества, повышающие скорость ферментативной реакции, называются активаторами, снижающие или блокирующие активность фермента — ингибиторами.
Ингибиторы, которые связываются с регуляторным (аллостерическим) центром, вызывают изменения пространственной конфигурации (конформации) фермента, приводящие к уменьшению его активности. Такой тип ингибирования называется аллостерическим (рис. 4-1.2, а).
Некоторые соединения, по структуре сходные с субстратом, могут связываться с активным центром фермента, но не способны подвергаться ферментативному превращению. Такие вещества препятствуют доступу субстрата в активный центр, тем самым снижая скорость ферментативной реакции. Поскольку молекулы субстрата и ингибитора конкурируют за активный центр, данный тип ингибирования назван конкурентным (рис. 4-1.2, б).
Известно также неконкурентное ингибирование, при котором ингибиторы присоединяются к молекуле фермента вне активного и регуляторного центров. Неконкурентные ингибиторы не мешают связыванию ферментов с субстратами, но вызывают такие изменения структуры, которые не позволяют ферменту превращать субстрат в продукт (рис. 4-1.2, в). Примером могут служить цианид-ионы (CN – ). Они подавляют активность ряда ферментов за счет связывания с ионами металлов, выполняющими роль кофакторов.*
*Ферменты широко используются в пищевой промышленности (при производстве сыров и других кисломолочных продуктов, соков, чая, овощных и фруктовых пюре, в хлебопечении, пивоварении, виноделии, для обработки мяса и т. п.). Их также применяют в сельском хозяйстве для получения кормов, в медицине для диагностики и лечения заболеваний, в текстильной и кожевенной промышленности для обработки тканей, кожи и меха, в производстве синтетических моющих средств и др.*
Кроме каталитической, белки выполняют и другие важные функции (таблица 4-1.1 ).
Функция
Пояснение и примеры
Являются биологическими катализаторами — повышают скорость протекания биохимических реакций, обеспечивая расщепление, синтез и внутримолекулярную перестройку различных соединений. Например, пищеварительные ферменты липазы ускоряют расщепление липидов, амилаза и мальтаза — углеводов, пепсин и трипсин — белков. *Рибулозодифосфат-карбоксилаза обеспечивает связывание углекислого газа в процессе фотосинтеза. Удвоение молекул ДНК происходит под действием фермента ДНК-полимеразы, образование РНК — под действием РНК-полимеразы*
Входят в состав всех компонентов клеток и различных внеклеточных структур. Например, кератин — основной компонент волос, ногтей, когтей, копыт, рогов, перьев. Эластин входит в состав стенок артерий, связок и др., коллаген — в состав кожи, сухожилий, костной, хрящевой и других тканей. *Склеротин является компонентом наружного скелета насекомых и паукообразных. Фиброин составляет основу коконов насекомых*
Переносят различные вещества от одних клеток и тканей к другим, обеспечивают их поступление в клетки, выведение из клеток, а также процессы внутриклеточного транспорта. Например, дыхательный пигмент гемоглобин переносит кислород и углекислый газ в крови позвоночных животных, а у многих моллюсков и ряда членистоногих эту функцию выполняет гемоцианин. *Глобулины плазмы крови транспортируют гормоны и ионы металлов (например, трансферрин — ионы железа, церулоплазмин — ионы меди), альбумины переносят высшие карбоновые кислоты и некоторые другие вещества*
Принимают участие во всех видах движения, к которым способны клетки и организмы. Например, белки актин и миозин обеспечивают сократимость гладкой и поперечнополосатой мышечных тканей. *В основе движения жгутиков и ресничек эукариотических клеток лежит скольжение друг относительно друга микротрубочек, входящих в их состав. Оно обеспечивается взаимодействием белков тубулина и динеина*
Регулируют протекание различных физиологических процессов. Например, гормоны инсулин и глюкагон регулируют уровень глюкозы в крови. Процессы роста и физического развития человека протекают под контролем гормона соматотропина. *Другие тропные гормоны, секретируемые передней и средней долями гипофиза, также представляют собой полипептиды. Например, тиреотропин, стимулирующий деятельность щитовидной железы, гонадотропины, регулирующие работу половых желез, пролактин, контролирующий развитие и функционирование молочных желез и т. п. Гормон щитовидной железы кальцитонин и паратгормон, вырабатываемый паращитовидными железами, регулируют содержание ионов Са 2+ в организме*
Некоторые мембранные белки в ответ на действие определенных химических веществ или раздражителей иной природы изменяют свою конфигурацию. Это приводит к изменению протекания тех или иных внутриклеточных процессов. Таким образом, рецепторные белки обеспечивают прием внешних сигналов и ответные реакции клеток на эти сигналы. Например, зрительные пигменты глаза — родопсин (содержится в палочках) и йодопсины (в колбочках) — обеспечивают восприятие света фоторецепторными клетками, их возбуждение и запуск нервного импульса. *Другими примерами могут служить мембранные рецепторы, которые связывают молекулы гормонов, нейромедиаторов и др. Светочувствительный белок фитохром обеспечивает реакцию растений на изменение длины светового дня (фотопериодизм). Он играет важную роль в регуляции цветения, прорастания семян, формирования листьев и т. д.*
Токсины, выделяемые многими бактериями (дифтерийный, ботулиновый, столбнячный, холерный и др.) по химической природе являются белками. Действующие вещества в составе ядов змей, некоторых пауков, скорпионов и насекомых также представляют собой белки
Запасаются в качестве источника аминокислот, например, резервные белки, которые откладываются в семенах растений *(легумин, запасающийся в семенах бобовых и др.)*, или обеспечивают запасание других веществ. Так, миоглобин играет важную роль в создании кислородного запаса в мышечных волокнах. *Ферритин выполняет роль основного внутриклеточного депо железа у человека и животных*
После гидролиза до аминокислот могут подвергаться дальнейшему расщеплению и окислению с высвобождением энергии. При полном окислении 1 г белка выделяется 17,6 кДж энергии. Однако белки используются в качестве источника энергии лишь в крайних случаях, когда истощаются запасы углеводов и жиров
*Натуральный шелк, получаемый из коконов шелкопряда, на 75 % состоит из фиброина и на 25 % из серицина. Фиброин — нерастворимый белок, вторичная структура которого (β-складчатый слой) обусловливает прочность шелка. Волокна шелка образованы фиброиновыми нитями. Снаружи они покрыты клейким водорастворимым серицином, который при производстве тканей удаляется. Шелковая нить имеет треугольное сечение и, как призма, преломляет свет, что вызывает красивое переливание и блеск. Шелк использовался для изготовления тканей еще в 4-ом тысячелетии до н. э. Шелковое волокно применяют в качестве шовного материала в хирургии.*
У пауков основу паутины составляет белок спидроин. Секрет паутинных желез выводится наружу в жидком виде. После этого структура спидроина изменяется, и он затвердевает в виде тонких нитей. В их составе участки β-складчатого слоя чередуются с эластичными полипептидными связками. Благодаря этому паутина обладает одновременно высокой прочностью и эластичностью. Она разрывается лишь при растяжении в 5 раз. По прочности паутина сопоставима со сталью, но при этом ее плотность в 6 раз меньше, чем у стали. Если бы паук создал нить длиной в земной экватор, она имела бы массу менее 500 г.
Строение и функции белков
Белки (протеины) составляют 50% от сухой массы живых организмов.
Белки состоят из аминокислот. У каждой аминокислоты есть аминогруппа и кислотная (карбоксильная) группа, при взаимодействии которых получается пептидная связь, поэтому белки еще называют полипептидами.
Структуры белка
Первичная – цепочка из аминокислот, связанных пептидной связью (сильной, ковалентной). Чередуя 20 аминокислот в разном порядке, можно получать миллионы разных белков. Если поменять в цепочке хотя бы одну аминокислоту, строение и функции белка изменятся, поэтому первичная структура считается самой главной в белке.
Вторичная – спираль. Удерживается водородными связями (слабыми).
Третичная – глобула (шарик). Четыре типа связей: дисульфидная (серный мостик) сильная, остальные три (ионные, гидрофобные, водородные) – слабые. Форма глобулы у каждого белка своя, от нее зависят функции. При денатурации форма глобулы меняется, и это сказывается на работе белка.
Четвертичная – имеется не у всех белков. Состоит из нескольких глобул, соединенных между собой теми же связями, что и в третичной структуре. (Например, гемоглобин.)
Денатурация
Это изменение формы глобулы белка, вызванное внешними воздействиями (температура, кислотность, соленость, присоединение других веществ и т.п.)
Функции белков
Их очень много, например:
Еще можно почитать
Задания части 1
Выберите один, наиболее правильный вариант. Водородные связи между СО- и NН-группами в молекуле белка придают ей форму спирали, характерную для структуры
1) первичной
2) вторичной
3) третичной
4) четвертичной
Выберите один, наиболее правильный вариант. Четвертичная структура молекулы белка образуется в результате взаимодействия
1) участков одной белковой молекулы по типу связей S-S
2) нескольких полипептидных нитей, образующих клубок
3) участков одной белковой молекулы за счет водородных связей
4) белковой глобулы с мембраной клетки
Выберите один, наиболее правильный вариант. Последовательность и число аминокислот в полипептидной цепи – это
1) первичная структура ДНК
2) первичная структура белка
3) вторичная структура ДНК
4) вторичная структура белка
Выберите один, наиболее правильный вариант. Первичная структура белка образована связью
1) водородной
2) макроэргической
3) пептидной
4) ионной
Выберите один, наиболее правильный вариант. В основе образования пептидных связей между аминокислотами в молекуле белка лежит
1) принцип комплементарности
2) нерастворимость аминокислот в воде
3) растворимость аминокислот в воде
4) наличие в них карбоксильной и аминной групп
БЕЛКИ
1. Выберите три варианта. Белки в организме человека и животных
1) составляют бо́льшую часть организма по массе
2) начинают расщепляться в ротовой полости
3) не содержат фосфора в составе молекулы
4) могут откладываться в запас
5) в качестве ферментов ускоряют химические реакции
6) служат основным строительным материалом
2. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Выберите только особенности строения белковой молекулы.
1) содержит атомы фосфора
2) состоит из аминокислот
3) мономеры удерживаются пептидными связями
4) состоит из одинаковых по строению мономеров
5) изменяет форму под действием температуры
6) четвертичная структура состоит из нескольких молекул
3. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Какие из перечисленных ниже признаков относятся к характеристикам молекул белков?
1) состоят из нуклеотидов
2) выполняют только структурную и двигательную функции
3) могут иметь форму глобулы
4) содержат в составе азот и серу
5) всегда нерастворимы в воде
6) являются нерегулярными полимерами
Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Какие из перечисленных ниже веществ относятся к белкам?
1) крахмал
2) коллаген
3) фибриноген
4) тестостерон
5) гемоглобин
6) сахароза
БЕЛКИ КРОМЕ
1. Все перечисленные признаки, кроме двух, можно использовать при описании яичного белка альбумина. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) состоит из аминокислот
2) пищеварительный фермент
3) денатурирует обратимо при варке яйца вкрутую
4) мономеры связаны пептидными связями
5) молекула образует первичную, вторичную и третичную структуры
2. Все перечисленные ниже признаки, кроме двух, можно использовать для описания молекулы белка. Определите два признака, «выпадающих» из общего списка, и запишите цифры, под которыми они указаны.
1) состоит из нуклеотидов
2) может иметь форму глобулы
3) имеет третичную и четвертичную структуры
4) образуется в ядре
5) бывают глобулярные и фибриллярные
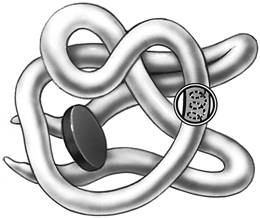
БЕЛКИ КРОМЕ РИС
1. Перечисленные ниже признаки, кроме двух, используются для описания строения, функций изображенного органического вещества. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) имеет структурные уровни организации молекулы
2) входит в состав клеточных стенок
3) является биополимером
4) служит матрицей при трансляции
5) состоит из аминокислот

2. Все перечисленные ниже признаки, кроме двух, используются для описания изображённой на рисунке структуры. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) вторичная структура молекулы белка
2) удерживается только пептидными связями
3) определяется методом рентгеноструктурного анализа
4) представляет собой глобулу
5) может выполнять ферментативные функции

3. Все перечисленные ниже характеристики, кроме двух, используют для описания изображенной на рисунке молекулы органического вещества клетки. Определите две характеристики, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) денатурация
2) репликация
3) транскрипция
4) аминокислоты
5) водородные связи
СТРУКТУРЫ БЕЛКА
Установите соответствие между характеристикой и структурой белка: 1) первичная, 2) третичная. Запишите цифры 1 и 2 в порядке, соответствующем буквам.
А) молекула в форме глобулы или фибриллы
Б) строгая последовательность аминокислотных остатков
В) аминокислотные остатки соединены только пептидными связями
Г) имеет дисульфидные мостики между радикалами аминокислот
Д) при ее разрушении наступает необратимая денатурация
Е) пространственная конфигурация полипептидной цепи
ФЕРМЕНТАТИВНАЯ
1. Все приведенные ниже признаки, кроме двух, можно использовать для описания ферментов. Определите два признака, «выпадающих» из общего списка, и запишите цифры, под которыми они указаны.
1) входят в состав клеточных мембран и органоидов клетки
2) играют роль биологических катализаторов
3) имеют активный центр
4) оказывают влияние на обмен веществ, регулируя различные процессы
5) специфические белки
2. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Ферменты – это вещества, которые
1) вырабатываются в железах внутренней секреции
2) являются белками
3) поступают в организм, как правило, вместе с пищей
4) являются в организме источником энергии
5) ускоряют протекание химических реакций
6) у человека выполняют свои функции при температуре около 36 градусов
ФУНКЦИИ БЕЛКОВ
Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Функциями белков в организме человека являются
1) строительная
2) передача наследственных признаков
3) защитная
4) запасающая
5) ферментативно-каталитическая
6) хранение генетической информации
ФУНКЦИИ БЕЛКОВ КРОМЕ
Все перечисленные характеристики используют для описания функций белков. Определите две характеристики, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) регуляторная
2) двигательная
3) рецепторная
4) образуют клеточные стенки
5) служат коферментами

Рассмотрите рисунок с изображением полипептида и укажите (А) уровень его организации, (Б) форму молекулы и (В) вид взаимодействия, поддерживающий эту структуру. Для каждой буквы выберите соответствующий термин или соответствующее понятие из предложенного списка.
1) первичная структура
2) вторичная структура
3) третичная структура
4) взаимодействия между нуклеотидами
5) металлическая связь
6) гидрофобные взаимодействия
7) фибриллярная
8) глобулярная

Рассмотрите схему химического вещества. Укажите (А) название класса органических веществ, (Б) уровень организации полимерной молекулы и (В) название мономеров, из которых состоит данная молекула. Для каждой буквы выберите соответствующий термин из предложенного списка.
1) ДНК
2) белок
3) альфа-спираль
4) вторичная структура
5) третичная структура
6) аминокислоты
7) нуклеотиды
8) рибоза

Рассмотрите рисунок с изображением полипептида. Укажите (А) уровень его организации, (Б) мономеры, которые его образуют, и (В) вид химических связей между ними. Для каждой буквы выберите соответствующий термин или соответствующее понятие из предложенного списка.
1) первичная структура
2) водородные связи
3) двойная спираль
4) вторичная структура
5) аминокислота
6) альфа-спираль
7) нуклеотид
8) пептидные связи

Проанализируйте таблицу «Уровни организации белка». Для каждой ячейки, обозначенной буквой, выберите соответствующий термин из предложенного списка.
1) глобула
2) двойная спираль
3) эфирные
4) гидрофильные
5) пептидные
6) нитчатая
7) вторичная
8) четвертичная
Известно, что белки – нерегулярные полимеры, имеющие высокую молекулярную массу, строго специфичны для каждого вида организма. Выберите из приведенного ниже текста три утверждения, по смыслу относящиеся к описанию этих признаков, и запишите цифры, под которыми они указаны. (1) В состав белков входит 20 различных аминокислот, соединенных пептидными связями. (2) Белки имеют различное количество аминокислот и порядок их чередования в молекуле. (3) Низкомолекулярные органические вещества имеют молекулярную массу от 100 до 1000. (4) Они являются промежуточными соединениями или структурными звеньями – мономерами. (5) Многие белки характеризуются молекулярной массой от нескольких тысяч до миллиона и выше, в зависимости от количества отдельных полипептидных цепей в составе единой молекулярной структуры белка. (6) Каждый вид живых организмов имеет особый, только ему присущий набор белков, отличающий его от других организмов.





