Особенности внутрикишечной опухолевой инвазии в проксимальном направлении при раке прямой кишки
И.А. Нечай, Г.И. Суханкина
Городская больница № 40
СПбГУ, медицинский факультет, кафедра хирургии
Аннотация. Представлены результаты гистологических исследований распространения «ракового поля» в проксимальном направлении при раке прямой кишки. Необходимость таких исследований обусловлена важностью сохранения дистальных отделов сигмовидной кишки, при выполнении передней резекции прямой кишки, с целью улучшения резервуарной и эвакуаторной функций. В результате определено минимальное расстояние от верхнего края опухоли, которое необходимо отступить при пересечении кишки, не нарушая онкологических принципов оперирования.
Клинические наблюдения о несомненной важности бережного отношения к дистальной части сигмовидной кишки при передних резекциях прямой кишки (ПК), побудили нас изучить распространенность ракового поля в проксимальном направлении от верхнего края раковой опухоли. Знания эти должны лечь в основу рекомендаций, насколько минимально допустимо отступать от верхнего края опухоли при резекции сигмовидной кишки, не нарушая онкологических принципов оперирования. Такая озабоченность связана с тем, что у больных, у которых при резекции ПК для анастомоза использовалась самая дистальная часть низводимой сигмовидной кишки, резервуарно-накопительная и эвакуаторная функции оказывались заметно лучше. Вместе с тем, заботясь об улучшении функциональных результатов операций, мы постоянно имели в виду важность соблюдения онкологических принципов оперирования, поскольку главным при лечении онкологических больных является, конечно, улучшение пятилетней выживаемости.
Распространение ракового процесса внутристеночно от края видимой опухоли ПК в дистальном направлении привлекало внимание ряда авторов. Такие исследования имеют чрезвычайно важное значение при оперативном лечении больных с низкой раковой опухолью ПК. При этой локализации злокачественной опухоли, с позиций функциональных результатов, важен каждый сантиметр сохраненной дистальной части кишки. Использование сшивающих аппаратов при резекции ПК позволяет в техническом плане проводить максимально низкие резекции кишки.
Распространенность инвазии в дистальном направлении при раке прямой кишки.
Распространенность раковой инвазии в дистальном направлении изучалась целенаправленными и тщательными морфологическими исследованиями. R.Willis приводит концепцию «опухолевого поля», в соответствии с которой новообразование развивается мультицентрически с формированием затем единого опухолевого узла. В.Ю.Клур с соавт. проводил серийные гистологические срезы не только в дистальном направлении, но и радиарно. Они установили, что контуры «опухолевого поля» имеют эксцентрическое распространение от основного узла с внутристеночной инвазией, которая в дистальном направлении составляет не менее 3,5-4,0 см при экзофитных опухолях, а при эндофитном росте увеличивается еще на 1,0-1,5 см. Г.И. Воробьев с соавт. исследовал 71 препарат прямой кишки, удаленный при брюшно-промежностной экстирпации. Они установили, что глубина опухолевой инвазии прогрессивно уменьшается в направлении от центра к периферии опухоли. Дистальный внутристеночный рост по подслизистому слою был зарегистрирован лишь в 2,2 % случаев и не превышал 15 мм. Глубина инвазии колоректального рака изучалась также с помощью компьютерного исследования, эндоректоэхографии. В результате была установлена незначительная по протяженности от опухолевого узла внутрикишечная инвазия опухолевого процесса в дистальном направлении. Практически это было претворено в жизнь, и на смену «правила 5 см» пришло «правило 2 см», т. е. достаточно отступить от нижнего края опухоли 2 см с тем, чтобы не нарушить основной онкологический принцип оперирования.
Распространенность опухолевой инвазии в проксимальном направлении в меньшей мере привлекала внимание специалистов. При пересечении кишки выше опухоли не возникает необходимости в строгой экономичности сохранения кишки, примыкающей к опухоли, так как всегда имеется достаточная часть остающегося участка левого фланга ободочной кишки. Вместе с тем наши специальные исследования с анализом длины сигмовидной кишки по дооперационным ирригограммам и размера резецированной части ее после передней резекции ПК показали несомненную важность максимально возможного сохранения для анастомоза дистальной части сигмовидной кишки. К подобному заключению нас подвело изучение функциональных результатов сфинктеросохраняющих резекций ПК. Все это побудило специально изучить распространенность ракового поля в проксимальном направлении от верхнего края видимой опухоли. Результаты таких исследований были нужны для определения минимального расстояния, которое необходимо отступать от верхнего края раковой опухоли при пересечении кишки для соблюдения онкологических принципов оперирования.
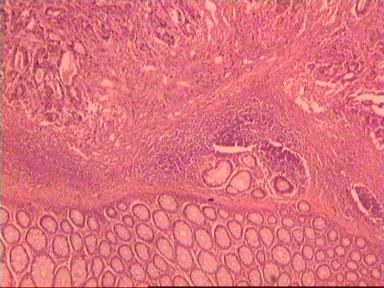
После фиксации препарата в проксимальном направлении от видимого верхнего края опухоли последовательно проводились пересечения кишечной стенки с интервалом 5мм (рис. 1).
Результаты исследования. Представляем наблюдение, характеризующее отсутствие опухолевой инвазии по кишечной стенке.
Мужчина 54 года, рак анального канала и ПК, выполнена брюшнопромежностная экстирпация ПК. Гистологическое исследование 31261−31272.
Макропрепарат: блюдцеобразно возвышающееся над поверхностью кишки новообразование диаметром 6 см, прорастает все стенки кишки. От края опухоли в проксимальном направлении макроскопически определяется инфильтрация стенки на протяжении 3,5 см.
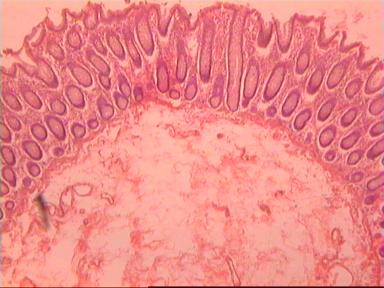
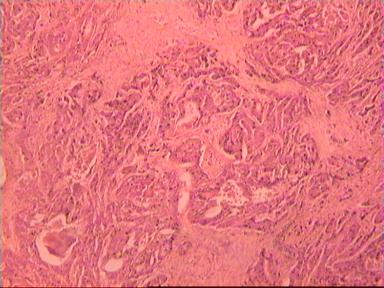
Микроскопическое исследование: высокодифференцированная слизеобразующая аденокарцинома ПК, прорастание всей толщи стенки кишки, врастание опухоли в жировую ткань. В опухоли очаги некроза, выраженная мононуклеарная реакция. От проксимального края видимой инвазии уже в 1 мм внутристеночного роста опухоли нет. (Рис. 2). Метастазов аденокарциномы в лимфатических узлах и жировой ткани не выявлено.
Рис. 2. Микропрепарат слизеобразующей аденокарциномы ПК
Такие данные были получены и при аденокарциноме, и при плоскоклеточном раке ПК. Приведем наблюдение, свидетельствующее о распространении опухолевого роста по кишке в проксимальном направлении. Мужчина 73 года, рак ПК, выполнена передняя резекция ПК. Гистологическое исследование № 869−870; 871−882. Макропрепарат: опухоль 5 см с кратером, циркулярно охватывающая просвет кишки, прорастание всех слоев кишки и прилежащей жировой ткани, участки абсцедирования.
Микроскопическое исследование: аденокарцинома разной степени дифференцировки. В 5 мм вне видимой опухоли − аденокарцинома в подслизистом, мышечных слоях, в клетчатке, с абсцедированием (рис 3). На срезах через 10 мм от видимого края новообразования опухолевого роста нет.
 | 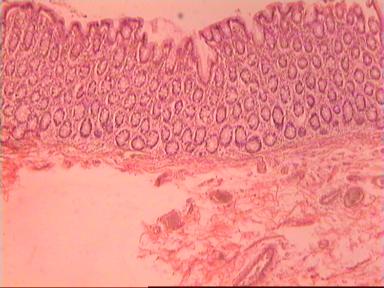 |
| А | Б |
Рис. 3. Микропрепарат аденокарциномы ПК разной степени дифференцировки
Приведем еще одно наблюдение, свидетельствующее о несомненном распространении опухолевого роста по кишке в проксимальном направлении. Женщина 73 года, рак ПК, выполнена резекция ПК по Гартману. Макропрепарат: экзофитная опухоль 5 х 5 см, прорастание всех слоев кишки, регионарные лимфоузлы не определяются.
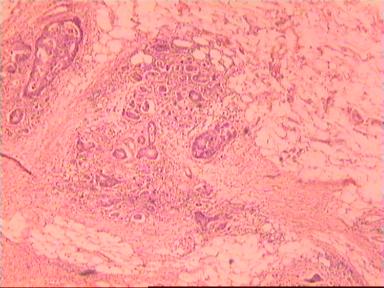 | 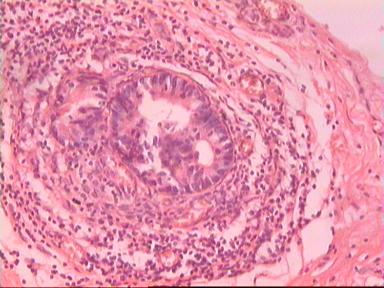 | 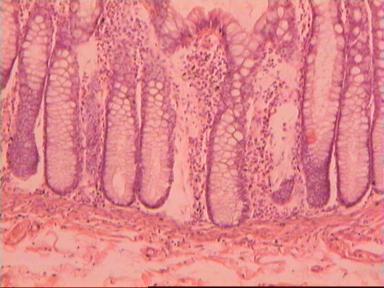 |
| А | Б | В |
Рис. 4. Микропрепарат аденокарциномы ПК разной степени дифференцировки
Рак прямой кишки. Инвазия опухоли. Обсуждение результатов исследования.
Данные исследования убедительно свидетельствуют, что раковая инвазия в проксимальном направлении от верхнего видимого края раковой опухоли ПК не имеет тенденции к значительному распространению, а в основном ограничена контурами макроскопического «ракового узла» или инвазией по кишечной стенке не более чем на 5мм от него. Лишь в 23,5 % случаев было установлено распространение ракового поля в проксимальном направлении, причем максимально зарегистрированная инвазия была в 20мм от видимого края опухоли ПК.
Вопреки ожиданиям не выявилось повышенной тенденции к внутристеночному росту при низкодифференцированной аденокарциноме, слизистых и плоскоклеточных формах рака ПК. Следовательно, отступление от верхнего края опухоли на 4−5 см в проксимальном направлении с онкологических позиций вполне оправдано и нет необходимости удалять здоровую и функционально полноценную часть кишки. Однако нужно учитывать, что уровень пересечения кишки выше опухоли во многом определяется высотой перевязки основного кровеносного сосуда, которым для этой зоны является нижняя брыжеечная артерия, особенностями кровоснабжения конкретного участка кишки и вовлеченностью в онкопроцесс лимфатического аппарата. Намечая линию пересечения сигмовидной или нисходящей части ободочной кишки, нужно учитывать эти обстоятельства и по возможности бережно, экономно относиться к удалению этого отдела толстой кишки, помня, что инвазия опухоли по стенке кишки незначительна.
Таким образом, внутрикишечная инвазия злокачественного роста в проксимальном направлении от видимого края опухоли ПК наблюдается в 23,5 % случаев и не превышает по протяженности 20 мм. В остальных случаях «раковое поле» ограничивается контурами основного видимого новообразования или распространяется не более чем на 5 мм от него.
Уровень пересечения кишки на 4−5 см выше проксимального края видимой раковой опухоли ПК онкологически оправдан, если учесть распространение «ракового поля» по кишечной стенке. Однако объем операции, конечно, зависит от особенностей кровоснабжения конкретного участка кишки, вовлеченностью в онкопроцесс лимфатических узлов и некоторых других факторов.
Экстрамуральная сосудистая инвазия как индикатор наличия метастазов рака нижнеампулярного отдела прямой кишки
Рак прямой кишки занимает одно из лидирующих мест в структуре смертности у представителей обоих полов, при этом единственным радикальным методом лечения остается хирургическое вмешательство. Для планирования оперативного лечения важной является оценка метастатического поражения локорегионарных лимфатических узлов и наличия экстрамуральной лимфососудистой инвазии, являющейся важным предиктором возникновения рецидива заболевания, а также ранним индикатором появления отдаленных метастазов. Эффективность и достоверность дооперационного стадирования рака нижнеампулярного отдела прямой кишки значительно возросла после внедрения в клиническую практику магнитно-резонансной томографии, а также комплексного предоперационного лучевого обследования пациентов. Статья посвящена проблемам дооперационного стадирования и определению статистически значимых взаимосвязей между наличием экстрамуральной сосудистой инвазии и морфологическим типом, стадией опухоли и наличием отдаленных метастазов при раке нижнеампулярного отдела прямой кишки.
Extramural vascular invasion as an indicator of the presence of distant metastases of low rectal cancer
Rectal cancer is one of the leading pathologies in the structure of mortality for both genders, and the surgical intervention is the only radical method of treatment. Assessment of metastatic lesion of locoregional lymph nodes and the presence of extramural lymphovascular invasion, which is an important predictor of disease recurrence, as well as an early indicator of the appearance of distant metastases, is important for planning surgical treatment. The effectiveness and reliability of preoperative staging of the low rectal cancer significantly increased after the introduction of magnetic resonance imaging in clinical practice, as well as a comprehensive preoperative radiological examination of patients. The article is devoted to the problems of preoperative staging and the determination of a statistically significant correlation between the presence of extramural vascular invasion and the morphological type, stage of the tumor and the presence of distant metastases in patients with low rectal cancer.
Рак прямой кишки (РПК) представляет собой одну из актуальных и сложных проблем современной онкоколопроктологии. Распространенность заболевания и смертность населения от этой патологии по-прежнему остаются высокими. Так, только в России в 2014 году зарегистрировано 26785 новых случаев рака прямой кишки, а смертность составила 9,2 %. В структуре онкологической заболеваемости рак прямой кишки занимает 6-е место (5,2 %) среди мужчин и 7-е место (4,7 %) среди женщин [1]. В ряду колоректальных раков особое место занимают раки прямой кишки низких локализаций (ниже 6 см), при лечении которых применяются комбинированные методы, а частота местных рецидивов, несмотря на выполнение зачастую инвалидизирующих операций, значительно выше.
Магнитно-резонансная томография является диагностическим методом, сочетающим в себе преимущества пространственного и контрастного разрешения в сочетании с отсутствием лучевой нагрузки. Для низких локализаций рака прямой кишки неоспорима диагностическая роль МРТ в прогнозировании вовлечения латерального края резекции, так как на уровне мышц, поднимающих задний проход, толщина мезоректума значительно тоньше, чем в верхне- и среднеампулярных отделах прямой кишки [2, 3]. Высокое пространственное разрешение МР-изображений в коронарных плоскостях позволяет четко визуализировать леваторы ануса, комплекс внутренних и наружных сфинктеров и межсфинктерное пространство, что используется для стадирования низких колоректальных опухолей и планирования объема хирургического вмешательства (стандартная операция, сфинктеросохраняющая резекция, экстралеваторная брюшно-промежностная экстирпация прямой кишки) [4–8].
С помощью магнитно-резонансной томографии возможно визуализировать как нормальные вены мезоректальной клетчатки в виде серпигиозных структур с низким МР-сигналом, так и венозные сосуды патологической структуры при опухолевой инвазии. Это позволяет включить МРТ-исследование в стандартный протокол определения распространенности нижнеампулярного рака прямой кишки в предоперационном стадировании низких раков, непосредственно влияющем на дальнейшую тактику их лечения [10–14].
Что значит сосудистая инвазия
Можно сказать, что раковые клетки в определенной степени не реагируют на механизмы, контролирующие рост и развитие нормальной ткани. При пролиферации нормальной ткани непосредственный контакт клетки со своими соседями обычно служит сигналом к прекращению размножения. Это контактное торможение отсутствует в опухолевых тканях.
При подкожном введении раковых клеток иммунодефицитным мышам происходит рост и развитие опухоли, что никогда не случается при введении здоровых клеток. Раковые клетки отличаются от здоровых по составу мембранных гликопротеинов, по микропотенциалам на клеточной мембране, а также характеризуются повышенным содержанием сиаловой кислоты. Локомоторный клеточный аппарат (микротрубочки и микрофиламенты) раковых клеток деградирует, клетка теряет присущие ей формы, отмечается миграция цитоплазмы раковой клетки в зону контакта со здоровыми клетками.
Одновременно раковые клетки становятся локально инвазивными, хотя биохимические основы этого свойства до сих пор четко не выявлены. Опухолевые клетки часто демонстрируют пониженную адгезивность в сравнении с нормальными клетками. Важным моментом механизма инвазии является секреция определенных ферментов. Некоторые ферменты играют ключевую роль в протеолизе внутриклеточного матрикса, который всегда сопровождает инвазию раковых клеток. К таким ферментам относится семейство матричных металлопротеиназ (ММП), которое включает в себя колллагеназы, желатиназы и стромолизины.
Эти ферменты экскретируются в неактивной форме. Последующий разрыв сульфгидрильной группы и присоединение атома металла (чаще всего цинка) приводят к изменению конформации фермента и переводят его в активное состояние. Тканевые ингибиторы металлопротеиназ (ТИМП) прекращают действие этих ферментов. Некоторые типы тканей изначально обладают повышенной устойчивостью к инвазии. Это, например, компактная костная ткань, ткани крупных сосудов и хрящевая ткань. Предположительно способность к инвазии у опухолевых клеток появляется в результате трансформации нормальных процессов реконструкции и восстановления здоровых тканей. Тем не менее к настоящему моменту неизвестно, какие конкретно изменения генетической структуры раковых клеток ответственны за инвазивный рост.
По мере роста опухоли она выделяет в кровь ангиогенные факторы, которые стимулируют прорастание опухоли кровеносными сосудами и формирование сети капилляров. Сосудистая система кровоснабжения опухоли может стать мишенью для различных видов противораковой терапии. Опухоль стимулирует пролиферацию эндотелиальных клеток, выделяя ангиогенные цитокины, такие как эндотелиальный фактор роста сосудов (ЭФРС), ТФР и факторы роста фибробластов. Эндотелиальные же клетки в свою очередь могут стимулировать рост клеток опухоли. В одном грамме опухолевой ткани может находиться до 10-20 млн эндотелиальных клеток, которые не являются неопластическими.
Антигены нормальных эндотелиальных клеток, включая и профакторы свертываемости крови, могут быть разрегулированы в активно пролиферирующей под действием опухоли эндотелиальной ткани. В дополнение к действию цитокинов, гипоксия, развивающаяся в сети опухолевого кровоснабжения, может стимулировать выбросы ЭФРС и других факторов. В ходе ангиогенеза эндотелиальные клетки внедряются в строму опухоли, активно делятся там с образованием зачатков новых капилляров, которые затем развиваются в сосудистую систему опухоли. Как и в случае инвазии опухолевых клеток, этот процесс идет с участием продуцируемых эндотелием ММП и их естественных ингибиторов.
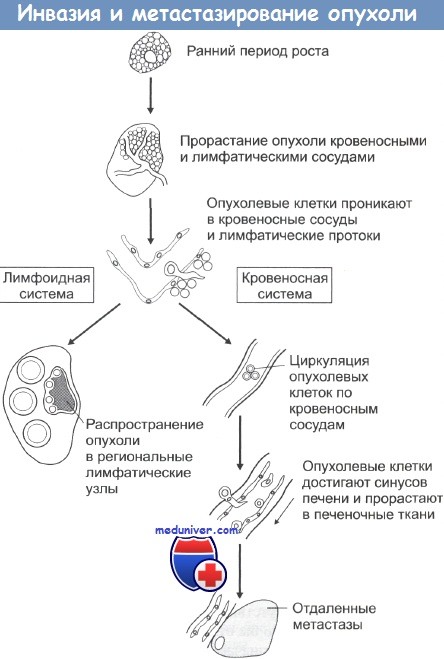
При локальной инвазии рака опухолевые клетки могут попадать в сосудистую систему и давать начало метастазам. Последовательность событий при метастазировании показана на рисунке. Распространение раковых клеток по лимфатической системе, что особенно характерно при карциномах, происходит при попадании опухолевых клеток в лимфатические протоки с последующим оседанием их в местах разветвления протоков и в ближайших лимфатических узлах. Вслед за этим обычно происходит инфильтрация опухолевыми клетками и отдаленных лимфоузлов. Распространение через кровяное русло проходит при проникновении раковых клеток в кровеносные сосуды рядом с местом первичной локализации опухоли либо через грудные протоки. Подхваченные током крови раковые клетки затем захватываются ближайшими капиллярными сетями, чаще всего сетями печени и легких, и оседают в них. При оценке направлений метастазирования очень важно учитывать первичную локализацию опухоли.
Например, опухоли пищеварительного тракта обычно метастазируют через воротную вену в печень. Опухоли также могут метастазировать непосредственно сквозь прилегающие ткани. Так возникающие в брюшной полости новообразования могут очень быстро рассеяться по всему внутрибрюшинному пространству, а клетки рака легкого могут мигрировать через плевру. Некоторые опухоли метастазируют в определенные органы и ткани, другие — бессистемно. Саркомы, например, почти всегда метастазируют в легкие, рак молочной железы поражает также ткани осевого скелета. Тем не менее биологических механизмов, объясняющих такую избирательность, пока не найдено.
Региональные лимфоузлы могут осуществлять барьерную функцию, предотвращая распространение метастазов за пределы области первичной локализации опухоли. До сих пор четко не выяснено, каким образом и за счет каких специфических иммунных механизмов лимфатические узлы создают барьер на пути распространения опухоли.
Проникая в кровеносное русло в районе первичной опухоли, раковые клетки затем могут достигать других органов и тканей. Для того чтобы дать начало новым очагам опухоли, эти клетки на новом месте должны, во-первых, проникнуть в ткани через эндотелий капилляров, а во-вторых, выжить при атаках местных иммунных систем защиты, таких как фагоцитирующие клетки и так называемые естественные киллеры (ЕК).
Способность к инвазированию и расселению в отдаленных органах и тканях у различных видов опухолей сильно варьирует. Эта способность, по-видимому, определяется степенью экспрессии того участка генома, который и обусловливает злокачественный рост клеток. Действительно, со временем почти все раковые опухоли накапливают все больше и больше генетических изменений в своих клетках и приобретают способности к инвазии и метастазированию. Но даже при клиническом обнаружении опухоли метастазы и инвазия могут проявиться лишь спустя несколько лет. Типичным примером является карцинома низкой степени злокачественности. Следует отметить, что даже однотипные виды рака с одинаковой степенью дифференцированности опухолевых клеток по-разному метастазируют у разных больных.
Все это говорит о необходимости поиска молекулярных маркеров, которые смогли бы предсказывать исход течения онкологического заболевания более точно, чем диагностика по гистологическому типу опухоли (хотя последний метод в настоящее время является наиболее точным из всех возможных). Кроме того, даже конкретная опухоль может быть в значительной степени гетерогенной и состоять из клеток, различных по своему метастатическому потенциалу, что было показано на клонированных субпопуляциях, выделенных из одной опухоли. Биологические причины такой вариабельности в настоящее время неизвестны.
Совершенно ясно, что для успешного лечения онкологических пациентов необходимо проводить масштабные исследования в области нахождения механизмов тканевой инвазии, метастатического роста и поиска биологических причин гетерогенности опухолей. Отсутствие гомогенности в опухолях, сходство опухолевых клеток со здоровыми клетками породившей ее ткани, и отсутствие четкого единичного критерия, по которому можно было бы отличить раковую клетку от здоровой, — все это вместе означает, что наши рассуждения о противоопухолевом иммунитете или о механизмах действия лекарственных цитостатических препаратов должны приниматься с изрядной долей скептицизма, особенно если они базируются на экспериментах с гомогенными опухолевыми культурами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инвазивный рак шейки матки
Инвазивный рак шейки матки – что это такое? Рак шейки матки занимает третье место среди всех злокачественных новообразований, которые поражают женщин репродуктивного возраста. На начальной стадии патологического процесса определяется неинвазивный рак шейки матки. В этом случае атипичные клетки растут медленно и распространяются в пределах слизистой шейки матки. Инвазивный рак шейки матки характеризуется интенсивным ростом клеток. Он может распространяться на другие органы и нарушать их функционирование. Процесс перехода неинвазивного рака шейки матки в инвазивный длится до 20 лет, но он неизбежен. Гинекологи Юсуповской больницы проводят своевременную диагностику заболевания с помощью новейшей аппаратуры ведущих мировых производителей?
Раннее лечение неинвазивного и микроинвазивного рака шейки матки позволяет улучшить прогноз пятилетней выживаемости. В Юсуповской больнице работает команда специалистов высокой квалификации: онкологи-гинекологи, химиотерапевты, радиологи. Врачи проводят лечение неинвазивного, преинвазивного и инвазивного рака шейки матки в соответствии со стандартами ASCO и NCCN. Профессиональный уход осуществляют медицинские сёстры, которые знают особенности течения ракового процесса, внимательно относятся к пожеланиям пациентов и их родственников.
Причины инвазивного рака шейки матки
Учёные установили, что необходимым условием для возникновения предраковых изменений в шейке матки является наличие определённых типов вирусов папилломы человека (ВПЧ). У больных раком шейки матки чаще всего выявляют ВПЧ шестнадцатого и восемнадцатого типов. Одних только причинённых вирусом повреждений недостаточно для возникновения патологического процесса, представленного новообразованной тканью, в которой изменения генетического аппарата клеток приводят к нарушению регуляции их роста и дифференцировки.
Различают следующие дополнительные факторы, которые оказывают влияние на проявление злокачественной активности внутри клеток эпителия шейки матки;
Никотин может участвовать в трансформации интраэпителиальных изменений шейки матки в инвазивный рак. Внутриматочные средства механической контрацепции при длительном неконтролируемом применении повреждают слизистую оболочку шейки матки. Во время многочисленных родов могут происходить разрывы шейки матки, образовываться грубые рубцы, которые являются фоном для развития злокачественного процесса.
Развитие рака шейки матки представляет собой последовательный процесс. Он характеризуется соответствующими изменениями цитологической и гистологической картины для каждой стадии. В результате инфицирования эпителия шейки матки, которое осуществляется в большинстве случаев половым путём, вирус папилломы человека может присутствовать у 10-15% молодого населения. После инфицирования полные копии вируса обнаруживаются в эписомах (генетических элементах) клетки хозяина. Здесь вирус завершает свой жизненный цикл и во многих случаях продуцирует транзиторную инфекцию. Она не вызывает значительных цитологических изменений. При наличии ВПЧ, не способного вызвать онкологический процесс, вирус исчезает в течение 6-9 месяцев.
Частицы полного вируса могут незначительно повредить плоский эпителий шейки матки. Повреждённые клетки выявляют при РАР-анализе мазков с эпителия шейки матки с последующей биопсией. Их классифицируют как интраэпителиальные повреждения, что соответствует первой, низкой степени дисплазии. На этой стадии патологического процесса риск развития последующих повреждений и переход в более тяжёлую степень дисплазии небольшой. У некоторых пациентов ВПЧ интегрирует собственную ДНК в геном клетки-хозяина. Это приводит к развитию дисплазии высокой степени. Повреждения, которые соответствуют низкой степени дисплазии и включают ДНК онкогенных ВПЧ высокого риска, имеют потенциальную возможность прогрессировать до средней и высокой степени дисплазии, которая выступает последним предвестником рака шейки матки.
Симптомы инвазивного рака шейки матки
Симптомы инвазивного рака шейки матки бывают общими и специфическими. Женщины отмечают следующие общие признаки онкологического заболевания:
Специфическая симптоматика непосредственно связана с поражением шейки матки. На ранних стадиях заболевание протекает бессимптомно. На третьей или четвёртой стадии возникают следующие признаки болезни:
При поражении метастазами паховых лимфатических узлов развивается отёчность нижних конечностей, лимфостаз. Если опухоль прорастает в малый таз, появляется выраженный болевой синдром, нарушение дефекации, болезненное и затруднённое мочеиспускание. Признаком возникновения свищей является появление мочи или кала во влагалище.
Инвазивный рак подтверждают на основании гистологического исследования тканей шейки матки, которые получают в рамках диагностического выскабливания, конизации или биопсии. Оптимальный объём обследования включает следующие процедуры:
Тактику лечения формируют коллегиально онколог, радиолог, химиотерапевт и прочие узкие специалисты. Алгоритм лечебного воздействия формируют исходя из следующих параметров:
При наличии инвазивного рака шейки матки онкологи выполняют объёмные хирургические вмешательства: экстирпацию матки (полное удаление матки с шейкой) с удалением лимфатических узлов (лимфодиссекцией). При наличии инвазии злокачественной опухоли в мочевой пузырь или прямую кишку, выполняют экзентерацию органов малого таза (удаление матки, шейки матки, прямой кишки и мочевого пузыря). При инвазивном раке шейки матки редко ограничиваются лишь хирургическим вмешательством. Лечение проводят в комплексе с химиолучевой терапией. Химиотерапию используют в качестве монотерапии или в дополнении к хирургическому лечению, радиотерапии. Использование фармакологических препаратов (гидроксикарбамида, блеомицина, цисплатина, этопозида) позволяет увеличить эффективность лучевой терапии, снизить риск развития метастазов, контролировать рецидив заболевания.
Радиотерапию широко применяют в комплексе с оперативным вмешательством на ранних стадиях заболевания. При распространённых формах инвазивного рака шейки матки лучевая терапия является единственным способом уменьшения объёма опухолевой массы. Для лечения применяют внутреннее (брахитерапия) и дистанционное облучение. В тех случаях, когда злокачественное новообразование шейки матки удалить невозможно по причине значительного местного распространения, наличия отдалённых метастазов, химиолучевое лечение применяют в качестве самостоятельного метода.
Преинвазивный рак шейки матки
Преинвазивный рак шейки матки представляет собой морфологически злокачественное изменение эпителия шейки матки, которые ещё не распространились за базальную мембрану (рак без инвазии). Инвазивный, или истинный, рак является состоянием, когда атипические клетки многослойного плоского эпителия проникают за базальную мембрану и прорастают в более глубокие ткани. Преинвазивный рак чаще всего развивается в плоском эпителии, у места стыка его с цилиндрическим. По этой причине его называют внутриэпителиальным раком.
Преинвазивный рак шейки матки встречается в любом возрасте, но чаще всего после 40 лет. При этой форме опухоли имеют место изменения в клетках всех слоев эпителия:
Такой изменённый плоский эпителий внедряется в железистый слой, иногда его полностью замещает, но никогда не проникает за пределы базальной мембраны. Преинвазивный рак может протекать по следующему сценарию:
Чаще всего преинвазивный рак выявляют при тех или иных патологических процессах на шейке матки (лейкоплакии, эрозии, эндоцервиците). Превращение внутриэпителиального рака в инвазивный рак шейки матки может продолжаться от одного до семнадцати лет. По этой причине у онкологов отсутствует единое мнение по поводу его лечения. Некоторые врачи считают, что при данной форме рака должна проводиться такая же терапия, как и при инвазивном раке шейки матки: радикальная операция (расширенная экстирпация матки с придатками по методу Вертгейма) с последующей лучевой терапией.
Другие хирурги проводят экстирпацию матки без придатков, третьи – ампутацию шейки матки с её серийным гистологическим исследованием или электроконизацию шейки матки. Применяют также кюритерапию преинвазивного рака (аппликацию на шейку матки радиоактивных веществ, обычно кобальта). Последняя методика противопоказана в репродуктивном возрасте.
Микроинвазивная карцинома шейки матки
Микроинвазивный рак шейки матки (микроинвазивная карцинома) характеризуется глубиной проникновения в подлежащие ткани до пяти миллиметров при диаметре опухоли не более семи миллиметров. При этом у пациенток сохраняется нормальная иммунологическая реактивность организма и существует крайне низкая вероятность регионарного распространения опухолевых клеток. Микроинвазивный рак невооруженным глазом не виден, его можно обнаружить только микроскопически.
От 60 до 80% пациенток, страдающих микроинвазивной карциномой шейки матки, не имеют специфических клинических симптомов. Около 40% женщин предъявляют жалобы на наличие белей водянистого характера, контактных или, реже, межменструальных кровянистых выделений из половых путей. Обследование пациенток с такими жалобами в Юсуповской больнице проводят с помощью следующих методов:
Оптимальным способом забора материала для гистологического исследования служит конизация шейки матки. В единичных случаях она является лечебным мероприятием.
Онкологи Юсуповской больницы индивидуально подходят к выбору метода лечения микроинвазивного рака шейки матки. При глубине инвазии до трёх миллиметров, отсутствии признаков поражения сосудистых структур и опухолевого роста по линии иссечения конуса выполняют гистерэктомию первого типа с сохранением яичников у женщин до 45 лет. Если при глубине инвазии злокачественного новообразования до 5 мм в препаратах, взятых путём конизации, определяется васкулярная инвазия, используют второй или третий тип радикальной гистерэктомии с последующей лимфаденэктомией тазовой области. Придатки у молодых женщин в Юсуповской больнице не удаляют.
Если в результате тщательного дооперационного обследования установлено поражение только влагалищной части шейки матки, молодым женщинам с целью сохранения детородной функции в отдельных случаях выполняют органосохраняющие операции – ампутацию шейки матки скальпелем или лазерным лучом. Эти методы применяют применены при глубине инвазии опухоли до 1-3 мм, отсутствии опухолевого роста по линии иссечения конуса шейки матки и признаков поражения сосудистого пространства.
Если у пациентки имеются общие противопоказания к хирургическому вмешательству, используют внутриполостную гамма-терапию с помощью метракольпостата на аппаратах типа «АГАТ» или «МикроСелектрон». Разовая доза составляет 5 Гр, частота облучения – 2-3 раза в неделю, суммарная доза –50 Гр. Молодым пациенткам, не имеющим сопутствующих заболеваний, проводят 3-4 сеансы по 10 Гр при ритме облучения 1 раз в неделю.
Прогноз выживаемости при инвазивном раке и микроинвазивной карциноме шейки матки улучшается в случае раннего выявления заболевания. По этой причине при появлении признаков патологии репродуктивных органов звоните по телефону Юсуповской больницы. Специалисты контакт центра запишут вас на приём к онкологу-гинекологу в удобное вам время.