Что значит экспрессия чужеродных генов
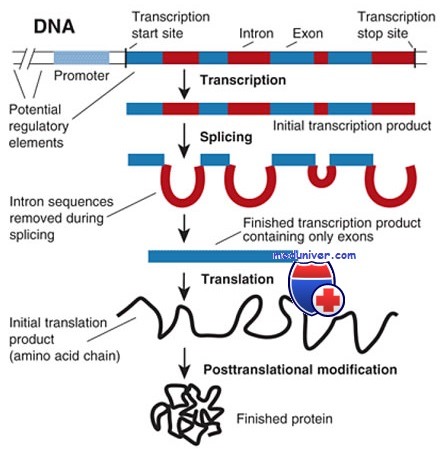
Для генов, кодирующих белки, движение информации от гена до полипептида включает несколько шагов. Инициация транскрипции гена происходит под влиянием промоторов и других управляющих элементов, а также специфических белков, известных как факторы транскрипции, взаимодействующих с определенными последовательностями в пределах управляющих областей гена и определяющих пространственную и временную схему экспрессии гена. Транскрипция гена начинается со «стартовой» точки в хромосомной ДНК в начале 5′-транскрибируемой, но не транслируемой области.
Процесс транскрипции идет непрерывно по ходу кодирующей последовательности вдоль хромосомы, проходя от нескольких сотен пар оснований до более миллиона пар, захватывая как интроны, так и экзоны, и завершаясь на конце кодирующей последовательности. После модификации обоих 5′ и З’-концов первичной копии РНК части, соответствующие нитронам, удаляются, а сегменты, соответствующие экзонам, сращиваются вместе.
После сплайсинга (сращивания) РНК результирующая мРНК (содержащая центральный сегмент, соответствующий кодирующей части гена), перемещается из ядра в цитоплазму клетки, где мРНК транслируется в аминокислотную последовательность закодированного полипептида. Каждая составляющая этого сложного пути подвержена ошибкам и мутациям, которые создают помехи и вызывают множество наследственных заболеваний.
Транскрипция
Транскрипция белок-кодирующего гена РНК-полимеразой-II (одна из нескольких классов РНК-полимераз) начинается в стартовом сайте транскрипции, в точке 5′-нетранслируемой области, соответствующей 5′-концу конечной РНК. Синтез первичной копии РНК идет по направлению от 5′ к З’-концу, поскольку нить считываемого гена, который служит шаблоном для синтеза РНК, действительно считывается в направлении от 3′ к 5′-концу в соответствии с направлением фосфатных связей дезоксирибозы.
Поскольку синтезированная РНК соответствует расположению и последовательности нуклеотидов (с заменой урацила на тимин) 5′-3′-нити ДНК, такую нить ДНК часто называют кодирующей или комплементарной ДНК (кДНК). 3′-5′-нить ДНК носит название некодирующей или антисмысловой. Транскрипция осуществляется как для интронных, так и для экзонных частей гена, до позиции в хромосоме, которая записывается на 3′-конец зрелой мРНК. Неизвестно, заканчивается ли транскрипция в определенной точке терминации на 3′-конце.
Затем в области 5′-конца первичной копии РНК происходит кэпирование, а в специфической точке 3′-конца — расщепление. Расщепление заканчивается присоединением к 3′-концевым звеньям множества остатков аденозина — поли-(А), что увеличивает стабильность полученной РНК. Позиция точки полиаденилирования частично определяется последовательностью AAUAAA (или вариантами этой последовательности), обычно обнаруживаемой в 3′-нетранслируемой части копии РНК. Описанные посттрансляционные модификации, как и процесс сплайсинга РНК, происходят в ядре.
Полностью обработанная РНК, теперь называющаяся мРНК, перемещается в цитоплазму, где происходит трансляция.
Трансляция и генетический код
В цитоплазме мРНК транслируется в белок под действием молекул тРНК, специфичной для каждой конкретной аминокислоты. Эти замечательные молекулы, каждая всего от 70 до 100 нуклеотидов длиной, добавляют к растущей полипептидной цепи определенную аминокислоту в соответствии с шаблоном мРНК. Белковый синтез происходит в рибосомах, макромолекулярных комплексах, состоящих из рРНК (кодируемой генами 18S и 28S) и нескольких десятков рибосомальных белков.
Ключ трансляции — код, который связывает специфическую аминокислоту с комбинацией из трех смежных оснований на мРНК. Каждое сочетание трех оснований составляет кодон, специфичный для конкретной аминокислоты. В теории существует почти бесконечное множество вариантов размещения оснований вдоль полинуклеотидной цепи. В каждом положении может быть один из четырех нуклеотидов (А, Т, С или G); таким образом, для трех оснований есть 43 или 64 возможные комбинации триплетов. Эти 64 кодона и составляют генетический код.
Поскольку на 20 аминокислот приходится 64 возможных кодона, некоторые аминокислоты определяются более чем одним кодоном; поэтому генетический код называют вырожденным. Например, основание в третьей позиции триплета часто может быть или пуриновым (А или G), или пиримидиновым (Т или С), а в некоторых случаях любое из четырех оснований не изменяет смысл сообщения. Лейцин и аргинин определяются сразу шестью кодонами. Только метионин и триптофан кодируются единственным, уникальным триплетом. Три кодона называются стоп-кодонами (или нонсенс-кодонами), поскольку они определяют завершение трансляции мРНК.
Трансляция зрелой мРНК всегда начинается с кодона, определяющего метионин. Следовательно, метионин — всегда первая аминокислота каждой полипептидной цепи, хотя обычно он удаляется до завершения синтеза белка. Кодон метионина (или кодон-инициатор, AUG) устанавливает рамку считывания мРНК; каждый последующий кодон считывается поочередно, указывая аминокислотную последовательность белка.
Молекулярные связи между кодонами и аминокислотами обеспечивают специфические молекулы тРНК. Конкретный участок (сайт) на каждой тРНК формирует антикодон из трех оснований, комплементарный (дополнительный) к специфическому кодону на мРНК. Соединение между кодоном и антикодоном приводит соответствующую аминокислоту на следующую позицию в рибосоме для присоединения с образованием пептидной связи к карбоксильному концу растущей полипептидной цепи. Рибосома затем скользит вдоль мРНК точно на три основания, захватывая следующий кодон для опознавания другой тРНК со следующей аминокислотой.
Таким образом, белки синтезируются, начиная от аминогруппы к карбоксильной группе, что соответствует трансляции мРНК в направлении от 5′-конца к 3′-концу.
Как упоминалось ранее, трансляция заканчивается, когда в той же рамке считывания, что и кодон-инициатор, встречается стоп-кодон (UGA, UAA или UAG). Стоп-кодоны в любой из других неиспользованных рамок считывания не читаются и, следовательно, не оказывают эффекта на трансляцию. Завершенный полипептид отделяется от рибосомы, и она становится доступной для начала синтеза другого белка.
Множество белков проходят существенную посттрансляционную модификацию. Полипептидная цепь, первичный продукт трансляции, скручивается и складывается в специфическую трехмерную структуру, определяемую аминокислотной последовательностью цепи.
Две и более полипептидные цепи, продукты одного или различных генов, могут объединяться, формируя один готовый белковый комплекс. Например, две цепи b-глобина и две цепи а-глобина нековалентно объединяются, формируя тетрамер молекулы гемоглобина. Белковые продукты также могут быть модифицированы химически, например добавлением в специфических местах метильных или фосфатных групп или углеводов.
Такие модификации могут иметь значимое влияние на функцию или количество модифицированного белка. Другие модификации могут включать расщепление белка с потерей специфических аминокислотных последовательностей после того, как они выполнили свою функцию, направив белок в правильную позицию в пределах клетки (например, белки, которые функционируют в пределах ядра или митохондрий) или разделение белковых молекул на меньшие полипептидные цепи.
Например, две цепи, формирующие готовый инсулин, содержащие одна 21, а вторая 30 аминокислот, первоначально представляют собой части проинсулина — первичного продукта трансляции из 82 аминокислот.
Транскрипция митохондриального генома
В предшествующих разделах описаны основы экспрессии генов, содержащихся в ядерном геноме. Митохондриальный геном имеет отличающуюся систему транскрипции и белкового синтеза. Для транскрипции митохондриального генома используется специализированная РНК-полимераза, закодированная в ядерном геноме, содержащая две взаимосвязанные последовательности промотора, для каждой нити кольцевой митохондриальной хромосомы. Каждая нить транскрибируется полностью, а полученные копии затем обрабатываются, порождая различные митохондриальные мРНК, тРНК и рРНК.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Экспрессии чужеродных генов



Одним из наиболее значимых достижений генетической инженерии является клонирование эукариотических генов, что дает возможность осуществлять синтез микробными клетками важнейших для народного хозяйства белков — ферментов, гормонов, иммуномодуляторов и др. Эукариотические организмы-доноры генетического материала характеризуются гораздо менее высоким уровнем продукции природных белков, чем генноинженерные штаммы-продуценты. Поэтому получение практически ценных белков для изучения их структуры и свойств, а также для использования в хозяйственных целях осуществляют чаще с использованием гибридных микробных штаммов, а не культур клеток растений и животных или их органов и тканей. Названным способом получены такие ценные белки, как гормон роста человека и некоторых животных, инсулин, фактор роста эпидермиса человека, фактор некроза опухолей человека и мыши, a-, b- и g-интерфероны, медиатор нервной системы соматостатин, гормон кальцитонин, миоглобин, гормоноподобные сигнальные белки интерлейкины, фактор свертывания крови, отсутствующий у больных гемофилией, обратная транскриптаза вируса лейкоза мышей, урокиназа, трипсин, некоторые онкобелки, вакцины против некоторых вирусов и др.
Когда ген в составе векторной молекулы переносится из клеток одного организма в клетки другого, возникают проблемы с его экспрессией—транскрипция и трансляция мРНК могут не осуществляться вовсе либо происходить с низкой частотой. Это является следствием специфичности ферментов, катализирующих процессы транскрипции и трансляции, к определенным последовательностям ДНК (мРНК), структура которых бывает уникальной у различных таксономических групп организмов. Чаще всего проблемы экспрессии наблюдаются при клонировании эукариотических генов в клетках прокариот, в частности потому, что сигналы инициации транскрипции высших эукариот не распознаются РНК-полимеразами бактерий.
Для достижения эффективной экспрессии клонированных генов используют несколько подходов: 1) увеличение числа копий гена в клетке (амплификация гена); 2) подстановку перед структурной частью чужеродного гена сильного промотора, распознаваемого РНК-полимеразой клетки-хозяина; 3) подстановку перед геном чужеродного белка регуляторного элемента, обеспечивающего эффективную инициацию трансляции; 4) стабилизацию образующейся мРНК и белкового продукта. Перечисленные методы достижения высокого уровня экспрессии генов наилучшим образом разработаны для бактерий E.coli. Поскольку наличие такой методологии является определяющим условием конструирования новых продуцентов, кишечная палочка рассматривается как один из самых перспективных организмов, используемых для этой цели.
Амплификация генов. Для усиления экспрессии генов можно увеличить их количество в клетке. Осуществляют это двумя способами: увеличивая число копий рекомбинантных плазмид или увеличивая число копий гена в составе плазмиды.
Наиболее прост первый способ. Уже указывалось, что для конструирования векторов предпочтительнее использовать мультикопийные плазмиды, находящиеся под нестрогим контролем репликации. В этом случае число копий плазмид составляет 10—200. Данный показатель можно увеличить до нескольких тысяч, если подавить синтез белков бактериальной клетки или использовать мутантные плазмиды. Применение таких векторов позволяет значительно увеличить дозу целевого гена, а значит, и выход белкового продукта. Следует, однако, учитывать, что чрезмерная амплификация плазмид может приводить к снижению жизнеспособности штамма-продуцента из-за высокой токсичности некоторых чужеродных белков для бактерий, а также из-за увеличения времени генерации клеток.
Копийность генов в составе векторных молекул обеспечивают, создавая опероны с повторяющимися идентичными цистронами чужеродных генов. Сочетание перечисленных методов позволяет повысить дозу гена в клетке от нескольких десятков до тысяч копий на нуклеоид и увеличить уровень синтеза соответствующих белков (в ряде случаев на 1—2 порядка).
Достижение высокого уровня транскрипции чужеродных генов. Для того чтобы эукариотические гены транскрибировались в прокариотических клетках, их обычно подставляют под контроль сильных промоторов (обеспечивают высокую частоту событий инициации транскрипции) прокариот.

Наиболее часто для этих целей используют сильные промоторы кишечной палочки: лактозного оперона — PlacUV5, триптофанового — Ptrp; гибридные промоторы, например Ptrp-lacUV5 (Ptac), а также промоторы фага λ— PR, PL идругих фагов (Т5, Т7, jХ174). Выделение этих промоторов и включение их в состав векторов осуществляют в ходе генно-инженерных манипуляций.
Еще более совершенной является методология использования регулируемых промоторов, которые инициируют процесс эффективной транскрипции лишь в определенных условиях. Такими промоторами являются, например, PR и PL фага λ. Их используют в клетках, содержащих температурочувствительный сI-репрессор, ген которого может быть расположен на векторе или совместимой с ним плазмиде. В таких клетках экспрессия чужеродного гена под контролем PR или PL будет происходить лишь после инактивации репрессора повышением температуры ферментации.
Использование прокариотических регуляторных элементов, расположенных на многокопийных плазмидах, позволяет достигать уровня синтеза мРНК чужеродного гена до 25% от всей РНК бактериальной клетки.
Достижение высокого уровня трансляции чужеродных генов. Еще одним условием эффективной экспрессии клонированных генов является наличие перед геном чужеродного белка оптимального сайта инициации трансляции мРНК. На частоту событий трансляции первостепенное значение оказывает структура участков мРНК, обеспечивающих ее связывание с рибосомой и тРНК. Показано, что олигонуклеотидная последовательность, расположенная на 5’-конце и непосредственно примыкающая к стартовому кодону, обеспечивает комплементарное спаривание с нуклеотидами антикодоновой петли тРНК. В то же время среди нуклеотидов мРНК, участвующих во взаимодействии с рибосомой, достоверно установлена роль пуринбогатого участка на расстоянии 3— 15 нуклеотидов от стартового кодона (последовательность Шайн—Дальгарно, или SD-последовательность). Длина SD-последовательности, а также ее расположение относительно стартового кодона существенно сказываются на связывании рибосом с мРНК, а значит, и на частоте событий инициации трансляции.
Известно три основных подхода к конструированию векторов, обеспечивающих трансляцию чужеродной ДНК в бактериальных клетках. Одним из наиболее распространенных является метод конструирования «гибридных участков связывания рибосом». Суть его заключается в том, что структурная часть чужеродного гена (с собственным стартовым кодоном и несколькими нуклеотидами перед ним) включается между последовательностью SD и стартовым кодоном прокариотического гена. Такой метод имеет преимущество, состоящее в образовании полноразмерного чужеродного белка. Однако существенным недостатком метода является трудность достижения оптимального удаления стартового кодона от SD-последовательности, что, как указывалось, очень существенно для инициации трансляции. Поэтому применяют другой подход, в котором чужеродный структурный ген, лишенный собственных регуляторных областей, внедряют в состав хорошо экспрессируемого бактериального гена. Для этих целей чаще всего используют lac-промотор с соответствующей последовательностью Шайна—Дальгарно. Сайт внедрения должен быть достаточно удален от места инициации трансляции, чтобы новая нуклеотидная последовательность не мешала эффективной инициации транскрипции и трансляции бактериального гена. При экспрессии векторов такого типа образуется гибридный белок, в котором N-концевая часть представлена аминокислотами прокариотического пептида. Поэтому для выделения эукариотической полипептидной цепи требуется дополнительная химическая или ферментативная обработка.
Наконец, третий подход к конструированию векторов, обеспечивающих эффективную трансляцию, использует принцип «перекрывания» генов. В этом случае чужеродный ген встраивают в концевую часть прокариотического гена таким образом, что SD-последовательность второго гена расположена непосредственно в кодирующей области первого. При этом терминирующий трансляцию кодон первого гена является частью инициирующего кодона второго гена. Этот метод разработан в 1985 г. в СССР. Он позволяет достигать 100%-ной инициации трансляции второго гена, поскольку рибосомы, транслировавшие первую часть полицистронной мРНК, не отсоединяются от нее, а происходит реинициация трансляции второго гена. Таким образом, примене ние векторов с частично перекрывающимися генами в оперонах позволяет обеспечить эффективность инициации трансляции чужеродного гена не ниже, чем у исходного прокариотического цистрона.
Стабилизация мРНК и белкового продукта чужеродного гена. Стабильность мРНК в клетках бактерий можно повысить введением мутаций, инактивирующих РНКазы. Кроме этого, на стабильность мРНК влияет полинуклеотидфосфорилаза (pnp). Известны мутанты E.coli по генам pnp, в которых время полужизни мРНК, определяющей чужеродные белки, увеличивается в 1,5 раза.
Серьезным препятствием при получении штаммов-сверхпродуцентов может стать протеолиз чужеродных белков в клетке. Ведь набор клеточных пептидаз как раз и предназначен в основном для быстрой деградации полипептидов с «аномальной» структурой, которые возникают, например, в результате ошибок трансляции. Для стабилизации чужеродных белков можно использовать в качестве реципиентов штаммы, дефектные по системе деградации белков (lon-, htpR или deg-мутанты). Можно также вводить в бактериальную клетку ген pin бактериофага Т4, который контролирует синтез ингибиторов протеиназ, или другие гены с похожими функциями.
Экспрессия чужеродных генов и системы трансформации
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Описание презентации по отдельным слайдам:
Описание слайда:
Экспрессия чужеродных генов и
системы трансформации
Описание слайда:
Что такое трансформация?
Это введение ДНК неполовым путем в клетку реципиента, проводящее к наследуемому изменению генотипа
Основной метод биотехнологии растений и мощнейшая экспериментальная методика
Убирает барьеры по переноске генов
Развитие трансформации E.coli, а также разрезание и сшивание ДНК in vitro дало начало генетической революции в 70-е годы
Не надо путать с генетической трансдукцией, представляющей собой частный случай пепеноса генов между хозяином и вирусом
Описание слайда:
Секвенирование геномов четко показало, что у бактерий существует горизонтальный перенос генов между разными видами при определенных селектинвых преимуществах (условиях отбора)
Формирование раковых клеток у животных под действием онкогенных вирусов, таких как SV40 и аденовирусов. Часть вирусной ДНК интегрируется в ДНК хозяина и вызывает неконтролируемый рост клеток (в биологии рака существует свое более узкое определение трансформации)
3. У растений, такких как бананы, табак и кокос tobacco, малые ДНК-вирусы (баднавирусы и нановирусы) интегрируются в виде множественных копий в ДНК хозяина при стрессе (вызывая потерю стрессоустойчивости). Это является существенной помехой программ селекции бабанов.
Трансформация происходит в природе
Описание слайда:
Описание слайда:
Важные требования к трансформации
Возможность ДНК экспессироваться в клетках хозяина (реципиента)
2. Клетки реципиента часто требуют специальной обработки для того, чтобы сделать их «компетентными» к трансформации
3. Система доставки ДНК
4. Системы селекции для распознавания и отбора трансформантов
Описание слайда:
Что такое экспрессия генов?
Это совокупность реакций, вследствие которых биологическая информация гена становится доступной клетке (работа или активность гена)
Описание слайда:
Описание слайда:
РНК-процессинг у эукариот
Описание слайда:
Конструирование генов для их экспрессии
в других видах
Нужно знать экспрессируется ли ген (часто уже известно).
Если ген из того же или близкого таксона, то ожидается, что он будет экспрессироваться точно также как в организме-источнике (доноре).
Например, ген из двудольных растений практически всегда будет нормально экспрессироваться в другом двудольном растении
Гены разных энтерических бактерий будут работать в таких же бактериях без дополнительных модификаций
Гены человека «работают» в мышах
Если кодирующая последовательность из другого царства, то очень вероятно, что она не будет фукнционировать. Такая последовательность потребует дополнительной добавки – последовательности совместимости, или промотера.
Таким образом. часто требуется создание нового гена – химерной последовательности или ХИМЕРЫ, которую можно создать in vitro (предыдущая лекция)
Все гены (химерные или немодифицированные) пропагируются (наращивается число их копий) при помощи трансформации на плазмидных векторах в бактериях или грибах.
Описание слайда:
Организм, орган или часть организма, содержащая две или более генетические составляющие. Получается в результате трансплантации органов, пересадок или генетической инженерии.
Вещество, такое как антитела, созданное из белков различных видов.
From Latin chimaera, from Greek khimaira, chimera, she-goat – она-коза – комбинаций двух зверей (чаще козы и льва)
Химера. Что это значит?
Описание слайда:
Пример генной кассеты (плазмидной конструкции высокой интенсивности) для трансформации растений
Плазмидный вектор
(pUC12)
CaMV 35S
promoter
CaMV polyadenylation sequence
Описание слайда:
Описание слайда:
Описание слайда:
Гены селективных маркеров
Бактерии:
Дрожжи:
Комплементация ауксотрофности
Например URA3 позволяет урацил-ауксотрофному мутанту расти на несодержащих урацил средах.
Описание слайда:
Гены селективных маркеров
Описание слайда:
Гены селективных маркеров в случае высших эукариот – это всегда химерные гены
Данный сайт дает некоторые идеи о ресурсах для трансформации
http://www.pgreen.ac.uk/a_pls_fr.htm
Описание слайда:
Трансформация бактерий
Некоторые бактерии могут быть трансформированы простым добавлением ДНК в культуру.
Непатогенный штамм Pneumococcus IIR может быть трансформирован в большие патогенные колонии посредством трансформации с ДНК IIIS-штамма с вероятностью 1 к 104 клеток
IIR
IIIS
Описание слайда:
Метод 1: Химическая трансформация бактерий.
Описание слайда:
Метод 2: Электропорация
Типичный протокол для Agrobacterium или Rhizobium
Культуры выращиваются до экспоненциальной фазы, охлаждаются и осаждаются центрифугированием
Клетки ресуспендируются при 1010 мл-1 в холодной стерильной дистиллированной воде
Вышеуказанный шаг повторяется дважды, чтобы отмыть клетки от солей
Клетки смешиваются с ДНК (при температуре льда) и переносятся в предварительно охлажденную электропорационную кювету
Напряжение 4000–8000 Вольт см-1 на несколько миллисекунд подается на кювету.
Клетки вводятся в среду для восстановления на некоторое время и переносятся на чашки (как в методе 1)
Описание слайда:
Описание слайда:
Эукариотическая генетика и молекулярная биология
могут эффективно продуцировать эукариотические гены
S. cerevisiae – стандартное орудие для молекулярно-биологических методик
Высокая стабильность трансформантов
Дрожжевые шаттл-вектора могут поддерживаться как искусственные хоромосомы и как плазмиды в E.coli
Можно получить вставочные мутанты
Известна рамка считывания
Дрожжи могут делать сплайсинг генов животных и растений
Дрожжевая РНК-полимераза распознает многие промотеры животных и растений
Трансформация дрожжей
Описание слайда:
Описание слайда:
Трансформация дрожжей
Все первоначальные (старые) методики, которые обязательно включали ферментативную обработку и получение сферопластов (протопласты грибов) уже не используются.
ДНК интродуцируется посредством кальциевого метода, как для бактерий.
Иначе ДНК может упаковываться в липосомы (липидные везикулы, которые могут сливаться с плазматической мембраной)
Часто используется электропорация.
Описание слайда:
Трансформация растений
Требования:
— способность генерировать целое нормально размножающееся растение (тотипотентность) из одиночной клетки
— требует знание и освоение методов культур клеток и тканей растений (выбор правильного гормонального режима)
— конструкции ДНК обычно содержат:
*интересующий нас ген(ы)
*ген(ы) селективного маркера
— подбор методов трансформации
— селекционная среда (антибиотик или гербицид)
Описание слайда:
Регенерация целого растения обычно достигается на питательной среде, содержащей определенную комбинацию фитогормонов – в частности, ауксинов и цитокининов.
Два типа регенерации:
Органогенез. Формируется стебель-побег, потом корень (например, табак)
Эмбриогенез. Образуется эмбрион. Который затем развивается в растение (злаки)
Трансформация растений
Разные виды растений и разные их части могут использоваться для трансформации (эмпирический подход в подборе – т.е. берется «то», что лучше трансформируется).
Типичные экспланты для трансформации:
Листовые диски (например, табака)
Диски из столонов (картофель)
Scutellar tissue – скутелла (злаки) C
Семядоли (томаты)
Стебли проростков (салат, капуста, крестоцв.)
Описание слайда:
Листовые диски табака, в которых регенерируются побеги
Регенрация томатов из листовых дисков и семядолей