Что значит четырехкамерное сердце
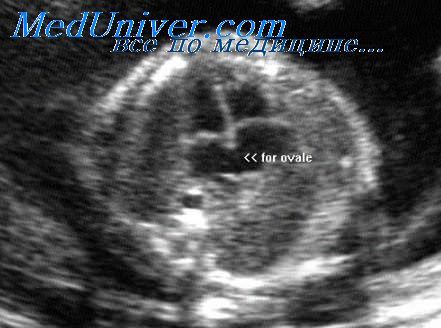
Четырехкамерный срез сердца получается в плоскости, которая проходит практически строго поперечно (аксиально) по отношению к грудной клетке плода. Важными ориентирами для получения этой плоскости являются верхушка сердца, его основание, межжелудочковая перегородка (МЖП), межпредсердная перегородка (МПП), два атриовентри-кулярных клапана (трикуспидальный и митральный), а также четыре камеры, отграниченные этими анатомическими структурами. В норме толщина межжелудочковой перегородки и стенок желудочков одинакова.
Идентификация левого предсердия осуществляется на основании визуализации впадения в него легочных вен. Ротируя датчик таким образом, чтобы левый желудочек и аорта располагались в одной плоскости, можно получить изображение левых отделов сердца. Его правые отделы исследуют, смещая датчик в краниальном направлении и несколько наклоняя его в сторону левого плеча.
На изображениях левой половины сердца определяются структуры, имеющие большое значение для диагностики. Между левым предсердием и левым желудочком визуализируется митральный клапан. Его задняя створка обычно несколько короче передней, которая является как бы продолжением задней стенки аорты. Передняя стенка аорты сливается с межжелудочковой перегородкой. У основания аорты находится аортальный клапан.
У плода имеются две артериальные дуги, которые следует различать при эхографическом обследовании. Дуга аорты дифференцируется с дугой артериального протока согласно следующим критериям. От нее отходят крупные брахиоцефальные сосуды к верхним конечностям и голове, в то время как артериальный проток не имеет ветвей. Ход дуги аорты характеризуется более правильной округлой формой кривизны, по сравнению с ходом протока, который образует легкие угловые изгибы.
Полые вены обнаруживаются при исследовании в продольной плоскости сканирования грудной клетки плода путем визуализации места их впадения в правое предсердие.
Что значит четырехкамерное сердце
ГБУ «Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе»
Трехкамерное сердце: необычное клиническое течение врожденного порока с летальным исходом в 58 лет
Журнал: Архив патологии. 2020;82(6): 41-43
Повзун С.А. Трехкамерное сердце: необычное клиническое течение врожденного порока с летальным исходом в 58 лет. Архив патологии. 2020;82(6):41-43.
Povzun SA. Three-chambered heart: the unusual clinical course of a fatal birth defect at 58 years old. Arkhiv Patologii. 2020;82(6):41-43.
https://doi.org/10.17116/patol20208206141
ГБУ «Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе»
ГБУ «Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе»
Даты принятия в печать:
Трехкамерное сердце — тяжелый врожденный порок, формирующийся на 3—4-й неделе беременности, когда происходит закладка межжелудочковой перегородки. В случае рождения таких детей до 2 лет доживает только около половины из них, до взрослого возраста — немногие. G. Restiano и соавт. [1], наблюдавшие женщину 57 лет с пороком сердца в виде единого желудочка, насчитали в литературе к моменту выхода их статьи всего 10 публикаций о пациентах с аналогичным пороком у лиц старше 50 лет. Жизнь таких людей со смертью во взрослом возрасте — исключительная казуистика, в связи с чем приводим собственное наблюдение.
На вскрытии: труп умеренно истощенной женщины с акроцианозом, пальцы рук в виде «барабанных палочек» и ногти в форме «часовых стекол». Кожа голеней и стоп с выраженным гиперкератозом, который, как установлено впоследствии, был проявлением приобретенного ихтиоза.
Рис. 1. Врожденный порок сердца у женщины 58 лет в виде общего желудочка и транспозиции магистральных сосудов.
Fig. 1. Congenital heart disease as the common ventricle and transposition of the great vessels in a 58-year-old woman.
Остальными патологическими находками на вскрытии были геморрагический инфаркт в левом легком размером 2×2 см, «мускатная печень», цианоз слизистых оболочек, культя матки длиной 3 см, отсутствие маточных труб, гематома в левой затылочной доле головного мозга с признаками его дислокации, гиперплазия костного мозга в средней трети бедренных костей (рис. 2).
Рис. 2. Гиперплазия костного мозга в средней трети бедренной кости как компенсация хронической гипоксии.
Fig. 2. Bone marrow hyperplasia in the middle third of the femur as compensation for chronic hypoxia.
Гистологическое исследование подтвердило гиперплазию костного мозга за счет эритроидного ростка с небольшим количеством мегакариоцитов, в легких проявление легочной гипертензии в виде утолщения и гиалиноза ветвей легочных артерий такой степени, которого автору до сих пор наблюдать не приходилось, со скоплением в интиме ксантомных клеток.
Патолого-анатомический диагноз сформулирован следующим образом.
Основное заболевание: врожденный порок сердца — единый желудочек, транспозиция магистральных артерий, общий атриовентрикулярный клапан, двухзаслоночный клапан легочного ствола (масса сердца 790 г, толщина миокарда желудочка 2,1 см).
Сопутствующие заболевания: атеросклероз аорты в стадии липидных пятен и полос. Состояние после надвлагалищной ампутации матки и удаления маточных труб в 1997 г. в связи с внематочной беременностью. Приобретенный ихтиоз кожи голеней и стоп. Выраженный левосторонний сколиоз поясничного отдела позвоночника.
После вскрытия удалось связаться с кардиологом, который наблюдал пациентку последние годы, и выяснить, что врожденный порок был диагностирован сразу после рождения. Матери говорили, что ребенок не доживет до 1 года, потом — до 5 лет. В итоге женщина закончила медицинский вуз, была замужем, до последнего дня работала врачом медико-социальной экспертизы. Уже будучи врачом, написала в берлинскую клинику Шарите, вероятно, относительно возможности хирургического лечения, с ее слов, ей не поверили. В связи с гемоконцентрацией с целью профилактики тромбозов постоянно получала низкомолекулярный гепарин. За несколько дней до поступления в НИИ скорой помощи им. И.И. Джанелидзе была госпитализирована в другой стационар с приступом пароксизмальной фибрилляции предсердий; ритм был восстановлен с помощью электроимпульсной терапии.
Таким образом, у больной с врожденным пороком сердца синего типа в связи с хронической системной гипоксией имелась компенсаторная гиперплазия костного мозга, сопровождавшаяся гемоконцентрацией, в связи с чем больная постоянно получала низкомолекулярный гепарин, прием которого, наиболее вероятно, спровоцировал тяжелую тромбоцитопению. На фоне тромбоцитопении, а также гепаринотерапии у нее развилось кровоизлияние в мозг, приведшее к смерти от отека и дислокации.
При обсуждении летального исхода с коллегами-терапевтами высказано мнение, что у пациентки скорее всего имелась гепарининдуцированная тромбоцитопения [2], обусловившая, казалось бы, парадоксальное в условиях гемоконцентрации кровоизлияние в головной мозг.
Представленное редкое наблюдение еще раз демонстрирует уникальные компенсаторно-приспособительные возможности организма человека.
Авторы заявляют об отсутствии конфликта интересов.
Что значит четырехкамерное сердце

Поиск
Комбинированный врожденный порок сердца – трехкамерное сердце (синдром единого желудочка) с атрезией митрального клапана, дефектом межпредсердной перегородки и высокой легочной гипертензией (случай из практики)
Представлено описание клинического случая редкого врожденного порока сердца — трехкамерное сердце.
Combined congenital heart disease — cor triloculare syndrome (single ventricle) with mitral valve atresia, atrial septal defect and pulmonary hypertension (case report)
It is presented the description of clinical case of rare congenital heart disease — cor triloculare syndrome (single ventricle).
Врожденные пороки сердца (ВПС) по частоте занимают второе место после пороков центральной нервной системы. По данным разных авторов, частота врожденных пороков сердца и крупных сосудов среди новорожденных составляет от 0,2 до 8%. Летальность среди детей первого года жизни с ВПС достигает 30-90%.
На сегодня не существует единой классификации ВПС. По мнению проф. А.С. Шарыкина (2007), это объясняется тем, что существует огромное количество вариантов пороков и их сочетаний, от поставленных исследователями задач меняются принципы, которые кладутся в основу классификации. В классификации, разработанной Институтом сердечно-сосудистой хирургии им. А.Н. Бакулева АМН СССР (Бураковский В.И., Иваницкий А.В., 1992), приводится более 30 ВПС с аномалией отхождения магистральных сосудов, которые распределены в первую очередь с учетом анатомических особенностей, а затем и гемодинамических расстройств. Среди них часто (более 50%) диагностируются комбинированные ВПС.
В нашей практике мы столкнулись с редким случаем комбинированного ВПС: трехкамерное сердце (синдром единого желудочка) с атрезией митрального клапана, вторичный дефект межпредсердной перегородки и высокой легочной гипертензией.
Ребенок Кристина Г., родилась 06.01.10. Вес при рождении 2030 г, рост — 46 см, окружность головы — 30 см. Группа крови матери — (II), ребенка — (III). Находилась на стационарном лечении в детском отделении РКБ № 3, ДРКБ с 13.01.10 по 09.04.10.
Перинатальный анамнез: Девочка родилась в родильном отделении 4-й городской больницы г. Казани. Мать от ребенка отказалась. Ребенок от V беременности. Предыдущие беременности заканчивались родами (2), медицинским абортом и выкидышем на сроке 15-16 недель. В связи с беременностью на учете в женской консультации не состояла, социальный анамнез отягощен: курение, алкоголизм. Экспресс-тест на ВИЧ — отрицателен.
Данные роды преждевременные, на сроке 35 недель, отягощенный акушерский анамнез, задержка внутриутробного развития плода, раннее излитие околоплодных вод. Оценка по Апгар — 7-8 баллов. Предварительный диагноз: синдром дыхательных расстройств I (СДР), ателектазы легких. Недоношенность I степени. Риск внутриутробного инфицирования (ВУИ). Перинатальное поражение центральной нервной системы (ППЦНС), гемолитическая болезнь новорожденного по ABO системе». Состояние в роддоме средней тяжести, стабильное, выслушивается систолический шум. Получала лечение: инфузионную терапию, антибиотикотерапию.
Из 4-й городской больницы ребенок переведен в отделение патологии новорожденных детского отделения РКБ № 3 13.01.10 с диагнозом: СДР, ателектазы легких. Врожденный порок сердца? Метаболическая кардиопатия. Недоношенность I степени.
В детском отделении РКБ № 3 проведено клинико-лабораторное обследование. Клинический диагноз: церебральная ишемия I, ППЦНС. Неонатальная желтуха. Недоношенность I. ВПС? Постгипоксическая ишемия миокарда. Состояние после СДР. Получила: внутривенную инфузию, антибиотики (цефалоспорины, аминогликозид), в/в иммуноглобулин.
19.01 консультация хирурга ДРКБ, диагноз: эпифизарный остеомиелит проксимального эпифиза левой плечевой кости? Абсцесс мягких тканей лобно-теменной области справа. Произведено вскрытие абсцесса, назначено лечение.
22.01 в связи с ухудшением общего состояния, нарастанием дыхательной недостаточности вызван реаниматолог ДРКБ и ребенок реанимационной бригадой переведен в ДРКБ. Клинический диагноз: ВУИ (неуточненной этиологии). Эпифизарный остеомиелит проксимального эпифиза левой плечевой кости. Абсцесс мягких тканей лобно-теменной области справа. Правосторонняя пневмония, ДН II-III степени. Церебральная ишемия II степени. ППЦНС в форме мышечной гипотонии. Абстинентный синдром. ВПС? Недоношенность 35 недель.
С 22.01 по 04.03.10 находилась на лечении и обследовании в отделении реанимации новорожденных ДРКБ, консультирована хирургом, кардиохирургом, кардиологом, проведено посистемное ультразвуковое обследование. На основании результатов обследования был поставлен диагноз: ВПС: Синдром единого желудочка. Гипоплазия левого желудочка, атрезия митрального клапана. Дефект межпредсердной перегородки вторичный. Двойное отхождение сосудов от правого желудочка. Высокая легочная гипертензия. Недостаточность кровообращения II Б степени ВУИ (недифференцированная). Очаговая пневмония на фоне ателектазов легких, тяжелой степени, острое течение, ДН III степени. Энтероколит. Артриты левого плечевого и тазобедренного суставов. Дисплазия левого тазобедренного сустава. Катаральный конъюнктивит. Церебральная ишемия II степени. Синдром пирамидной недостаточности. Анемия смешанной этиологии тяжелой степени. Недоношенность I степени. Постнатальная гипотрофия II степени.
Рекомендовано: осмотр и консультация кардиолога и кардиохирурга ДРКБ через месяц. 04.02.10 поступила в ОНД РКБ № 3 в возрасте 1 месяца 28 дней. Продолжена терапия, назначенная в ДРКБ (инфузионная терапия, дигоксин, верошпирон, капотен). С 04.02 по 12.02 инфузионная и антибактериальная терапия проводились через катетер левой яремной вены, с 12.02 по 17.02 — через периферический доступ.
14.02.10 — состояние с отрицательной динамикой: фебрильная температура, выраженное беспокойство, одышка, ДН II, снижение сатурации до 76%, в крови лейкоцитоз до 36,9 г/л, сдвиг лейкоформулы (п — 18%, с — 64%), токсигенная зернистость нейтрофилов, СРБ — 30 мг/л. На рентгенограмме — правосторонняя пневмония. Назначен в/в сульперацеф, иммуноглобулин. С 17.02.10 — клинико-лабораторно-инструментальная положительная динамика: снизилась активность в крови, на рентгенограмме уменьшились инфильтративные и отечно-застойные изменения в правом легком. Посев крови на стерильность роста микрофлоры не выявил.
При наблюдении ребенка в клинике состояние далее оставалось тяжелым за счет кардиореспираторной недостаточности: НК IIБ, ДН I-II, висцеральных дисфункций. Кожные покровы бледные, с сероватым оттенком. Отмечалась выраженная кислородозависимость. Постоянная оксигенотерапия через носовые канюли. Сатурация в пределах 72-84%, ЧД — 30-62, ЧСС — 138-162, АД — 90/50 мм рт. ст. За 2 недели прибавка в весе 75,0 г. Кормится через зонд по 30,0-35,0 мл смесью «преНАН», усваивает. Живот мягкий, стул ежедневно. Диурез адекватный. Центральный катетер функционирует.
09.04.10 состояние ребенка внезапно резко ухудшилось, усилилась одышка, общее беспокойство, отмечалось снижение показателей сатурации кислород до 40%, падение АД, появилось вздутие кишечника, усилился общий цианоз, появились нарушения ритма дыхания и сердца. Терапия усилена за счет подключения допамина, вводился прозерин, респираторная поддержка с увеличением концентрации кислорода.
В связи с нарастанием брадикардии в/в введен 0,01%-ный раствор адреналина — 1,0. Вызвана бригада реанимации ДРКБ. В связи с остановкой сердца в/в повторно введен р-р адреналина и атропина, терапия — без эффекта. Аппаратная ИВЛ и внутрисердечное введение адреналина признаны нецелесообразными ввиду непредотвратимости летального исхода при данном ВПС. В 14.30 ребенок экзитировал при явлениях легочно-сердечной недостаточности.
Диагноз при направлении на вскрытие: ВПС: Синдром единого желудочка. Гипоплазия левого желудочка, атрезия митрального клапана, дефект межпредсердной перегородки вторичный. Двойное отхождение магистральных сосудов от правого желудочка. Высокая легочная гипертензия. НК II Б стадии. Отек мозга? ВУИ (неуточненной этиологии). Очаговая пневмония на фоне ателектазов легких, острое течение, ДН III степени. Энтероколит. Артриты левого плечевого и тазобедренных суставов Дисплазия левого тазобедренного сустава. Катаральный конъюнктивит. Церебральная ишемия II степени. Синдром пирамидной недостаточности. Анемия смешанной этиологии тяжелой степени. Недоношенность I степени. Постнатальная гипотрофия II степени.
Протокол патологоанатомического вскрытия № 18 от 10.04.2010 г.
3-месячный недоношенный ребенок весом 2030 г и ростом 46 см, гипостенического телосложения, пониженного питания. Кожные покровы и видимые слизистые оболочки бледно-синюшные. Мягкие ткани головы и кости черепа без изменений. Мягкие оболочки головного мозга отечны.
Плевральные полости свободны, легкие слегка поджаты к позвоночнику, вес правого легкого 80 г, левого легкого — 64 г; легочная ткань плотноватой консистенции, на разрезе темно-красного цвета (вырезанные кусочки легких тонут в воде).
Сердце (вес 36 г) — отмечено увеличение правого желудочка (толщина его стенки 0,6 см, толщина миокарда левого желудочка — 0,2 см), дефект межпредсердной перегородки (0,2 х 0,3 см), полностью отсутствует межжелудочковая перегородка (трехкамерное сердце); выявлено полное заращение митрального отверстия и атрезия клапанов легочной артерии со стенозом ее устья (периметр легочной артерии — 2,0 см). Выявлено незаращение артериального протока.
Печень (вес 126 г) увеличена, поверхность гладкая, на разрезе красно-коричневой окраски с сероватыми участками. Селезенка (вес 20 г) увеличена, капсула гладкая, пульпа темно-красного цвета. Почки (вес 22 г) — капсула гладкая, поверхность дольчатая, граница между слоями сохранена.
Надпочечники, поджелудочная железа, желудочно-кишечный тракт и вилочковая железа без видимых изменений.
Гистологическое исследование
Легкие — выраженное полнокровие межальвеолярных перегородок, очаги ателектазов и геморрагических инфарктов, артериосклероз в ветвях легочной артерии.
Сердце — интерстициальный отек и очаги фрагментации мышечных волокон, эндокард правого желудочка резко утолщен и склерозирован, что свидетельствует о фиброэластозе. Легочная артерия — выраженное утолщение и фиброз интимы.
Головной мозг — гиперемия и стазы в сосудах, периваскулярный отек.
Печень — гиперемия в центральных венах и синусоидах, мелкокапельная жировая дистрофия в гепатоцитах.
Патологоанатомический диагноз
Комбинированный врожденный порок сердца: трехкамерное сердце (синдром единого желудочка), заращение митрального клапана. Дефект межпредсердной перегородки. Легочная гипертензия (синдром Эйзенменгера). Атрезия клапанов легочной артерии и фиброэластоз эндокарда правого желудочка. Незаращение артериального протока. Ателектатическая и отечно-геморрагическая формы пневмопатии с очагами геморрагических инфарктов в легких, артериолосклероз в ветвях легочной артерии с развитием гипертензии в малом круге кровообращения. Отек головного мозга. Общая гипотрофия.
Таким образом, нами описан сложный комбинированный врожденный порок сердца: трехкамерное сердце (синдром единого желудочка — отсутствие межжелудочковой перегородки) в сочетании с дефектом межпредсердной перегородки, стеноз легочной артерии, вторичная гипертрофия правого желудочка) и синдромом Эйзенменгера (легочная гипертензия). Следует отметить, что атрезии клапанов и стенозу легочной артерии сопутствовал выраженный фиброз интимы этого сосуда на всем его протяжении вплоть до мелких ветвей и фиброэластоз эндокарда правого желудочка. Кроме того, имело место заращение левого атриовентрикулярного отверстия и незаращение артериального протока.
Вопрос о происхождении столь необычного порока сердца у данного ребенка остается открытым, однако, учитывая социальный анамнез женщины, не исключается, что речь может идти о ВПС в рамках алкогольной эмбриофетопатии. Известно, что этанол оказывает не только соматогенное и гаметогенное влияние, но также обладает выраженным эмбриотоксическим действием. Являясь женщиной из группы социального риска, мать ребенка во время беременности не прошла облигатного ультразвукового мониторинга, что не позволило уже внутриутробно диагностировать неоперабельный ВПС и решить вопрос о прерывании беременности.
К.М. Абдрашитов, Н.Н. Архипова, С.А. Золотоносова, В.П. Нефедов,
Д.Р. Салманидина, Л.Г. Хисамова, Э.М. Шакирова
Республиканская клиническая больница № 3 МЗ РТ
Казанская государственная медицинская академия
Нефедов Валерий Петрович — кандидат медицинских наук, доцент, зав. патологоанатомическим отделением РКБ 3 МЗ РТ
Что значит четырехкамерное сердце

ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА ПОРОКОВ СЕРДЦА, ТЕЧЕНИЕ БЕРЕМЕННОСТИ, КЛИНИЧЕСКИЕ СЛУЧАИ СОЧЕТАНИЯ КАРДИАЛЬНОЙ ПАТОЛОГИИ ПЛОДА С АНОМАЛИЯМИ ДРУГИХ ОРГАНОВ
Сердечная патология является одной из основных причин детской смертности и находится на втором месте среди причин младенческой смертности. Частота составляет 8 случаев на 1000 новорожденных [1, 2].
Неблагоприятный прогноз для жизни представляют сложные врожденные пороки сердца (ВПС). Под термином «сложный» понимают такие сердечные аномалии, как гипоплазированные камеры сердца, атрезии клапанов, аномальное отхождение магистральных сосудов, единственный желудочек, то есть изменения в сердце, при которых невозможно выполнить полную хирургическую коррекцию [3].
Критические пороки сердца, требующие хирургического вмешательства в ранний неонатальный период, составляют 25 % от всех врожденных сердечных аномалий. В первую неделю умирает 29 % новорожденных, к концу первого года жизни – 87 % [4].
Первое ультразвуковое скрининговое обследование (11–13 недель) является важным осмотром. В случае обнаружения увеличения толщины воротникового пространства, отклонения сердечной оси, рекомендуется расширенное обследование сердца (фетальная эхокардиография). При рутинном ультразвуковом исследовании лишь в 40 % выявляются пороки сердца у плодов, при том что детальный осмотр позволяет выявлять до 90 % сердечных пороков внутриутробно. Для своевременного выявления врожденных пороков сердца необходимо детально обследовать сердце плода ультразвуковым методом при втором скрининговом обследовании (18–22 недели) [5, 6].
Применяя фетальную эхокардиографию, возможно определить структуру порока и спрогнозировать исход для плода [7]. Особенно это касается сложных пороков сердца, так как имеет место позднее выявление патологии, при осмотре неонатологом в родильном доме или после выписки домой [8].
Данная тема является актуальной. Врачи пренатальной диагностики встречаются с трудностями точного определения структуры сердечных пороков, что связано с большой вариабельностью кардиальной аномалии у плодов.
Задачей врачей-гинекологов является правильная тактика ведения беременной после установки диагноза, так как своевременная хирургическая помощь спасает жизни детей и влияет на качество дальнейшей жизни.
Цель исследования: проанализировать течение беременности при выявлении кардиальной патологии у плодов, определить точность внутриутробной диагностики, описать случаи сочетания сердечных пороков с патологией развития других органов плода.
Материалы и методы исследования
В центре диагностики матери и плода «Family» г. Бишкек с января 2019 г. по ноябрь 2020 г. было осмотрено 48 беременных женщин с пороками сердца плода, требующими хирургической коррекции после рождения. Всем новорожденным было проведено эхокардиографическое обследование после родов врачами-кардиологами для уточнения структуры пороков. В случаях прерывания беременности, для подтверждения диагноза проводилось патологоанатомическое вскрытие.
Осмотр беременных выполнялся на ультразвуковых аппаратах General Electric (GE) Voluson E8 и E10, c использованием программы fetal heart. Также использовалась программа STIC (постобработка снимков, полученных в режиме объемного сканирования), основным являлся двумерный режим с цветовым и импульсным доплеровским картированием. У всех пациентов было получено информированное согласие на участие в нашем исследовании. Результаты были обработаны путем вычисления относительных величин (в %).
Результаты исследования и их обсуждение
Среди 48 плодов с ВПС сложные пороки сердца были в 40 случаях (83,3 %). Из общего количества умерли после родов 23 ребенка (47,9 %). Прервали беременность 3 женщины (6,2 %), в двух случаях проводилось патологоанатомическое вскрытие плодов. Третья беременная после заключения медицинской комиссии прервала беременность в сроке 31 неделя, в связи с плохим прогнозом для жизни ребенка. Диагноз был подтвержден методом эхокардиографии.
Из факторов риска, по анализам обменных карт, острые респираторные вирусные инфекции (ОРВИ) до 12 недели перенесли 14 женщин (29,1 %), ОРВИ во втором триместре перенесли 4 женщины (8,3 %). Анемия легкой степени имела место в 12 случаях (25,0 %), хроническая ревматическая болезнь сердца у матери – один случай (2,0 %). Многоплодные беременности как фактор риска в нашем случае встречались в двух случаях (4,1 %), обе дихориальные, диамниотические двойни.
Количество плодов мужского пола составило – 31 (64,5 %), женского 17 (35,4 %). Маловесными (вес менее 2600 г.) родились 9 детей (18,7 %), из них 8 имели сочетание порока сердца с ненормальным развитием других органов, в одном случае порок сердца был изолированным.
При ультразвуковом исследовании фетоплацентарное нарушение кровотока 1 степени выявлено у одной беременной (2,0 %), задержка внутриутробного развития у 4 (8,3 %), маловодие у 2 (4,1 %), многоводие у 5 (10,4 %), причем избыточное количество вод во всех случаях сочеталось с множественными пороками развития.
Сложности при ультразвуковом осмотре вызывали неправильное положение плода, большой срок гестации (после 35 недель), многоводие, маловодие. Необходимо отметить, что технология STIC информативна при осмотрах четырехкамерной проекции сердца (пороки атривентрикулярных клапанов, гипоплазии желудочков, дефекты межжелудочковой перегородки). Для осмотра выходных трактов желудочков, особенно при повороте оси сердца, осмотр в двумерном режиме является предпочтительным. Также для осмотра органов других систем маловодие и неудобное положение плода являются помехами для трехмерного ультразвука.
Структура выявленных пороков оказалась многообразна. Нами были диагностированы: у 5 плодов (10,4 %) двойное отхождение сосудов от правого желудочка, аномалия Эбштейна – 1 (2,0 %), транспозиция магистральных сосудов – 3 (6,2 %), стеноз легочной артерии – 7 (14,5 %), изолированный перимембранозный дефект межжелудочковой перегородки – 3 (6,2 %), декстрапозиция аорты с дефектом межжелудочковой перегородки – 5 (10,4 %), атрезия легочной артерии – 4 (8,3 %), атриовентрикулярный канал –5 (10,4 %), тетрада Фалло – 6 (12,5 %), перерыв дуги аорты – 1 (2,0 %), атрезия трикуспидального клапана – 1 (2,0 %), атрезия митрального клапана – 4 (8,3 %), из них в двух случаях аортальный клапан был атрезирован, также в двух случаях имелось двойное отхождение сосудов от правого желудочка. Коарктация аорты составила один случай (2,0 %), единственный желудочек – 2 (4,1 %).
После рождения вскрытие проводилось в одном случае – ребенку с аномалией Эбштейна, который умер в родильном доме на вторые сутки. Согласно заключению патологоанатома, причиной смерти стала острая сердечная недостаточность, дилатация полостей сердца, острый венозный застой внутренних органов.
В двух случаях единственного желудочка диагностика оказалась затруднительной как внутриутробно, так и после родов. В первом случае трикуспидальный клапан был атрезирован и полость правого желудочка практически отсутствовала, также имелся единый сосуд, исходящий из функционально единого желудочка. После родов рекомендовалась компьютерная томография для уточнения диагноза. При телефонном разговоре с матерью мы узнали, что в возрасте 10 месяцев ребенок еще не прошел полного обследования, но в развитии значительно отставал, не мог переворачиваться и самостоятельно не сидел.
Во втором случае мы диагностировали правосформированное, праворасположенное сердце в сочетании с единым атриовентрикулярным клапаном, двойным отхождением сосудов от правого желудочка, ребенок умер в первый месяц жизни.
Среди плодов с кардиальной патологией в 6 случаях (12,5 %) было сочетание с хромосомными аберрациями и генетическим заболеванием: синдромом Дауна – 4 случая, синдромом Ди Джорджи – один случай; также наблюдался один случай редкой генетической патологии (синдром Холта – Орама, наследственное заболевание, сочетание порока сердца с отсутствием первого пальца на кистях обеих рук до аплазии лучевой кости).
После родов успешно прооперированы были двое детей с тетрадой Фалло, также двое детей со стенозом клапана легочной артерии. Один ребенок с диагнозом двойного отхождения сосудов от правого желудочка благополучно оперирован в Турции. К сожалению, в случаях транспозиции магистральных сосудов и единственного желудочка детям было отказано в проведении оперативного лечения как местными, так и зарубежными хирургами в связи с высоким риском смерти сразу после операции.
Приводим наблюдение о несовпадении нашего диагноза с эхокардиографическим заключением после родов. В нашем центре при плановом обследовании на 30 неделе беременности был установлен диагноз коарктации аорты с дефектом межжелудочковой перегородки. В родильном доме при проведении эхокардиографии был выявлен только дефект мышечной перегородки, коарктация была исключена. Ребенок умер через 2 недели после родов, от вскрытия родители отказались. Мы пришли к выводу, что портативные ультразвуковые аппараты, на которых обследуют детей в родильных домах, могут вызывать сложности визуализации и неполную диагностику, что связано с менее четким изображением, чем на стационарном оборудовании.
По данным литературы, внутриутробная диагностика пороков сердца возможна с 13 недели беременности, в частности таких сложных для выявления ВПС, как атрезия легочной артерии [9]. В нашем центре плод с атрезией легочной артерии и дефектом межжелудочковой перегородки был выявлен в 18 недель беременности. Данная беременность была прервана в связи с неблагоприятным прогнозом для жизни. Патологоанатомическое вскрытие подтвердило диагноз. По нашему мнению, 18 неделя беременности (второе скрининговое обследование) является наиболее ранним сроком для точного определения структуры порока. Связано это с тем, что магистральные сосуды сердца плода плохо видны в сроки первого скринингового обследования, что может приводить к неточной диагностике.
Из 48 случаев с ВПС 16 плодов (33,3 %) имели множественные пороки развития, причем такие изменения, как гидроцефалия, укорочение трубчатых костей, выявлялись на сроках после 30 недель. А случаи атрезии ануса были обнаружены только при рождении детей. Таким образом, выявление любых изменений в сердце является поводом для обязательного повторного ультразвукового обследования в сроки 25–30 недель (таблица).
Сочетание врожденных пороков сердца с аномалиями других органов
Название порока сердца
Сочетание ВПС с патологией других органов
Сроки выявления ВПС (неделя беременности), исход
1. Перимембранозный дефект межжелудочковой перегородки