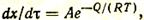Что делает металл при нагреве
Нагрев металлов перед ковкой является важной и ответственной операцией, от которой во многом зависит не только качество будущих деталей, но также производительность труда, работа оборудования, стойкость инструмента и себестоимость продукции.
В процессе нагрева изменяется строение металла, его свойства, состояние поверхностных слоев и др. Каждый сплав имеет температурный интервал обработки давлением и определенный режим нагрева. Нарушение указанных параметров нагрева ведет к снижению качества деталей, а возможно и к разрушению металла. Поэтому для будущего специалиста необходимо изучение явлений, происходящих в металле при нагревании.
Влияние усадки на форму и размеры поковки особенно сказывается при ковке заготовок деталей сложной формы с длинными отростками, так как усадка может привести к сильному короблению поковки. Очень важно учитывать усадку металла при изготовлении рабочих ручьев штампов для объемной штамповки, особенно при точной объемной штамповке дорогостоящих сплавов.
Образование окалины ведет к потерям металла, увеличению припусков на механическую обработку, снижает производительность труда и, являясь твердым веществам, снижает стойкость инструмента при обработке давлением и обработке резанием.
Неравномерность нагрева и выравнивание температуры по сечению заготовки. Прогрев заготовки по сечению осуществляется за счет теплопередачи от наружных слоев к внутренним. Чем меньше коэффициент теплопередачи металла, больше скорость нагрева* и площадь поперечного сечения заготовки, тем больше разность температур между наружными и внутренними слоями заготовки. Под действием высокой температуры наружные слои расширяются больше внутренних и между ними возникают большие напряжения, которые могут привести даже к разрушению. Большинство заготовок из углеродистых конструкционных сталей сечением до 100 мм «не боится» быстрого нагрева и поэтому их можно закладывать холодными в печь с температурой до 1300’С.
Высокоуглеродистые и высоколегированные стали и многие сложные сплавы имеют низкую теплопроводность и во избежание образования трещин требуют медленного нагрева. Такие стали и сплавы загружают сначала в печь, имеющую невысокую температуру, некоторое время выдерживают при этой температуре и только после прогрева всего сечения начинают дальнейший подъем температуры.
После того как наружные слои заготовки нагреются до ковочной температуры, заготовки оставляют еще некоторое время в печи для выравнивания температуры металла по всему сечению. Это время называется временем выдержки.
Ковать неравномерно нагретую заготовку опасно из-за неравномерной по его сечению деформации металла и возможного его разрушения. При объемной штамповке и ковке в подкладных штампах неравномерный нагрев приводит к незаполнению рабочего ручья штампа и к снижению стойкости инструмента.
Аналогично нагреву охлаждение поковок из легированных сталей также должно выполняться с небольшой скоростью. При быстром охлаждении возникают термические напряжения, из-за которых могут появиться трещины в поковках и привести к браку.
* Скорость нагрева представляет собой увеличение температуры заготовки в единицу времени (за одну минуту или за один час, ‘С/ч).
С понижением температуры растворимость углерода в Fey уменьшается.
* В цементите углерода содержится 6,67%.
При 723С выпадает такое количество цементита, что концентрация углерода в аустените составит 0,8%. В доэвтектоидных сталях (С
Явления, происходящие в металле при нагреве,



И режимы нагрева
При нагревена поверхности заготовок образуется слой оксидов, Называемый окалиной,толщина которого зависит от температуры и времени нагрева, состава печной атмосферы, химического состава сплава и расположения заготовок в печи. Наиболее интенсивно сплавы окисляются при температуре 900. 1200 °С.
Нагрев углеродистых сталей приводит также к выгоранию углерода поверхностного слоя на глубину до 2 мм. Уменьшение содержания углерода, называемое обезуглероживанием,ведет к снижению прочности и твердости стали. Особенно вредно обезуглероживание для заготовок небольших размеров, имеющих малые припуски на механическую обработку и подвергаемых последующей закалке.
Для уменьшения окалинообразования и обезуглероживания применяют нагрев в защитной атмосфере или вакууме, скоростной нагрев, защитные засыпки и обмазки, наносимые на заготовки перед нагревом.
Высокоуглеродистые и высоколегированные стали и многие сложные сплавы, имеющие низкие теплопроводность и пластичность, во избежание трещин требуют медленного нагрева. Заготовки из таких сталей и сплавов загружают в печь при невысокой температуре, выдерживают при этой температуре для равномерного прогрева заготовки по всему объему и затем повышают температуру печи. Крупные слитки из легированных сталей при нагреве подвергают нескольким выдержкам при различных температурах.
Выбор режима нагрева перед обработкой давлением заключается в определении рационального температурного интервала (температур начала и конца обработки) и времени нагрева. Нижняя граница температурного интервала обработки давлением стальных заготовок превышает 727 °С, а верхняя должна быть на 100. 150 °С ниже температуры начала плавления. При нагреве до более высоких температур в металле появляются два вида дефектов — перегрев и пережог. При перегреверазмеры зерен увеличиваются, пластичность уменьшается и ухудшаются механические свойства. Этот вид брака можно для некоторых сталей устранить дополнительной обработкой давлением и нормализацией.
Пережог— окисление металла по границам зерен при нагреве до температур, близких к температуре плавления. В результате связь между зернами нарушается и металл при обработке. давлением разрушается. Пережог является неисправимым браком.
Температурный интервал обработки зависит от марки обрабатываемого сплава. Для сталей температуру начала и конца обработки давлением можно определить по диаграмме Fe-C (рис. 16.9). Из диаграммы видно, что низкоуглеродистые стали имеют широкий (до 500 °С) температурный интервал обработки.
 Рис. 16.9.Диаграмма состояния Fe—С: 1 — пережог; 2 — перегрев; 3 — область горячей обработки давлением Рис. 16.9.Диаграмма состояния Fe—С: 1 — пережог; 2 — перегрев; 3 — область горячей обработки давлением |
Время нагрева определяют исходя из двух противоречивых требований. С одной стороны, с целью уменьшения образования окалины и повышения производительности необходимо сократить время нагрева, увеличив его скорость, с другой (во избежание образования трещин) — уменьшить скорость нагрева и увеличить его продолжительность. Последнее особенно важно для заготовок большого сечения из высоколегированных сплавов. Для заготовок из углеродистых сталей сечением до 100 мм 2 допускается высокая скорость нагрева и их можно загружать холодными в печь, имеющую температуру 1300 °С.
Время нагрева Т (ч) в этом случае можно определить по формуле Н.Н. Доброхотова
гдеk— коэффициент, зависящий от марки стали (для углеродистых и низколегированных сталей fe = 10, для высокоуглеродистых и высоколегированных сталейk— 20);D— диаметр или сторона квадрата заготовки, м; а — коэффициент, учитывающий способ укладки заготовок в печи (рис. 16.10). Чем плотнее уложены заготовки в печи (меньше расстояние I), тем больше коэффициент а и длительнее нагрев заготовок.
Заготовки из высоколегированных сталей нагревают в два этапа из-за возможного их разрушения в результате возникновения термических напряжений при большой скорости нагрева:
а = 1,25
Рис. 16.10.Влияние способа укладки заготовок в печи на коэффициент а

сначала их медленно подогревают до 650 °С, а затем, когда Пластичность сплава увеличивается, окончательно нагревают с большой скоростью до температуры горячей пластической деформации. Общее время нагрева составляет т-т1 +т2,где Т, и Т2 — время соответственно первого и второго этапов нагрева:
Процесс охлаждения(особенно заготовок из легированных сталей) при обработке давлением является ответственной технологической операцией, которая при неправильном выполнении может привести к браку, так как при охлаждении трещины в заготовках образуются чаще, чем при нагреве. Скорость охлаждения не должна превышать допустимых значений. Заготовки из низко- и среднеуглеродистых сталей можно охлаждать на воздухе поштучно или группами на стеллажах. Крупные поковки из легированных сталей охлаждают медленно вместе с печью, давая выдержки по нескольку часов при определенных температурах. Цикл охлаждения заготовок зависит от их химического состава и размеров и для крупных поковок может длиться несколько суток.
Превращения, происходящие в железе и стали при нагреве и охлаждении
Строение стали
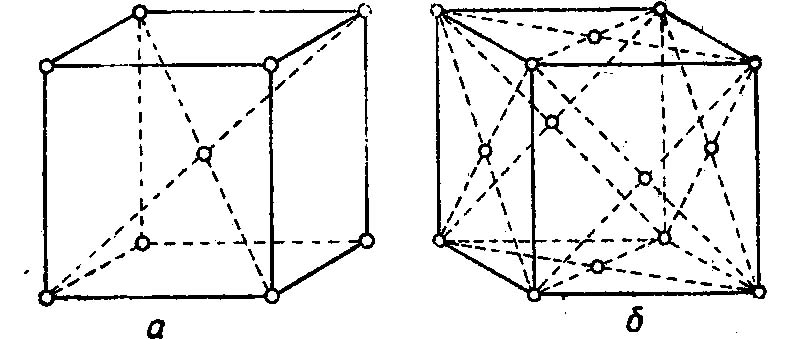
Внимательно всмотревшись в излом металла, ясно можно увидеть, что он представляет собой нагромождение (совокупность) отдельных кристаллов (зерен), крепко сцепленных между собой. Мельчайшей частицей металла, как и всякого другого вещества, является атом. В элементарных ячейках, из которых состоят кристаллы железа, атомы расположены в определенном порядке. Это расположение изменяется в зависимости от температуры нагрева. При любой температуре ниже 910° атомы в ячейках кристаллов располагаются в виде куба, образуя так называемую кристаллическую решетку альфа-железа. В этом кубе восемь атомов расположены в углах решетки и один в центре.
При нагреве свыше 910° происходит перегруппировка атомов и кристаллическая решетка представляет собою форму куба с четырнадцатью атомами; условно ее называют решеткой гамма-железа. При температуре 1390° решетка гамма-железа перестраивается в решетку с девятью атомами, носящую название дельта-железо. Эта решетка отличается от решетки альфа-железа несколько большим расстоянием между центрами атомов и сохраняется до момента расплавления железа, т. е. до 1535° (Рис. 1).
Перестройка кристаллической решетки при медленном охлаждении происходит в обратном порядке: дельта-железо при 1390° превращается в гамма-железо, а гамма-железо при 898° превращается в альфа-железо.
Рис. 1. Строение кристаллической решетки: а — альфа и дельта железа; б — гамма железа.
Критические точки превращения
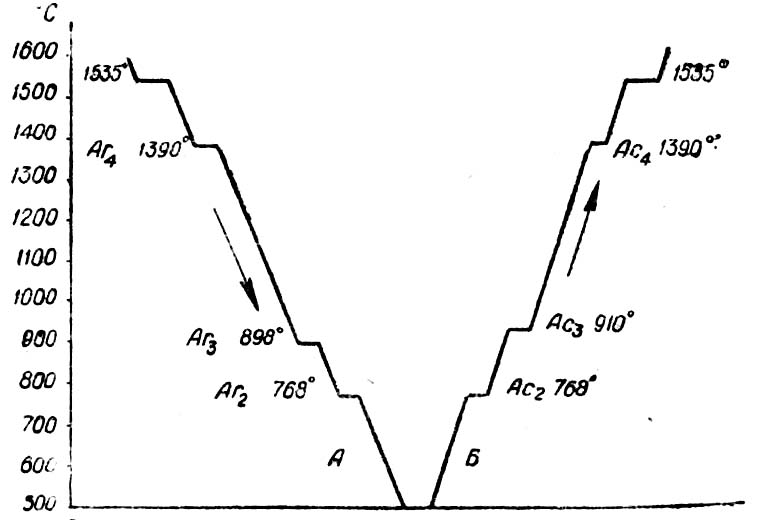
На рис.2 показаны кривые охлаждения и нагревания чистого железа. Как видно из этих кривых, в процессе перестройки одной решетки в другую, а также при расплавлении и затвердевании железа происходят температурные остановки, являющиеся результатом выделения дополнительного количества тепла при охлаждении и поглощении дополнительного количества тепла при нагревании.
Рис. 2. Кривые охлаждения и нагрева чистого железа.
Температурные остановки, при которых происходят перестройки решеток, называются критическими температурами или критическими точками и обозначаются Аrпри охлаждении и Ас при нагревании. В точках Аr2и Ас2,не происходит перестройка атомной решетки, а изменяются магнитные свойства железа. При температуре выше 768° железо теряет способность притягиваться магнитом. При очень малой скорости нагревания и охлаждения критические точки А с3и Аr3не совпадают друг с другом на 12°. При увеличении скорости охлаждения несовпадение критических точек увеличивается, так как температура значительно снижается и железо переохлаждается. Это явление, носит название гистерезис.
При нагревании и охлаждении стали происходит также перестройка атомной решетки, но температуры критических точек не постоянны. Они зависят от содержания углерода и легирующих примесей в стали, а также от скорости нагревания и охлаждения.
На рис. 3 представлена диаграмма состояния углеродистой стали при медленном охлаждении и нагревании.
Рис.3. Диаграмма состояния углеродистых сталей.
Структура стали
Структурой стали называется внутреннее ее строение. Углерод в стали находится в виде химического соединения с железом, и это соединение называется — цементит. Кроме цементита, в стали имеется феррит, представляющий собой почти чистое железо. В зависимости от содержания углерода большая или меньшая часть феррита находится в механической смеси с цементитом, образуя новую структуру — перлит. Если небольшой кусок металла прошлифовать, отполировать и протравить в специальном реактиве, то под микроскопом можно различить структуры. Ниже приводится описание структур железоуглеродистых сплавов.
Аустенит представляет собою твердый раствор углерода и других элементов в гамма-железе. Наибольшее содержание углерода, которое может раствориться в ау-стените — это 2%. Аустенит образуется при затвердевании жидкой стали и при нагреве твердой стали выше критических температур.
В обычных сталях аустенит устойчив только лишь при температуре выше критических точек. При охлаждении, даже самом быстром, с этих температур аустенит превращается в другие структуры. При комнатной температуре аустенит полностью сохраняется в ряде марок нержавеющих сталей, в высокомарганцовистой стали и в незначительном количестве остается при закалке некоторых марок инструментальной и конструкционной сталей.
Аустенит мягок, пластичен, тягуч, мало упруг. Твердость его по Бринелю находится в пределах 170—220.
Аустенит немагнитен, обладает невысокой электропроводностью.
Феррит представляет собой твердый раствор углерода и других элементов в альфа-железе. Наибольшее содержание углерода, которое может раствориться в феррите, это 0,04%. Феррит устойчив при температурах ниже критической точки AC1. Он выделяется из аустенита при медленном охлаждении последнего ниже A6i. Феррит мягок, сильно тягуч. Твердость HB= 60—100. Феррит магнитен до 768°. Свыше этой температуры он теряет магнитные свойства.
Цементит представляет собой химическое соединение железа с углеродом Fe3C—карбид железа. Цементит содержит углерода 6,67%. Выделяется из жидкого и твердого раствора при медленном охлаждении. Цементит весьма тверд и хрупок. Твердость его НB= 800—820. Он магнитен до 210°. Выше этой температуры цементит теряет магнитные свойства.
Перлит представляет собой механическую смесь феррита и цементита. Он образуется из аустенита при медленном его охлаждении. Температура превращения аустенита в перлит 723°С. При весьма медленном переходе через эту температуру цементит образуется в виде зерен (глобулей), и тогда перлит называется зернистым. При более быстром охлаждении цементит приобретает форму пластинок, и такой перлит называется пластинчатым. При весьма быстром охлаждении в результате значительного переохлаждения аустенита вместо перлита получаются другие структуры, о которых речь будет ниже.
Перлит магнитен, прочен и пластичен. Твердость его находится в пределах от 160 до 230 кг/мм 2 по Бринелю. При обработке резанием наиболее чистую поверхность дает структура зернистого перлита.
Мартенсит образуется в результате весьма быстрого охлаждения (закалки) аустенита. При быстром охлаждении успевает произойти перестройка кристаллической решетки гамма-железа в решетку альфа-железа, выделение же углерода в карбид железа не успевает произойти, и он весь остается растворенным в решетке альфа-железа. Так как нормально альфа-железо может растворить в себе не более 0,04% углерода, то такой раствор называют пересыщенным. Он отличается весьма большой твердостью (свыше Rc= 60) и хрупкостью. Следует указать, что решетка альфа-железа, получающаяся в результате закалки, имеет искаженную форму. Так, размеры ее граней не одинаковы — в одном направлении они удлинены за счет других (см. рис. 4). Такая решетка называется тетрагональной. Чем больше в стали углерода, тем больше тетрагональность решетки и тем более велики внутренние напряжения. При нагревании до температур 100—200° тетрагональность мартенсита уменьшается, форма кристаллической его решетки приближается к форме правильного куба, и вместе с этим уменьшаются внутренние напряжения. Мартенсит магнитен.
Рис. 4. Строение кристаллической решетки стали, закаленной на мартенсит.
Троостит представляет собой высокодисперсную (мелкораздробленную) смесь феррита и карбидов. Он образуется при охлаждении аустенита с замедленной против закалки скоростью или в результате нагрева (отпуска) мартенсита в пределах 250—400°.
При нагреве закаленной стали происходит постепенное выделение углерода из кристаллической решетки с образованием карбидов. Троостит менее прочен, более пластичен, чем мартенсит. Твердость его НB330—400. При охлаждении аустенита в горячих средах в интервале 250—400° (изотермическое превращение аустенита) происходит образование игольчатого троостита, несколько более прочного, чем обычный троостит.
Сорбит представляет собой дисперсную смесь феррита и карбидов. Он образуется при охлаждении аустенита с небольшой скоростью или при нагреве (отпуске) мартенсита до 400—650°. Карбиды сорбита более крупные, чем троостита. Сорбит пластичен, вязок и магнитен. Твердость НВ 270—320.
Ледебурит представляет собой эвтектическую смесь аустенита и цементита. Он содержит углерода 4 3% Образуется ледебурит при затвердевании жидкого сплава с содержанием углерода свыше 2%. Ледебурит хрупок.
На рис. 5. представлены фотоснимки структур стали с различным содержанием углерода.
Структура стали с содержанием углерода 0,83% состоит из сплошного перлита и называется эвтектоидной; при меньшем содержании углерода структура стали состоит из перлита и феррита и носит название доэвтектоидной, а при большем содержании углерода — из перлита и цементита и называется заэвтектоидной. Температура 723°, при которой перлит переходит в аустенит, также называется критической и обозначается Ас.
Для того чтобы доэвтектоидную и эвтектоидную сталь полностью отжечь, нормализовать или закалить, их нужно нагреть до такой температуры, при которой они перешли бы в аустенитное состояние.
Рис. 5. Микроструктура отожженной углеродистой стали:
Превращения, происходящие в стали при нагревании
По диаграмме на рис. 3 можно проследить за изменениями структуры трех разных марок стали при нагревании:
Линия на диаграмме, обозначенная буквами GS, соответствует окончанию растворения феррита в аустените в доэвтектоидных сталях, а линия SE соответствует окончанию растворения цементита в аустените в заэвтектоидных сталях.
Следует указать, что заэвтектоидные стали при операциях термической обработки не нагревают выше линии Аcт(такая высокая температура нагрева приведет к перегреву и ухудшению свойств стали), а ограничиваются нагревом выше первой критической точки ACl, что полностью обеспечивает получение необходимых свойств.
Превращения, происходящие в стали при медленном охлаждении
В сталях, нагретых до аустенитного состояния, при весьма медленном охлаждении произойдут обратные превращения, а именно:
а) в стали с содержанием углерода 0,83% аустенит превратится в перлит;
б) в стали с содержанием углерода 0,4% сначала из аустенита начнет выделяться феррит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит и
в) в стали с содержанием углерода 1,2% сначала из аустенита выделится цементит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит.
Даже при весьма медленном охлаждении температура распада аустенита не совпадает с теми температурами, при которых аустенит образовался при нагревании. Чем скорость охлаждения больше, тем больше становится гистерезис, т. е. разница между критическими температурами (точками) при нагревании и охлаждении.
Превращения, происходящие в стали при быстром охлаждении
Рис. 6. Микроструктура закаленной стали:
а — игольчатый мартенсит;
В легированных сталях, благодаря присутствию специальных элементов, для образования мартенсита не требуется столь большой скорости охлаждения, как для углеродистых сталей, и мартенсит образуется при охлаждении в масле, а для быстрорежущих сталей — и при охлаждении на воздухе.
Троостит и сорбит можно получить не только в результате ускоренного охлаждения, нои путем нагрева закаленной стали, имеющей структуру мартенсита, до температуры ниже Aс1, т. е. путем отпуска стали. В этом случае троостит получается при нагреве стали до 400°, а сорбит—при нагреве до 650°. При нагреве до промежуточных температур получаются смешанные структуры: при нагреве от 250—400° — мартенсит и троостит и при нагреве от 400—650° — троостит и сорбит. В производственных условиях троостит и сорбит получают путем отпуска закаленной стали.
Превращения, происходящие в стали при охлаждении в среде, имеющей температуру выше 200° (изотермическое превращение)
Если деталь, нагретую выше критической точки, поместить в среду, имеющую температуру от 700 до примерно 200°, и выдержать в ней до выравнивания температуры по всему сечению, то аустенит превратится в ту структуру, которая соответствует превращению при данной температуре.
О поведении стали при изотермической обработке, выборе температуры и времени выдержки судят по кривым изотермического превращения, построенным для разных марок стали.
Рис. 7. Диаграмма изотермического превращения аустенита углеродистой стали.
На рис. 7 дан вид диаграммы изотермического превращения в стали. На горизонтальной оси отложено время начала и конца превращения, а на вертикальной— температура, при которой оно происходит. Линия А с соответствует переходу аустенита в перлит, а линия Мн — образованию мартенсита из аустенита. На кривой I начинаются, а на кривой II заканчиваются структурные превращения.
Если углеродистую инструментальную сталь, нагретую до 800°, поместить в масло, расплавленную соль или щелочь при температуре 250°, в ней образуется игольчатый троостит с высокой твердостью Rc=45—55. Если эту же сталь охладить в среде, имеющей температуру свыше 600°, в ней образуется перлит и такая сталь легко обрабатывается на станках. При охлаждении стали в среде с промежуточными температурами образуются структуры троостита и сорбита с соответствующей твердостью.
Изотермический отжиг нашел большое применение при термической обработке инструментальных сталей как процесс, резко уменьшающий время по сравнению с другими видами отжига.
Изотермическая закалка в инструментальном деле применяется редко из-за недостаточной для инструмента твердости, достигаемой при этом процессе.
Источник:
Остапенко Н.Н.,Крапивницкий Н.Н. Технология металлов. М. Высшая школа,1970г.
Каменичный И.С. Практика термической обработки инструмента. Киев, 1959 г.
Глава ІІІ НАГРЕВ МЕТАЛЛА
Окисление и обезуглероживание стали
Общие сведения
Нагрев металла — это процесс либо предшествующий обработке металла давлением (прокатке, ковке), либо являющийся частью основного процесса термической обработки металла. Нагрев металла имеет важное значение, так как от его качества зависят качество конечной продукции и работа прокатного (кузнечного) оборудования. Нагрев металла проводят по определенной технологии, характер которой зависит от цели нагрева.
Процесс нагрева металла сопровождается некоторыми нежелательными явлениями, из которых наиболее характерными являются его окисление (угар) и обезуглероживание.
Необходимо отметить, что время нагрева, являющееся важным фактором технологии нагрева, определяет основные размеры рабочего пространства нагревательных печей.
Нагрев стали в печах прокатных, кузнечных и некоторых термических цехов проводят в атмосфере продуктов сгорания топлива. При этом происходит взаимодействие окружающих нагреваемую сталь газов с железом, углеродом и легирующими элементами, которое приводит к окислению и обезуглероживанию ее поверхности.
Вследствие окисления возникают невозвратимые потери металла, составляющие при каждом нагреве от 1—2 (в термических печах) до 5% (в кузнечных печах). При этом увеличивается также трудоемкость последующей обработки изделий в связи с необходимостью удаления образовавшейся окалины. Повышенная твердость окалины вызывает более быстрый износ инструментов и увеличение брака при ковке и прокатке. Вследствие того что окалина по сравнению со сталью имеет меньшую теплопроводность, время нагрева металла в печах увеличивается, что приводит к снижению их производительности при прочих равных условиях; осыпающаяся окалина образует шлаковые наросты на
поду печей и вызывает необходимость более частых ремонтов и повышенный расход огнеупорных материалов.
Обезуглероживание поверхностного слоя металла ухудшает механические свойства стали, понижая ее пределы прочности, текучести и выносливости. Для получения заданных механических свойств изделия приходится удалять обезуглероженный слой (до 2 мм), что, естественно, увеличивает трудоемкость обработки изделия. Особенно нельзя допускать обезуглероживания изделий, которые в последующем подлежат поверхностной термической обработке.
При выборе режимов нагрева стали в печах необходимо принимать во внимание оба указанных выше процесса, так как они тесно связаны между собой.
Окисление стали
Окисление стали представляет собой процесс взаимодействия окисляющих газов с железом и легирующими элементами. Этот процесс определяется не только химическими реакциями окисления, но и закономерностями образования окисной пленки, которая по мере ее роста все более и более изолирует сталь от окислительных газов. Поэтому скорость роста окалины зависит не только от протекания химического процесса окисления стали, но и от условий передвижения ионов металла (от металла и внутренних слоев окалины к наружным) и атомов кислорода (споверхности металла к его внутренним слоям), т. е. от условий протекания физического процесса двусторонней диффузии. Скорость диффузии какого-либо вещества выражается первым законом Фика:
где т — количество вещества, диффундирующего через единицу сечения в единицу времени, кг/(м 2 ×с); D — коэффициент пропорциональности, называемый коэффициентом диффузии, м 2 /с.
Отношение dc/dx показывает, насколько изменяется концентрация диффундирующего вещества с при изменении толщины слоя, в котором происходит диффузия на величину dх. Таким образом, скорость диффузии увеличивается с возрастанием коэффициента диффузии и разности концентраций диффундирующего компонента. Коэффициент диффузии зависит от физических свойств взаимодействующих веществ и температуры.
Диффузионный механизм образования окалины обусловливает трехслойную структуру слоя оксидов, образующегося при нагреве стали в печах. Во внутреннем слое (примыкающем к металлу) содержится больше всего монооксида железа, образующегося по реакции
Средний слой — магнетит Fе3О4 — образуется при последующем окислении монооксида железа по реакции
В этом слое железа содержится меньше и в сравнении с первым слоем он обогащен кислородом, хотя и не в такой мере, как наиболее богатый кислородом Fе2О3, образующийся в третьем слое по реакции
Состав каждого из трех слоев не постоянен по сечению, а постепенно изменяется в результате взаимодействия с примесями компонентов окалины, более богатых кислородом вблизи поверхности.
Окисление стали при ее нагреве в печах происходит не только благодаря ее взаимодействию со свободным кислородом, но и со связанным кислородом, входящим в состав продуктов полного сгорания топлива а топливных печах: СО2, Н2О и SО2. Эти газы, так же как и О2, называют окислительными в отличие от восстановительных СО, Н2 и СН4. Азот, обычно присутствующий в продуктах сгорания или в воздухе, является нейтральным газом. Атмосфера в большей части топливных печей представляет собой смесь N2, СО2, Н2О, SО2 с небольшим количеством свободного кислорода, поскольку только при полном сгорании топлива в печи развивается требуемая температура. Наличие большого количества восстановительных газов в печи свидетельствует о неполном сгорании и в обычных печах недопустимо, так как топливо используется не рационально. Этим, объясняется то обстоятельство, что атмосфера обычных топливных печей имеет окислительный характер.
Окислительная и восстановительная способность всех перечисленных газов по отношению к стали зависит от их концентрации в атмосфере печи и температуры. Увеличение доли нейтрального газа в печной атмосфере уменьшает скорость окисления. Скорость окисления очень сильно зависит от содержания SО2 и Н2S в печной атмосфере. Присутствие в печных газах даже очень небольших количеств SО2 резко увеличивает скорость окисления, так как при температуре, превышающей 1373 К, на поверхности стали образуются легкоплавкие соединения из оксидов и сульфидов железа, ускоряющие процесс образования окалины.
Соединение Н2S может присутствовать и в восстановительной атмосфере; его воздействие на металл (наряду с SО2) приводит к увеличению содержания серы в поверхностном слое. Качество стали при этом сильно ухудшается, причем особенно вредное влияние сера оказывает на легированные стали, так как они поглощают ее в большей мере, чем простые углеродистые стали, а никель образует с серой легкоплавкую эвтектику. Вредное влияние серы уменьшается при наличии восстановительных газов в атмосфере печи. При этом следует отметить, что вредное воздействие Н2S на сталь значительно слабее, чем влияние SО2.
Толщина образующегося слоя оксидов на поверхности стали и его структура зависят не только от атмосферы, в которой нагревается металл, но и от ряда других факторов, к которым в первую очередь относятся температура и время. Чем выше температура металла, тем большее количество окалины образуется за одно и то же время его пребывания в печи. Экспериментально установлено, что скорость роста пленки оксидов dх/dt, как и во всяком диффузионном процессе, связана с температурой следующим уравнением:
где R — газовая постоянная; Т — абсолютная температура; Q и А — постоянные величины, зависящие от природы пленки оксидов и условий процесса.
Образование окалины при температуре до 873 К происходит с очень малой скоростью, а при температуре свыше 898 — 923 К скорость окисления стали резко возрастает и увеличивается согласно приведенному выше уравнению по экспоненциальному закону. Время пребывания металла в печи оказывает очень сильное влияние на количество образующейся окалины. Увеличение времени нагрева до заданной температуры приводит к росту слоя окалины, хотя скорость окисления несколько падает со временем вследствие увеличения толщины слоя и, следовательно, уменьшения скорости диффузии через него ионов железа и атомов кислорода. Время нагрева до заданной температуры может быть сокращено увеличением температуры в печи (если получающаяся при этом скорость нагрева позволяет вести процесс без возникновения опасных напряжений в металле), что способствует уменьшению количества образующейся окалины.
Факторы, влияющие на скорость диффузии кислорода к поверхности нагреваемой стали из атмосферы печи, не оказывают существенного влияния на рост слоя оксидов. Это обусловлено тем, что диффузионные процессы в слое окалины протекают медленно и являются определяющими. Поэтому, например, увеличение скорости движения газов над поверхностью металла выше 0,1 м/с (скорость движения газов в печах обычно больше) не приводит к ускорению окисления стали. Однако движение продуктов сгорания в общем может оказывать заметное влияние на окисление, так как местные перегревы металла, обусловленные неравномерным полем температур газов в печи (это может быть вызвано большим углом наклона горелок, их неправильным размещением по высоте и длине печи и т. д.), неизбежно приводят к местному интенсивному окалинообразованию.
Условия перемещения стальных заготовок и деталей внутри печей, состав стали и качество ее поверхности также оказывают заметное влияние на скорость образования окалины. Так, при перемещении металла в печи может происходить отслаивание и отделение окалины, что способствует более быстрому последующему окислению незащищенных поверхностных участков. Состояние поверхности металла играет важную роль, так как образующийся на гладкой поверхности слой оксидов оказывается более плотным и прочным и защищает сталь от дальнейшего окисления. Наличие в стали некоторых легирующих элементов (Cr, Ni, Si и др.) может обеспечить образование тонкой и плотной, хорошо прилегающей к поверхности металла пленки оксидов, надежно предупреждающей последующее окисление. Такие стали, называемые жаростойкими, хорошо сопротивляются окислению при нагреве.
Следует отметить, что сталь с большим содержанием углерода в меньшей мере подвержена поверхностному окислению, чем малоуглеродистая. Углерод, содержащийся в стали, окисляясь, превращается в СО2, диффундирующую к поверхности и препятствующую окислению железа. Окисление стали сильно увеличивается при плавлении окалины.
Количество образовавшейся окалины можно определить по изменению массы окислившегося образца двумя способами: 1) по увеличению массы образца, покрытого окалиной (увеличение массы характеризует количество кислорода, входящего в состав окалины), и 2) по уменьшению массы образца после полного снятия слоя окалины (уменьшение массы показывает, какое количество железа входило в состав снятой окалины). Кроме этого, иногда проводят изучение микро- и макроструктуры слоя образовавшейся окалины и определяют ее химический состав.