Гонадотропные гормоны
Содержание
Гонадотропные гормоны [ править | править код ]
К гонадотропным гормонам гипофиза относят фолликул-стимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). Хорионический гонадотропин (ХГ) тоже влияет на половые железы, но синтезируется плацентой. Эти три гормона вместе с тиреотропным гормоном (ТТГ) сходны по строению и образуют семейство гликопротеидных гормонов. Все они состоят из двух субъединиц: а-субъединица у всех одинаковая, а β-субъединицы различаются и обеспечивают специфическую активность. При этом β-субъединицы всех гормонов достаточно схожи, за исключением β-субъединицы ХГ, которая содержит дополнительный участок из 30 аминокислотных остатков на С-конце и несколько дополнительных углеводных остатков. Углеводные остатки увеличивают период полувыведения (Т1/2) этих гормонов в сыворотке, а также участвуют в их связывании с рецепторами. У человека ген, кодирующий β-субъединицу ФСГ, локализуется в сегменте 11р13, а β-субъединицу ЛГ — в сегменте 19ql2.32, по соседству по меньшей мере с 7 генами, кодирующими β-субъединицу ХГ. Ген, кодирующий а-субъединицу этих гормонов, локализуется в сегменте 6q21—q23.
Секреция гонадотропных гормонов [ править | править код ]
Регуляция секреции гонадолиберина [ править | править код ]
Механизм действия гонадолиберина [ править | править код ]
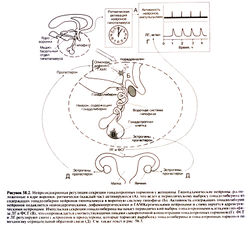
Рецептор гонадолиберина относится к рецепторам, сопряженным с G-белками; его ген находится в сегменте 4q21. При связывании гонадолиберина или его аналогов с рецептором происходит активация белков Gq и GM, которые, в свою очередь, активируют фосфолипазу С, что приводит к увеличению внутриклеточной концентрации кальция. Это в итоге стимулирует синтез и секрецию ЛГ и ФСГ. Хотя цАМФ не принимает заметного участия в передаче сигнала от рецептора гонадолиберина, активация этого рецептора увеличивает активность аденилатциклазы. Рецепторы гонадолиберина присутствуют также в яичниках и яичках, однако их физиологическое значение остается неизвестным.
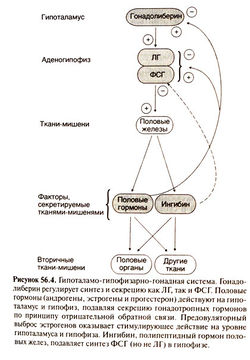
Половые гормоны также регулируют синтез ЛГ и ФСГ, воздействуя на гипоталамус и в меньшей степени — на гипофиз. Эта регуляция по-разному осуществляется у мужчин и женщин и зависит от возраста и фазы менструального цикла. У женщин низкие концентрации эстра-диола и прогестерона подавляют синтез гонадотропных гормонов за счет опосредованного опиоидами действия на нейроны, отвечающие за импульсную секрецию гонадолиберина. Однако длительное повышение концентрации эстрадиола действует по принципу положительной обратной связи, приводя к предовуляторному выбросу ЛГ. У мужчин синтез гонадотропных гормонов подавляется тестостероном, причем частично это обусловлено его прямым действием, а частично — превращением в эстрад иол.
Ингибин — пептидный гормон, образующийся в половых железах и играющий важную роль в регуляции секреции гонадотропных гормонов. Он синтезируется клетками гранулярного слоя фолликулов в яичниках и клетками Сертоли в яичках в ответ на стимуляцию гонадотропными гормонами и местными факторами роста. Ингибин действует непосредственно на гипофиз, избирательно подавляя секрецию ФСГ, но не Л Г. Ингибин относится к тому же семейству гликопротеидов, что и трансформирующий фактор роста |3 и фактор регрессии мюллеро-вых протоков.
Механизм действия гонадотропных гормонов [ править | править код ]
ЛГ и ХГ связываются с рецептором Л Г (ген этого рецептора находится в сегменте 2р21), а ФСГ — со своим рецептором (ген этого рецептора находится на длинном плече 2-й хромосомы). Оба рецептора сопряжены с G-белками и обладают большим внеклеточным гликозилированным доменом, ответственным за распознавание гормона. При связывании рецептора с лигандом G,-белок активирует аденилатциклазу, что ведет к повышению концентрации цАМФ. При высокой концентрации лиганда рецепторы через Gq-белок активируют также протеинкиназу С и увеличивают концентрацию кальция за счет активации фос-фолипазы С. Все или почти все эффекты гонадотропных гормонов можно воспроизвести введением в клетку аналогов цАМФ, поэтому значение протеинкиназы С и Са2+ во внутриклеточной передаче сигнала остается неясным.
Физиологические эффекты гонадотропных гормонов [ править | править код ]
ЛГ и ФСГ были названы в соответствии с их действием на яичники; функция этих гормонов у мужчин была изучена позднее. У мужчин ЛГ действует на клетки Лейдига, стимулируя синтез андрогенов, в основном тестостерона. Тестостерон обеспечивает половое влечение, развитие вторичных половых признаков и сперматогенез в извитых семенных канальцах. ФСГ действует на клетки Сертоли, стимулируя образование ими белков и питательных веществ, необходимых для созревания сперматозоидов.
У женщин действие ФСГ и ЛГ более сложно. ФСГ стимулирует рост и развитие фолликулов, а также индуцирует экспрессию гена рецептора ЛГ на текоцитах и клетках гранулярного слоя в яичниках. Кроме того, ФСГ активирует ароматазу в клетках гранулярного слоя, стимулируя синтез эстрадиола. ЛГ действует на текоциты, стимулируя образование в них андростендиона, основного предшественника эстрадиола в яичниках у женщин детородного возраста. ЛГ необходим также для разрыва фолликула при овуляции и для синтеза прогестерона желтым телом. Наконец, связывание ЛГ со своим рецептором на клетках гранулярного слоя увеличивает экспрессию гена рецептора ФСГ, что усиливает действие последнего.
Значение гонадотропных гормонов в регуляции функций половых органов отчетливо выявляется при мутациях генов самих гормонов или их рецепторов (Achermann and Jameson, 1999). У женщин с мутациями генов рецептора ФСГ или β-субъединицы самого ФСГ наблюдаются первичная аменорея и бесплодие, у них не созревают фолликулы, отсутствуют желтые тела и не развиваются молочные железы. Эти данные, а также эффективность ФСГ при некоторых формах бесплодия (см. ниже) красноречиво свидетельствуют о важной роли ФСГ в функционировании яичников. У мужчин при таких же мутациях уменьшен размер яичек и наблюдается олигозооспермия, хотя в некоторых случаях сохраняется фертильность.
Описан только один случай мутации с потерей функции гена β-субъединицы Л Г: у 46-летнего мужчины отсутствовало половое развитие, наблюдались гипоплазия клеток Лейдига и бесплодие. Наружные половые органы у него были развиты по мужскому типу, что, видимо, объясняется синтезом андрогенов под действием ХГ во время внутриутробного развития. Проявления мутаций с потерей функции гена рецептора ЛГ при мужском кариотипе варьируют от мужского гипогонадизма до развития наружных половых органов по женскому типу и отсутствия полового развития. Вероятно, вирилизации наружных половых органов не происходит из-за нарушения действия как ЛГ, так и ХГ во время внутриутробного развития. У женщин, гомозиготных по мутантным аллелям гена рецептора Л Г, отмечаются первичная аменорея или олигоменорея и бесплодие, а при гистологическом исследовании выявляются множественные кисты яичников.
Мутации, ведущие к постоянной активации рецептора ЛГ, возникают преимущественно у мужчин и наследуются аутосом-но-доминантно. Они ведут к преждевременному половому развитию из-за неуправляемого синтеза тестостерона во внутриутробном и в препубертатном периодах. При некоторых из этих мутаций высок риск опухолей яичка.
Применение гонадолиберина и его аналогов [ править | править код ]
В табл. 56.3 перечислены синтетические аналоги гонадолиберина, применяемые в клинике. Синтетический гонадолиберин называется гонадорелином. Замена аминокислотного остатка в положении 6 защищает аналоги гонадолиберина от протеолиза, а замена С-концевого остатка повышает сродство к рецептору. Такие аналоги обладают большей активностью и более длительным действием по сравнению с нативным гонадолиберином, Т1/2 которого составляет всего 2—4 мин.
Антагонисты гонадолиберина, в отличие от его аналогов длительного действия, не вызывают кратковременного повышения уровней гонадотропных гормонов в сыворотке. Современные антагонисты гонадолиберина, по-видимому, не приводят к местному и системному выбросу гистамина и анафилакгоидным реакциям, что ограничивало применение первых препаратов этой группы. Два антагониста гонадолиберина гаиреликс и цетрореликс применяют при искусственном оплодотворении для подавления выброса ЛГ во время стимуляции яичников. Ганиреликс доступен в США, а цетрореликс—только в Европе. Теоретически быстрое подавление выброса ЛГ дает возможность лучше контролировать стимуляцию яичников (см. ниже) и тем самым сокращает цикл искусственного оплодотворения. Однако практическую ценность этих препаратов при искусственном оплодотворении еще предстоит уточнить в клинических испытаниях.
Диагностическое применение [ править | править код ]
Один из препаратов гонадорелина (гонадорелина гидрохлорид) применяют для дифференциальной диагностики гипофизарного и гипоталамического поражения при вторичном гипогонадизме. Уровень ЛГ в сыворотке измеряют до введения гонадорелина в дозе 100 мкг п/к или в/в и в течение 2 ч (через 15,30,45,60 и 120 мин) после введения. Увеличение секреции ЛГ свидетельствует о наличии функционирующих гонадотропных клеток аденогипофиза. При длительном дефиците гонадолиберина чувствительность гонадотропных клеток к нему может снижаться, поэтому низкий уровень ЛГ при проведении пробы с гонадолиберином не обязательно говорит о поражении гипофиза. Пробу с гонадолиберином можно также использовать для дифференциальной диагностики истинного (связанного с секрецией гонадолиберина) и ложного преждевременного полового развития.
Лечение бесплодия [ править | править код ]
Другой препарат гонадорелина (гонадорелина ацетат) используют при нарушениях репродуктивной функции, связанных с дефицитом гонадолиберина. Препарат вводят в/в с помощью специального инфузионного насоса в импульсном режиме, имитирующем физиологическую секрецию, 2,5 мкг каждые 60—90 мин. Если овуляция не наступает, доза, вводимая за один импульс, может быть постепенно увеличена до 10 мкг. Принципы введения и дозы указаны в инструкции изготовителя. Гонадорелин реже, чем гонадотропные гормоны, вызывает многоплодную беременность. При лечении гона-дорелином не требуется столь тщательно контролировать уровень эстрогенов в сыворотке и проводить УЗИ яичников. Побочные реакции возникают редко, чаще всего развивается флебит в месте введения. При лечении гонадорелином у женщин восстанавливается физиологическая секреция половых гормонов, устанавливается менструальный цикл и происходит овуляция. Однако из-за технической сложности этот метод лечения применяют только в специализированных клиниках (Hayes et al., 1998).
При бесплодии у мужчин с помощью гонадорелина можно добиться роста яичек, нормальной секреции половых гормонов и сперматогенеза. Однако метод относительно дорог и требует постоянного ношения инфузионного насоса. К тому же гонадорелин не одобрен ФДА для лечения мужского бесплодия. Поэтому обычно предпочтение отдают гонадотропным гормонам.
Аналоги гонадолиберина длительного действия применяют также при индукций овуляции. Эти препараты подавляют предовуляторный выброс ЛГ и предотвращают лютеинизацию неовулирующего фолликула. Разработано несколько схем лечения, при которых длительно или краткосрочно вводят аналоги гонадолиберина совместно с гонадотропными гормонами, обеспечивающими созревание фолликула (см. ниже), а затем для индукции овуляции назначают ХГ (Lunenfeld, 1999).
Подавление секреции гонадотропных гормонов [ править | править код ]
Как уже говорилось, аналоги гонадолиберина длительного действия ведут к десенситизации рецепторов гонадолиберина, в результате чего секреция гонадотропных, а соответственно и половых, гормонов резко снижается. Такая «медикаментозная кастрация» оказалась очень удобной в тех случаях, когда нужно сократить выработку половых гормонов. Очевидное показание к подобному лечению — истинное преждевременное половое развитие у детей, при котором длительное введение аналогов гонадолиберина очень эффективно и почти не сопровождается побочными реакциями.
Аналоги гонадолиберина длительного действия в целом хорошо переносятся и вызывают вполне предсказуемые побочные эффекты, обусловленные нарушением синтеза половых гормонов: приливы, сухость влагалища, атрофический вагинит, снижение плотности костной ткани. В связи с этим при таких заболеваниях, как эндометриоз и миома матки, лечение обычно продолжают не более 6 мес или дополнительно назначают эстрогены для поддержания плотности костной ткани.
Диагностическое применение гонадотропных гормонов [ править | править код ]
Тест на беременность [ править | править код ]
В крови и моче беременных в больших количествах присутствует ХГ, поэтому в качестве теста на беременность можно использовать иммунохимическое выявление β-субъединицы ХГ. Качественное определение β-субъединицы ХГ в моче лежит в основе тестов на беременность для домашнего применения, продаваемых в США без рецепта. Эти тесты позволяют быстро выявить беременность уже через несколько дней после задержки менструации.
Количественное определение концентрации ХГ в плазме в клинических и научных целях проводят с помощью РИА. Обычно это делают для оценки прогрессирования беременности, а также при подозрении на внематочную беременность, пузырный занос или хориокарциному.
Определение времени овуляции [ править | править код ]
Диагностика расстройств репродуктивной функции [ править | править код ]
Количественное измерение уровня ФСГ и ЛГ в плазме методом РИА (по уровню β-субъединиц) используют для диагностики некоторых нарушений репродуктивной функции. Низкие или неопределяемые уровни ФСГ и ЛГ свидетельствуют о вторичном гипогонадизме и о поражении гипофиза или гипоталамуса. При первичном гипогонадизме уровни этих гормонов, наоборот, высокие. При аменорее у женщин или задержке полового развития у мужчин и женщин определение уровня ФСГ и ЛГ позволяет отличить поражение половых желез от поражения гипоталамо-гипофизарной системы.
По уровню ФСГ на 3-й день менструального цикла можно судить о фертильности. Даже при нормальном менструальном цикле уровень ФСГ 15 МЕ/мл и более говорит о низкой фертильности, и успех искусственного оплодотворения при этом маловероятен (см. ниже).
Проба с ХГ используется у мужчин для оценки функции клеток Лейдига по степени стимуляции синтеза тестостерона. Эту пробу попользуют при подозрении на нарушение функции клеток Лейдига (например, при задержке полового развития). Уровень тестостерона в сыворотке определяют после нескольких инъекций ХГ. Сниженная секреция тестостерона говорит о патологии клеток Лейдига, а нормальная — о поражении гипоталамо-гипофизарной системы.
Лечебное применение гонадотропных гормонов [ править | править код ]
Изначально гонадотропные гормоны для клинического применения получали из человеческих гипофизов (трупный материал) и из мочи женщин. Препараты гипофиза сейчас не используют из-за риска передачи возбудителя болезни Крейтцфельдта—Якоба. Из мочи получают несколько препаратов. ХГ, который по действию аналогичен Л Г, получают из мочи беременных. Из мочи женщин в постменопаузе получают препарат менотропин, который содержит примерно одинаковые количества ЛГ и ФСГ, а также другие белки мочи. Поскольку менотропин относительно плохо очищен, во избежание аллергических реакций его вводят в/м. Другой препарат — урофоллитропин — представляет собой очищенный ФСГ, получаемый путем удаления ЛГ иммунологическими методами. Урофоллитропин сверхвысокой очистки получают при помощи моноклональных антител к ФСГ. Он очищен настолько, что его можно вводить п/к.
Методами генной инженерии получена линия клеток млекопитающих, синтезирующая а- и р-субъединицы ФСГ. Получающийся при этом рекомбинантный ФСГ близок по характеру гликозилирования к нативному ФСГ. Сегодня выпускается два препарата рекомбинантного ФСГ — фоллитропин а и фоллитропин Р; их углеводные структуры слегка различаются. Оба эти препарата вводят п/к, поскольку они намного чище препаратов, получаемых из мочи, и значительно лучше стандартизованы. Рекомбинантные препараты стоят намного дороже нативных, однако данных за то, что они эффективнее или реже вызывают такие побочные реакции, как синдром гиперстимуляции яичников, пока нет. Вероятно, в будущем методами генной инженерии удастся получить аналоги гонадотропных гормонов более длительного действия и с более высокой активностью.
Женское бесплодие [ править | править код ]
Бесплодием страдают около 10% супружеских пар детородного возраста. Для лечения бесплодия все шире применяют гонадотропные гормоны (Vollenhoven and Healy, 1998); часто их используют при искусственном оплодотворении. Хотя основным показанием к их назначению служит хроническая ановуляция в результате вторичного гипогонадизма (группа 1 по классификации ВОЗ), гонадотропные гормоны используют и для индукции овуляции при синдроме поликистозных яичников (группа II по классификации ВОЗ) в том случае, когда кломифен неэффективен (гл. 58). Кроме того, гонадотропные гормоны применяют при бесплодии на фоне нормальной овуляции, хотя в этих случаях сначала пробуют лечение кломифеном. Назначать гонадотропные гормоны должны врачи с достаточным опытом лечения бесплодия и эндокринных расстройств.
При хронической ановуляции назначение одного ФСГ в большинстве случаев вызывает овуляцию. Обычно ФСГ назначают в дозе 75 МЕ/сут в течение первых 6—7 дней цикла, после чего при помощи влагалищного УЗИ оценивают число и размер созревающих фолликулов. УЗИ обычно проводят каждые 2—3 сут. Созревание фолликула считается адекватным, если обнаружен фолликул диаметром 18 мм. Если обнаружено три и более фолликула диаметром более 16 мм, ФСГ отменяют из-за опасности синдрома гиперстимуляции яичников (см. ниже) и применяют барьерные методы контрацепции для предотвращения многоплодной беременности. Определяют также концентрацию эстрадиола, которая должна находиться в диапазоне 500—1500 пг/мл. Более низкие значения указывают на недостаточную стимуляцию яичников, а более высокие — на опасность синдрома гиперстимуляции яичников. При недостаточной стимуляции яичников доза ФСГ может быть увеличена до 150 МЕ/сут.
Для завершения созревания фолликула и индукции овуляции на следующий день после отмены ФСГ назначают ХГ в дозе 5000—10 000 ME. При лечении гонадотропными гормонами в 10—20% случаев развивается многоплодная беременность, что связано с развитием нескольких третичных фолликулов и выходом нескольких яйцеклеток.
Гонадотропные гормоны используют при искусственном оплодотворении, в том числе при экстракорпоральном оплодотворении и микроинъекции сперматозоидов в цитоплазму яйцеклетки. С помощью ФСГ стимулируют развитие фолликулов, а для окончательного их созревания назначают ХГ, после чего зрелые яйцеклетки извлекают из третичных фолликулов хирургическим путем. Затем производят экстракорпоральное оплодотворение полученных яйцеклеток с помощью спермы или микроинъекции сперматозоидов в цитоплазму яйцеклетки. Эмбрионы переносят в полость матки или в маточную трубу. При искусственном оплодотворении риск многоплодной беременности зависит от числа перенесенных эмбрионов.
Помимо многоплодной беременности и ее возможных осложнений основным побочным эффектом гонадотропных гормонов является синдром гиперстимуляции яичников. Для этого синдрома характерно быстрое накопление жидкости в полости брюшины, плевральной полости и даже перикарде. Считается, что причина этого синдрома — выделение яичниками вещества, повышающего сосудистую проницаемость. Синдром гиперстимуляции яичников проявляется вздутием живота, болью в животе, тошнотой, рвотой, поносом, выраженным увеличением яичников, одышкой и олигурией. Синдром гиперстимуляции яичников может осложниться гиповолемией, водно-электролитными нарушениями, гемоперитонеумом, РДСВ, тромбоэмболиями и нарушением функции печени. При подозрении на развитие этого синдрома ХГ не назначают.
В некоторых исследованиях выдвигалось предположение, что гонадотропные гормоны увеличивают риск рака яичников, однако это осталось недоказанным. Важно отметить, что при стимуляции яичников ФСГ и менотропином не возрастает риск пороков развития у детей, рожденных из стимулированных яйцеклеток.
Мужское бесплодие [ править | править код ]
Лечение гонадотропными гормонами может быть эффективно, если причина бесплодия — их дефицит. Поскольку гонадотропные гормоны относительно дороги, а при длительном приеме может развиться резистентность к ним, обычно половое развитие стимулируют андрогенами, а гонадотропные гормоны применяют позже, для достижения собственно фертильности.
Лечение, как правило, начинают с введения ХГ в дозе 1000— 5000 ME в/м 3 раза в неделю до нормализации синтеза половых гормонов, о чем судят по клиническим признакам и уровню тестостерона в плазме. После этого дозу ХГ снижают до 2000 ME 2 раза в неделю и дополнительно вводят менотропин в дозе по 75—150 ME ЛГ и ФСГ 3 раза в неделю. Наиболее частое побочное действие гонадотропных гормонов — гинекомастия; она возникает почти у каждого третьего больного и, вероятно, связана с повышенной продукцией эстрогенов: Для созревания яичек требуется примерно 6 мес, а для установления полноценного сперматогенеза лечение приходится продолжать до 2 лет. После начала сперматогенеза или его возобновления (при вторичном гипогонадизме, возникшем после полового созревания) для продукции спермы достаточно поддерживающей терапии I ХГ. Как уже говорилось, все большую роль в лечении бесплодия, вероятно, будут играть рекомбинантные гонадотропные гормоны.
Крипторхизм [ править | править код ]
Читайте также [ править | править код ]
Предупреждение [ править код ]

Гонадотропин хорионический 5000 МЕ : инструкция по применению
Состав
1 флакон с препаратом содержит:
действующее вещество: гонадотропин хорионический – 5000 ME,
вспомогательное вещество: маннитол (маннит) – 20,0 мг.
1 ампула с растворителем содержит:
натрия хлорид – 9 мг, вода для инъекций – до 1 мл.
Описание
Препарат: лиофилизированный белый или почти белый порошок.
Растворитель: прозрачная бесцветная жидкость.
Фармакотерапевтическая группа
Фармакологические свойства
Препарат Гонадотропин хорионический содержит хорионический гонадотропин человека (ХГЧ). Этот гормон обладает биологической активностью, сходной с воздействием лютеинизирующего гормона (ЛГ). ЛГ незаменим для нормального роста и созревания женских и мужских гамет и для образования половых гормонов.
У женщин: препарат Гонадотропин хорионический применяется в качестве заменителя выброса в середине цикла эндогенного ЛГ, чтобы индуцировать заключительную фазу созревания фолликулов, приводящую к овуляции. Препарат Гонадотропин хорионический применяется также в качестве заменителя эндогенного ЛГ во время лютеиновой фазы.
У мужчин: препарат Гонадотропин хорионический применяется для стимуляции клеток Лейдига для ускорения процесса образования тестостерона.
Данные собственных исследований фармакокинетики гонадотропина хорионического производства ФГУП «Московский эндокринный завод» РФ отсутствуют. Согласно литературным данным, при внутримышечном введении хорионического гонадотропина человеческого максимальные уровни ХГЧ в плазме крови достигаются приблизительно через 2-6 часов (в зависимости от дозы). Хорионический гонадотропин элиминирует в 2 фазы. Биологический период полувыведения в первой фазе составляет приблизительно 8-12 часов, в то время как во второй фазе (медленно) – от 23 до 37 часов. ХГЧ метаболизируется в основном в почках (от 80 до 90%). Вследствие медленной элиминации ХГЧ может кумулировать при применении препарата с короткими интервалами (например, ежедневно).
Показания к применению
— индукция овуляции при бесплодии, обусловленном ановуляцией или нарушением созревания фолликулов;
— подготовка фолликулов к пункции в программах контролируемой стимуляции яичников (для методик вспомогательной репродукции);
— поддержка лютеиновой фазы (в том числе, в период проведения контролируемой стимуляции яичников при вспомогательной репродуктивной технологии (ВРТ)) с применением аналогов гонадотропин-рилизинг гормона или других средств для стимуляции овуляции при женском бесплодии в результате ановуляции, обусловленной недостаточностью эндогенных эстрогенов (недостаточность яичников I группы классификации ВОЗ).
— бесплодие, связанное с идиопатическими диспермиями;
— задержка полового созревания, обусловленная недостаточностью гонадотропной функции гипофиза;
— крипторхизм, не обусловленный анатомической обструкцией.
Противопоказания
• повышенная чувствительность к гонадотропинам человека или к любому компоненту препарата;
• установленные или подозреваемые опухоли, зависимые от половых гормонов (рак яичника, рак молочной железы и рак матки у женщин, и рак предстательной железы, рак грудной железы – у мужчин);
• органические поражения центральной нервной системы (ЦНС) (опухоли гипофиза, гипоталамуса);
• тромбофлебит глубоких вен;
У мужчин (дополнительно):
• бесплодие, не связанное с гипогонадотропным гипогонадизмом;
У женщин (дополнительно):
• неправильное формирование половых органов, несовместимое с беременностью;
• фиброзная опухоль матки, несовместимая с беременностью;
• синдром гиперстимуляции яичников (СГЯ) в анамнезе;
• синдром поликистозных яичников (СПКЯ);
• первичная недостаточность яичников;
• кровотечение или кровянистые выделения из влагалища неясной этиологии;
• беременность и период грудного вскармливания.
Особые указания и меры предосторожности
• при беременности, возникшей после индукции овуляции гонадотропными препаратами, существует повышенный риск многоплодной беременности;
• поскольку у бесплодных женщин, подвергающихся ВРТ, и в особенности экстракорпоральному оплодотворению, часто имеются патологии маточных труб, то частота возникновения эктопических беременностей может увеличиваться. Поэтому важным является раннее ультразвуковое подтверждение, что беременность внутриматочная;
• частота потери беременности у женщин, подвергающихся ВРТ, выше, чем в обычной популяции;
• следует исключить наличие неконтролируемых внегонадных эндокринопатий (например, заболевания щитовидной железы, надпочечников или гипофиза);
• частота возникновения врожденных пороков развития после ВРТ может быть немного выше, чем в результате спонтанных зачатий. Считается, что это немного повышенная частота связана с особенностями родителей (материнский возраст, характеристики спермы), а также с высокой частотой многоплодной беременности после ВРТ. Нет указаний на то, что повышенный риск врожденных пороков развития связан с применением гонадотропинов во время ВРТ.
• Нежелательная гиперстимуляция яичников
У больных, получающих комбинированную терапию ФСГ/ХГЧ по поводу бесплодия, обусловленного ановуляцией или нарушением созревания фолликулов, применение ФСГ-содержащего препарата может привести к нежелательной гиперстимуляции яичников.
Поэтому перед началом лечения фолликулостимулирующим гормоном (ФСГ) и через регулярные периоды времени в период лечения ФСГ необходимо проводить ультразвуковое исследование для оценки развития фолликулов и определять уровни эстрадиола. Кроме возможного одновременного развития большого количества фолликулов, уровни эстрадиола могут повышаться очень быстро, например, в течение двух или трех последовательных дней может наблюдаться более чем суточное удвоение (возрастать более чем в 2 раза), и, возможно, достигнуть чрезвычайно высоких значений. Диагноз нежелательной гиперстимуляции яичников может быть подтвержден при ультразвуковом исследовании. В случае возникновения нежелательной гиперстимуляции яичников (т.е. не как часть лечения, направленного на подготовку для in vitro оплодотворения с переносом эмбриона (ЭКО/ЭТ), внутриутробного переноса гаметы (ВРТ) или внутриплазматической инъекции сперматозоида (ИКСИ)), введение ФСГ-содержащего препарата необходимо немедленно прекратить. В этом случае необходимо избежать беременности и не вводить препарат Гонадотропин хорионический, поскольку введение ЛГ-активного гонадотропина может вызвать дополнительно к множественной овуляции, синдром гиперстимуляции яичников (СГЯ).
Это предупреждение особенно важно в отношении больных с поликистозом яичников. Клиническими симптомами СГЯ умеренной тяжести являются желудочно-кишечные нарушения (боль, тошнота, диарея), болезненность молочных желез, увеличение яичников и кист яичников легкой и умеренной степени. Сообщалось о связанных с СГЯ временных отклонениях результатов тестов функции печени, свидетельствующих о печеночной дисфункции, которая может сопровождаться морфологическими изменениями при биопсии печени.
В редких случаях возникает тяжелый СГЯ, который может представлять угрозу жизни. Он характеризуется большими кистами яичников (склонными к разрыву), асцитом, увеличением массы, часто гидротораксом и в некоторых случаях – тромбоэмболией.
• У женщин, имеющих факторы риска тромбоза (личный или семейный анамнез, ожирение (индекс массы тела >30 кг/м 2 ) или тромбофилия), может быть повышен риск венозной или артериальной тромбоэмболии во время или после лечения гонадотропинами. У этих женщин необходимо взвесить преимущества применения ВРТ и возможные риски.
• Препарат гонадотропин не следует применять для снижения массы тела. ХГЧ не оказывает влияния на метаболизм жира, распределение жира или аппетит.
Лечение пациентов мужского пола с помощью ХГЧ приводит к повышению продукции андрогенов. Поэтому:
• пациенты с латентной или явной сердечной недостаточностью, нарушением функции почек, артериальной гипертензией, эпилепсией или мигренью (или при наличии этих состояний в анамнезе) должны находиться под строгим врачебным контролем, поскольку обострение болезни или рецидив иногда могут являться результатом повышенной продукции андрогенов;
• ХГЧ следует с осторожностью применять мальчикам в пубертатном возрасте во избежание преждевременного закрытия эпифизов или преждевременного полового созревания. Следует регулярно контролировать развитие скелета.
Перед началом применения препарата необходимо провести обследование с целью исключения гипотиреоза, недостаточности коры надпочечников, гиперпролактинемии, опухолей гипофиза или гипоталамуса и соответствующего специфического лечения при выявлении этих состояний/заболеваний/факторов риска.
Если у Вас одно из перечисленных заболеваний, перед приемом препарата обязательно проконсультируйтесь с врачом.
Длительное введение может привести к образованию антител к препарату.
Применение гонадотропина в геронтологии необходимо ограничить, в связи с возможностью возникновения гонадотропин-секретирующих опухолей.
С осторожностью у лиц с заболеваниями почек.
Содержание натрия: приготовленный раствор гонадотропина хорионического содержит менее 1 ммоль (23 мг) натрия на 10000 ME, то есть по сути не содержит натрия.
Применение при беременности и в период грудного вскармливания
Препарат Гонадотропин хорионический можно применять для поддержания лютеиновой фазы, но нельзя применять в период лактации.
Влияние на способность управлять автомобилем или другими механизмами
По имеющимся данным препарат не оказывает влияния на скорость психомоторных реакций и концентрацию внимания.
Способ применения и дозы
После добавления растворителя к лиофилизату, восстановленный раствор гонадотропина хорионического вводится внутримышечно. Восстановленный раствор гонадотропина хорионического прозрачный, бесцветный или слегка желтоватого цвета. Приготовленный раствор хранению не подлежит, поскольку дальнейшее сохранение стерильности раствора не гарантировано. Указанные дозировки являются приблизительными, лечение должно корректироваться врачом индивидуально в зависимости от необходимой реакции на введение препарата.
• При индукции овуляции при бесплодии, обусловленном ановуляцией или нарушением созреванием фолликулов
Обычно вводится одна инъекция препарата Гонадотропин хорионический в дозе от 5000 до 10 000 ME для завершения лечения препаратами ФСГ;
• При подготовке фолликулов к пункции в программах контролируемой стимуляции яичников (КСЯ)
Обычно вводится одна инъекция препарата Гонадотропин хорионический в дозе от 5000 до 10 000 ME для завершения лечения препаратами ФСГ;
• Поддержка лютеиновой фазы у женщин в период проведения контролируемой стимуляции яичников при ВРТ
Может быть сделано от двух до трех повторных инъекций препарата в дозе от 1000 ME до 3000 ME каждая в течение 9 дней после овуляции или переноса эмбриона (например, на 3, 6 и 9 день после индукции овуляции).
Дозы, указанные ниже, имеют ориентировочный характер и должны регулироваться индивидуально в зависимости от клинического ответа.
• Гипогонадотропный гипогонадизм и идиопатические диспермии
1000-2000 ME препарата 2-3 раза в неделю. В случае бесплодия, связанного с диспермией, возможно сочетание препарата Гонадотропин хорионический с дополнительным препаратом, содержащим фоллитропин (ФСГ) 2-3 раза в неделю. Курс лечения должен продолжаться не менее 3 месяцев до ожидаемого улучшения сперматогенеза. Во время этого лечения необходимо приостановить заместительную терапию тестостероном. Когда улучшение сперматогенеза достигнуто, для его поддержания достаточно, в некоторых случаях, изолированного применения ХГЧ.
• При задержке полового созревания, обусловленной недостаточностью гонадотропной функции гипофиза
1500 ME 2-3 раза в неделю. Курс лечения – не менее 6 месяцев.
• При крипторхизме, не обусловленном анатомической обструкцией:
в возрасте до 2 лет – вводится 250 ME дважды в неделю в течение 6 недель;
в возрасте до 6 лет – вводится 500-1000 К1Е дважды в неделю в течение 6 недель;
в возрасте старше 6 лет – вводится 1500 ME дважды в неделю в течение 6 недель.
Курс лечения в случае необходимости может быть повторен.
Указания по разведению
Лиофилизат для приготовления раствора для внутримышечного введения разводится добавлением растворителя (раствор препарата Гонадотропин хорионический 5000 ME)
1. Возьмите пустой стерильный флакон;
2. Добавьте 1 мл раствора препарата Гонадотропин хорионический 5000 ME
3. Добавьте 4 мл стерильного 0,9 % раствора натрия хлорида;
4. Осторожно взболтайте до смешивания компонентов;
5. Отберите нужное количество раствора препарата исходя из того, что 1 мл разведенного раствора содержит 1000 ME гонадотропина хорионического
6. Выбросьте оставшийся разведенный раствор препарата Гонадотропин хорионический.
Побочное действие
Связанные с действием лекарственного препарата нежелательные реакции перечислены ниже по классам систем органов и частоте. Частота определяется следующим образом: очень часто (≥ 1/10), часто (≥ 1/100,
Передозировка
Показано, что острая токсичность препаратов гонадотропина, полученного из мочи человека, очень низкая. Тем не менее, существует вероятность, что слишком высокая доза ХГЧ может привести к СГЯ (см. раздел «Особые указания и меры предосторожности»).
Взаимодействие с другими лекарственными средствами
Поскольку взаимодействие препарата Гонадотропин хорионический с другими лекарственными препаратами не изучено, такое взаимодействие нельзя исключать.
В течение 10 дней после прекращения лечения препаратом Гонадотропин хорионический, он может оказывать влияние на значения иммунологических тестов на содержание ХГЧ в сыворотке/моче, что может привести к ложноположительному результату теста на беременность.
Форма выпуска
Лиофилизат для приготовления раствора для внутримышечного введения 5000 ME в комплекте с растворителем (натрия хлорид, раствор для инъекций 9 мг/мл).
По 5000 ME препарата во флаконы из стекла первого гидролитического класса, укупоренные пробками резиновыми и обкатанные колпачками алюминиевыми.
По 1 мл растворителя в ампулы из бесцветного стекла первого гидролитического класса.
По 5 флаконов с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой или без фольги.
По 5 ампул с растворителем помещают в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой или без фольги.
По 1 контурной ячейковой упаковке с препаратом и 1 контурной ячейковой упаковке с растворителем вместе с инструкцией по применению препарата, скарификатором или ножом ампульным помещают в пачку из картона.
При упаковке ампул с надрезами (насечками) и точками или кольцами излома скарификаторы или ножи ампульные не вкладывают.
Условия хранения
В защищенном от света месте при температуре от 8 °C до 15 °C.
Хранить в недоступном для детей месте.
Срок годности
Лиофилизат – 3 года, растворитель – 5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту врача.
Федеральное государственное унитарное предприятие «Московский эндокринный завод»
Производство готовой лекарственной формы:
Россия, 109052, г. Москва, ул. Новохохловская, д. 25, стр. 2
Выпускающий контроль качества:
Россия, 109052, г. Москва, ул. Новохохловская, д. 25, стр. 1
Владелец регистрационного удостоверения/наименование, адрес организации, принимающей претензии потребителя:
Федеральное государственное унитарное предприятие «Московский эндокринный завод»
Россия, 109052, г. Москва, ул. Новохохловская, д. 25