Химиотерапия при раке: что влияет на эффективность лечения
Химиотерапия (ХТ) – один из основных методов лечения онкологических пациентов. Использование современных протоколов в совокупности с комплементарной и поддерживающей терапией, полноценной реабилитацией позволяют онкологам свести к минимуму осложнения и улучшить результат лечения. Разбираемся, какие еще факторы повышают эффективность химиотерапии.
От чего зависит эффективность химиотерапии?
Полностью исключить неблагоприятное действие химиопрепаратов на организм человека невозможно, так как они содержат высокотоксичные вещества – цитостатики. Цитостатики наносят вред не только опухолевым, но и здоровым клеткам, пусть и в меньшей степени.
Эффективность химиотерапевтического лечения рака зависит от ряда факторов, включая:
Когда лучше начинать химиотерапию?
Решение о начале лечения принимает врач в зависимости от конкретной ситуации. Если химиотерапия проводится в комплексе с операцией, то она может назначаться перед ней либо после. В первом случае химиотерапия называется неоадъювантной, во втором – адъювантной.
Любой способ воздействия на злокачественную опухоль приносит наилучший результат на самых ранних стадиях, когда новообразование еще не вышло за пределы органа, не «обзавелось» собственными сосудами, не создало комфортную «среду обитания».
Химиотерапия – не исключение. Но из-за токсичности при раннем обнаружении заболевания ее назначают не всегда. Например, если опухоль можно полностью удалить и риск рецидива ничтожен, онколог может назначить только операцию.
Некоторые виды рака очень агрессивны и начинают метастазировать раньше, чем дают о себе знать и становятся заметны на снимках. В случае с такими опухолями химиотерапию обычно назначают сразу же.
Кроме того, химиотерапия может показывать хорошие результаты при прогрессирующем раке – рост опухоли останавливается, метастазы исчезают, состояние человека улучшается.
Можно определить заранее, поможет ли химиотерапия?
К сожалению, врач способен только предположить вероятность и полноту ответа опухоли на действие цитостатиков. Однако сейчас это можно сделать с достаточно высокой точностью. Например, химиотерапевты ведущих современных онкоцентров имеют возможность спрогнозировать эффективность химиотерапии с помощью молекулярно-генетического теста. Точность такого прогноза около 80%. Остальным 20% пациентов потребуется скорректировать лечение – подобрать другие препараты, изменить дозы, количество курсов и их продолжительность.
Эффективность химиотерапии может меняться
Рак коварен и «воюет до последнего солдата»: если после окончания химиотерапии в организме осталась хотя бы одна жизнеспособная раковая клетка, из нее рано или поздно вырастет новая опухоль – рецидивы могут повторяться неоднократно. Химиопрепараты, с помощью которых удалось быстро и без серьезных осложнений вывести пациента в ремиссию, при рецидивах часто оказываются малоэффективными или бесполезными, потому что вновь образовавшиеся опухоли приобретают устойчивость ко всем ранее использованным препаратам. В этом случае врачи переходят к другим схемам лечения – химиотерапии второй линии. При повторных рецидивах схему химиотерапии снова приходится менять, переходя к противоопухолевым средствам третьей, четвертой линии.
Как онкологи добиваются максимальной эффективности химиотерапии
В каждом конкретном случае вопрос о необходимости назначения химии, ее составе, схеме и объеме решается лечащим врачом, а нередко и консилиумом:
Во время химиотерапии онкологический пациент находится под постоянным врачебным контролем. При низкой эффективности лечения или ее отсутствии врач корректирует дозы, кратность и продолжительность курсов, принимает решение о смене препаратов.
Для повышения лечебного эффекта параллельно с системной химиотерапией, при которой препарат вводится в кровь и распространяется по всему организму, пациенту могут назначить внутриполостные инъекции цитостатиков, в частности:
Научный редактор текста: Екатерина Коробейникова, онколог-химиотерапевт, резидент Высшей школы онкологии
Как в фильмах не будет: что должен знать о химиотерапии каждый пациент
Химиотерапия — страшно и невыносимо. Об этом говорит нам медиапространство, и неудивительно, что из-за такой гиперболизации многие пациенты боятся ее едва ли не больше, чем самого заболевания. Однако ни один фильм и ни один роман не рассказывает, что это такое, как работает и насколько оправдан страх лекарственного лечения. Вместе с химиотерапевтом клиники «Луч» и научным сотрудником СПбКнПЦСВМП(о) Марией Степановой мы составили инструкцию для пациентов и разобрались, что такое лекарственная терапия и от чего зависит схема лечения.
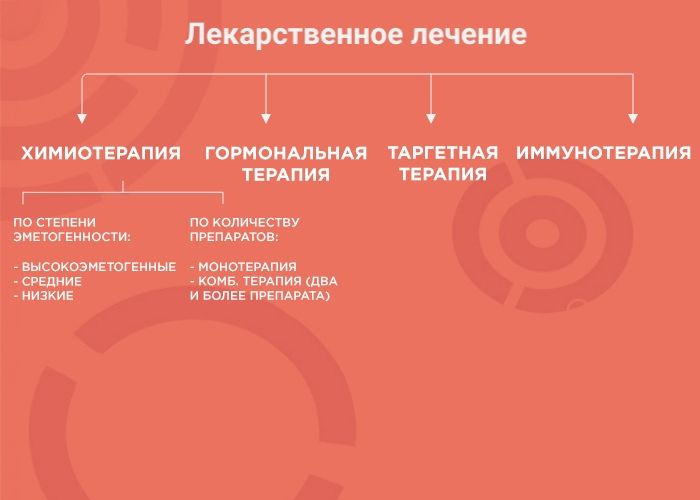
Что такое лекарственное лечение
Лекарственная терапия — один из вариантов лечения онкологических заболеваний. Ее возможности и эффективность зависят от типа злокачественного образования. В лекарственной терапии выделяется четыре вида: химиотерапия, наиболее изученный вид терапии; гормонотерапия; таргетная терапия (англ. target «цель, мишень») и иммунотерапия, самый молодой и мало изученный вид лечения. Чтобы понять, почему врач выбирает тот или иной вид терапии, давайте рассмотрим каждый из них более подробно.
Химиотерапия (ХТ)
Некоторые до сих пор ошибочно считают, что лекарственная терапия сводится исключительно к химиотерапии. Действительно, долгое время лекарственное лечение злокачественных опухолей отводилось цитостатикам, противоопухолевым препаратам, принцип действия которых — разрушение быстро делящихся клеток. В том числе — злокачественных.
— Для пациента, который беспокоится о выраженности тошноты важно знать, какие препараты входят в конкретно его схему лечения. Я всегда рассказываю об этом и при необходимости назначаю препараты для снижения побочных эффектов. Чаще всего это сочетание внутривенного и таблетированного вариантов противорвотных препаратов. Однако, плохое самочувствие может нагнать пациента уже дома, и тогда я обсуждаю это и назначаю препараты, которые он может принимать без надзора врача.
— Получается, как в фильмах бывает редко?
— Крайне редко! Конечно, мутить будет, и многие сравнивают это ощущение с токсикозом во время беременности. В таких случаях я рекомендую пить чай с имбирем, использовать жевательные резинки, карамель с кислым вкусом, соленые и кислые продукты.
При химиотерапии используют множество препаратов с разным механизмом действия, ориентированным под разные особенности опухоли. Поэтому врачи используют либо монотерапию (один препарат), либо комбинированное лечение (два и более препарата). Это позволяет усилить противоопухолевый эффект и уменьшить вероятность развития устойчивости опухоли к лечению.
Выделяют также чувствительные к ХТ опухоли (например, герминогенные опухоли, хорионкарциномы, лимфомы) и опухоли, малочувствительные к ХТ (меланома, некоторые виды сарком). Чтобы найти оптимальные варианты лечения для увеличения продолжительности жизни, сейчас активно ведутся клинические исследования о возможности комбинировать этот вид терапии с иммунотерапией.
Гормональная терапия (ГТ)
При гормональной терапии применяются препараты, подавляющие выработку в организме его естественных гормонов или их взаимодействие с рецепторами. Самый частый вариант опухоли, где применяется данный вариант лечения, — рак молочной железы (РМЖ). При выполнении иммуногистохимического (ИГХ) исследования и наличии положительных рецепторов эстрогена и/или прогестерона, оптимальной опцией лечения является гормонотерапия. С ее помощью, можно остановить опухолевый рост и даже добиться полного или частичного исчезновения опухоли.
— Особенность применения этих препаратов, в том что они в подавляющем случае в таблетированной форме и имеют приемлемую токсичность по сравнению с ХТ. Это позволяет пациентам совмещать лечение с работой, хобби и путешествиями.
Таргетная терапия (ТТ)
В отличие от ХТ таргетные (целенаправленные) препараты атакуют только опухолевые клетки. Опухоль для ТТ — своего рода мишень, уничтожение которой означает прекращение репликации (воспроизведения) клеток и метастазирования.
Все началось с того, что врачи отметили недостаточный эффект от цитостатиков и начали внедрять иммуногистохимические параметры. Иммуногистохимическое исследование (ИГХ) выявляет в образце ткани белки, специфичные для того или иного вида клеток. Это позволяет отличать один вид опухоли от другого и выявлять маркеры, которые отвечают за лекарственную чувствительность опухолевой ткани.
— Таргетная терапия начинается с немелкоклеточного рака легкого: в порыве клинических исследований врачи разработали препарат, который начали применять в рамках клинических исследований. Широкое использование Ирессы в клинической практике сопровождалось преимущественно разочарованиями, связанными с редкостью проявления лечебного эффекта. Загадка разрешилась достаточно быстро: анализ нуклеотидной последовательности гена EGFR, проведенный тремя независимыми исследовательскими коллективами, установил, что опухоли легких, характеризующиеся чувствительностью к Ирессе или Тарцеве, содержат мутированную форму этого рецептора. Таким образом, с 2009 года Ирессу внедрили в клиническую практику для пациентов имеющих мутацию в гене EGFR. Особенность механизма действия ТТ, заключается в блокировании мутации, в результате чего опухоль не может делиться, — поясняет Мария.
Побочные эффекты при таргетной терапии менее выражены, и пациенту чаще всего не нужно находиться в стационаре. Некоторые таргетные препараты используются в таблетированной форме, во время их приема качество жизни пациента значительно не страдает, и пациенты могут вести привычный образ жизни.
Иммунотерапия (ИТ)
Иммунотерапия — самая молодая отрасль лекарственного лечения. Существует несколько групп иммунопрепаратов с разными механизмами действия. Одни воздействуют на звено образования кровеносных сосудов в опухоли и блокируют их развитие (после чего опухоль перестает получать питание и погибает), а другие активируют и направляют иммунные силы организма на борьбу с опухолью. занимает много времени, имеет свой спектр побочных эффектов, а также требует внимания врачей и тщательной оценки динамики состояния пациента.
— По идее мы с помощью введения препаратов обучаем иммунную систему распознавать клетки опухоли и разрушать их. Это все равно что установить антивирус, — объясняет Мария.
Цели и оценка эффективности лекарственного лечения
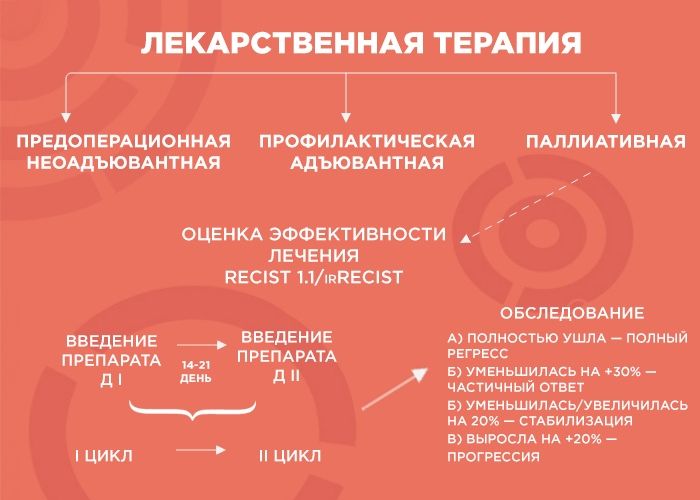
Лекарственная терапия бывает трех видов: предоперационная (неоадъювантная), профилактическая (адъювантная) и паллиативная (поддерживающая).
— Как проходит лечение в каждом из случаев?
— Начнем с предоперационной лекарственной терапии. Например, в отделение поступает пациент с диагнозом рак желудка. Результаты КТ показывают, что отдаленных метастатических очагов нет, однако в связи с распространением первичной опухоли операция на первом этапе невозможна. В этом случае лечение выглядит так: четыре курса терапии, затем — операция, а после нее — еще четыре курса адъювантной терапии. Зачем еще? Формально опухоль убрали, но есть риск возврата образования, и адъювантная терапия помогает его отсрочить.
Паллиативную терапию врач выбирает, когда хирургические методы бессильны (например, при отдаленных метастазах в легкие, печень, лимфоузлы и т.д.). Тогда лечение, в первую очередь, направлено на поддержание качества жизни пациента и контроль заболевания, и продолжительность лечения зависит от его эффекта. В химиотерапии врачи пользуются REСIST 1.1 — системой критериев оценки ответа опухоли на терапию, а в иммунотерапии — irRECIST.
— Объясню, как это работает, на примере пациента с опухолью толстой кишки и с множественными метастазами в печени и легких. Чтобы оценить серьезность ситуации, мы проводим обследование, выявляем наиболее измеряемые очаги и проводим два-три цикла химиотерапии. Большая часть курсов ХТ — введение препарата. Между первым введением и вторым — 14-21 дней — и этот временной промежуток называется циклом.
Далее мы смотрим и сравниваем. Если опухоль уменьшилась более чем на 30% — это частичный ответ, и нужно продолжать терапию до шести курсов. Если она ушла — это полный регресс, и тоже добавляем четыре курса, чтобы закрепить результат. Если опухоль увеличилась или уменьшилась на 20% — это стабилизация, мы делаем еще два курса и снова смотрим: если ситуация не изменилась, пациент отправляется на химиотерапевтические каникулы до прогрессирования заболевания, а потом схема повторяется.
Но если опухоль на фоне лечения выросла больше чем на 20% — мы имеем дело с прогрессией, вероятнее всего, это говорит нам об агрессивности опухоли. В этом случае я объясняю пациенту, что с ним происходит и почему мы меняем лечение.
— Как уговорить пациента на лечение?
— К каждому нужен индивидуальный подход. Я всегда говорю: «Химия может ухудшить ваше состояние, но бояться этого не стоит — мы попытаемся подобрать оптимальную симптоматическую терапию, которое уменьшит нежелательные явления». Если после этого во время лечения появятся данные о плохой переносимости, мы подумаем об уменьшении дозы цитостатика. Бывают случаи, когда я буквально уговариваю пациента пойти на терапию и объясняю ему, за что мы боремся. И объясняю это вне зависимости от серьезности случая — если при агрессивной опухоли человек настроен бороться до последнего, моя обязанность ему эту возможность дать.
Химиотерапия: необходимость и целесообразность. 5 вопросов онкологу
Есть надежда, что не когда-нибудь, а в ближайшее время эффективность лечения одного из самых опасных заболеваний на земле, станет гораздо выше.
1. Химиотерапия при онкологии
Какой метод лечения рака считается основным? И к какому врачу нужно идти больному в первую очередь: к хирургу, онкологу, химиотерапевту?
Чаще всего люди, узнавшие о своем онкологическом диагнозе, бегут к хирургу, рассчитывая, что тот отрежет пораженный опухолью орган и одним махом избавит от бед. Но ведь рак — не хирургическое, а системное заболевание, которое касается не только отдельного органа, а всего организма. Хирург, даже если он не раз оперировал таких больных – лишь один из участников лечения.
Для борьбы с раком есть три равнозначных метода: хирургия, лекарственная и лучевая терапия. Иногда нужны все три, иногда достаточно лишь двух, или даже одного. В идеале вопрос тактики лечения должен решаться коллегиально: хирургом, онкологом и радиологом (специалистом по лучевой терапии).
2. Эффективность химиотерапии
Почему некоторым людям при одном и том же виде рака (и даже одинаковой стадии) лечение помогает, а другим – нет? Ведь химиотерапия, как известно, проводится по специальным протоколам, единым во всем мире.
Да, протоколы одни и те же, но лечение — индивидуальное. Ведь даже рак даже одного органа – это не одна болезнь, а много разных – в зависимости от биологического подтипа опухоли, генетических мутаций. И лечатся они по-разному. Кроме того, важен выбор не только лекарства, но и его дозировки (зависит от веса и роста, состояния здоровья и прочих особенностей больного).
Есть болезни, которые встречаются очень часто (рак молочной железы, например), а есть редкие виды онкологии. Если с первыми можно успешно лечиться у любого онколога, то со вторыми лучше искать врача, который именно на этой теме специализируется.
3. Лекарственная терапия при онкологии
Что нового в последнее время появилось в лекарственном лечении рака? И улучшилась ли переносимость химиотерапии?
Современная «химия» сильно отличается от той, которой она была всего пару десятилетий назад. Поддерживающая, сопроводительная терапия помогает улучшить переносимость этого лечения и избавиться от большинства побочных явлений. К тому же наука не стоит на месте. Например, сегодня активно развивается иммунотерапия, обещающая сделать лечение рака не только более эффективным, но и менее токсичным. Появились новые цитостатики. – лекарства, поднимающие на борьбу с опухолью собственную иммунную систему человека. Например, в лечении меланомы в мире сегодня применяют онколитические вирусы, благодаря которым удалось значительно продлить жизнь людям с этим одним из самых агрессивных видов рака. Введенные в виде инъекций в опухоль, они уничтожают ее.
4. Когда химиотерапия не нужна
Тетя недавно перенесла операцию по поводу рака молочной железы. «Химию» ей не назначили, сказали просто регулярно проходить обследование. Разве так правильно?
Иногда с раком удается справиться и без химиотерапии (правда, таких ситуаций немного). А некоторым больным такое лечение просто не показано. Например, при определенных видах рака химия может быть нецелесообразна у пациентов очень пожилого возраста (ведь с годами деление клеток замедляется, поэтому у стариков опухоли растут медленнее).
От лечения отказываются и тогда, когда лекарство имеет высокий профиль токсичности, а общее состояние пациента – крайне слабое, или есть большой «букет» сопутствующих заболеваний. В таких случаях вред химиотерапии перевешивает пользу.
Иногда бывает лучше сразу перейти к паллиативному лечению, направленному не на исцеление, а на облегчение симптомов и поддержание качества жизни.
5. Когда эффективнее делать «химию»: до или после операции?
Необходимость и целесообразность проведения «химии», а также выбор момента, когда ее назначать, зависит от нескольких моментов. Главные из них – это размер опухоли, ее распространенность и биологическая характеристика, которая определяется с помощью гистологического, иммуногистохимического, а иногда и молекулярного анализа. Последний момент особенно важен, ведь иногда большой рак с метастазами менее опасен, чем маленькая, но агрессивная опухоль.
В большинстве случаев химиотерапию назначают после операции – чтобы уничтожить раковые клетки и микрометастазы, которые могли остаться незамеченными. Но «химию» делают и до операции. Или даже вместо нее. А иногда и до, и после. При метастатическом раке такое лечение зачастую проводится пожизненно.
Предоперационная «химия» помогает уменьшить размеры опухоли, и иногда настолько, что вместо большой операции можно провести вмешательство гораздо меньшего объема. Например, при раке молочной железы химиотерапия, сделанная до операции, в некоторых случаях может позволить даже сохранить пациентке грудь. Есть данные, что некоторые виды рака уже сегодня можно победить только с помощью «химии».
Онлайн консультации врачей
в мобильном приложении Доктис
Дежурный терапевт и педиатр консультируют бесплатно
Правила проведения химиотерапии: что нужно знать пациенту
Лекарственную противоопухолевую терапию получают практически все пациенты, болеющие злокачественными новообразованиями. Особенностью этого лечения является его длительность и повторяемость. Отдельные курсы введения препарата проводятся на протяжении нескольких лет, иногда в течение всей жизни больного. Какие правила необходимо соблюдать при получении этого вида лечения, чтобы сохранить качество жизни, рассказала кандидат медицинских наук Елена Викторовна Ткаченко – онколог, химиотерапевт, заведующая отделением краткосрочной химиотерапии НМИЦ онкологии имени Н.Н. Петрова.
– Елена Викторовна, когда применяют химиотерапевтическое лечение?
– Химиотерапию применяют на разных стадиях онкологического заболевания: на начальной стадии проводят предоперационную (неоадъювантную) и послеоперационную (адъювантную) терапию, также на более поздних стадиях, когда оперативное вмешательство по каким-то причинам уже невозможно. Противоопухолевая лекарственная терапия проводится и тогда, когда заболевание вернулось после радикального лечения. Поэтому многие наши пациенты получают это лечение и месяцы, и годы. И в этом нет ничего страшного или удивительного. Например, пациенты с сахарным диабетом, гипертонической или ишемической болезнями постоянно соблюдают определенные условия жизни и принимают специальные препараты. Так и онкологическое заболевание является хроническим, и, к сожалению, нередко даже после завершения лечения, через некоторое время вновь приходится его возобновлять.
– Какие побочные действия у химиотерапии?
– Побочные действия свойственны всем видам противоопухолевого лечения, даже если оно проводится по современным стандартам. Это связано с механизмом действия противоопухолевых препаратов. Осложнения бывают четырех степеней: побочные эффекты первой и второй степени больше тревожат самих пациентов, но врачи к ним относятся спокойно, потому что эти осложнения часто неизбежны и угрозы для жизни не представляют. В основном это изменения самочувствия пациента и лабораторных показателей, нетребующие лечения, например, выпадение волос или некоторое снижение лейкоцитов по результатам анализов. К третьей и четвертой степеням относятся так называемые жизнеугрожающие осложнения, они требуют серьезного внимания со стороны лечащего врача.
– Лекарственное противоопухолевое лечение пациент в основном получает через вену. Есть ли способы подготовить вены, чтобы избежать возможных побочных эффектов?
– Да, существует ряд рекомендаций, выполняя которые пациент может научиться тренировать свои вены перед введением препаратов.
– Какие побочные эффекты от введения препаратов бывают?
– При внутривенном введении цитостатиков нередко развиваются воспалительно– склеротические реакции со стороны вен. Они проявляются разнообразно: от выраженной боли по ходу сосудов уже во время инъекции до подострых флебитов, тромбофлебитов, флеботромбозов с исходом в облитерацию вен, иначе говоря, зарастание вены. При длительном введении фторурацила стенки сосудов пропитываются препаратом. Этот побочный эффект возникает практически в 100% случаев при применении некоторых препаратов. Зуд и эритема кожи по ходу вены во время введения цитостатиков отмечаются примерно в 3% инфузий, они проходят в течение 30 минут без осложнений и не свидетельствуют о подтекании препарата. Попадание под кожу раздражающих препаратов (цисплатин, дакарбазин, этопозид, фторурацил, паклитаксел, винорельбин) может вызвать жгучую боль и покраснение в месте инъекции, но если принять правильные меры, то к некрозу это не приведет.
– Существуют способы избежать осложнений или их облегчить?
– Медицинский персонал знает, как профилактировать осложнения со стороны вен. Полезно это знать и пациентам. Дело в том, что инъекции растворов цитостатиков вводятся только в минимально допустимых концентрациях. Капельные инфузии с большим количеством жидкости служат лучшим способом предупреждения повреждений стенки вен (только в случаях, когда это рекомендовано как способ введения цитостатика). Если препарат необходимо вводить струйно, то его разводят в 20-30 мл рекомендуемого растворителя, а после инъекции промывают вены изотоническим раствором NaCl. При попадании некоторых препаратов под кожу возникает гиперемия, воспаление. В трети случаев может возникнуть некроз, который без вмешательства не заживет. В этом случае необходимо обратиться за хирургической помощью.
– Что нужно делать, если химиопрепарат всё-таки попал под кожу?
– Подачу препарата необходимо остановить, но иглу или катетер вытаскивать из вены не нужно, через них медсестра извлечет попавший под кожу препарат. Для некоторых химиопрепаратов существуют антидоты (противоядия), но, к сожалению, есть они не для всех препаратов. Антидотом медсестра обколет место инъекции, а затем уже удалит из вены иглу или катетер. Пораженной конечности следует придать приподнятое положение на 48 часов, чтобы уменьшить риск воспаления и отека. Для этого достаточно закрепить руку в согнутом положении с помощью перевязки или косынки.
При попадании под кожу таких препаратов как винкристин, винбластин, винорельбин, этопозид прикладывают теплый компресс на 15-20 минут не менее четырех раз в сутки в течение 24- 48 часов. При воспалительной реакции возможна аппликация гидрокортизоновой мази.
Если развился флебит (т.е. воспаление вены), то он лечится по таким же принципам, как и обычные флебиты вне химических ожогов: применяются низкомолекулярные гепарины, антикоагулянты непрямого действия, антиагреганты.
– Почему лекарственное противоопухолевое лечение можно получать только в специализированных клиниках?
– Дело в том, что у каждого препарата свой срок и скорость введения, и для дробного и длительного введения применяется специальное оборудование. Именно поэтому ни в коем случае нельзя капать химиотерапию дома или в поликлинике, где не знают, что такое противоопухолевая лекарственная терапия. Давно уже, по крайней мере, в Санкт-Петербурге, комитетом по здравоохранению врачам, медсестрам запрещено капать противоопухолевые препараты на дому после смерти нескольких пациентов. Вы можете проводить химиотерапию только в специализированной клинике, где можно быть уверенным, что врач и медсестра понимают, что делают. Препараты должны определенным образом разводиться, капаться, храниться, их нельзя смешивать. Есть только пара препаратов, которые смешивают в одном флаконе. Все остальные должны капаться поочередно, да еще и между препаратами необходимо промывать систему физраствором. Каждый препарат должен разводиться определенным раствором: глюкозой, раствором Рингера, водой для инъекций или физраствором. Это сложная наука.
– Какое оборудование для введения препаратов сегодня используется?
– Существует несколько типов медицинского оборудования для длительного и дробного введения препаратов. Например, перфузоры – это устройства, позволяющие вводить медикаментозные препараты и растворы с исключительно высокой точностью. Порой счёт идет на десятые доли миллилитров в час (особенно часто это применяется в отделении реанимации, где скорости введения медикаментов, как правило, 1 мл/час, 5.6 мл/час и т.д.). Перфузоры могут быть механическими или электронными. Они имеют несколько названий: инфузоматы, линеаматы, шприцевые насосы, шприцевые дозаторы и др. Есть микроинфузионная помпа (инфузор) – безопасное и эффективное медицинское изделие, предназначенное для длительного, дозированного, контролируемого введения лекарственных препаратов, используемых в медикаментозной терапии (в том числе и химиотерапии). Как правило, такие помпы называют инфузор или инфузомат. Так же можно встретить названия: шприцевой насос, дозатор медицинский, инфузионный насос и др.
При использовании микроинфузионной помпы обеспечивается постепенное поступление препарата в организм за счет механизма сокращения резервуара и трубки инфузора.
– Какие правила введения противоопухолевых препаратов должен знать пациент?
– Введение противоопухолевых препаратов должно выполняться только в отделениях, специализирующихся на цитотоксической химиотерапии исключительно под наблюдением компетентного врача. Этот метод лечения требует специальной подготовки, тщательности при приготовлении растворов препаратов и соблюдения всех правил их введения, указанных в инструкциях. Поэтому к выполнению работ с цитостатиками должны допускаться медицинские сестры, прошедшие специальную подготовку, обученные безопасным методам и приемам работы. Также необходимо соблюдать последовательность и скорость введения препаратов, учитывать химические свойства при использовании оборудования для их введения. Соблюдать правила и сроки хранения препаратов как в аптечной упаковке, так и после их приготовления. Ни в коем случае нельзя смешивать препараты «в одном флаконе», если в инструкции по применению данных препаратов нет для этого особых указаний. Необходимо знать и соблюдать все условия хранения препарата и его транспортировки, если он приобретается и доставляется в клинику самим пациентом. Это очень важно. Потому что многие пациенты говорят: «Я куплю, привезу, а вы мне прокапайте!» Если вы купите, например, герцептин в аптеке и привезете его к нам не в холодильнике, а в обычной упаковке, что мы получим? В лучшем случае – воду. В случае личного приобретения препаратов уточните правила хранения и транспортировки у своего врача.
– Какие способы внутривенной доставки препаратов сегодня используются?
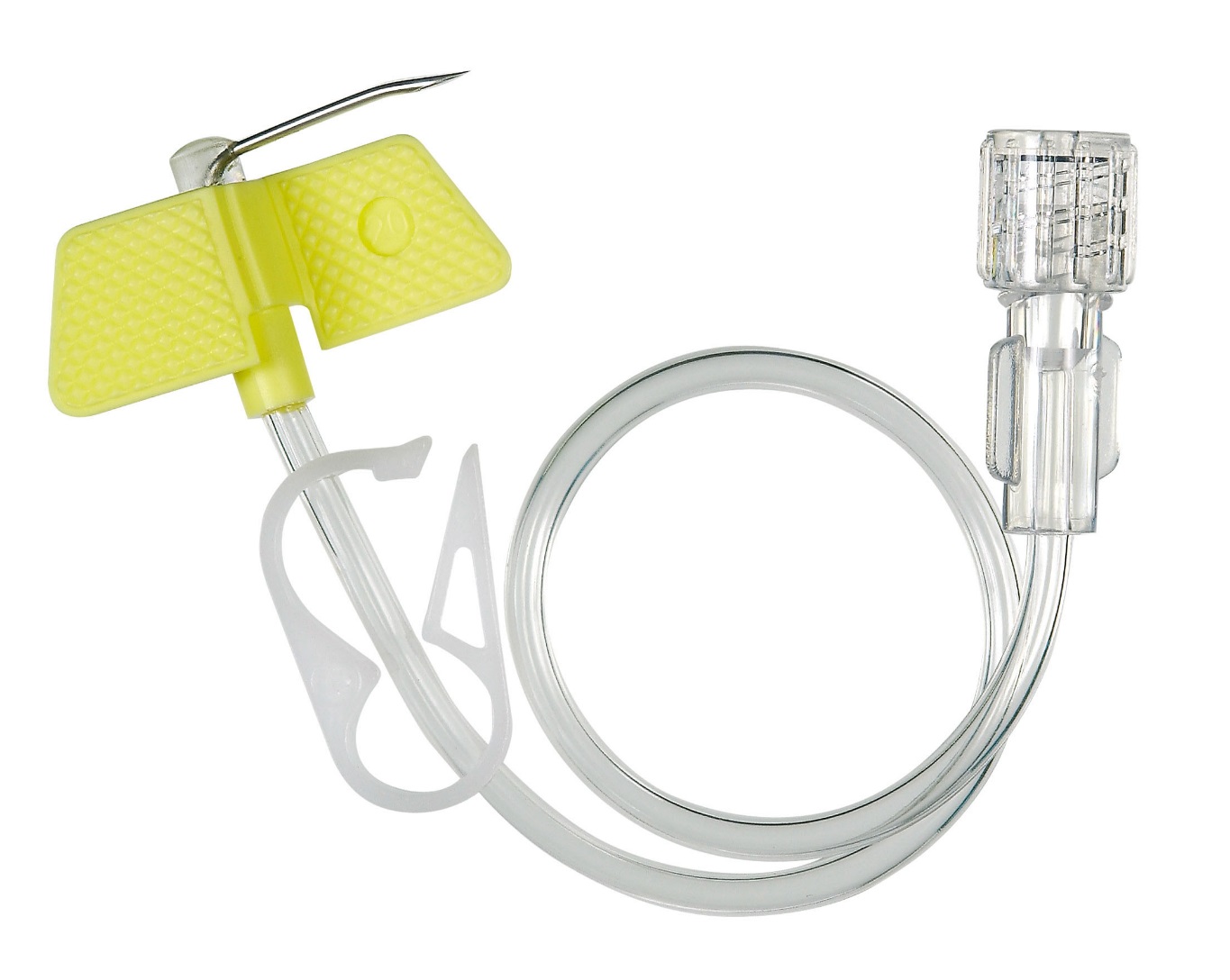
– На сегодняшний день существует несколько способов: через иглу, переферический венозный катетер, центральный венозный катетер и имплантируемый порт. Вы знаете, когда я начала работать в медицине, мы работали еще многоразовыми иглами. Они были тупые, поэтому могли долго стоять в вене. А как только появились одноразовые иглы, стали возникать сложности. Они же острые, чуть пациент шевельнулся, она прокалывает вену моментально. Поэтому если необходимо вводить препарат долго, то делать это лучше через переферический венозный катетер. Если его устанавливать в асептических условиях, правильно ухаживать, то до 10 дней им можно пользоваться.
Для более длительного венозного доступа используют центральный венозный катетер, особенно в тех случаях, когда необходимо обеспечить полное парентеральное питание у хронических больных. Край центрального венозного катетера вводится в пустотелую вену. У этих катетеров много преимуществ. Но неправильный уход за ними может привести и к серьезным осложнениям. Поскольку если возникнет воспаление, то оно будет не местным, а общим. Поэтому центральный венозный катетер требует профессионального использования и тщательного ухода.
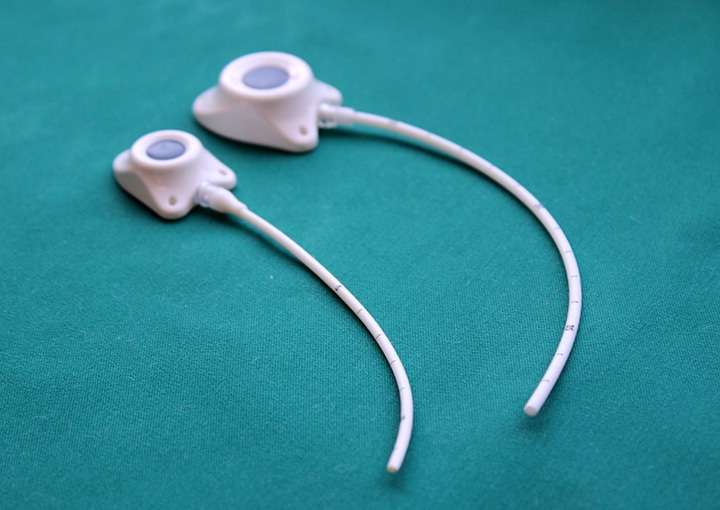
Еще существует порт-система. Это инвазионный порт, который представляет собой титановый резервуар в виде толстой монеты диаметром около 4-4,5 см и толщиной около 1 см, который покрыт изнутри биоинертным полимером. На верхней плоской части установлена мембрана из многослойного силикона, через которую вводят лекарственные препараты. Порт имеет тонкую трубочку-катетер длиной до 10-15 см, которая пропускается в яремную вену и реже в артерию.
Показания к применению порт-системы:
Есть свои противопоказания, но они все относительны, и доктора сами принимают решение, учитывать их или нет.
– Какие очевидные преимущества у порт-системы?
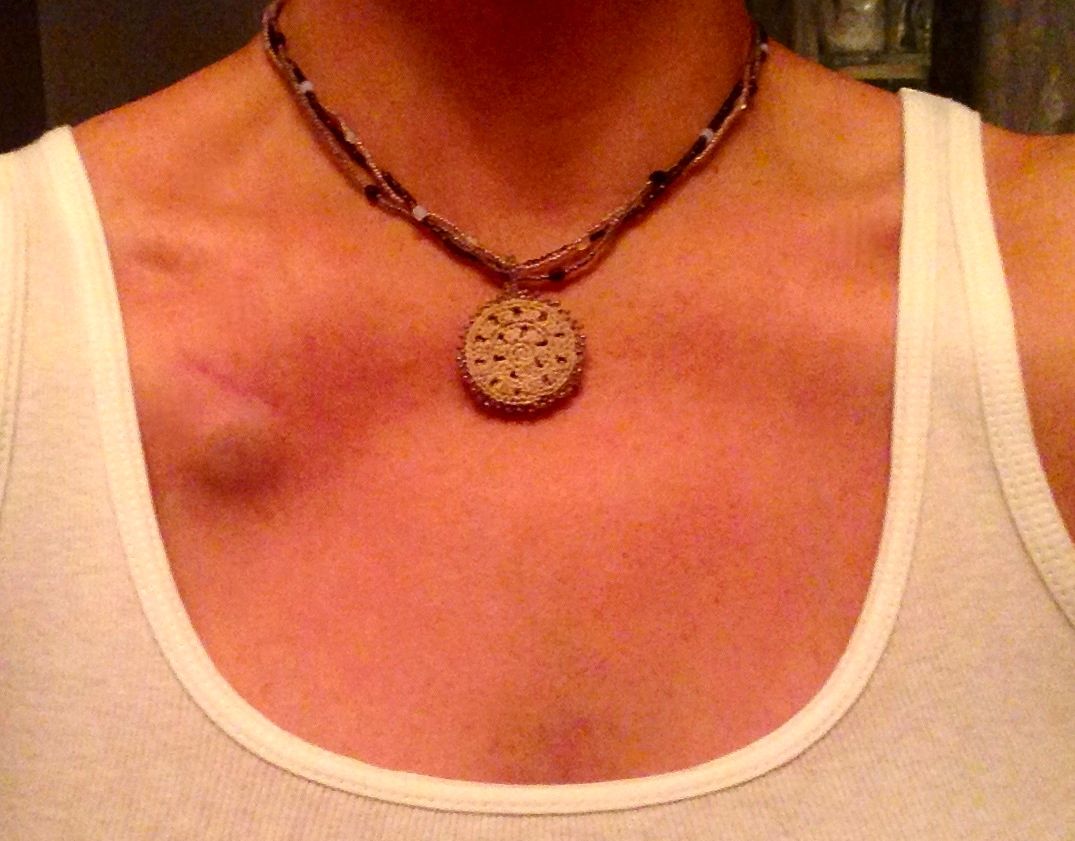
– Их много. Главное, что человек может вести привычный образ жизни. Венозный порт имплантируется под кожу пациента, он не виден снаружи, поэтому не может быть задет одеждой, инфицироваться при приеме ванны, «выскочить» из вены. Люди с установленными портами могут заниматься спортом, выполнять физическую нагрузку, плавать, путешествовать, отдыхать заграницей и т.д. Им можно проходить МРТ и КТ исследования, он совместим с магнитным полем. При правильной эксплуатации порт-система может работать 5-7 лет. Существуют наблюдения, что если за порт-системой правильно ухаживать, то фактически она может использоваться пожизненно. В некоторых странах установка порт-системы является неотъемлемой частью «золотого стандарта» лечения. В Западной Европе порты широко применяются у пациентов с впервые выявленным онкологическим заболеванием, которым планируется проведение множественных сеансов химиотерапии, особенно цитостастическими препаратами, которые вызывают повреждение периферических вен. Кроме того, инфузионные порты устанавливаются пациентам с тонкими периферическими венами на верхних и нижних конечностях. В отечественной онкологической практике порты пока используются редко.
– Как происходит установка инфузионного порта?
– Процедура имплантации порта проводится под местной анестезией и абсолютно безболезненна. Порт, как правило, имплантируется в правую подключичную область, хотя место может быть любым, главное, чтобы рядом была проходимая вена. Процедура занимает от 10 до 30 минут и не требует длительной госпитализации. Пациент находится в стационаре около часа после установки, а потом самостоятельно может ехать домой. Врач предоставляет ему необходимую информацию о правилах поведения после операции и о лекарствах, которые необходимо принимать в течение нескольких дней после процедуры.
– Как ухаживать за порт-системой?
– О каких «сигналах тревоги» должен знать пациент с установленным портом?
– Надо понимать, что при использовании порт-системы бывают и осложнения. Пациент должен насторожиться и обратиться к врачу в случае:
Источники
Материал подготовила:
НАТАЛЬЯ СУББОТИНА
специалист по связям с общественностью
НМИЦ онкологии им Н.Н. Петрова,
Кемеровский государственный университет, факультет филологии и журналистики, отделение журналистики
Материал подготовила:
ЮЛИЯ КОБЛЯКОВА
специалист по связям с общественностью
НМИЦ онкологии им Н.Н. Петрова,
Санкт-Петербургский политехнический университет Петра Великого
Кафедра рекламы и связей с общественностью