«Глисты»: как выявить непрошенных гостей
Глистные инвазии в современных условиях многим кажутся чем-то казуистическим, и потому настороженности не вызывают. На деле же, «глисты» по-прежнему занимают видное место в структуре устойчивых дефицитных состояний (особенно часто железа), патологии печени, кожи, бронхолегочной системы. А их выявление требует понимания ряда особенностей.
«Глистные» симптомы
Стоит отметить, что паразитам «не выгодна» гибель хозяина. Поэтому их присутствие, как правило, долгое время не сопровождается какими-либо признаками.
1. На первый план может выходить снижение аппетита и немотивированное похудение.
2. Также характерны рецидивирующие дефицитные состояния, «пищевое» или какое-либо другое происхождение которых уже исключено. А наиболее часто «носители глистов» страдают от железодефицитной анемии.
3. Кроме того, паразиты раздражают иммунную систему, за счет могут провоцировать развитие аллергических (включая бронхиальную астму) и атопических заболеваний.
4. Если черви и личинки «выбрали» для обитания кишечник, среди первых признаков инвазии могут быть диспептические явления, как тошнота, нарушения стула, метеоризм, периодические боли в животе, а также непереносимость некоторых продуктов питания.
5. А, когда «под удар» попадает печень – чаще всего «находка» бывает случайной, в виде «необъяснимого» повышения маркеров печеночного воспаления (АЛТ, АСТ) или изменений на УЗИ.
Поэтому, в первую очередь обследование показано тем, кто уже имеет подобные патологии неясного происхождения, или высокий риск инфицирования (например, трихинеллез при употреблении недожаренного мяса свиней и кабанов или сала с прослойками мяса).
Когда «кал» не информативен
Самым известным исследованием, бесспорно, является «кал на яйца глист». Однако этот анализ имеет ряд объективных недостатков, ввиду которых не способен обеспечивать высокую выявляемость паразитов.
Во-первых, кал может помочь в выявлении только тех гельминтов, которые «остановились» на уровне кишечника. В то время как личинки способны мигрировать в ряд других органов, среди которых печень, мышцы, легкие и даже головной мозг.
Во-вторых, анализ рассчитан на выявление только яиц червей, то есть имеет сильную зависимость от жизненного цикла паразита.
«Угадать» в какой момент времени черви «решат» отложить яйца – задача, очевидно, невыполнимая. Ведь никаких наглядных признаков этого этапа их «жизни» не существует.
Поэтому исследование кала на гельминты рекомендуется сдавать несколько раз (не менее 3-х) с перерывами в несколько дней. И даже в этом случае, «шансы» на выявление паразитов остаются достаточно низкими.
Анализ крови на антитела к гельминтам такими недостатками не обладает, а чувствительность исследования к разным видам червей достигает высоких 75-90%.
При этом антитела IgG появляются в крови спустя 3-4 недели от инфицирования. Анализ можно проводить как прицельно к интересующему виду паразитов, так и комплексно, с учетом наиболее распространенных паразитозов.
Выявление в крови антител к паразитам – обоснованный повод для применения препаратов и углубленного обследования органа-мишени, даже в том случае, если обследуемого ничего не беспокоит.
А, помимо прочего, такой анализ успешно дополняет традиционную диагностику по анализу кала.
Дирофиляриоз: симптомы, подкожный и внутренний дирофиляриоз у человека, лечение и профилактика
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз: симптомы, подкожный и внутренний дирофиляриоз у человека, лечение и профилактика
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз (Dirofilariasis) — относится к ларвальным гельминтозам. То есть, при этом заболевании паразитирует не взрослая особь нематоды, а ее личинка, не достигшая половой зрелости. Разносчиками заразы являются комары, поэтому наиболее часто этот гельминт встречается в теплом климате: от Австралии, Южной Америки и Африки до Юга России и Средней Азии. На протяжении последних лет наибольшее количество заболевших дирофиляриозом регистрировалось в Иране и Греции. Но в последние годы все чаще регистрируют эту болезнь и в умеренном климате.
Так, на территории Российской Федерации на протяжении нескольких лет выявляют по 35-40 случаев дирофиляриоза ежегодно. Причем география заражения весьма обширна — от теплого Ростова, умеренных климатических зон Тулы и Рязани, до морозной Сибири. На самом же деле уровень заболеваемости может быть значительно выше. Поскольку этот вид гельминтоза долго считался присущим только животным, то медики его не изучали, и на сегодняшний день о нем мало знают и не сразу могут поставить верный диагноз.
Большинству инфицированных дирофилярией пациентов, при обращении за медицинской помощью первоначально ставят диагноз либо фурункулез, либо киста или опухоль. Первое описание заболевания человека дирофиляриозом относится к середине 19-го века, которое сделал врач из Португалии Лузитано Амато после того, как удалил гельминта из глазного яблока у ребенка. В России первым зарегистрированным случаем дирофиляриоза считается описанный земским доктором Владыченским в 1915 году.
Причины возникновения дирофиляриоза
В буквальном смысле с латыни дирофилярия «diro, filium» переводится как «злая нить». Как уже упоминалось ранее, в человеческом организме может жить личиночная стадия глиста — микрофилярия. Наиболее часто люди инфицируются нематодами Dirofilaria repens и Dirofilaria immitis, которые живут в организме домашних любимцев — собак и кошек. Крайне редко дирофилярия может передаться человеку от дикого животного — эти нематоды паразитируют у всех представителей семейств псовых и кошачьих, у приматов, у медведей, у тигров, у выдр. Именно поэтому большая доля заболевших дирофиляриозом приходится на охотников.
Как происходит заражение дирофиляриозом?
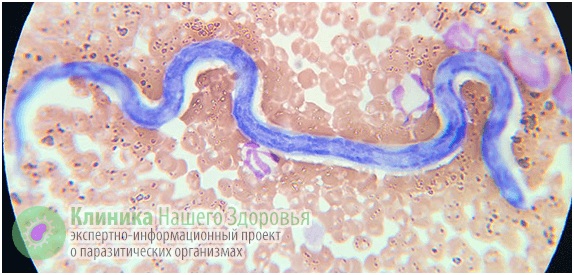
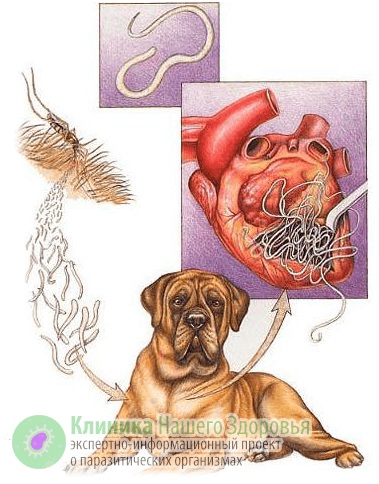
Механизм заражения у людей — трансгемный, то есть инфицирование происходит через кровь. Передается болезнь, зачастую, через укусы комаров. Реже, через укусы блох, слепней и других видов кровососущих насекомых. А источником заразы, как это ни прискорбно, выступают наши домашние животные. В первую очередь собаки, изредка кошки. По данным ветслужбы до 30% собак, живущих в городах, страдают от упомянутой инвазии. В сельской местности этот показатель еще выше. В организме животного взрослые дирофилярии паразитируют в сердце, легких, бронхах и крупных кровеносных сосудах. Самки выделяют в кровь тысячи личинок-микрофилярий, которые имеют микроскопический размер — до 0,3 мм в длину. Именно поэтому они с кровотоком и лимфотоком разносятся по всему организму.
Микрофилярии так микроскопичны, что с кровью и лимфой попадают не только во все органы и ткани человека или животного, но даже преодолевают плацетнарный барьер и внутриутробно инфицируют плод. С кровью животного микрофилярия попадает к промежуточному хозяину — комару. Насекомое, в свою очередь, кусает инвазированное животное, личинки попадают в его брюшную полость, но часть из них остается в хоботке комара. Когда насекомое кусает следующую жертву — часть паразитов из хоботка попадает в кровоток следующего хозяина. Так дифиляриоз передается от животного к животному и к человеку.
У людей тотальная восприимчивость к дирофилриозу – то есть, если человека кусает инфицированный комар, то он заразится со 100% вероятностью. Но в наибольшей зоне риска заражения дирофиляриозом находятся некоторые категории людей, среди которых:
Этапы развития дирофиляриий
Когда комар (реже другое кровососущее насекомое) заглатывает личинку нематоды с кровью, та около суток остается у него в кишечнике. Затем микрофилярии мигрируют в обратном направлении — к хоботку комара, где дозревают до инвазивной стадии. В этот период, комар, кусает жертву и заражает ее дирофиляриозом.
У нового хозяина около трех месяцев личинки остаются в месте комариного укуса: в коже или в подкожной клетчатке. Именно тут микрофилярии линяет и уже более жизнеспособными попадают в кровоток и разносятся по организму. Паразитировать микрофилярия может около трех лет.
До половозрелости дирофилярия развивается только в организме животных. Человеческий организм для нее тупиковый вариант, так как большинство личинок все же гибнут в крови людей. Это значит, что человек не может быть источник заражения.
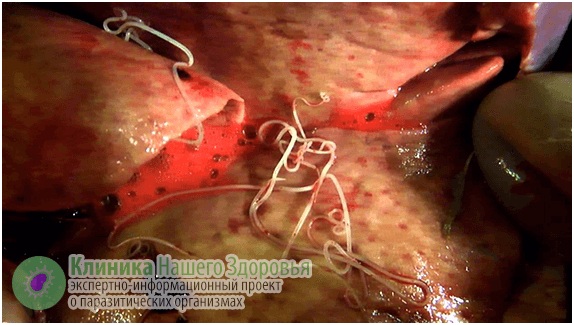
Воздействие дирофилярий на человека
Обычно, у больного дирофиляриозом обнаруживается только один паразит, а развитие этой особи проходит в течение 8-9 месяцев. Зачастую гельминт не покидает места внедрения — живет под кожей, где его оставил комар после укуса.
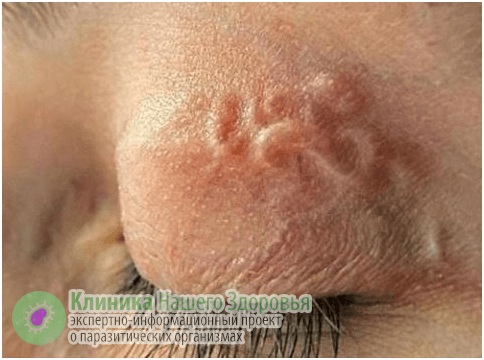
Главная опасность дирофиляриоза — первичные реакции на месте внедрения микрофилярии. Может возникнуть сильная аллергическая реакция. Кроме того, кожа воспаляется, образуются уплотнения (шишки) довольно большого диаметра. Внутри этих уплотнений находится серозная жидкость и/или гной, внутри этого содержимого и обитает какое-то время дирофилярия. Часто паразит погибает, тогда уплотнение постепенно может само рассосаться. Но чаще все же требуется хирургическое вмешательство.
Виды дирофиляриоза
Инвазионное заболевание вызывает червь-паразит. Личинки нитевидной нематоды, вызывающие болезнь, бывают нескольких разновидностей, и поэтому заражение ими приводит к разным формам заболевания.
Dirofilaria repens и Dirofilaria immitis — основные виды, поражающие собак и реже кошек. Именно эти разновидности гельминта являются самыми распространенными среди заболевших людей, ведь в подавляющем большинстве случаев дирофиляриоз у человека появляется при укусе комара-переносчика, контактировавшего до этого с данными животными.
В России и странах ближнего зарубежья встречается в основном подкожный дифиляриоз. Висцеральный дирофиляриоз распространен в жарких странах Азии, Японии, Индии, США, Африке, Канаде, Вьетнаме, Австралии, на юге Европы.
Симптомы и места распространения дирофиляриоза
Скрытая форма дирофиляриоза у человека длится от 1 до 12 месяцев. Основным симптомом является появление под кожей или слизистой, болезненного уплотнения, с покраснением и зудом на месте внедрения. При этом гельминт под кожей может перемещаться (со скоростью до 15 мм в сутки), что может быть заметно для человека, как по ощущениям, так и визуально. Часто, заметив на теле уплотнение похожее на опухоль, пациенты обращаются к хирургу, а тот решает, что это липома, опухоль, фиброма, атерома и т.п., а затем уже в ходе операции обнаруживает гельминта.
У дирофилярий есть любимые места на теле человека — это органы зрения, ноги и руки, шея, лицо, грудь, мошонка. Могут появиться такие симптомы, как слабость, пассивность, тошнота, нервозность, бессонница, повышенная температура, боли в голове и в области поражения паразитом. В 50 % случаев обычно поражаются органы зрения. Человек жалуется на ощущение чего-то ползающего в глазу, у него наблюдается покраснение век и глаз, блефароспазм. При перемещении гельминта возникает боль, слезотечение и зуд. Иногда через конъюнктиву виден сам гельминт.
При нахождении дирофилярии в глазу вокруг нее образуется гранулема, что вызывает развитие экзофтальма и диплопии. Поражение глаз приводит к ослаблению зрения. Человек способен увидеть мигрирующего паразита. Наблюдения показали, что его перемещения усиливается под воздействием тепла.
Дифиляриоз обычно носит хронический характер, с рецидивами, характеризующимися периодами вспышек и затихания заболевания. Если вовремя не заняться лечением, вероятны воспаления тканей, и возникновение абсцесса.
Симптомы внутреннего дирофиляриоза
При этой разновидности паразитом поражаются легкие. Личинка живет в левом желудочке сердца и легочных артериях, образуя при этом фиброзную капсулу. Обычно болезнь протекает бессимптомно, реже вызывает боль в груди, кашель и кашель с кровью.
Заболевание часто выявляется случайно, например, при рентгене грудной клетки (видны узелки размером 1-2 см) или при оперировании легких.
Диагностика дирофиляриоза у человека
Диагностика заболевания представляет определенную сложность, так как её симптоматика схожа со многими другими заболеваниями, поэтому врачами часто ставится ложный диагноз и своевременное лечение затягивается. Основными жалобами пациентов являются появление мигрирующих подкожных узлов, ощущения перемещения паразита.
Диагноз дирофиляриоза можно подтвердить, сдав следующие анализы:
Кроме того, перед постановкой диагноза специалист проводит анализ условий проживания больного, времени года, его деятельности. Факторами риска являются наличие домашних и бездомных собак и кошек, комаров, выезд в лес, на рыбалку, на дачу или в сад.
Риск заболевания дирофиляриозом особенно увеличивается в период высокой активности комаров. В связи с чем важны профилактические меры, производимые санитарными службами по ликвидации насекомых на территории водоемов. Известно, что заболевание носит сезонный характер, поэтому основное количество заболевших фиксируется весной и летом. Пики заболеваемости приходятся на периоды июнь-июль и октябрь-ноябрь.
Диагностика дирофиляриоза у животных
Для профилактики заболевания домашним животным необходимо регулярно давать противоглистные препараты. Признаками заболевания паразитами служат различные высыпания, уплотнения, ранки, опухоли на коже.
Больше всего при поражении страдает сердечно-сосудистая система животного. Поведение его становится пассивным, теряется аппетит, отмечается температура, кашель. Собака может прихрамывать и страдать от судорог.
Лечение дирофиляриоза
Форма болезни диктует методы лечения. Обычно у человека паразитирует одна неполовозрелая особь. Основной метод избавления от паразита — хирургический. Чтобы исключить перемещение паразита применяют дитразин. Редко применяется терапия медикаментами с использованием ивермектина или диэтилкарбамазина. Дополнительно при лечении используются успокаивающие и антигистаминные лекарства, нестероидные противовоспалительные средства, глюкокортикостероиды.
При глазном дирофиляриозе основным методом лечения будет удаление гельминта с помощью операции и последующие назначение дезинфицирующих и противовоспалительных препаратов для глаз, иногда также прописываются капли дексаметазона для уменьшения воспаления. Обязательно назначаются антигистаминные средства.
Профилактика дирофиляриоза
В России 4-30% (в зависимости от географии их проживания) домашних и уличных собак являются хозяевами-переносчиками микрофилярий. Самый большой процент зараженных животных в Греции и Иране- 25-60%.
Профилактика заболевания включает в себя истребление комаров и ограничение контакта с ними животных и человека, своевременное выявление дирофилярий животных и их лечение, борьба с бродячими животными, противоглистная профилактика у домашних питомцев.
Так как очагами дирофиляриоза являются водоемы около жилых районов, очевидна эффективность мер, применяемых санитарными органами по борьбе с кровососущими насекомыми. К тому же необходима борьба с комарами в подвалах жилых домов, ведь здесь эти паразиты могут с комфортом обитать весь год. Из подвалов жилых домов комары и другие насекомые попадают по вентиляционной системе в квартиры.
В лесу и около водоемов необходимо использовать репелленты и защищать участки тела с помощью одежды. Животным кроме репеллентов могут быть одеты специальные ошейники. По возможности старайтесь отказаться от прогулок в вечернее и ночное время суток.
Человек сам в ответе за собственное здоровье, а также за здоровье своих детей, родных и близких, поэтому отправляясь в отпуск в теплые страны, будьте бдительны! Легче предотвратить болезнь, соблюдая профилактические меры, чем лечить ее последствия!
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).