Критические точки стали. Открытия Дмитрия Чернова
Сегодня мы расскажем вам об одном из самых главных открытий в деле производства металлопроката. Открытии, которое было сделано нашим соотечественником.
В середине 19 века металлургия в России развивалась весьма активно. К сожалению, качество не всегда успевало за количеством. Так, например, оставлял желать лучшего даже металл, изготавливаемый в России для отливания артиллерийских орудий. В 1866-68 г. решить проблему все большего количества брака при производстве пушек взялся уже достаточно известный к тому времени русский металлург и изобретатель Дмитрий Константинович Чернов.
Изучив особенности производства на военных заводах, он пришел к выводу, что под влиянием различных температур сталь претерпевает определенные полиморфические превращения. Температурные границы, при которых это происходит, впоследствии были названы критическими точками стали или точками Чернова.
Точки a, b, c и d
Если не нагреть сталь до точки b (около 1420 К), она не поменяет своей структуры.
Точка c по Чернову – это точка плавления стали (приблизительно 1300-1500 градусов по Цельсию). Выше этой температуры нагревать сплав не имеет смысла.
Чуть позже, чем первые три (в 1878 г.), была открыта и точка d (470К или 196.85 С). Согласно исследованию Дмитрия Чернова, именно до этой температуры необходимо охладить сталь для ее полной закалки.
Влияние открытий Чернова
Результаты своих первых исследований Дмитрий Чернов опубликовал в одном из номеров «Записок Русского технического общества». По утверждению многих историков промышленности именно эта публикация положила начало металлургии, как науке, а не как обычному ремеслу.
Точки Чернова до сих пор используются при производстве металлопроката. Получив новые буквенные обозначения, они были лишь незначительно подкорректированы в 20 веке.
Критические точки сталей (точки Чернова)



Открытие Д. К. Черновым в 1886 г. критических точек стали послужило фундаментом для создания науки о металлах и построения диаграммы железоуглеродистых сплавов. Важнейшее значение работ Чернова – установление связи между обработкой стали, ее структурой и свойствами. Это обеспечило возможность назначения режимов термической обработки сталей.
Критические точки сталей обозначают буквой А с индексом, указывающему, какому процессу соответствует критическая точка: нагреву – индекс «с», охлаждению – «r». Кроме того, каждая точка имеет постоянный номер, который соответствует определенной температуре (линии диаграммы).
Для определения критических точек сталей рассмотрим «стальную часть» диаграммы на рис. 24. Сечение I здесь соответствует доэвтектоидной стали (С
Затем сечение пересекает линию PSK, температура – 727°С, критическая точка Ас1 – превращение перлита в аустенит (начало перекристаллизации). Далее сечение пересекает линию МО, температура – 768°С, точка Ас2 – превращение железа-альфа в немагнитное бета-железо, сталь становится немагнитной. Дальнейшее повышение температуры приводит к пересечению линии GS – точка Ас3, сталь переходит в однофазное аустенитное состояние (конец перекристаллизации).
Температура точки Ас3 зависит от содержания углерода в стали, поскольку линия диаграммы GS наклонная.
При охлаждении номера точек не меняются. В точке Аr3 (линия GS) начнется перекристаллизация стали, в точке Аr2 (768°С) бета-железо переходит в магнитное альфа-железо, в точке Аr1 (727°С) аустенит переходит в перлит и заканчивается перекристаллизация стали, а в точке Ar0 цементит становится магнитным. Следовательно, доэвтектоидные стали имеют критические точки А0, А1, А2 и А3.
У заэвтектоидных сталей С > 0,8 % (сечение II на рис. 24). При температуре 210°С в точке Ас0 цементит теряет магнитные свойства. Дальнейший нагрев вызывает превращение перлита в аустенит в точке Ас1, температура – 727°С (начало перекристаллизации). Затем сечение пересекает линию диаграммы ES. На этой линии перекристаллизация заканчивается и происходит переход стали в однофазное аустенитное состояние. Точка на линии ES номера не имеет, она обозначается буквой m (Асm). Температура этой точки зависит от содержания углерода в стали. Следовательно, заэвтектоидные стали имеют три критические точки: А0, А1 и Аm.
Исходя из вышеизложенного, можно утверждать, что эвтектоидные стали (углерода 0,8 %) будут иметь две критические точки: А0 и А1 (см. рис. 24).
Как указывал Д. К. Чернов, важнейшими значениями температуры (критическими точками) стали будут А1, А3 и Аm. От температуры нагрева до указанных значений зависят фазовый состав, структура, а следовательно, и свойства стали.
Итак, при охлаждении на линии AC (см. рис. 22) из жидкого раствора начинают выделяться кристаллы твердого раствора углерода в гамма-железе – аустенита. По линии CD из жидкого раствора начинают выделяться кристаллы цементита первичного. Под этой линией в области CDF все сплавы будут двухфазными: жидкий раствор и кристаллы цементита первичного. В точке С диаграммы (1147°С), соответствующей концентрации 4,3 % углерода, где линии АС и CD пересекаются, происходит одновременная кристаллизация аустенита и цементита первичного с образованием мелкой смеси их кристаллов – эвтектики. Эвтектика в железоуглеродистых сплавах называется ледебуритом.
Точка С диаграммы – эвтектическая, а линия ECF, проходящая через эту точку, – эвтектическая прямая, и в каждой точке этой прямой сплавы заканчивают первичную кристаллизацию образованием эвтектики. Сплавы с содержанием углерода более 2,14 %, в которых при первичной кристаллизации образуется эвтектика (ледебурит), называют чугунами. Излом таких чугунов светлый, блестящий (белый излом), поэтому такие чугуны называют белыми. В белых чугунах весь углерод находится в химически связанном состоянии в виде цементита.

Чугуны, содержащие менее 4,3 % углерода, называются доэвтектическими, 4,3 % – эвтектическими, более 4,3 % – заэвтектическими.
Доэвтектические чугуны имеют в избытке гамма-железо, которое, растворяя углерод, образует аустенит (рис. 25, а). Поэтому в первую очередь в них образуются его кристаллы. Так будет до тех пор, пока жидкий сплав не приобретет эвтектический состав (4,3 % углерода); после этого он кристаллизуется на линии ЕС диаграммы состояния, образуя ледебурит. После окончания первичной кристаллизации эти сплавы состоят из кристаллов аустенита, окруженных эвтектикой, – ледебуритом.
У эвтектического чугуна, как у чистого металла кристаллизация начинается и заканчивается в точке С при постоянной и самой низкой для всех сплавов температуре – 1147°С. Его структура – мелкая смесь кристаллов аустенита и цементита – ледебурит.
Заэвтектические чугуны в избытке имеют углерод, который способствует образованию, в первую очередь, кристаллов цементита первичного. За счет выделения углерода состав жидкого сплава изменяется, и когда в нем останется 4,3 % углерода, он закончит кристаллизацию на линии СF при температуре 1147°C образованием ледебурита, структура его будет состоять из кристаллов цементита первичного и ледебурита (рис. 25, б).
Рис. 25. Микроструктура белых чугунов (´ 500):
а – доэвтектический; б – заэвтектический
При охлаждении белых чугунов после окончания процесса кристаллизации в них будут происходить структурные и фазовые изменения. В доэвтектических чугунах в интервале температур от 1147 до 727°C вследствие понижения растворимости углерода от 2,14 до 0,8 % из аустенита будет выделяться цементит вторичный. На линии PSK при температуре 727°C произойдет эвтектоидное превращение аустенита в перлит и ледебурит будет состоять из перлита и цементита. Следовательно, структура этих чугунов будет перлит, цементит вторичный и ледебурит (см. рис. 25, а).
В эвтектических и заэвтектических чугунах в процессе охлаждения после первичной кристаллизации будет происходить только эвтектоидное аустенито-перлитное превращение на линии PSK при температуре 727°C. Входящий в структуру этих чугунов ледебурит также будет состоять из перлита и цементита (см. рис. 25, б).
Классификация и маркировка углеродистых сталей и чугунов
— по диаграмме состояний – доэвтектоидные, эвтектоидные и заэвтекто-идные;
— по структуре – феррит + перлит, перлит, перлит + цементит вторичный;
— по способу выплавки – выплавленные в конверторах (конверторные), мартеновских и электрических печах (мартеновские и электростали);
— по содержанию углерода – низкоуглеродистые (менее 0,3 %), среднеуглеродистые (0,3 – 0,7 %) и высокоуглеродистые (0,7 % и более);
— по степени раскисления и характеру затвердевания – спокойные (сп), полуспокойные (пс), кипящие (кп). Кипящие стали содержат минимальное количество кремния (не более 0,07 %), дешевы, хорошо поддаются холодной листовой штамповке, но по сравнению со спокойными имеют высокий порог хладноломкости, и их нельзя использовать для изготовления ответственных конструкций в условиях Сибири и Севера. Порог хладноломкости – отрицательная температура, при которой металл переходит в хрупкое состояние;
— по качеству – обыкновенного качества, качественные и высококачественные. Под качеством стали понимается совокупность свойств, определяемых металлургическим процессом ее производства. Основными показателями для их разделения служат нормы содержания вредных примесей – серы и фосфора;
— по назначению – конструкционные и инструментальные. Конструкционные стали предназначены для изготовления металлоконструкций, деталей машин и должны обладать высокой конструктивной прочностью (определенным комплексом механических свойств), иметь хорошие технологические свойства.
Обычно они содержат не более 0,6 – 0,7 % углерода и имеют ферритно-перлитную структуру, т. е. являются сталями доэвтектоидными. Инструментальные стали, содержащие не менее 0,7 % углерода, должны обладать высокой твердостью, прочностью и износостойкостью, предназначены для изготовления инструментов. Это стали эвтектоидные и заэвтектоидные, их структура – перлит или перлит и цементит вторичный.
Критические точки стали
Что такое критические точки стали
Критические точки стали или точки Чернова — критические температуры, при которых происходит изменение фазового состояния и структуры стали при нагреве или охлаждении её в твёрдом виде. Установлены Черновым Дмитрием Константиновичем в 1868 году.
Критические точки обозначают буквой А. Нижняя критическая точка соответствует линии PSK диаграммы состояния железо-углерод. Эта точка называется А1 и соответствует превращению аустенита в перлит при охлаждении или перлита в аустенит при нагреве. Верхняя критическая точка называется А3. Критическая точка А3 для доэвтектоидных сталей лежит на линии GS диаграммы железо-углерод и соответствует началу выделения феррита при охлаждении или концу его растворения при нагреве. Критическая точка А3 для заэвтектоидных сталей лежит на линии SE и соответствует началу выделения вторичного цементита при охлаждении или концу его растворения при нагреве.
В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс “с” при нагреве (от французского слова chauffage – нагрев) и индекс ”r” (от французского слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Точка Mn в таблице обозначает температуру начала мартенситного превращения.
При термической обработке сталей, значения критических точек чаще всего используют чтобы определить температуру нагрева под закалку.
Как выбрать температуру нагрева под закалку
Для доэвтектоидных сталей (содержание углерода в стали менее 0.8%) обычно выбирают температуру закалки по формуле Ас3+30. 50°C. На практике встречаются случаи, когда доэвтектоидные стали закаливают с интервала температур между Ас1 и Ас3. В этом случае структура стали будет состоять из мартенсита и нерастворенного феррита. Такой процесс называется неполной закалкой и теоретически является браком. На практике к такую схему используют, чтобы снизить коробление деталей или исключить трещинообразование в высоколегированных сталях.
Заэвтектоидные стали обычно нагревают под закалку до температур Ас1+30. 50°C. После закалки, структура стали будет состоять из мартенсита и вторичного нерастворённого цементита, который повышает твердость и износостойкость изделий.
ТОЧКИ ЧЕРНОВА
Инженер Д. К. Чернов в 1866 году начал работу в сталеплавильном цехе военного завода в Петербурге.
Дмитрий Константинович Чернов (родился в 1839 году, умер в 1921 году).
Почему одни пушки, выпускаемые заводом, прочны и долговечны, а другие быстро разрушаются? Не зависит ли прочность стали от её обработки? Вот вопросы, которые поставил перед собой инженер Чернов.
Первые же исследования убедили Чернова в том, что непрочная орудийная сталь всегда оказывается крупнозернистой. Но почему в одних случаях в стали образуются крупные зёрна, а в других — мелкие? Может быть, величина зерна зависит от режима ковки и закалки?
Чернов начал выяснять, что происходит со сталью при закалке. Он нашёл, что при нагревании сталь не остаётся неизменной: при определённых температурах меняются и размеры кристаллов (зёрен) и свойства стали. Эти температуры Чернов назвал критическими точками а и Ь теперь их называют точками Чернова.
Сталь имела темновишнёвый цвет (около 700°), а в точке
Ь — матово-красный (800—850°). В своих лекциях по металлургии в Артиллерийской академии Д. И. Чернов приводит шкалу всех критических температур для стали:
200° 450° промежуток
О ■ 1 I I ■ ■ II | | I _ I
Температура Температура (___ | Температура
Охлаждения полного Красное плавления
Для полней отпуска каление закалки
Какое же значение имеют эти критические точки?
Между точками х и с лежат температуры плавления различных сталей. Точка а — это та температура, при которой сталь уже способна принимать закалку. «Сталь, как бы она тверда ни была,— писал Чернов,— будучи нагрета ниже точки а, не принимает закалки», то-есть не становится более твёрдой при последующем быстром охлаждении в воде или в масле. «Сталь, нагретая ниже точки Ь,— писал далее Чернов, — не изменяет своей структуры, медленно ли или быстро после того она охлаждается. Как только температура стали возвысилась до точки 6, масса стали быстро переходит из зернистого (или, вообще говоря, кристаллического) в аморфное (воскообразное) состояние».
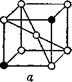
Позже было, однако, установлено, что при нагревании выше точки b сталь сохраняет кристаллическое строение, но кристаллическая решётка железа изменяется: из
кубической объемноцентрированной (альф а-железо) она превращается в кубическую гранецентрированную решётку (гамма-железо). Если такую сталь очень быстро охладить в воде, то структура стали снова резко изменяется. Под микроскопом мы увидим тёмные перекрещивающиеся друг с другом иглы (рис. 9). Это так называемый мартенсит. Он-то и придаёт стали очень высокую твёрдость и хрупкость после закалки. Мартенсит неустойчив и может распадаться даже при комнатной температуре, правда, очень медленно. При нагревании мартенсит распадается быстро.
Точка (I — 200° — соответствует температуре охлаждения для полной закалки. До этой Рис- 9* Иглы мартенсита, гочки нужно быстро охлаждать
Сталь при закалке, чтобы сталь была твёрдой. При 200° в стали образуется мартенсит.
Инструментальная сталь (для зубил, отвёрток, пил, резцов и т. д.) нагревается при отпуске обычно только до 200° — при этой температуре твёрдость понижается мало, но хрупкость устраняется в значительной степени.
Отпуск стальных пружин и некоторых штампов производят при температурах до 400—500°; при этом твёрдость заметно снижается и сталь становится пластичной.
Конструкционные стали, из которых делаются ответственные детали автомобилей, тракторов, самолётов, после закалки, как правило, подвергаются высокому отпуску, нагреваются до 550—650°. При этом сталь приобретает благоприятные сочетания прочности и пластичности; детали, изготовленные из такой стали, долговечны.
Точка е соответствует температуре 450°. Это — точка полного отпуска: мартенсит, сообщающий стали высокую твёрдость и хрупкость, при 450° распадается полностью.
Чернов изучил и режим ковки: болванку нужно нагреть до температуры 1200—1250°, и когда сталь станет пластичной, ковать её до тех пор, пока она не остынет до точки Ь (800—850°). При высоких температурах сталь имеет крупнозернистое строение, и если ковку кончить не в точке fr, а при температуре, допустим, 1000°, крупные зёрна останутся нераздроблёнными, и сталь получится непрочная.
Д. К. Чернов впервые в истории науки указал, что свойства сплава зависят от его внутреннего строения и, чтобы придавать сплавам те или другие ценные свойства, нужно подробно изучать все изменения, которые происходят при термической и механической обработке сплавов.
Значение работ Д. К. Чернова для науки о металлах и техники чрезвычайно велико. В 1900 году на Всемирной выставке в Париже французский металлург Поль ‘Монгольфье обратился к собравшимся со следующими словами: «Считаю своим долгом открыто и публично заявить в присутствии стольких знатоков и специалистов, что наши заводы и всё сталелитейное дело обязаны настоящим своим развитием и успехом в значительной мере труду и исследованиям русского инженера Чернова».
Известный советский учёный А. А. Байков в статье, посвящённой столетию со дня рождения Д. К. Чернова, так оценивает значение работ Д. К. Чернова: «Д. К. Чернов является величайшим гениальным учёным, который своими замечательными исследованиями произвёл в металлургии полную революцию. Значение Д. К. Чернова для металлургии можно сравнить со значением Д. И. Менделеева для химии. Подобно тому как химия в своём дальнейшем развитии будет итти по пути, указанному Д. И. Менделеевым, так и металлургия стали будет развиваться в том направлении, которое было указано Д. К. Черновым».
Мы уже знаем, что сплавы — это кристаллические вещества, состоящие из атомов двух или нескольких химических элементов.
Сплавы получаются обычно путём сплавления либо металлов друг с другом, либо металлов с неметаллами. Расплавленные металлы обычно хорошо растворяются один в другом и дают однородный жидкий раствор. Так, медь растворяется в никеле, свинец — в сурьме. Получаемые таким путём сплавы называются литыми.
В настоящее время ряд сплавов получают также спеканием. Для этого из металлов, которые должны войти в состав сплава, приготовляют тонкие порошки, перемешивают их, прессуют, а затем спекают при соответствующих температурах и таким образом получают нужные сплавы. Спекание применяется иногда для получения подшипниковых сплавов (железа с графитом, железа со свинцом) и сплавов из тугоплавких металлов, например из кобальта и карбидов (соединений с углеродом) вольфрама и титана. Прессование и спекание смеси порошков производится в специальных пресс-формах, имеющих точную форму и размеры будущих изделий, и поэтому дальнейшая обработка сплавов оказывается ненужной.
Свойства сплава зависят не только от его химического состава, но и от внутреннего строения, структуры сплава. Поэтому в настоящее время при изучении сплавов строению их уделяется большое внимание.
Строение различных сплавов не одинаково. Составные части сплава могут образовать либо механическую смесь, либо химическое соединение, либо твёрдый раствор.
Что представляет собой механическая смесь?
Если тщательно смешать порошок мела и порошок серы и посмотреть на полученную смесь в лупу, то можно увидеть отдельные зёрнышки мела и серы. Они не взаимодействуют друг с другом химически, а находятся в смеси в виде самостоятельных частиц. Подобные смеси и называют механическими. Такие смеси встречаются часто среди сплавов. Например, сплав свинца и сурьмы — механическая смесь. Если посмотреть на этот сплав в микроскоп, то можно различить мельчайшие кристалики свинца и сурьмы (рис. 10). Механические смеси может давать
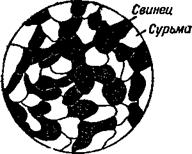
Рис. 10. Сплав свинца и сурьмы туре более высокой.
(схемз структуры). Меняя в сплаве весо
Вые количества отдельных элементов, можно получать сплавы с различными температурами плавления. Если, например, в 100 граммах сплава свинца с сурьмой содержится только 5 граммов сурьмы, то сплав плавится при температуре 296°, если сурьмы 10 граммов, температура плавления равна 260°, 20 граммов — 280°, 40 граммов — 395° и т. д. Весьма характерным для таких сплавов является то обстоятельство, что все они начинают плавиться вне зависимости от состава при температуре плавления эвтектики (246°), а заканчивают — при разных температурах.
Эвтектические сплавы очень ценны. Они представляют собой смесь чрезвычайно мелких кристаликов, имеют однородное строение и обладают сравнительно высокой прочностью и хорошими литейными свойствами, то-есть хорошо заполняют литейную форму и дают небольшую усадку (усадка — это уменьшение объёма отливки при переходе сплава из жидкого состояния в твёрдое).
Эвтектический сплав, содержащий 45,3% висмута, 12,3% кадмия, 17,9% свинца и 24,5% олова, плавится при 70°. Из него делаются электрические предохранители.
Эвтектические сплавы алюминия с кремнием — силумины — применяются для изготовления некоторых деталей в авиамоторостроении.
Познакомимся теперь с твёрдыми растворами.
Мы уже знаем, что расплавленные металлы могут растворяться один в другом: атомы одного металла равномерно распределяются в другом металле — растворителе. Это такой же процесс, как и растворение сахара в воде. При застывании сплава атомы растворённого металла так и остаются «рассеянными» в другом металле, и образуется твёрдый раствор.
В никеле может раствориться сколько угодно меди. Точно так же и в меди могут растворяться неограниченные количества никеля. (Конечно, когда в грамме никеля растворяется килограмм меди, растворителем считают не никель, а медь.) Однако такая неограниченная растворимость присуща далеко не всем металлам. Многие из них обладают ограниченной растворимостью. Свинец, например, плохо растворяется в цинке, в меди, в железе. Если расплавить вместе цинк и свинец, то образуется два жидких слоя: в верхнем слое будет жидкий цинк с небольшим количеством растворённого в нём свинца, а в нижнем — свинец, растворивший немного цинка. При затвердевании расплава оба эти слоя так и остаются один над другим.
В твёрдом растворе атомы растворённого металла «рассеяны» среди атомов металла-растворителя. Но ведь твёрдый раствор — кристаллическое тело. Как же построены в нём кристаллы?
Рентгеновские исследования показали, что твёрдые растворы могут быть построены по-разному (рис. 11).
Если твёрдый раствор содержит металлы, атомы которых имеют приблизительно одинаковые размеры (диа-
Метры их различаются не больше, чем на 15%), то атомы растворённого металла не занимают каких-либо особых положений,— они могут замещать атомы растворителя в любом месте кристаллической решётки (рис. 11, а). Поэтому такие сплавы называются твёрдыми растворами замещения. Это наиболее часто встречающийся тип твёрдого раствора. Сплавы железа с хромом, никелем, марганцем, сплавы меди с никелем, кобальта с никелем образуют твёрдые растворы замещения. Если атомные диаметры металлов отличаются
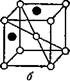
Рис. 11. Строение твёрдых растворов: а — раствор внедрения, б — раствор замещения.

Растворителем может быть не только чистый металл, но и химическое соединение. Так, например, химическое соединение алюминия с никелем может растворить в себе как никель, так и алюминий.
У твёрдых растворов есть одно замечательное свойство. Мы уже знаем, что атомы внутри кристалла находятся в непрерывном колебательном движении. Советские учёные А. Ф. Иоффе и Я. И. Френкель показали, что в то время, как один из колеблющихся атомов на какой-то момент времени покидает своё место в кристаллической решётке, соседний атом может проскочить на освободившееся место. В результате таких «перескоков» внутри кристаллической* решётки происходит непрерывное перемещение атомов, тем более оживлённое, чем выше температура сплава. На свободное место решётки, лежащей в поверхностном слое сплава, способны перескочить и атомы другого вещества,
Соприкасающиеся со сплавом. Эти «посторонние» атомы могут проникать, диффундировать и в глубь сплава, иначе говоря, растворяться в нём.
Способность сплавов-твёрдых растворов быть растворителями имеет громадное значение в технике. Во многих машинах и механизмах есть детали — коленчатые валы, шестерни, втулки и т. д., — сердцевина которых должна быть упругой и вязкой, а поверхность — твёрдой, прочной и стойкой к истиранию. Такие детали делают из вязкой и мягкой малоуглеродистой стали, а затем проводят следующую операцию. В железный ящик, куда насыпана смесь древесного угля с другими веществами, содержащими углерод (например, углекислым барием) кладут детали, плотно закрывают ящик и несколько часов нагревают его до 900—950°. После этого поверхность детали становится твёрдой и прочной. Почему это происходит? При высокой температуре углерод растворяется в поверхностном слое металла, и на детали образуется «корка» из твёрдой высокоуглеродистой стали. Насыщение поверхности металла углеродом называют цементацией.
Таким же путём можно азотировать сталь, то-есть насыщать её поверхность азотом (чтобы сделать сталь более твёрдой) »хромировать — насыщать хромом (чтобы сталь была твёрдой и химически стойкой) и т. д.
Иногда при сплавлении отдельные части сплава соединяются друг с другом химически. Так, например, вольфрам соединяется с углеродом, и в сплаве образуется новая составная часть — карбид. Кристалики химических соединений существуют в структуре сплава самостоятельно, как одна из составных частей механической смеси, или твёрдого раствора. Сплавов, которые состояли бы только из одних химических соединений, нет.
Кристалики химических соединений обычно обладают большой твёрдостью и хрупкостью. Особенной твёрдостью отличаются карбиды таких металлов, как вольфрам, хром, титан, ванадий, молибден. Поэтому они всегда находятся в структуре твёрдых сплавов и быстрорежущих сталей.
Мир сплавов весьма разнообразен. Среди них часто встречаются сплавы, которые, как мы уже видели, являются только механическими смесями, либо только твёрдыми растворами. Таких сплавов очень много среди простых сплавов, состоящих лишь из двух элементов.
В сложных сплавах — из трёх и более элементов — могут встречаться одновременно твёрдый раствор и химическое соединение, смесь чистого металла с его химическим соединением и т. д.
Для примера мы познакомимся с внутренним строением самого распространённого в технике сплава — стали.