Чего нельзя делать при аденоме гипофиза
Аденомы гипофиза наиболее часто возникает в возрасте от двадцати до пятидесяти лет с одинаковой частотой среди мужчин и женщин. Статистически заболевание занимает долю 18% от всех опухолей мозга.
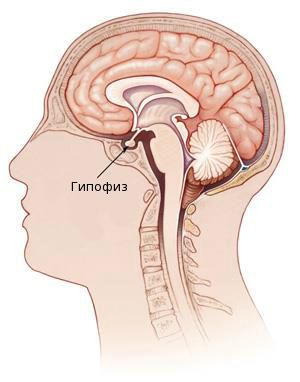
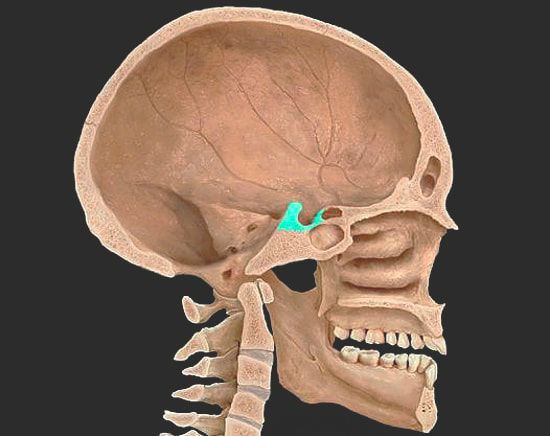
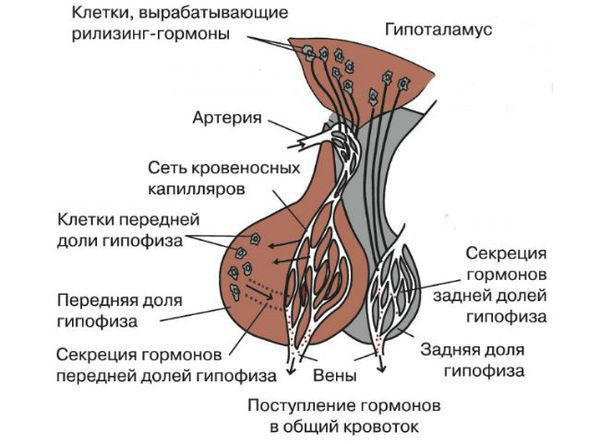
Гипофиз – «дирижер» всех желез внутренней секреции человеческого тела и часть центральной нервной системы, состоит из трех долей: передней (аденогипофиз), средней или промежуточной и задней (нейрогипофиз). Железа эта по-королевски сидит в турецком седле (костное образование в центре мозга) и секретирует жизненно важные гормоны:
. Любовь зарождается в гипофизе вместе с эндорфином фенилэтиленамином.
Тиреотропин (гликопротеин, клеток-тиреотрофов всего 5%, при гипотиреозе они активируются).
. В романе М.А. Булгакова «Собачье сердце» гипофиз пересаживается от человека собаке с целью омоложения, а получается, что он влияет на личность и превращает собаку Шарика в отпетого маргинала!
Окситоцин и вазопрессин не секретируются в гипофизе, но накапливаются в его задней доле. При аденомах гипофиза из-за синдрома сдавления может нарушаться активация окситоцина и вазопрессина, что ведет к несахарному диабету и нарушению сократительной способности матки (особенно в родах).
ПРИЧИНЫ АДЕНОМ ГИПОФИЗА
Аденомы гипофиза занимают долю 18% от всех опухолей мозга, распространенность их 0,00002% среди населения. Возникает заболевание статистически в возрасте от двадцати до пятидесяти лет с одинаковой частотой среди мужчин и женщин из-за:
ВИДЫ АДЕНОМ ГИПОФИЗА
Гормонально-активные (вырабатывают соответственно соматотропин, пролактин, адренокортикотропин, тиреотропин, лютеинизирующий и фолликулостимулирующий гормон), примерно 60%.
Гормонально-неактивные (инсиденталома, из промежуточной средней доли гипофиза), около 40%.
Злокачественные (аденокарцинома), менее 5%.
По размеру аденомы делятся на микроаденомы: от 1 мм до 20 мм, макроаденомы – более 20 мм.
ЧЕМ ОПАСНЫ АДЕНОМЫ ГИПОФИЗА?
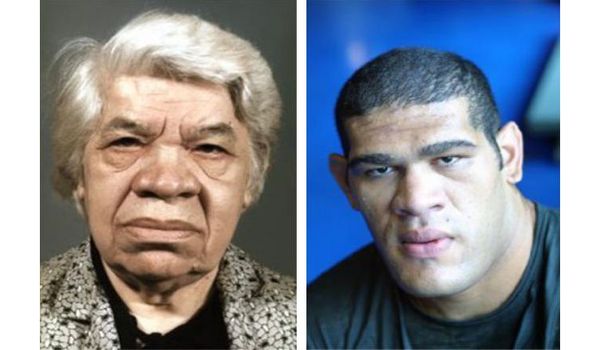
Соматотропинпродуцирующая (соматропинома): среди всех аденом 20-25%, частота всего в популяции 0,0005-0,0007%, развивается в возрасте 20-40 лет, при данном диагнозе в 10 раз чаще пациенты гибнут от сердечно-сосудистой патологии. Симптомы: отечность, сальность кожи и волос, себорея, укрупнение черт лица, стоп, кистей, расхождение зубного ряда (акромегалия во взрослом состоянии) и гигантизм в детстве с преждевременным половым развитием;
. Самые высокие люди своим ростом обязаны соматотропиноме: Роберт Валдов (США) – 286 см, Зенг Зин Ля (Китай) – 244 см. Библейский гигант Голиаф был убит Давидом из-за нарушения зрения (битемпоральная гемианопсия), хрупкости костей черепа (гиперпаратиреоз) в результате соматотропиномы.
Пролактинсекретирующая (пролактинома): самая частая аденома (40%), медленно растет и вызывает набухание молочных желез и выделение молока, снижение либидо и потенции, бесплодие;
Адренокортикотропинпродуцирующая (кортикотропинома): медленнорастущая, среди всех аденом занимает 7%, характерен инвазивный рост с разрушением турецкого седла, чаще у женщин 20-40 лет. Вызывает злокачественную болезнь Иценко-Кушинга: характерное ожирение, нарушение трофики и цвета кожи, неконтролируемая артериальная гипертензия, гирсутизм, кардиомиопатия, диабет, остеопороз, иммунодефицит, психоз, сердечная недостаточность. Высока вероятность озлокачествления;
Тиротропинпродуцирующая (тиреотропинома): 3% всех аденом, возникает при гипотиреозе и плохо поддается лечению. Вызывает тиреотоксикоз;
Фоллитропинпродуцирующая или лютропинпродуцирующая (гонадотропинома): нарушение либидо и эрекции, гинекомастия, нарушения менструального цикла, бесплодие, маточные кровотечения.
Клиника зависит от вида и интенсивности гормоновыделения аденомой, размера и скорости ее роста. Пролактиномы часто вообще не диагностируются, и только опытные специалисты нашей клиники смогут заподозрить аденому гипофиза как причину бесплодия и нарушения половой функции, которую пациент безрезультатно лечит много лет!
СИМПТОМЫ АДЕНОМЫ ГИПОФИЗА
Первые две группы симптомов возникают оттого, что гипофиз соседствует с внутренними сонными артериями, венозными синусами, несущими кровь от лица, третьей, четвертой и пятой парами черепно-мозговых нервов, зрительным перекрестом, третьим желудочком и гипоталамусом. При неврологической и зрительной симптоматике мы рекомендуем как можно быстрее лечить аденому, чтобы она не привела к катастрофическим последствиям.
. Зрение при аденоме восстанавливается иногда до года, а ухудшение неврологических признаков – следствие кровоизлияния в аденому и показание к неотложном вмешательству!
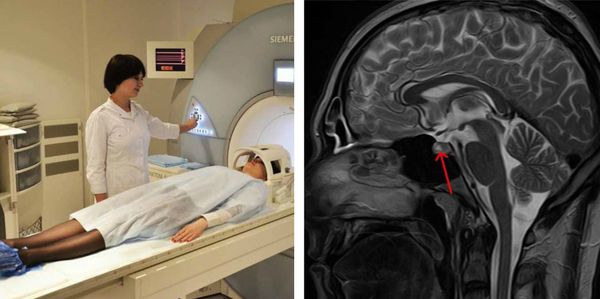
ДИАГНОСТИКА АДЕНОМЫ ГИПОФИЗА
Клиника Н. оборудована современной клинико-биохимической лабораторией, в которой при подозрении на аденому гипофиза делается развернутый анализ на гормоны, причем специалисты подробно обучают пациента подготовке к нему. Это, вкупе с современными реагентами и методиками диагностики, позволяет с первого раза получить точный результат! Также мы владеем методикой МРТ-диагностики аденом гипофиза с контрастом и без, а это золотой стандарт визуализации гипофиза, аденом и их осложнений (кисты и кровоизлияния).
ЛЕЧЕНИЕ АДЕНОМЫ ГИПОФИЗА
Медикаментозное («химическое» удаление аденомы): антагонисты пролактина или агонисты дофамина (парлодел, бромокриптин, каберголин), антагонисты соматотропина и аналоги соматостатина (гормона гипоталамуса, снижающего выработку соматотропина типа октреотида), антагонисты серотонина и кортизола. Так лечатся некоторые пролактиномы (пролактин более 500 нг/л) и соматотропиномы (бессимптомное лечение, высокие уровни гормонов после операции).
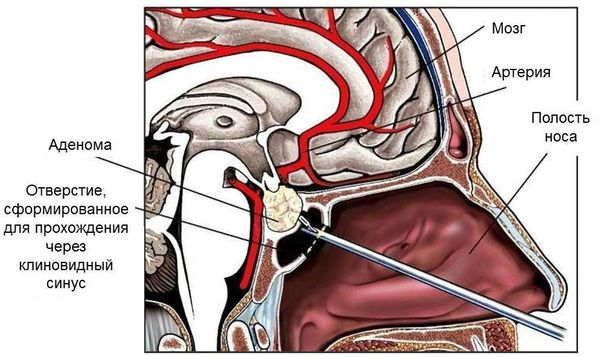
Оперативное: при нарушениях зрения, кистах, кровоизлияниях через транссфеноидальный доступ полуэндоскопическим или эндоскопическим путем (97%), реже транскраниально (трепанация черепа при больших опухолях). В принципе, такому лечению подлежат все кортикотропиномы и соматотропиномы! Операция проводится под наркозом, период восстановления от трех до десяти дней.
При микроаденомах выздоровление наблюдается в 85% случаев, при макроаденомах возможен рецидив через 5 лет. Без лечения пациенты с аденомой гипофиза более подвержены риску сердечно-сосудистых заболеваний, сахарному диабету, слепоте (особенно в случае кортикотропиномы), бесплодию. Так что при симптомах аденомы гипофиза мы рекомендует обратиться в нашу клинику за консультацией эндокринолога, он, в свою очередь, поставит диагноз и наметит альтернативные варианты лечения, обрисует риски и перспективы заболевания.
ПОДГОТОВКА К УДАЛЕНИЮ АДЕНОМ ГИПОФИЗА
ЖИЗНЬ ПОСЛЕ АДЕНОМЫ
Пациенту после «химического», хирургического или лучевого удаления аденомы рекомендуется наблюдаться у эндокринолога, воздерживаться от нагрузок, опасных видов и деятельности, требующей внимания. «Гормонального» выздоровления при современном уровне медицины мы добиваемся в 85-90% случаев, наши пациенты ведут обычный образ жизни и при соблюдении врачебных рекомендаций и не вспоминают о болезни!
Что такое аденома гипофиза? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бабинцевой Марины Юрьевны, эндокринолога со стажем в 27 лет.
Определение болезни. Причины заболевания
Аденома гипофиза (pituitary adenoma) — это доброкачественная опухоль, которая происходит из клеток передней доли гипофиза. Она может протекать бессимптомно или иметь выраженные проявления: от головных болей до заметных гормональных нарушений. Клиническое течение аденомы гипофиза зависит от её размеров и степени гормональной активности.
Термин «аденома гипофиза» объединяет многочисленную группу заболеваний, одним из этиологических факторов которых является наличие доброкачественной опухоли (аденомы) в гипофизе. Все эти заболевания можно условно разделить на две большие группы – гормонально-неактивные (инцинденталомы) и гормонально активные опухоли. Клинические проявления, диагностика и лечение каждого из этих заболеваний будут значительно различаться.
Считается, что провоцирующими факторами развития аденом гипофиза могут служить:
К появлению опухоли приводят и другие факторы, влияющие на гормональную активность гипофиза. Например, тиреотропинома может развиться при длительном некомпесированном гипотиреозе, гонадотропинома — при первичном поражении половых желёз. Аденомы гипофиза также возникают при наличии эктопических образований, продуцирующих рилизинг-гормоны. Такие образования состоят из нейроэндокринных клеток диффузной эндокринной системы и могут быть расположены в других (неэндокринных) органах. Так, например, адренокортикотропный гормон может продуцироваться при мелко- и немелкоклеточном раке лёгкого.
Симптомы аденомы гипофиза
При гормонально неактивной аденоме гипофиза большого размера и её росте с выходом за пределы турецкого седла возникают офтальмологические симптомы.
Рост аденомы в сторону гипоталамуса проявляется следующими симптомами:
При давлении опухоли на III желудочек головного мозга пациент ощущает:
Повышенная выработка пролактина у женщин вызывает:
У мужчин гиперпролактинемия проявляется:
Клинические проявления сомтатропиномы (аденомы гипофиза, секретирующей гормон роста — соматотропин) зависят от времени её возникновения. При появлении опухоли в зрелом возрасте после формирования костного роста у пациента развиваются симптомы акромегалии (состояние, вызванное повышенной и непрерывной выработкой гормона роста):
Если соматотропинома возникает у детей и подростков до завершения костного роста, то развивается гигантизм. При этом у пациента пропорционально увеличивается как длина костей, так и общий рост — более 190 см у женщин и более 2 м у мужчин. Если избыточная секреция соматотропина сохраняется и в более позднем возрасте, в клинической картине начинают проявляться симптомы акромегалии.
При развитии кортикотропиномы (опухоли, продуцирующей аденокортикотропный гормон) отмечается:
При возникновении тиреотропиномы (доброкачественной опухоли гипофиза, вырабатывающей тиреотропный гормон) проявления заболевания могут быть различными: от гипотиреоза до тиреотоксикоза.
Первичная тиреотропинома вызывает повышенную секрецию гормонов щитовидной железы и проявляется типичными признаками тиреотоксикоза:
Вторичная тиреотропинома, которая появляется в ответ на длительный некомпенсированный гипотиреоз, сопровождается:
В связи с тем, что аденомы гипофиза часто имеют смешанную гормональную активность, эндокринные проявления этого заболевания весьма разнообразны и могут маскировать друг друга.
Кроме того, когда аденома достигает больших размеров, усиливаются неврологические симптомы:
Иногда наличие аденомы гипофиза начинают подозревать только после появления неврологической симптоматики, несмотря на предшествующие эндокринные проявления.
Патогенез аденомы гипофиза
Гипофиз — это небольшой отдел головного мозга, расположенный в его основании в гипофизарной ямке турецкого седла клиновидной кости. Гипофиз относится к железам внутренней секреции и, соответственно, является эндокринным органом.
Гипофиз разделяется на переднюю долю (аденогипофиз) и заднюю (нейрогипофиз). Различные клетки аденогипофиза (соматофоры, лактофоры, хромофилы и др.) под влиянием стимулирующих рилизинг-гормонов гипоталамуса вырабатывают гормоны: пролактин, соматотропный и адренокортикотропный гормоны, гонадотропы (фолликулостимулирующий и лютеинизирующий гормоны).
При избыточном росте лактофоров (пролактинсекретирующие клетки) у пациента возникает синдром гиперпролактинемии. Однако к ней может привести любая макроаденома гипофиза. Это происходит из-за сдавливания ножки гипофиза большой опухолью и утраты сдерживающего влияния гипоталамуса на секрецию пролактина.
Гиперсекреция соматотропина приводит к избыточной продукции факторов роста. В результате возникает повышенное отложение мукополисахаридов (хондроитинсульфата, гиалуроновой кислоты и т. д.), увеличивается выработка коллагена и происходит разрастание костей, хрящей, мягких тканей и появляются основные симптомы акромегалии.
Избыточная выработка адренокортикотропного гормона приводит к неконтролируемому росту уровня глюкокортикоидов и развитию болезни Иценко-Кушинга.
Классификация и стадии развития аденомы гипофиза
Аденомы гипофиза классифицируют по различным признакам.
По происхождению аденомы могут быть:
В зависимости от размера выделяют:
Исходя из гормональной активности, выделяют неактивные (не вызывающие повышенную секрецию гормонов гипофиза) и активные аденомы гипофиза.
Гормонально активные аденомы гипофиза подразделяются на:
Осложнения аденомы гипофиза
Осложнения аденомы гипофиза можно условно разделить на неврологические и гормонозависимые.
Неврологические осложнения возникают при распространении опухоли за пределы турецкого седла и зависят от направления её роста.
При супраселлярном росте (вверх по направлению к зрительному перекрёсту) опухолевая ткань сдавливает зрительные нервы, в результате возникает одно- или двухстороннее нарушение зрения. Вначале эти нарушения носят обратимый характер, затем с развитием атрофии зрительных нервов становятся необратимыми. Дальнейший супраселлярный рост аденомы может проявляться различной дополнительной клиникой.
При росте опухоли кпереди возникает лобная симптоматика:
При распространении аденомы вбок в сторону височных долей проявляются:
Рост аденомы за пределы турецкого седла в других направлениях клинически проявляется только при значительных размерах опухоли. Распространение опухоли в основную пазуху и/или в носоглотку осложняется затруднением носового дыхания, глотания и истечением из носа спинномозговой жидкости.
При распространении опухоли в заднюю черепную ямку вследствие поражения IX, X и XII пар черепно-мозговых нервов могут проявиться бульбарные нарушения, которые проявляются затруднением глотания, смазанностью речи, слюнотечением, нарушением мимики.
При росте кпереди и проникновении опухоли в орбиту возникают грубые нарушения зрения и экзофтальм (выпячивание глазного яблока вперед, «пучеглазие») на поражённой стороне.
Гормонозависимые осложнения аденомы гипофиза являются последствиями тех эндокринных нарушений и заболеваний, которые и вызвала аденома.
Пролактиномы являются причиной:
Соматотропиномы вследствие избыточного производства гормона роста вызывают:
К основным осложнениям гиперкортицизма относят:
При тиреотропиноме осложнения связаны с тиреотоксикозом и токсическим воздействием избытка гормонов щитовидной железы на сердечную мышцу и проводимость. В результате возникают тахиаритмия, мерцание и трепетание предсердий, а иногда и желудочков сердца, что может привести к летальному исходу.
Аденома гипофиза может осложниться также гипопитуитаризмом, который возникает либо вследствие сдавления опухолью здоровых тканей гипофиза, либо по причине кровоизлияния в аденому.
Диагностика аденомы гипофиза
Диагностика аденом гипофиза начинается со сбора врачом-эндокринологом жалоб, характерных для поражения той или иной железы внутренней секреции.
Самым характерным признаком соматотропиномы является повышение секреции соматотропина, который стимулирует выработку печенью инсулин-подобного фактора роста 1 (ИФР-1). Под влиянием ИФР-1 у взрослых пациентов развиваются симптомы акромегалии. Возникают характерные изменения во внешности: увеличение нижней челюсти, надбровных дуг, губ, носа, расширение межзубных промежутков, несмыкание зубов, увеличение кистей и стоп, изменение кожи, увеличение языка. Пациентов беспокоят:
При осмотре и на УЗИ наблюдается увеличение внутренних органов: селезёнки, печени, сердца, щитовидной железы.
Кортикотропиномы под воздействием избытка адренокортикотропного гормона проявляются характерными симптомами болезни Иценко-Кушинга: ожирения, сахарного диабета, стероидного остеопороза, артериальной гипертензии с повышением систолического и диастолического артериального давления, трофических нарушений кожных покровов. Нарушение метаболизма миокарда в сочетании с артериальной гипертензией приводит к сердечной недостаточности. Вторичный иммунодефицит, развивающийся на фоне гиперкортицизма, проявляется гнойничковыми поражениями кожи, микозами, трофическими язвами, пиелонефритом, блефаритом, септическими состояниями.
Для диагностики гиперкортицизма используют анализ уровня кортизола в слюне, а также кортизола в сыворотке крови после стимуляции дексаметазоном. Дифференциальная диагностика АКТГ-зависимого гиперкортицизма (возникшего вследствие повышенной секреции адренокортикотропного гормона) от гиперкортицизма проводится с помощью определения уровня АКТГ и МРТ головного мозга.
Основное проявление тиреотропиномы гипофиза — это повышение уровня тиреотропного гормона и, как следствие, избыток гормонов щитовидной железы: тироксина и трийодтиронина. В результате гормонального нарушения развиваются симптомы тиреотоксикоза:
Со стороны неврологической симптоматики отмечается тремор рук и век, дрожь во всём теле. Однако при тиреотропиноме отсутствуют аутоиммунные проявления, типичные для диффузного токсического зоба (эндокринная офтальмопатия, претибиальная микседема, акропатия). В сложных случаях при стёртой симптоматике проводят стимуляционные тесты с тиреотропин-рилизинг-гормоном. Также необходимо визуализировать аденому на МРТ.
При подозрении на аденому гипофиза обязательным является осмотр офтальмолога, на котором определяются поля и острота зрения. Выпадение полей зрения, особенно симметричное с двух сторон в височной области, может говорить о наличии аденомы гипофиза, имеющей супраселлярный рост (распространение опухоли в полость черепа) и сдавливающей зрительные нервы.
Для визуализации области турецкого седла используют рентгеновские методы, КТ и МРТ. На краниографии (рентгенографии черепа) можно заметить увеличение размеров турецкого седла, расширение его входа, сглаженность спинки. Однако эти признаки выявляются только при наличии макроаденомы. Изменения, вызванные микроаденомами, с помощью рентгена не определяются.
Главным методом, подтверждающим наличие аденомы гипофиза, является МРТ головного мозга (МРТ гипофиза). МРТ может проводиться с дополнительным контрастным усилением для лучшей визуализации патологических образований. Иногда, как дополнительную к МРТ методику, применяют спиральную компьютерную томографию.
Лечение аденомы гипофиза
В лечении аденом гипофиза используют три основных метода и их сочетание:
Целью лечения является устранение клинических симптомов, нормализация уровня гормонов и их суточных ритмов, снижение количества осложнений, уменьшение размера или полное удаление опухоли. Выбор метода и последовательность их применения зависит от вида аденомы, степени её активности и размера.
Лечение пролактином начинают с приёма агонистов дофамина. Наиболее часто используются производные алкалоидов спорыньи: бромокриптин (абергин) и каберголин (достинекс). Бромокриптин является неселективным агонистом дофамина. Он воздействует не только на Д2-рецепторы пролактофоров, но и на другие дофаминовые рецепторы. Этим объясняется его побочные действия, такие как тошнота, рвота, головокружение, общая слабость, запоры. Каберголин селективно влияет на дофаминовые рецепторы гипофиза, поэтому таких побочных эффектов у него нет. К преимуществам каберголина также относят продолжительность действия — он поддерживает нормопролактиемию в течение недели, тогда как бромокриптин необходимо принимать дважды в сутки.
При невозможности достигнуть нормальных значений пролактина с помощью медикаментозной терапии, а также при присоединении неврологической или офтальмологической симптоматики, показано оперативное лечение.
Для соматотропином методом выбора является нейрохирургическое лечение. После проведённой операции эффект наступает очень быстро, это основное преимущество хирургического метода. Успех хирургического вмешательства зависит от размера опухоли, отсутствия признаков инвазии и атипии клеток аденомы.
Чтобы снизить или избежать осложнений гиперкортицизма при кортикотропиномах, нейрохирургическую операцию требуется провести как можно скорее.
Гормонально неактивные опухоли подлежат оперативному лечению только при их выраженном росте и возникновении неврологической симптоматики или истечении из носа спинномозговой жидкости.
Прогноз. Профилактика
Чем раньше выявлено заболевание, тем благоприятнее его прогноз. Развитие и исход аденомы гипофиза зависят также от направления её роста, гистологических особенностей и возможностей радикального лечения.
Течение пролактином на фоне медикаментозной терапии в целом благоприятное. При нормализации уровня пролактина у пациенток возможно полное восстановление репродуктивной функции и наступление беременности.
Хирургическое лечение или лучевая терапия потребуются при невозможности стабилизировать состояние, резистентности опухоли к терапии и продолжающемся росте аденомы.
При других гормонально активных опухолях (соматотропиномах, кортикотропиномах, тиреотропиномах) методом выбора является оперативное лечение. Своевременное нейрохирургическое лечение приводит к более благоприятному прогнозу. Во-первых, потому что повышается вероятность радикального удаления микроаденомы, во-вторых, на ранних стадиях гормональные нарушения ещё не привели к выраженным осложнениям.
Первичной профилактики аденомы гипофиза не существует, так как неизвестны причины её возникновения. Вторичная профилактика аденомы гипофиза состоит в раннем выявлении симптомов заболевания и как можно более раннем начале терапии.
Чего нельзя делать при аденоме гипофиза
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Исследование качества жизни больных с аденомами гипофиза в до- и послеоперационном периодах
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2019;83(2): 11-16
Черебилло В. Ю., Курнухина М. Ю. Исследование качества жизни больных с аденомами гипофиза в до- и послеоперационном периодах. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2019;83(2):11-16.
Cherebillo V Yu, Kurnukhina M Yu. Quality of life in patients with pituitary adenomas in the pre- and postoperative period. Zhurnal Voprosy Neirokhirurgii Imeni N.N. Burdenko. 2019;83(2):11-16.
https://doi.org/10.17116/neiro20198302111
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
Цель исследования — оценить изменения качества жизни у больных до и после удаления аденомы гипофиза. Материал и методы. Проведено клиническое исследование 42 больных с аденомами гипофиза. Установление диагноза основывалось на клинико-лабораторных данных и результатах лучевых и инструментальных методов исследования. Удаление аденомы гипофиза осуществлялось трансфеноидальным доступом. Анализ качества жизни проводился у больных в дооперационном и раннем послеоперационном периодах. Больные были в возрасте от 22 до 63 лет (медиана 45 лет). Для оценки качества жизни в до- и послеоперационном периодах нами был выбран специальный опросник — EORTC QLQ-C30, созданный группой оценки качества жизни Европейской организации исследования и лечения рака. Он используется во многих международных клинических исследованиях. Результаты. У исследованных больных отмечена положительная динамика в послеоперационном периоде по всем функциональным шкалам. По симптоматическим шкалам отмечено снижение утомляемости, выраженности болевого синдрома, проявлений тошноты и рвоты, одышки. После операции нормализировалась моторика кишечника, снизилась частота проявления диареи и запоров, стабилизировался сон. Исследуемые также отмечали улучшение показателя общего здоровья и уменьшение ожидаемых финансовых затруднений. Заметным показателем было снижение аппетита. Выводы. При исследовании различных показателей качества жизни до и после операции у пациентов с аденомами гипофиза выявлено, что оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных.
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Аденома гипофиза — это опухоль эндокринной системы, которая проявляется гипер- или гипосекрецией гормонов передней доли гипофиза, а также клиническими симптомами, вызванными влиянием новообразования на окружающие селлярную область анатомические структуры [1].
Согласно статистическим данным, ежегодно в России и странах СНГ выявляется около 3 тыс. вновь заболевших [2]. Среди интракраниальных опухолей аденомы гипофиза занимают 3-е место, составляя от 7,3 до 18% всех верифицированных опухолей мозга, и поражают преимущественно лиц работоспособного возраста, на который приходится около 75% всех случаев заболевания [3].
Цель любого из видов лечения опухолей гипофиза (хирургического вмешательства, лекарственной или лучевой терапии) — нормализовать секрецию гипофизарных гормонов, ликвидировать клинические проявления их гиперсекреции, уменьшить размеры крупной опухоли, сдавливающей жизненно важные структуры головного мозга, или полностью устранить ее, а также избежать отдаленных рецидивов, сохранив функцию передней доли гипофиза [4].
К настоящему времени накоплен большой опыт по удалению аденом гипофиза трансфеноидальным доступом [5—7]. Несомненным преимуществом в методике эндоскопического удаления опухолей хиазамально-селлярной области является возможность панорамного обзора структур этой зоны в условиях хорошей освещенности [8]. Это позволяет четко отдифференцировать основные анатомические структуры, избежать их повреждения, а также более радикально удалять опухоли. Применение увеличительной оптики, операционных микроскопов и эндоскопов, использование микрохирургической техники при удалении опухолей гипофиза существенно улучшило результаты оперативных вмешательств, уменьшило летальность, количество рецидивов заболевания и интраоперационных осложнений [4]. Использование оптического увеличения с разным углом зрения позволяет удалять опухоли «из-за угла» (в том числе и новообразования, расположенные латеральнее внутренней сонной артерии), под непосредственным визуальным контролем [9].
Важным направлением современной медицины является исследование качества жизни пациентов. В настоящее время часто в медицинской сфере используется термин «качество жизни, связанное со здоровьем» (health-related quality of life — HRQOL) [10, 11]. В конце XX века силами ВОЗ было осуществлено исследование по разработке основополагающих критериев HRQOL. В основу современных опросников по HRQOL были положены выстроенные связи вопросов и ответов, которые затем использовались для вычисления по методу суммирования рейтингов. Существуют общие опросники, которые направлены на оценку здоровья населения в целом, независимо от патологии, и специальные — для определенных заболеваний. Каждый опросник имеет свои критерии и шкалы оценки [12].
Цель настоящего исследования — анализ и оценка изменений качества жизни больных до и после удаления аденомы гипофиза.
Материал и методы
Проведено исследование 42 больных (25 женщин и 17 мужчин в возрасте от 22 до 63 лет) с гистологически подтвержденным диагнозом аденомы гипофиза. Средний возраст пациентов 43,95±11,3 года, медиана 45 лет. Установление диагноза у этих больных основывалось на клинико-лабораторных данных, результатах лучевых и инструментальных методов исследования. У всех пациентов использован трансфеноидальный доступ с применением эндоскопической ассистенции.
Для определения степени инвазии аденомы гипофиза в полость кавернозного синуса использовались МРТ-срезы на уровне турецкого седла и Knosp Scale [13]. В нашей серии наблюдений присутствовали разные степени заболевания: Grade 0 (нормальное расположение внутренней сонной артерии и венозных пространств) — у 14,3% больных, Grade I (опухоль проникает через медиальную касательную линию, но не распространяется за интракаротидную линию) — у 83,3%, Grade II (аденома распространяется за внутрисонную линию, но не переходит за латеральную) — у 2,4%.
Степень радикальности операции оценивалась через 3—6 мес после оперативного лечения. У исследуемых пациентов, по данным МРТ головного мозга, не было выявлено остатков опухоли, что подтверждало тотальность удаления образования.
Клинический анализ включал выяснение анамнеза заболевания исследуемых, оценку лабораторных, инструментальных данных, особенностей оперативного вмешательства, определение послеоперационных изменений качества жизни исследуемых.
Анализ изменений качества жизни проводился у больных в дооперационном и раннем послеоперационном периодах (первые 5—7 дней после оперативного лечения, до выписки из стационара).
В настоящее время существуют различные опросники для оценки качества жизни больных с аденомой гипофиза (Anterior Skull Base Questionnaire — ASBQ), Sino-nasal outcome test (SNOT-22), EORTC QLQ-C30). Опросник ASBQ включает 35 вопросов, объединенных в группы, которые характеризуют продуктивность, двигательную активность, выносливость, боль, эмоции, специфические симптомы [14]. Тест SNOT-22 включает 22 вопроса, посвященных характеру выделений из носа, наличию заложенности носа, болевого синдрома, головокружений, нарушению обоняния/вкуса, сна, описанию эмоционального состояния, снижению концентрации внимания [15].
Специальный опросник EORTC QLQ-C30 сходен с указанными предыдущими опросниками. Он был создан Группой оценки качества жизни Европейской организации исследования и лечения рака [16] и используется во многих международных клинических исследованиях. EORTC QLQ-C30 высокочувствителен и применим для оценки качества жизни у больных независимо от вида онкологического заболевания. Опросник состоит из 30 вопросов и различных шкал: общего состояния здоровья; 5 функциональных шкал — физической, ролевой, когнитивной, эмоциональной и социальной функций; шкал симптоматики. В симптоматическую шкалу входят такие симптомы, как усталость, тошнота/рвота и боль. Кроме того, в EORTC QLQ-C30 вошли 6 отдельных пунктов — бессонница, потеря аппетита, запор, диарея, диспноэ, финансовые трудности [17—19].
Для нашего исследования мы выбрали опросник EORTC QLQ-C30, так как он, в отличие от ASBQ и SNOT-22, включает оценку самим пациентом своего здоровья и качества жизни.
Ответы на вопросы каждой шкалы опросника EORTC QLQ-C30 подвергались переводу в числовой диапазон от 0 до 100. Таким образом, при более высоких значениях в функциональных, симптоматических шкалах предполагались высокий уровень функционирования и меньшая выраженность определенных симптомов, токсичности. И наоборот, чем ниже были показатели по шкалам общего статуса здоровья, тем выше была оценка пациентом общего состояния своего здоровья до и после оперативного лечения [19].
Полученные в процессе исследования данные обрабатывались c помощью лицензионной программы SPSS Statistics 22.0 в два этапа. На первом этапе оценивался вид распределения признаков в выборках, на втором — в зависимости от вида распределения рассчитывали среднее значение и его стандартное отклонение (М±SD) или медиану и интерквартильные интервалы (Me; 25/75). Для анализа качественных переменных использовали критерий χ 2 Пирсона.
Проверка закона распределения при необходимости анализа количественных переменных проводилась при помощи теста Колмогорова—Смирнова. Для определения силы связи в случае ненормального распределения переменных использовали двухсторонний ранговый корреляционный анализ Спирмена, в случае нормального распределения — двухсторонний корреляционный анализ (r) Пирсона. Оценивали также значимость различий между группами (p). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии различий и влияний) принимали равным 0,05 [20, 21].
Результаты
У исследуемых пациентов для удаления аденомы гипофиза был выбран трансфеноидальный доступ. Радикальное удаление всех аденом гипофиза — тотальная резекция. Средняя длительность оперативного вмешательства составила 33,57±9,96 мин, средняя продолжительность анестезии — 63,69±17,22 мин. Длительность госпитализации исследуемых составила 7,74±3,07 дня. Нами была проведена оценка общего состояния больных (performance status) с использованием шкалы Карновского и ECOG-ВОЗ. Таким образом, выявлено, что все исследуемые больные в дооперационном периоде соответствовали 90% по шкале Карновского (пациент способен к нормальной деятельности, отмечаются незначительные симптомы или признаки заболевания), и 1 баллу по ECOG-ВОЗ (есть симптомы заболевания, но ближе к нормальному состоянию). В послеоперационном периоде 7,1% исследуемых отмечали улучшение — отсутствие жалоб (100% по шкале Карновского, 0 баллов по ECOG-ВОЗ) [22—24].
Проведен анализ жалоб больных при поступлении. Основные жалобы больных в дооперационном периоде: головная боль диффузной локализации (69%), ухудшение памяти (57,1%), зрительные расстройства (42,9%). Реже пациенты отмечали головокружение (9,5%), головную боль определенной локализации (4,8%), тошноту и боль в суставах (2,4%). У 31% больных отмечалась акромегалия, у 11,9% — гормональная дисфункция. Выявлена корреляционная связь между возрастом и жалобами на болевой синдром в дооперационном периоде: чем старше пациент, тем более выраженным был у него болевой синдром (r=0,523; p=0,001).
Зрительные расстройства были представлены у пациентов снижением остроты зрения. При этом выявлена корреляционная связь между снижением остроты зрения и возрастом пациентов (r=0,408; р=0,007), жалобы на снижение остроты зрения перед операцией чаще отмечались у лиц более старшего возраста. Кроме того, у пациентов наблюдалось также выпадение полей зрения — гемианопсия. У пациентов с гомонимной гемианопсией отмечалось выпадение височного поля зрения только с левой стороны (левосторонняя гемианопсия). Гомонимная гемианопсия в дооперационном периоде отмечена у 11,9% исследуемых, в послеоперационном периоде — лишь у 4,8%. Битемпоральная гемианопсия до операции была у 19% пациентов, в послеоперационном периоде она сохранилась у 11,9%.
Оценка качества жизни больных проводилась в до- и послеоперационном периодах. Произведен анализ показателей качества жизни по функциональным и симптоматическим шкалам.
У пациентов отмечена положительная динамика в послеоперационном периоде по всем функциональным шкалам. Так, после операции улучшилось физическое (с 89,7±11,7 до 94,7±8,9), ролевое (с 85±22 до 94,5±15,8), когнитивное (с 69,4±24,4 до 91,7±13,8), эмоциональное (с 69±24,7 до 92,9±18,8, p 
Показатели качества жизни у больных с аденомами гипофиза в динамике по функциональным шкалам (EORTC QLQ-C30).
По симптоматическим шкалам отмечено снижение утомляемости (c 62,9±25,9 до 77,1±19,8), выраженности болевого синдрома (с 71,4±30,4 до 84,9±22), проявлений тошноты и рвоты (с 95,6±12,3 до 96±9,6), одышки (с 86,6±24,5 до 90,5±22,4). У больных после операции нормализировалась моторика кишечника, снизилась частота проявления диареи (с 96,8±12,3 до 100) и запоров (с 90,5±18,4 до 95,3±13,9), стабилизировался сон с изменением показателя с 72,3±33,7 до 81,1±28,6. Кроме того, после оперативного вмешательства исследуемые отмечали уменьшение своих ожидавшихся финансовых затруднений (с 89,7±23,9 до 98,4±7,1). При опросе пациентов о причине уменьшения финансовых трудностей в послеоперационном периоде мы выявили, что после операции пациенты испытывали облегчение в связи с тотальностью удаления образования, улучшением общего состояния и готовы были приступить к своим служебным обязанностям вовремя, не нуждаясь в длительном периоде реабилитации.
После операции пациенты отмечали прогрессирование симптома «снижение аппетита» (с 91,3±19,5 до 89,8±20,1). Отмечено улучшение показателя общего здоровья (с 46,5±19 до 25,3±13).
Таким образом, мы выявили положительную динамику в 14 из 15 шкал качества жизни EORTC QLQ-C30. Получен достоверно положительный результат по 1 шкале — эмоциональное функционирование. Отрицательная динамика отмечена только по одной симптоматической шкале — снижение аппетита.
У исследуемых больных отсутствовали интра- и послеоперационные осложнения.
Установлена корреляционная связь между шкалой общего здоровья и функциональными, симптоматическими шкалами у исследуемых в послеоперационном периоде. Более высоко оценили свое состояние здоровья после операции те пациенты, которые были удовлетворены своим положением в обществе (социальным статусом) (r=0,350; p=0,023), и те, у которых улучшился аппетит (r=0,433; p=0,004).
На основании того, что по 14 из 15 шкал качества жизни в послеоперационном периоде у больных отмечена положительная динамика, мы пришли к заключению, что оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных. Мы предполагаем, что такие значимые улучшения качества жизни больных в раннем послеоперационном периоде, возможно, вызваны повышенным эмоциональным фоном. На момент выписки исследуемые нами пациенты были счастливы от того, что самый важный этап в их лечении (оперативное лечение) уже позади, опухоль доброкачественная, удалена тотально и отсутствуют осложнения. А это значит, что вернуться к прежнему ритму жизни больные смогут быстрее, чем планировали до операции.
Была проанализирована литература по теме исследования. Ранее C. Andela и соавт. [25] изучили изменения качества жизни у больных с аденомой гипофиза. В их анализ было включено 102 работы. Авторами отмечено, что хирургические и фармакологические мероприятия по лечению аденом гипофиза улучшают, но не нормализуют качество жизни.
Заключение
Оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных. После операции пациенты отмечали отрицательную динамику только по одному симптому — снижение аппетита. Более высокие оценки своего состояния здоровья после операции давали пациенты с более высоким социальным статусом (r=0,350; p=0,023) и те, у которых улучшился аппетит (r=0,433; p=0,004). Отмечены полное улучшение и отсутствие жалоб после операции у 7% исследуемых (100% по шкале Карновского, 0 баллов по ECOG-ВОЗ).
Авторы заявляют об отсутствии конфликта интересов.
Комментарий
При любой плановой нейрохирургической операции важно не только сохранить жизнь пациенту, минимизировать осложнения, но и обеспечить достойный уровень качества жизни в послеоперационном периоде, который у пациентов с аденомой гипофиза зависит от зрительных функций, гормонального фона и других факторов.
Сопоставив состояние больных до и после трансназальных аденомэктомий, авторы выявили лишь один отрицательный момент в серии из 42 пациентов — прогрессирование снижения аппетита в послеоперационном периоде. Наиболее вероятно, что это могло быть связано с усугублением вторичного гипокортицизма. Важно было бы провести корреляцию этого осложнения с точки зрения исходного и послеоперационного гормонального статуса.
Статья, безусловно, актуальна, ибо динамика качества жизни все шире применяется для оценки результатов в хирургии. Однако дефектом планирования работы можно считать, что послеоперационное состояние больных оценивалось только в раннем послеоперацинном периоде — до момента их выписки из стационара. Возможно, поэтому данные, полученные авторами, в основном говорят о повышенном эмоциональном фоне пациентов в раннем послеоперационном периоде, а не о реальном улучшении качества жизни. Сами авторы отмечают, что пациенты (и их близкие) счастливы от того, что перенесли операцию без серьезных осложнений, опухоль оказалась доброкачественной, она удалена тотально.
В то же время опыт Московского нейрохирургического центра им. Бурденко и данные других исследователей говорят о том, что в первые недели после трансназальной аденомэктомии качество жизни пациентов может заметно ухудшаться: отек слизистой после операции нарушает носовое дыхание днем и ночью, возникают временные нарушения обоняния, в течение длительного времени сохраняются кровяные выделения из носа и другие послеоперационные проявления. Кроме того, пациенты в первые недели после операции весьма ограничены физически, им противопоказаны физические нагрузки, наклоны, чиханье, натуживание, т.е. все то, что может привести к повышению внутричерепного давления (в целях профилактики послеоперационной ликвореи). В раннем послеоперационном периоде часто нарастают или появляются симптомы гипопитуитаризма и транзиторного несахарного диабета, гормональная перестройка организма требует в первые недели после операции приема гормональной заместительной терапии, что также не может заметно улучшить качество жизни.
Поэтому, по нашему мнению и по данным ряда авторов (E. McCoul. J Neurosurg. 2015;123:813-820), качество жизни после трансназальной операции возвращается на дооперационный уровень лишь через 6 нед. В связи с этим исследовать качество жизни целесообразно не только в раннем послеоперационном периоде, но и через 3, 6, 12 нед и т.д.
Тем не менее очевидная польза от этой публикации состоит в том, что она ориентирует широкий круг специалистов (нейрохирургов, эндокринологов и специалистов смежных специальностей) на возможность использования в практике различных современных оценочных критериев их работы.
П.Л. Калинин, А.Н. Шкарубо (Москва)