Bloomberg Creative / Getty Images
С 1750 года люди увеличили количество метана в атмосфере примерно на 150%. Добыча ископаемых видов топлива, таких как нефть, газ и уголь, является крупнейшим источником выбросов метана. Люди также увеличили выбросы метана из-за интенсивных методов ведения сельского хозяйства, животноводства и удаления отходов. (2)
По данным NASA, около 30% выбросов метана приходится на водно-болотные угодья. Еще 30% приходится на добычу нефти, газа и угля. Сельское хозяйство, особенно животноводство, выращивание риса и управление отходами составляют 20%. Остальные 20% поступают из более мелких источников, включая океан, сжигание биомассы, вечную мерзлоту и – подождите – термитов. (3)
Природный газ представляет собой крупнейший антропогенный источник выбросов метана и выделяется при добыче нефти и газа. Нефтяные и газовые резервуары, которые часто встречаются вместе, существуют на тысячи метров ниже поверхности Земли. Чтобы добраться до них, нужно выкопать глубоко в земле колодцы. После добычи нефть и газ перемещаются по трубопроводам.
Метан имеет много полезных применений. Природный газ используется для отопления, приготовления пищи, в качестве альтернативного топлива для некоторых автомобилей и автобусов, а также для производства органических химикатов. Десять лет назад промышленность продвигала природный газ в качестве более чистого «мостового топлива», помогающего отказаться от нефти. Но хотя в момент сгорания природный газ выделяет меньше парниковых газов, он производит на самом деле не меньше выбросов, чем другие ископаемые виды топлива, на протяжении всего своего жизненного цикла из-за широко распространенных утечек.
Воздействие метана
Выбросы от ископаемого топлива
Утечки газа могут происходить из труб и другой инфраструктуры в сетях природного газа, а также из простаивающих и заброшенных скважин. Сжигание и сброс во время добычи – два других значительных источника антропогенных выбросов метана. Если вы когда-нибудь видели, как при добыче нефти или газа из высокой трубы вырывается пламя – это сжигание природного газа в воздухе. (6)
Производители и дистрибьюторы нефти и газа оценивают выбросы во время бурения, удаления газов и сжигания в факелах, а также любого газа, который вытекает из миллионов труб и соединений, составляющих газовую сеть. Но независимые исследования показывают, что выбросы метана намного больше, чем сообщается в отраслевых отчетах. (7)
Новые исследования показывают, что пластиковые изделия, такие как пластиковые пакеты, предметы домашнего обихода и синтетическая одежда, являются дополнительными источниками выбросов метана. Это вызывает обеспокоенность, поскольку производство пластика может удвоиться в следующие два десятилетия, однако прямые выбросы от пластиковых изделий не учитывались ни в глобальном бюджете метана, ни в климатических моделях. (8)
Сельское хозяйство, животноводство и пищевые отходы
Tim Graham/ Getty Images
Выбросы метана в сельском хозяйстве включают животноводство, выращивание риса и сточные воды. Животноводство составляет самую большую долю, а также растущую долю, поскольку мировое потребление мяса продолжает расти. По данным Продовольственной и сельскохозяйственной организации ООН (FAO), животноводство составляет 14,5% от общих антропогенных выбросов парниковых газов. (9, 10)
Основная часть выбросов домашнего скота происходит от жвачных, таких как крупный рогатый скот, буйволы, овцы и верблюды, которые производят много метана во время пищеварения, большая часть которого выделяется при отрыжке. Навоз домашнего скота вносит дополнительный вклад, особенно в системах интенсивного сельского хозяйства. Из выбросов метана от жвачных животных наибольший вклад вносят мясной и молочный скот. (10)
Пищевые отходы – еще одна серьезная проблема. По данным FAO, около трети всех продуктов питания, производимых в мире для потребления человеком, никогда не употребляется в пищу. Эти пищевые отходы вносят значительный вклад в общие выбросы парниковых газов (около 8%) и являются основным источником выбросов метана при разложении пищевых продуктов. (11)
Хотя наиболее важными источниками антропогенных выбросов метана являются сельское хозяйство и добыча ископаемого топлива, люди вносят свой вклад в выбросы другими способами. По данным EPA, полигоны твердых бытовых отходов являются третьим по величине источником антропогенных выбросов метана. Есть также косвенные воздействия изменения климата. Потепление планеты приводит к таянию вечной мерзлоты, что может привести к выбросу большего количества метана. Еще одна причина – сжигание биомассы от лесных пожаров и преднамеренное сжигание. (12, 13, 14, 15)
Последствия для здоровья человека
Регулирование
Одно недавнее исследование показало, что быстрое сокращение выбросов метана может замедлить скорость потепления Земли на целых 30%. Но времени мало: в 2020 году уровень метана резко увеличился. Важные меры по обращению вспять этой тенденции включают сокращение утечек, связанных с нефтью и газом, и преднамеренных выбросов газа, очистку заброшенных угольных шахт, сокращение потребления мяса и молочных продуктов, использование кормовых добавок для крупного рогатого скота, снижающих отрыжку, а также внедрение технологий для улавливания выбросов со свалок. (20, 21)
В 2020 году Европейский союз принял стратегию по сокращению выбросов метана в рамках Европейского зеленого курса, в котором изложен амбициозный план по достижению углеродной нейтральности к 2050 году, включая сокращение выбросов метана. По мере того, как мир готовился к саммиту по климату COP26 в Глазго, на Китай также нарастает давление, чтобы он делал больше. Неизвестно, хватит ли коллективных усилий, чтобы замедлить глобальное потепление и избежать катастрофической переломной точки, но импульс набирает обороты. (22)
Научный журналист, освещающий широкий круг тем, касающихся окружающей среды, климатического кризиса, загрязнения и жизни людей. Внештатный автор сайта «Знание – свет».
Метан
| Метан | |||||||||||||||||||||||||
 | |||||||||||||||||||||||||
  | |||||||||||||||||||||||||
| Общие | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Химическая формула | CH4 | ||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||
| Молярная масса | 16,04 г/моль | ||||||||||||||||||||||||
| Плотность | газ (0 °C, 1013 гПа) 0,72 кг/м³; жидкость (−161,6 °C) 0,42 г/см³ | ||||||||||||||||||||||||
| Термические свойства | |||||||||||||||||||||||||
| Температура плавления | -182,5 °C | ||||||||||||||||||||||||
| Температура кипения | -161,6 °C | ||||||||||||||||||||||||
| Химические свойства | |||||||||||||||||||||||||
| Растворимость в воде | 0,35 [1] г/100 мл | ||||||||||||||||||||||||
| Классификация | |||||||||||||||||||||||||
| Рег. номер CAS | 74-82-8 | ||||||||||||||||||||||||
| SMILES | C | ||||||||||||||||||||||||
| Безопасность | |||||||||||||||||||||||||
| Токсичность | |||||||||||||||||||||||||
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
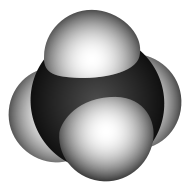
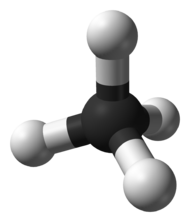
Строение метана
В молекуле метана встречаются связи C–H. Связь C–H ковалентная слабополярная. Это одинарная σ-связь. Атом углерода в метане образует четыре σ-связи. Следовательно, гибридизация атома углерода в молекуле метана– sp 3 :


Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |


Изомерия метана
Для метана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства метана
Метан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для метана характерны только радикальные реакции.
Метан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
Для метана характерны реакции радикального замещение.
1.1. Галогенирование
Метан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:

Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:

| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
Бромирование протекает более медленно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:

Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:

Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:
1.2. Нитрование метана
Метан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в метане замещается на нитрогруппу NO2.
Например. При нитровании метана образуется преимущественно нитрометан: 2. Реакции разложения метана (д егидрирование, пиролиз)
Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен: Пиролиз метана – промышленный способ получения ацетилена. 3. Окисление метанаАлканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеАлканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С. Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода: Эта реакция используется для получения сажи. 3.2. Каталитическое окисление
Продукт реакции – так называемый «синтез-газ». Получение метана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)2. Водный или кислотный гидролиз карбида алюминияЭтот способ получения используется в лаборатории для получения метана. 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. 4. Синтез Фишера-ТропшаИз синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды: Это промышленный процесс получения алканов. Синтезом Фишера-Тропша можно получить метан: 5. Получение метана в промышленности |






















