Система для аутогемотрансфузии Cell Saver® 5+
 |  |
| Производитель | Haemonetics Corporation |
| Страна происхождения | США |
| Цена | Снят с производства |
Cell Saver 5+ представляет собой пятое поколение систем для получения аутологичной крови, продукт тридцатилетних испытаний, совмещающий в себе ранее достигнутые преимущества с последними разработками микропроцессорной и сенсорной технологии.
Информация о системе:
Кровь собирается, смешивается с антикоагулянтом, фильтруется и поступает в стерильный резервуар. При достижении достаточного объема автоматически запускается цикл обработки, включающий процессы гемоконцентрации и отмывания клеток крови стерильным физиологическим раствором. По окончании циклов отмытые эритроциты перекачиваются в пластиковый мешок для реинфузии.
Показания к применению : операции на открытом сердце и сосудах, аневризмах, операции на суставах и позвоночнике, операции на печени и селезёнке, разрывная эктопическая беременность и некоторые нейрохирургические процедуры.
Простота и удобство использования
Аппарат для реинфузии эритроцитов Cell Saver 5+
Любые роды сопровождаются кровопотерей. Наибольшая кровопотеря происходит при оперативном родоразрешении, а именно операции кесарева сечения. В Семейной клинике «Роддом на Фурштатской» появилась новая технология переливания собственных эритроцитов у пациенток, которые имеют высокий риск кровопотери в родах с использованием аппарата для реинфузии эритроцитов Cell Saver5+.
Как известно, человеческая кровь состоит из форменных элементов (клеток определенной формы) и плазмы. Плазма — это жидкая часть крови, в которой находятся форменные элементы. Представляет собой однородную, несколько мутную (иногда почти прозрачную) желтоватую жидкость. К форменным элементам относятся лейкоциты, эритроциты, тромбоциты. И именно эритроциты придают красный оттенок крови. Основной их функцией является перенос кислорода и оксида углерода. Также они участвуют в переносе питательных веществ, иммунных реакциях и помогают поддержать кислотно-основное равновесие
Долгое время вопрос с переливанием решался использованием донорской крови. Особенно это было распространено в СССР. Но со временем, исследователи стали отмечать появление определенных осложнений:
· различные иммунологические реакции, приводящие к снижению собственного иммунитета
· передача инфекции — вирусы гепатита В и С, ВИЧ, вирусы лейкоза, простого герпеса, возбудители малярии, сифилиса и.т.п.
· несовместимость крови и развитие гемолитических осложнений из-за погрешностей в хранении, логистике, заготовке; ошибок в определении группы и.т.п.
· недостаток доноров в отдаленных местностях, в случае военных конфликтов, катастроф.
Какие же преимущества имеет переливание собственных эритроцитов пациентки:
Показания к проведению переливания собственных эритроцитов пациентки при кесаревом сечении:
Таким образом, все наши пациентки смогут избежать многих осложнений при родоразрешении путем операции кесарева сечения благодаря наличию в Семейной клинике «Роддом на Фурштатской» современной технологии.
Аппарат для аутотрансфузии крови Cell Saver Elite, «Haemonetics Corporation», США
Информация о системе:
Аппарат для аутотрансфузии крови Cell Saver Elite, компании Haemonetics®, обеспечивает интра- и послеоперационный сбор крови при хирургических вмешательствах, которые сопровождаются кровопотерей средней и тяжелой степени, обработку крови посредством центрифугирования и отмывания, с последующей закачкой отмытых эритроцитов в мешок для реинфузии под действием силы тяжести либо в артериальную линию экстракорпоральной магистрали пациента.
Основные преимущества процедуры:
Отсутствие риска передачи трансмиссивных заболеваний, не возникнет нежелательных реакций при переливании, а также отсутствие дополнительных манипуляций с донорской кровью.
Показания к применению: операции на открытом сердце и сосудах, аневризмах, операции на суставах и позвоночнике, операции на печени и селезёнке, разрывная эктопическая беременность и некоторые нейрохирургические процедуры.
Особенности:
Автоматическая работа
Простота и удобство использования
Маневренность и портативность
Основные технические характеристики Cell Saver 5+:
Объем центрифужного колокола: 70, 125 и 225 мл.
Скорость центрифуги: от 2050 до 5650 об./мин со ступенью 100 об./мин. для колокола 225 и 125 мл.
Размеры аппарата без стойки(ГхВхШ) – 54,6х41,9 х29,8 см
Размеры аппарата с тележкой(см) – 67,3х 121,9 х53,3 с учётом сложенной стойки.
Альтернативы (4) Cell Saver
В прошлом посте я писал о том, какие есть альтернативы применению донорской крови в акушерской практике. И один из комментаторов высказался в том смысле, что «Основной причиной кровопотери как при ЕР, так и при КС является отслойка плаценты, при котором может случиться критическая кровопотеря за считанные минуты. И тогда будь то США, Россия или любая другая страна, необходимо переливание крови»
Я не буду ничего в ответ говорить от себя, дам слово специалистам:
ФГБУ «Северо-западный Федеральный Медицинско исследовательский центр», г. Санкт-Петербург Интраоперационная аппаратная реинфузия эритроцитов в акушерстве и гинекологии Таюрская М.О. Врач акушер-гинеколог Высшей категории КДО ПЦ
В нашем центре с 6 июня 2012 года в алгоритм ведения родов и в план гинекологических операций включена и успешно применяется интраоперационная аппаратная реинфузия эритроцитов.
Полное предлежание плаценты с признаками врастания по данным МРТ Пациентка 44 года. Роды 3 срочные в 39 недель 3 дня. Рубец на матке после кесарева сечения в 2006 г. Полное предлежание плаценты. Объем кровопотери 1450,0, объем реинфузии 700мл (Ht 50%) выписана на 4 сутки с Hb 104г/л. Трансфузионная терапия не проводилась.
Множественная миома матки Пациентка 32 года, удаленно 13 интрамурально субсерозных узлов, общая кровопотеря 1200,0, объем реинфузии 750мл (Ht 31%) выписана на 6 сутки с Hb 95г/л. Трансфузионная терапия не проводилась.
Гигантская миома матки Пациентка 26 лет, объем кровопотери 1300,0, объем реинфузии 750мл (Ht 47%) выписана на 7 сутки с Hb 122г/л. Трансфузионная терапия не проводилась.
Выводы Значительно сокращена трансфузионная терапия в послеоперационном периоде. Улучшено течение послеоперационного периода, уменьшено время пребывания в отделении реанимации и длительность пребывания в стационаре. Необходимо шире использовать интраоперационную реинфузию в экстренных случаях, в частности при ПОНРП. Для этого необходимо иметь в каждой дежурной бригаде обученного специалиста. Ни у одной из 90 пациенток не потребовалось расширения объёма операции до экстирпации матки даже при массивной и сверхмассивной кровопотерях. Возможно это связано с более спокойной и комфортной работой оперирующей бригады, неограниченной временем и объемом кровопотери.
Заключение Таким образом, включение интраоперационной аппаратной реинфузии эритроцитов в алгоритм ведения родов и в план гинекологических операций у женщин с миомой матки, предлежанием плаценты, врастанием плаценты в рубец на матке является обоснованным и высоко эффективным при кровопотере любого объема.
В Центре травматологии и ортопедии ФГКУ «ГВКГ им. Н.Н. Бурденко» МО РФ с декабря 2009 г. при эндопротезировании коленного и тазобедренного сустава используются системы для реинфузии дренажной крови в послеоперационном периоде. Проведено 930 аутогемотрансфузий. Гемотрансфузионных осложнений при реинфузии дренажной крови не отмечено, в то время как при переливании донорской крови их количество по нашим данным составляло до 5,7 %.
Заключение: реинфузия дренажной крови позволяет практически полностью отказаться от использования донорских компонентов крови при эндопротезировании крупных суставов, тем самым значительно уменьшая посттрансфузионные реакции и осложнения и обеспечивая существенную экономию денежных средств медицинского учреждения
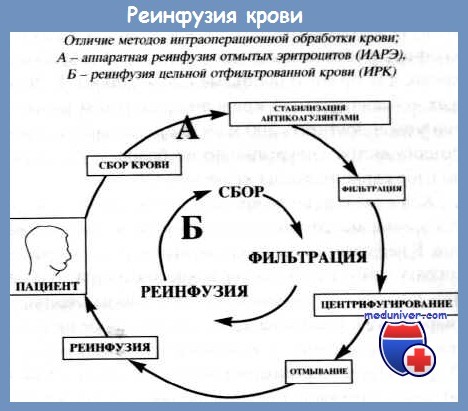
История развития интраоперационной реинфузии
В 1818 г Джемс Бланделл (James Blundell) провел серию опытов по реинфузии на собаках и рекомендовал ее использовать у больных. В России в 1865 г Василий Васильевич Сутугин высказал идею о возвращении крови в сосудистое русло больному. В 1874 г Вильям Хеймор (Highmore) предложил собирать и дефибринизировать кровь, излившеюся после родов, затем согревать ее до температуры тела и переливать пациентке при помощи шприца Хиггинсона. В 1914 г немецкий гинеколог Иоганнас Тисс (J. Thiess) провел первую успешную реинфузию при операции по поводу внематочной беременности. В России первую реинфузию больной с внутрибрюшным кровотечением при нарушенной внематочной беременности произвел А.Н Филатов в 1918 г. После чего этот метод стал широко использоваться в гинекологической практике.
Однако после внедрения в 1935 г техники консервирования донорской крови практика реинфузии сошла на нет. До 1968 г в литературе описаны единичные случаи применения реинфузии. Возобновление развития реинфузии начинается с 1968 г, когда американский военный хирург Джеральд Клебанов (Gerald Klebanoff) предложил использовать кардиотомный резервуар и роликовый насос для сбора, антикоагуляции, фильтрации и реинфузии интраоперационно излившийся крови. Клебанов участвовал в разработке первого промышленного аппарата для реинфузии Bentley ATS 100, который успешно применялся во время вьетнамской войны. Этот аппарат был далек от совершенства, имел низкую степень отчистки крови, что вызывало расстройство гемокоагуляции, воздушную эмболию и почечную недостаточность.
Более 20 лет фирма Haemonetics имела патент на выпуск этих аппаратов и лишь с конца 90-х годов стали появляться аналогичные аппараты, работающие по принципу «перевернутой чаши» или т.н. «колокола». Особенностью этих аппаратов является то, что они работают по принципу «шаг за шагом», то есть заполнение, концентрирование и отмывка происходят поэтапно один за другим. В 90-х годах компания Fresenius разработала проточную непрерывную систему для реинфузии C.A.T.S. (Continuous AutoTransfusion System). Особенность этого аппарата в том, что в нем установлены три насоса, которые работают одновременно. Первый подает кровь из резервуара для очистки, второй подаёт промывочный раствор, а третий транспортирует очищенную кровь в мешок для реинфузии.
Как видишь, мой дорогой читатель, реинфузия имеет весьма давнюю историю.
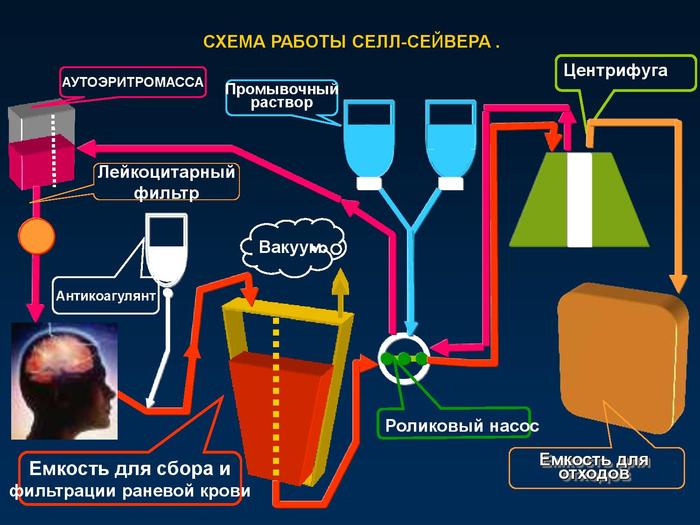
Принципиальное устройство большинства современных селл-сейверов схематично представлено на рисунке и мало чем отличается у различных производителей (сейчас такое оборудование производят не менее пяти фирм).
Основными компонентами любого селл-сейвера являются:
— отсосная двухпросветная линия и кардиотомный резервуар;
— центрифуга с магистралями;
— роликовый насос (насосы), обеспечивающий движение всех жидкостей в контуре селл-сейвера;
— емкость для сбора отмытых эритроцитов.
И снова пусть высказываются специалисты:
Реинфузия крови в хирургии. Современное состояние проблемы
А.Ю. Лубнин, В.В. Громова
Как и любой методике, РК присущи определенные осложнения, хотя в огромном исследовании, приводимом DeAndrade et al. (более 43 000 пациентов), общая частота осложнений аппаратной РК оказалась экстремально низкой — от 0 до 0,0006 %.
Идея компенсации операционной кровопотери при хирургических вмешательствах с помощью возврата излившейся раневой крови оперируемому больному, возникшая много десятилетий назад, прошла сложный путь и в настоящее время реализована в эффективную медицинскую технологию. Реинфузия крови позволяет существенно снизить трансфузионную нагрузку на больного донорскими компонентами крови, а в ряде случаев, при успешном сочетании с другими кровесберегающими методиками, полностью отказаться от применения донорских компонентов. Методика РК не только развивается технически, но и получает все большее клиническое распространение.
Cell saver что это
Обратное переливание пострадавшему собственной крови, излившейся в результате ранения сосудов в серозные полости, возвращая собственные клеточные элементы и иммунные тела, является наиболее физиологичным методом восполнения кровопотери.
В то же время для крови, собранной из серозных полостей, характерно полное отсутствие фибриногена на фоне высокой фибринолитической и тромбопластической активности, повышенное содержание свободного гемоглобина и ионов калия, что при реинфузии трех и более литров крови может повлиять на показатели гемостаза циркулирующей крови и на полноценность клубочковой фильтрации, особенно при нестабильной гемодинамике [Абакумов М.М. и др.].
В 1988 г. нашим сотрудником Н. В. Лебедевым была выполнена научная работа, в которой изучено влияние массивной реинфузии на систему гемостаза у пострадавших с травмой груди и живота. Было выяснено, что кровь, излившаяся в серозные полости при травме внутренних органов и находящаяся там в течение различного времени, претерпевает некоторые изменения. Исследованы образцы крови у 82 пострадавших с травмой груди и живота.
В этой крови было снижено количество эритроцитов до 3,9+0,77 х 10 12 /л, тромбоцитов до 181+42,4х10 9 /л, увеличено содержание свободного гемоглобина (1,7±0,5 г/л) за счет частичного разрушения форменных элементов. Обращало на себя внимание полное отсутствие фибриногена в излившейся в полость крови, а также повышение ее фибринолитической активности до 27,2±4,7 мин при травме груди и 54+10 мин при травме живота. Уровень плазминогена составлял 1,9±0,1 КЕ/мл, а содержание плазмина — 0,31±0,13 КЕ/мл.
Содержание ингибиторов протеолиза было несколько снижено и в среднем составляло 53,8+1,6 КЕ/мл.
Таким образом, кровь из брюшной полости не отличается от крови из грудной полости, за исключением величины фибринолитической активности плазмы.
Влияние массивной (более 1 л) реинфузии крови на состояние системы гемостаза циркулирующей крови изучено у 44 пострадавших с травмой груди и живота. Анализ системы гемостаза циркулирующей крови у пострадавших с внутриполостным кровотечением (до реинфузии) выявил выраженные гипокоагуляционные изменения. При этом временные показатели тромбоэластограммы (Р и К) были удлинены соответственно на 25% и в 1,5 раза, а максимальная амплитуда (МА) снижена на 20-25%. Содержание фибриногена находилось на уровне нижней границы нормы, а время рекальцификации плазмы было удлинено на 30-35% (составляя в среднем 175+21,5 с при травме живота и 210+21,0 с при травме груди).
Фибринолитическая активность крови была повышена на 11-22% по сравнению со средним уровнем, но не выходила за пределы физиологической нормы. При этом более выраженная активация фибринолиза отмечена в группе больных с ранениями груди, а гипокоагуляционные изменения в большей степени выражены у пострадавших с ранениями живота.
Переливание пострадавшим 1 л и более крови, изъятой из грудной или брюшной полостей, приводило к кратковременному усугублению гипокоагуляционных изменений. В первые часы после массивной реинфузии показатели R и К тромбоэластограммы удлинялись в 1,5-2 раза, амплитуда МА снижалась на 5-10% по сравнению с исходным уровнем, а величина фибриногена достигала 1,6-1,8 г/л. Время рекальцификации удлинялось до 196+20,9 с после реинфузии крови из брюшной полости и до 231+21,4 с при травме груди. Фибринолитическая активность изменялась незначительно и была в пределах нормы.
Содержание плазмина после реинфузии снижалось до 2,4 КЕ/мл (при норме 3,8-4,2 КЕ/мл,). В этот период наблюдалась тенденция к нормализации протеолитической активности и ингибиторов протеолиза.
Реинфузия оказывала влияние и на тромбоцитарное звено гемостаза: количество тромбоцитов в венозной крови снижалось до (140-180)х10 9 /л, а их агрегационная способность уменьшалась в 1,5 раза по сравнению с нормой.
Состояние выраженной гипокоагуляции сохранялось после реинфузии в течение суток. Однако уже начиная со вторых суток наблюдалась тенденция к нормализации показателей плазменного звена системы гемостаза циркулирующей крови. Так, к концу первых суток после операции и реинфузии уровень фибриногена достигал своих физиологических параметров, время рекальцификации плазмы снижалось до 218+24 с, сокращались временные показатели R и К тромбоэластограммы, максимальная амплитуда удлинялась до 21±2,9 мм при ранениях живота и до 35,9+2,0 мм при ранениях груди. Содержание плазминогена оставалось к концу суток сниженным до 2,55+0,24 КЕ/мл при ранениях живота и 2,97+0,34 КЕ/мл при ранениях груди.
В дальнейшем отмечалась постепенная нормализация показателей тромбоэластограммы, времени рекальцификации плазмы. В течение 6-11 сут после реинфузии в состоянии гемостаза у больных отмечались изменения, характерные для воспалительных и репаративных процессов, сопровождающих посттравматический и послеоперационный периоды: резко увеличивалось содержание фибриногена (до 5-7 г/л), возрастали протеолитическая и антипротеиназная активности крови. Содержание плазминогена к 7-8-м суткам после реинфузии приближалось к физиологическому уровню, достигая 3,4-3,5 КЕ/мл.
Данные тромбоэластограммы свидетельствовали о нормализации коагуляционных свойств крови. Количество и агрегационная способность тромбоцитов к концу наблюдений были в пределах нормы. У обследованных пострадавших не было отмечено клинического проявления ДВС-синдрома в виде различного вида геморрагии или тромботических осложнений.
Таким образом, данные, полученные при исследовании системы гемостаза у пострадавших с ранениями органов грудной и брюшной полостей, позволяют утверждать, что непосредственное влияние реинфузии на состояние гемостаза сказывается только в первые сутки. В последующем развиваются такие изменения в системе гемостаза, которые в целом характерны для патологических состояний, протекающих с воспалительными реакциями. Реинфузия крови на фоне гипокоагуляции не приводит к устойчивым патологическим сдвигам в системе гемостаза, которые требовали бы специфической коррекции.
В настоящее время во всех странах признана высокая эффективность такого метода восполнения кровопотери. Наибольшее распространение получила реинфузия аппаратом Cell Saver. Следует заметить, что еще в 1986 г. Н. В. Лебедевым совместно с инженером Всесоюзного Научно-исследовательского института медицинского приборостроения И. Н. Швырковым был создан и применен в клинической практике у 42 пострадавших с ранениями груди первый в СССР аппарат для реинфузии крови АРПК-1. Однако в силу исторических событий немедицинского характера этот аппарат после демонстрации на ВДНХ был благополучно забыт. (Стоимость аппарата Cell Saver в ценах 2010 г. колеблется от 30 до 50 тыс. евро.)
При использовании аппарата Cell Saver кровь, удаленная из серозной полости, попадает в систему центрифуг, позволяющую отделять эритроциты от плазмы и их промывать. Кровь пропускается сначала через макрофильтр с величиной пор 180-200 мкм, а затем через микрофильтр с величиной пор 20-40 мкм. Отмытые эритроциты, взвешенные в изотоническом растворе хлорида натрия, насосом перекачиваются в емкость для реинфузии. Использование аппаратов Cell Saver позволяет быстро осуществить забор крови из серозных полостей, в течение 5-10 мин ее обработать и начать реинфузию клеточного компонента.
Технология этого процесса сводится к сбору крови в стерильную емкость через фильтры, ее стабилизации, аппаратной фрагментации на компоненты (плазму и клетки), отмыванию клеток, повторную фрагментацию и концентрацию клеточного компонента.
Сбор крови осуществляет хирург с помощью двухпросветной трубки, на наконечник которой по микроканалу со скоростью 40-60 капель в минуту подается раствор антикоагулянта и по основному каналу с разрежением 100-150 мм рт. ст. кровь поступает в стерильный резервуар. В качестве стабилизатора обычно используют стандартный раствор цитрата натрия (АСД) в соотношении 15 мл цитрата на 100 мл крови.
Собранная кровь поступает в сепаратор, где центрифужным методом отделяется основная часть плазменной фракции, а оставшаяся клеточная часть крови разбавляется изотоническим раствором хлорида натрия, что обеспечивает более полное отмывание неизмененных клеток от их фрагментов и оставшейся части плазмы. Оставшийся клеточный компонент представляет собой концентрат клеток в изотоническом растворе, в котором практически нет плазмы (с концентрацией общего белка не более 1,7 г/л). Уровень гематокрита в этом клеточном концентрате составляет около 70 %, уровень гемоглобина — около 200 г/л.
Удаляя 97-98 % белков плазмы, методика Cell Saver обеспечивает освобождение клеточного компонента крови от активаторов плазминогена, плазмина, продуктов распада фибрина и других биологически активных веществ, влияющих на систему гемостаза. Отсутствие фибринолитической активности в компонентах крови, возвращаемых пациенту, позволяет избежать таких нежелательных последствий, как развитие ДВС-синдрома в случаях реинфузии объемов крови, превышающих ОЦК.
В то же время применение аппаратной реинфузии крови сопряжено с рядом трудностей. Во-первых, метод требует полноценного замещения плазменных компонентов путем инфузии не только и не сколько кристаллоидных и коллоидных растворов, сколько больших объемов свежезамороженной плазмы.
Во-вторых, при наличии в серозных полостях большого количества сгустков крови объем забора жидкой крови резко уменьшается, и в таких случаях глобулярный объем приходится восполнять переливанием донорской крови.
При продолжающемся массивном кровотечении может наступить тромбирование всех стерильных магистралей аппарата Cell Saver, что требует их срочной замены.
Резкое уменьшение объема возвращаемого клеточного компонента (по сравнению с объемом забранной крови) наблюдается при попытке подвергнуть реинфузии гемолизированную «старую» кровь. В таких случаях в процессе сепарации удаляются все неполноценные и фрагментированные эритроциты и возвращается не более 20-25 % клеточного компонента.
Наконец, и при аппаратной реинфузии существует проблема микробной контаминации. При ранениях полых органов брюшной полости (в меньшей степени — бронхов) и при массивной кровопотере (более 3,5 л) появляются жизненные показания для реинфузии, например, у пострадавших с редкой группой крови или при отсутствии донорской крови (эритромассы). Как показал опыт НИИ СП им. И. В. Склифосовского, в таких случаях многократное отмывание контаминированной крови позволяет в 10-12 раз снизить уровень контаминации микроорганизмов в клеточном компоненте, реинфузия которого не приводит к бактериемии [Кобзева Е. Н.]. С целью профилактики гнойно-септических осложнений этим пациентам проводится антибактериальная и иммунная терапия.
Таким образом, эффективность аппаратной реинфузии крови при ранениях шеи, груди, живота, и тем более при сочетанных ранениях,— несомненна. Но этот метод достаточно дорог. Кроме того, его широкое применение требует создания специальной трасфузиологической службы, введение в состав дежурной бригады специалиста — трансфузиолога. Поэтому во многих стационарах страны реинфузия осуществляется без аппаратов.
Обычно кровь собирают из полостей специальным черпаком в стерильный сосуд емкостью 1000 мл, содержащий 150 мл 4% раствора натрия цитрата (из расчета 15 мл стабилизирующего раствора на 100 мл крови). После стабилизации кровь переливается во флакон для внутривенной инфузии через самодельный фильтр (8 слоев марли). Однако такая методика несовершенна: эвакуация крови происходит слишком медленно, что затрудняет поиск источника кровотечения, открытое переливание из черпака во флакон и из флакона с консервантом в резервуар для реинфузии увеличивает опасность загрязнения крови.
Поэтому большинство хирургов используют закрытые аспирационные системы. Самая простая система состоит в следующем. Пробку стерильного флакона емкостью 500 мл, содержащего 75 мл 4 % раствора цитрата натрия, обрабатывают антисептическим раствором и прокалывают двумя иглами для гемотрансфузии: к длинной игле, конец которой опускают до дна флакона, присоединяют трубку с наконечником, обернутым в несколько слоев марли и забирающим кровь из серозной полости, а к короткой игле — шланг от электроотсоса. После наполнения флакона его переворачивают пробкой вниз и устанавливают в штатив для переливания крови.
Для предотвращения разрушения эритроцитов величина разрежения не должна превышать 100-140 мл рт. ст. Трубка, соединяющая наконечник отсоса с флаконом, должна быть из силиконизированной резины и должна быть цельной, без отдельных отрезков с переходниками, что увеличивает турбулентность крови и ее повреждение в ходе аспирации.
При массивной реинфузии (более 1,5-2 л) для нейтрализации гипокоагуляционного эффекта рекомендуется одновременно вводить фибриноген, раствор аминокапроновой кислоты. Для предупреждения нежелательного побочного действия больших доз цитрата натрия при реинфузии каждых 500 мл аутокрови внутривенно следует вводить 10% раствор хлорида или глюконата кальция.
Показанием к реинфузии является наличие 500 мл и более жидкой крови в плевральных или брюшной полостях. Постоянная готовность дежурных бригад к проведению реинфузии позволяет использовать ее у каждого пострадавшего с кровотечением.
Абсолютных противопоказаний для реинфузии крови в неотложной хирургии практически нет. Считается, что реинфузия противопоказана при повреждении полых органов брюшной полости или крупных бронхов, при длительном (свыше суток) нахождении крови в серозной полости и при выраженном гемолизе.
1. Ранения полых органов. Ясно, что при умеренной кровопотере и стабильном состоянии пострадавшего реинфузия контаминированной крови абсолютно противопоказана. Она противопоказана и при массивной кровопотере, если в наличии имеется достаточное количество компонентов донорской крови. Но как поступить при кровопотере 3-4 л и недостатке донорской крови или отсутствии крови подходящей группы?
К настоящему времени в литературе опубликованы около 400 наблюдений реинфузии контаминированной крови. Все эти наблюдения можно разделить на непреднамеренные и преднамеренные.
Реинфузия контаминированной крови является непреднамеренной, когда хирург собрал большое количество крови и принял решение о начале реинфузии еще до завершения тщательной ревизии органов. Как правило, это происходит в условиях дефицита донорской крови и критическом состоянии пострадавшего. К моменту, когда обнаруживается повреждение полого органа брюшной полости, реинфузии может подвергнуться 1000 мл крови.
На преднамеренную реинфузию хирурги шли в безвыходной ситуации, когда пациент практически погибал, а донорской крови не было в достаточном количестве (или не было вообще).
По данным отечественных и зарубежных авторов — Е. А. Вагнера и соавт.; С.Д.Попова и соавт.; И.И.Дерябина и соавт.; R.N. Smith и соавт.; J.W. Hauer и соавт., во всех этих наблюдениях имелась быстро проходящая бактериемия, которая исчезала под влиянием антибактериальной терапии в течение 3-5 дней. Ни в одном наблюдении у выживших пациентов не развился сепсис. Но при этом многие авторы предостерегают об опасности развития смертельного эндотоксического шока в случае добавления антибиотиков непосредственно в емкость с контаминированной кровью.
В НИИ СП им. Н. В. Склифосовского реинфузия крови при повреждении органов желудочно-кишечного тракта произведена 22 пострадавшим. У пяти пострадавших реинфузия производилась до ревизии органов брюшной полости и выявления повреждения кишечника, у 17 — в связи с тяжелым или терминальным состоянием пострадавшего, вызванным шоком и крово-потерей и недостаточным количеством донорской крови.
Общий объем перелитой аутокрови при ранении органов желудочно-кишечного тракта составил 21 050 мл (в среднем 1 л крови на пострадавшего). Ни в одном случае летальные исходы и осложнения не были связаны с проведением реинфузии крови.
Проведенный клинический анализ позволил нам сделать вывод, что при большой кровопотере, угрожающей летальным исходом, и при отсутствии достаточного количества донорской крови можно пренебречь наличием повреждения полых органов и произвести реинфузию. В подобных случаях обратное переливание излившейся в полости крови может сыграть решающую роль в спасении жизни пострадавшего.
2. Длительная экспозиция крови в серозных полостях. В настоящее время нет оснований полагать, что кровь, находившаяся в плевральной или брюшной полости без повреждения полых органов в течение 24 ч, непригодна для реинфузии. Кровь остается стерильной в течение 2-3 сут, а уровень свободного гемоглобина не превышает 500 мг% (310 мкмоль/л). По жизненным показаниям реинфузию следует применять и через 48 ч: наш опыт показал, что такая кровь остается стерильной, а концентрация свободного гемоглобина не достигает 200 мг% (124 мкмоль/л). Разумеется, чем дольше кровь находится вне сосудистого русла, тем меньше ее биологическая ценность; в ней уменьшается количество эритроцитов и тромбоцитов и увеличивается степень гемолиза.
3. Гемолиз. Патологическое действие гемолиза зависит от степени его выраженности во всем объеме циркулирующей крови, т.е. от концентрации свободного гемоглобина в реинфузируемой крови и от объема реинфузии.
Например, при реинфузии 2 л крови с содержанием свободного гемоглобина 800 мг% (596 мкмоль/л) его концентрация в циркулирующей крови пациента в первые часы достигнет уровня всего 30-40 мг% (18,6-24,8 мкмоль/л). Через сутки концентрация свободного гемоглобина в циркулирующей крови, независимо от степени его повышения сразу после реинфузии, не отличается от физиологической нормы.
Появление интенсивного розового окрашивания плазмы после центрифузирования крови означает, что уровень свободного гемоглобина более 800 мг%, что служит относительным противопоказанием для реинфузии более 2 л такой крови.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021