Cdkl5 что это мутация
Вызвано мутациями в гене CDKL5, который обнаружен на Х-хромосоме.
Хотя многие случаи были выявлены у мальчиков, из-за расположения гена это расстройство в основном затрагивает девочек. Причина мутации CDKL5 и частота расстройства CDKL5 в настоящее время неизвестны.
Ген CDKL5 дает указания для создания белка, который необходим для нормального развития мозга и нейронов. Хотя относительно функции белка известно немного, он может играть определенную роль в регуляции активности других генов, включая ген MECP2 синдрома Ретта. Белок CDKL5 действует как фермент, который изменяет активность других белков путем добавления к ним атомов кислорода и фосфата (фосфатной группы) в определенных положениях.
CDKL5 является редким расстройством. Мутации CDKL5 были обнаружены у детей с диагнозами: Инфантильный спазм, синдром Веста, синдром Lennox-Gastaut, синдром Ретта, церебральный паралич, аутизм и эпилепсия неизвестного происхождения. Однако важно отметить, что ученые и врачи не знают, что вызывает мутацию CDKL5 или полный спектр расстройств CDKL5. Вероятно, есть много людей CDKL5, у которых есть мягкие симптомы и нет приступов.
Диагностика. Большинство детей с CDKL5, страдают от судорог, которые начинаются в первые часы, дни, недели или месяцы жизни. Некоторые матери описали чувство приступов даже в предродовой период. Приступы проявляются в виде тонических приступов с миоклоническими кластерами и клоническими судорогами. Обычно они происходят во сне. Со временем они могут появляться и во время бодрствования.
Обычно эти первые судороги не обнаруживаются на ЭЭГ, и некоторые дети могут ошибочно диагностироваться как Миоклонус-эпилепсия или синдром Сандифера. Важно отметить, что отсутствие активности на ЭЭГ (или «нормальной» ЭЭГ) не исключает диагноз, связанный с CDKL5. В то время как расстройство CDKL5 в основном выявляется у девочек, его нельзя исключать как диагноз у мальчиков.
Дополнительные симптомы: задержка развития, аутизм, низкий тонус мышц, апраксия, сколиоз, изолированное поражение коры головного мозга в зрительной области, маленькие холодные стопы, ограничение действия рук, отсутствие или задержка речи, трудности при кормлении, гастроинтестинальные проблемы.
С введением сложного генетического тестирования расстройство CDKL5 сейчас диагностируется у детей в относительно раннем возрасте.
Совсем недавно некоторые лаборатории использовали буккальный мазок щек. Мазок крови или слюны затем отправлялся в специальную лабораторию, которая выполняла генетический тест. В последнее время тестирование CDKL5 стало широко доступным методом, позволяющим одновременно тестировать множество потенциальных генов, вызывающих заболевание, с такой же стоимостью, как и тестирование только гена CDKL5.
Клинические проявления.
Вздутие живота может быть связано с гастропарезом, обструкцией, запором или аэрофагией, которое обычно сопровождает аномальное дыхание некоторых детей с CDKL5. В этом случае назначаются лекарственные препараты, а в очень тяжелых случаям может помочь чрескожная гастростомия. Для диагностики патологических состояний со стороны желудочно-кишечного тракта проводится рентгенография живота, исследование опорожнения желудка (двигательная активность желудка), эндоскопия и тестирование для оценки наличия пищевой аллергии.
Аэрофагия может быть значительной и мешать еде и дыханию. Причина заглатывания воздуха до конца не понята, но может быть поведенческой, из-за боли, дискомфорта или беспокойства.
Апраксия является результатом дисфункции полушарий головного мозга, особенно теменной доли, и часто присутствует у людей с CDKL5. Апраксия включает в себя лимбино-кинетическую апраксию (невозможность тонких, точных движений с помощью руки или ноги), идеомоторную апраксию (невозможность сделать правильное движение в ответ на словесную команду), идеальную апраксию (невозможность координировать действия с несколькими последовательными движениями, такими как одевание, прием пищи и купание), словесная апраксия (затруднение координации движения рта и речи), конструктивная апраксия (невозможность скопировать, нарисовать или построить простые фигуры) и окуломоторную апраксию (затруднение перемещения глаз по команде ). Апраксия может сопровождаться афазией. Как правило, лечение людей с апраксией включает физическую, речевую или профессиональную терапию.
Аспирационная пневмония может возникнуть в результате нарушенной координации и низким тонусом мышц, участвующих при глотании. Надгортанник должен закрывать трахею, чтобы предотвратить вдыхание пищи или жидкости, но это не всегда удается, поэтому очень важно исследование процесса глотания. Специальная поза, а также текстура пищи и консистенция жидкости являются ключевыми моментами для правильного глотания.
Аутизм. Лица с CDKL5 могут проявлять разную степень нарушения социального взаимодействия, например, избегать зрительного контакта. Могут возникать повторяющиеся виды поведения, такие как уборка, маниакальная ходьба и манипулирование объектами. Другие особенности включают трудности моторной координации и внимания, поведенческие вспышки и отсутствие осведомленности о безопасности.
Плотность кости. Пока неизвестно, как часто происходит остеопороз при CDKL5. Тем не менее, есть много сообщений о низкой плотности и переломах костей.
Плотность кости должна контролироваться эндокринологом, особенно если есть предположение о преждевременном половом созревании. Остеопороз следует искать особенно у тех лиц, кто никогда не ходил или у которых были переломы. На плотность костей также влияют антиконвульсанты. В этих случаях должна проводить рентгеновская денситометрия.
Бруксизм. Скрежет зубами может возникать в дневное время или во время сна.
Сердечные проблемы. Некоторые лица имеют удлиненный интервал QT, который чаще ассоциируется с синдромом Ретта. Другие сердечные проблемы: аномалии сердечного ритма, такие как тахикардия и брадикардия, а также неспецифические изменения, связанные с Т-волнами. Поэтому люди с расстройством CDKL5 должны ежегодно делать ЭКГ и проводить мониторирование сердечного ритма особенно, если регистрируются аритмии. В ряде случаев необходимо проведение ЭХО-КГ.
Запоры часто регистрируются с лиц с наличием CDKL5. Им важно проводить лечение и профилактику. Повреждения кишечника могут быть источником боли и дискомфорта. Даже если количество пищевых волокон достаточно, необходимо контролировать ежедневное потребление воды, которое может быть низким.
Кортикальное ухудшение зрения представляет собой форму нарушения зрения, которая связана с мозгом, а не с глазами. Дети с расстройством CDKL5 имеют характерный боковой взгляд.
Ручная стереотипия проявляется как постукивание пальцами, отмечаются моющие и скручивающие движения рук и т.д. У многих развивается нарушение функционирования рук.
Гипотония наблюдается почти у всех детей с CDKL5. Для оценки наличия и степени выраженности сколиоза, нарушений со стороны тазобедренного и других суставов, ребенка важно регулярно наблюдать ортопедами.
Нарушение сна связанно с пробуждением среди ночи, ночными ужасами, навязчивым смехом и вздрагиванием. После пробуждения дети испытывают трудности, чтобы заснуть снова из-за нарушения дыхания, судорожной активности и общего беспокойства. Многие пациенты имеют значительное ухудшение сна. У них могут быть дни и ночи без сна или наоборот длительные периоды сна. По назначению невролога многие дети с CDKL5 применяют лекарственные препараты для его улучшения.
Неконтролируемое поведение. Многие семьи сообщают о плаче, смехе без видимой причины и неконтролируемом поведении детей. Когда ребенок становится старше, родители могут считать, что такое поведение может быть связано с болью, геластическими припадками, вызывающими смех, или оно развивается в результате судорожной активности. Следует помнить, что плачущий ребенок с расстройством CDKL5, нуждается в экстренной медицинской консультации для исключения острого заболевания или возможной кишечной непроходимости.
Мобильность. Некоторые пациенты CDKL5 никогда не будут ходить, в то время как другие ходят самостоятельно или с помощью взрослых. Тоже касается и целенаправленных движений рук. Одни дети почти не имеют никаких навыков, в то время как другие выполняют целенаправленные действия.
Контрактуры могут формироваться у детей, которые самостоятельно не двигаются, что легко определяется путем проведения пассивных движений. Для поддержания хорошего диапазона движений этим пациентам должна проводиться физическая и профессиональная терапия на протяжении всей жизни.
Позвоночник (сколиоз / кифоз / лордоз). Вероятность развития сколиоза возрастает с возрастом. Необходимо тщательное наблюдение за изменениями со стороны позвоночника. При выявлении деформации рекомендуется направить такого ребенка к хирургу-ортопеду.
Stimming – это термин, часто используемый при аутизме. Проблемой многих детей с CDKL5 является повторяющееся и ограниченное поведение, которое также встречается при аутизме и синдроме Ретта, например, покачивание головой, хлопки руками, постоянное нахождение предметов и пальцев рук во рту.
Вазомоторные (вегетативные) нарушения. У детей с CDKL5 из-за нарушения вегетативной регуляции наблюдается увеличение симпатического тонуса, симптомами которого являются нарушения сердечного ритма, наличие холодных конечностей.
Cdkl5 что это мутация
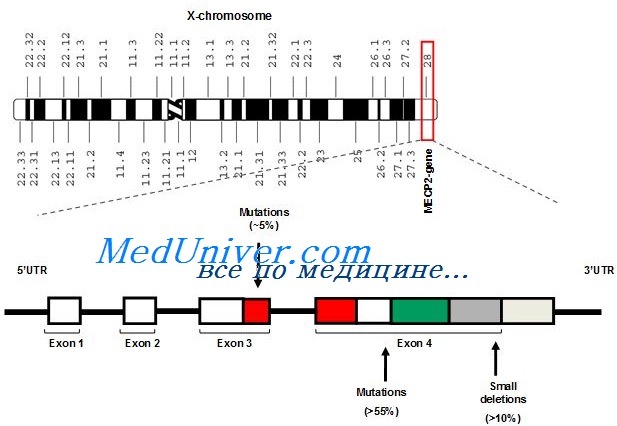
Этиология и встречаемость синдрома Ретта. Синдром Ретта (MIM № 312750) — панэтническое Х-сцепленное доминантное заболевание с распространением среди девочек 1 на 10 000-15 000.
Вызывается мутациями с утратой функции в гене МЕСР2. Описано несколько мальчиков с выраженными нарушениями развития и неврологическими аномалиями с мутациями, вызывающими частичную потерю функции МЕСР2, но обычно у мужчин типичного синдрома Ретта не бывает, кроме случаев кариотипа 47.XXY или соматического мозаицизма.
У нескольких пациентов с атипическим синдромом Ретта найдены мутации в одном, также Х-сцепленном, аллеле гена CDKL5. Белок CDKL5 — киназа треонина и серина, но о его функции мало известно.
Патогенез синдрома Ретта
Мозг у пациентов с синдромом Ретта небольшого размера, с атрофией коры и мозжечка, но без потери нейронов; синдром Ретта, следовательно, не относится к типичным нейродегенеративным заболеваниям. В коре и гиппокампе нейроны пациентов с синдромом Ретта имеют меньшие размеры и более плотно упакованы, чем в норме, и имеют упрощенное ветвление дендритов.
Эти наблюдения указывают, что белок МеСР2 важен для возникновения и поддержки межнейронного взаимодействия, а не для пролиферации предшественников нейронов или их дифференцировки.
Фенотип и развитие синдрома Ретта
Классический синдром Ретта — прогрессирующее неврологическое заболевание, встречаемое почти исключительно у девочек. После периода внешне нормального развития до 6-18-месячного возраста, у больных начинается короткий период замедления и остановки развития с задержкой роста.
Впоследствии они быстро теряют речь и приобретенные двигательные навыки, особенно целенаправленного использования рук. В ходе непрерывного протекания болезни у них развиваются стереотипные движения рук, нерегулярное дыхание, атаксия и судороги.
После краткого периода псевдостабилизации, обычно в дошкольном или ранним школьном возрасте, состояние пациентов вновь ухудшается, появляется выраженная умственная отсталость, прогрессирующая спастичность, ригидность и сколиоз. Больные обычно доживают до взрослого возраста, однако продолжительность жизни уменьшена из-за повышения встречаемости необъяснимой внезапной смерти.
Кроме синдрома Ретта, мутации в гене МЕСР2 вызывают широкий спектр болезней, поражающих как мальчиков, так и девочек. Среди девочек симптоматика колеблется от сильно пораженных пациентов, не способных говорить, поворачиваться, сидеть или ходить, имеющих выраженную эпилепсию, до слабо пораженных пациентов, которые говорят, имеют сохранные двигательные функции, а также сравнительно хорошо сохранившуюся функцию рук.
У мальчиков колебания симптоматики — от внутриутробной гибели, врожденной энцефалопатии до умственной отсталости с различными неврологическими симптомами, или изолированной легкой умственной задержки; классический синдром Ретта описан только у мальчиков с соматическим мозаицизмом по мутации МЕСР2 или с дополнительной Х-хромосомой.
Лечение синдрома Ретта
Заподозренный на основе клинических признаков, диагноз синдрома Ретта обычно подтверждается ДНК-тестированием; тем не менее в настоящее время такое тестирование обнаруживает мутации в гене МЕСР2 только у 80-90% пациентов с типичным синдромом Ретта.
Клинические критерии диагноза для типичного синдрома Ретта включают нормальный пренатальный и перинатальный период, нормальную окружность головы при рождении, сравнительно нормальное развитие до 6-месячного возраста, задержку роста в возрасте между 6 и 48 мес, утрату приобретенных способностей и целенаправленных движений руками к 5-30 мес жизни, и последующее развитие стереотипных движений руками, потерю речевых навыков, выраженную психомоторную отсталость и развитие апраксическои походки и атаксии в возрасте между 12 и 48 мес жизни.
К настоящему времени эффективного лечения синдрома Ретта нет, и помощь сосредоточена на уходе и симптоматическом лечении. Медицинская помощь включает антиконвульсанты при судорогах, прием ингибиторов серотонина, карбидопы или леводопы при ригидности и мелатонина для улучшения сна. Семьи часто нуждаются в социальной поддержке, во взаимодействии с аналогичными семьями через группы взаимопомощи, а в некоторых случаях и в профессиональном консультировании.
Риски наследования синдрома Ретта
Приблизительно 99% случаев синдрома Ретта спорадические; большинство мутаций МЕСР2 возникают вновь, хотя в редких случаях они могут наследоваться от здоровой или мало пораженной матери со смещенной инактивацией Х-хромосомы. По крайней мере, 70% новых мутаций возникают в половых клетках отцов.
Если пара имеет больного ребенка, но мутация в гене МЕСР2 у родителей не выявлена, риск для будущих детей низкий, хотя и выше, чем в общей популяции, из-за возможности необнаруженного полового мозаицизма. Если же мать несет мутацию гена МЕСР2, каждый ребенок, независимо от пола, имеет 50% риск унаследовать мутацию.
Тем не менее недостаточная корреляция между генотипом и фенотипом у пациентов с мутациями в гене МЕСР2 обычно не позволяет давать прогнозы, разовьется ли у женского плода с мутацией МЕСР2 классический синдром Ретта или другая патология. Аналогично, идентификация мутации МЕСР2 у плода мужского пола также не позволяет предсказать внутриутробную гибель, развитие врожденной энцефалопатии или другой патологии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Новости и события
Эпилептические приступы могут быть признаками мутации CDKL5. Мутации в гене CDKL5 (cyclin-dependent kinase-like 5) приводят к редкому генетическому заболеванию. Первые описания клинических случаев были в 2004 году. В 2012 году «расстройство CDKL5» было признано отдельным заболеванием. Такие пациенты требуют многопрофильного подхода к тактике наблюдения и лечения. Подробно нам рассказала старший научный сотрудник НИКИ педиатрии к.м.н. Александра Пивоварова
Мутация в гене CDKL5
Это заболевание вызывается мутациями в гене CDKL5 (циклинзависимая киназа 5) находящимся на Х-хромосоме. Ген CDKL5 обеспечивает инструкции для создания белка, который необходим для нормального развития мозга и нейронов. Хотя относительно мало известно о функции этого белка, он может играть определенную роль в регуляции активности других генов, в том числе гена MECP2 синдрома Ретта. Из-за расположения гена это расстройство в основном затрагивает девочек, но также выявлялось много случаев заболевания у мальчиков.
Изменения в этом гене впервые были выявлены в 2004 году. Но до настоящего времени точной причины мутации в гене CDKL5, и частоты возникновения CDKL5 расстройства не известны.
Тем не менее, за десятилетие, прошедшее с тех пор, как изменения гена CDKL5 впервые были связаны с синдромом Ретта, о расстройстве CDKL5 стало известно намного больше. Несмотря на то, что у людей с мутациями CDKL5 есть определенные общие клинические симптомы с теми, у кого мутации MECP2 вызывают синдром Ретта, на настоящий момент известно, что их следует рассматривать как отдельные расстройства. И в 2012 году «расстройство CDKL5» было признано отдельным заболеванием.
Как распознать расстройство CDKL5
Наиболее характерной особенностью расстройства CDKL5 является раннее начало судорог. Приступы могут начаться в первые часы, дни, недели или месяцы жизни. Дети, у которых диагностировано расстройство CDKL5, могут страдать судорогами, которые начались в течение нескольких часов после рождения или в возрасте от 8 месяцев до 2 лет. Некоторые матери описывают ощущение судорог даже в дородовой период. Судорожные приступы могут быть тоническими с миоклоническими кластерами и тоническими / клоническими Чаще развиваются во сне или могут быть связаны с засыпанием и пробуждением, но в дальнейшем могут появиться и в часы бодрствования.
Обычно эти первые судороги не выявляются на ЭЭГ, и у некоторых детей может быть неправильно диагностирован доброкачественный миоклонус сна или синдром Сандифера. Важно отметить, что отсутствие судорожной активности на ЭЭГ (или “нормальной” ЭЭГ) не обязательно исключает диагноз ”эпилепсия” связанный с CDKL5.
Основные симптомы расстройства CDKL5
— Низкий мышечный тонус
— Отсутствует или ограничена речь
— Ограниченные навыки рук
Как диагностируется расстройство CDKL5
Диагноз основывается на простом анализе крови. В последнее время некоторые лаборатории используют мазок буккального эпителия щек. Затем мазок крови или слюны отправляется в специальную лабораторию, где проводится генетический тест. В последнее время тестирование CDKL5 стало широко доступным в генетических панелях эпилепсии и задержки развития, что позволяет одновременно тестировать несколько потенциальных генов, вызывающих заболевание, что по стоимости, является аналогичным тестированию одного гена CDKL5.
Люди с расстройством CDKL5 требуют многопрофильного подхода к тактике наблюдения и лечения. Основной целью является улучшение качества жизни пациентов и их семей. Главным приоритетом является обеспечение пациентов и их семей своевременной и точной информацией и поддержкой в процессе принятия решений. Список специалистов, необходимых в команде наблюдения за пациентами:
На сегодняшний день существуют следующие подходы к лечению:
Противоэпилептические препараты/медикаменты (AEDs)
Судороги при расстройстве CDKL5 трудно поддаются лечению. Важно отметить, что некоторые семьи очень успешно живут на монотерапии с низкой дозировкой; однако, некоторые используют вспомогательную терапию. Часто ребенок проходит через несколько антиэпилептических препаратов или их комбинации.
Кетогенная диета
Кетогенная диета так же оказалась очень успешной для отдельных пациентов, отмечалось повышение осознанности и внимания, а также о снижение частоты судорожных приступов Кетогенная диета является подходящим вариантом для перорального кормления, а также назо-желудочной трубки или G-трубки.
Установка стимулятора блуждающего нерва (VNS)
Нейрохирургическое лечение
Так же есть варианты нейрохирургического лечения, помогающие контролировать судорожные приступы, когда другие методы лечения не работают.
Гормональная терапия
Гормональная терапия так же показала некоторую эффективность у пациентов с инфантильными спазамим. Имеются данные о том, что некоторые пациенты с модифицированной гипсаритмией или безсудорожным эпилептическим статусом давали положительную динамику на фоне применения гормональной терапии.
Также необходимо использовать такие реабилитационные методы как:
Иппотерапия – улучшает силу и контроль над телом, равновесие, моторное планирование и создани общей постуральной силы и выносливости. Этот вид терапии может включать использование механической лошади.
Гидротерапия (водолечение) – позволяет улучшить осанку, улучшить мобильность суставов. Сопротивление воды во время упражнений позволяет обеспечить безопасную среу для решения проблем с равновесием, силы и постурального дефицита.
Трудотерапия – позволяет улучшать мелкую моторику, обеспечивает участие в большом колическтве мероприятий изо дня в день. Трудотерапевт может подсказать идеи для изменения окружающих вещей для удовлетворения потребностей ребенка (например модифицированные чашки для питья, посудп, головоломки, игрушки и т.д.)
Физиотерапия – поможет поддерживать, восстанавливать и улучшать движение, активность и здоровье пациентов. Важна для предотвращения развития сколиоза и деформаций суставов, развития или поддержания переходных навыков, улучшения двигательной способности, стимуляции использования рук, улучшение осознания тела, уменьшения мышечной боли.
• отслеживание глаз и объединение глаз
• способность фокусировки глаз
На сегодняшний день одним из самых эффективных методов коррекции аутизма является поведенческая терапия или метод прикладного анализа поведения ABA (Applied behavior analysis).
генетическая эпилепсия, вызванная мутациями в гене CDKL5, как пример эпилептической энцефалопатии и энцефалопатии развития: обзор литературы и собственные наблюдения
Полный текст:
Аннотация
Заболевание, вызванное мутациями в гене CDKL5 (циклинзависимая киназа 5-го типа (cyclin-dependent kinase 5, CDK5), относится к группе ранних (младенческих) эпилептических энцефалопатий, обусловленных генетическими причинами. В настоящее время заболевание носит название «энцефалопатия развития и эпилептическая энцефалопатия 2-го типа». Данное заболевание представляет собой сложный симптомокомплекс, который формируется при дефиците или полном отсутствии в организме продукта гена CDKL5 (фермента серин-треонин киназы). ген CDKL5 локализован на Х-хромосоме, заболевание имеет Х-сцепленный доминантный тип наследования. Авторы представляют обзор современной литературы, посвященный заболеванию, вызванному мутацией в гене CDKL5 (включая генетические и эпидемиологические аспекты, клинические проявления, особенности течения эпилепсии, принципы диагностики, терапевтические подходы), а также описание собственных наблюдений пациентов с генетическими нарушениями с участием гена CDKL5.
Ключевые слова
Об авторах
Константин Юрьевич Мухин
108841 Москва, Троицк, ул. Нагорная, 5
119579 Москва, ул. Акад. Анохина, 9
Ольга Анатольевна Пылаева
108841 Москва, Троицк, ул. Нагорная, 5
119579 Москва, ул. Акад. Анохина, 9
108841 Москва, Троицк, ул. Нагорная, 5
119579 Москва, ул. Акад. Анохина, 9
119579 Москва, ул. Акад. Анохина, 9
Список литературы
1. Белоусова Е.Д. Эпилептическая энцефалопатия с продолженной спайк-волновой активностью во сне. Русский журнал детской неврологии 2012;7(1):3–8. [Belousova E.D. Epileptic encephalopathy with continuous spikeswaves activity during sleep. Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2012;7(1):31–8. (In Russ.)].
2. Белоусова Е.Д., Шарков А.А. Трудности в диагностике, прогнозе и лечении генетических эпилептических энцефалопатий: взгляд невролога. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски 2019;119(11–2): 34–40. [Belousova E.D., Sharkov A.A. Difficulties in the diagnosis, prognosis, and treatment of genetic epileptic encephalopathies: a neurologist’s view. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. Special issues 2019;119(11–2):34–40. (In Russ.)]. DOI: 10.17116/jnevro201911911234.
3. Дадали Е.Л., Акимова И.А., Коновалов Ф.А. и др. Клинико-генетические особенности пациентов с ранней эпилептической энцефалопатией 2-го типа, обусловленной мутациями в гене CDKL5. Русский журнал детской неврологии 2019;14(3):28–36. [Dadali E.L., Akimova I.A., Konovalov F.A. et al. Clinical and genetic characteristics of patients with type 2 early infantile epileptic encephalopathy caused by CDKL5 gene mutations. Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2019;14(3): 28–36. (In Russ.)]. DOI: 10.17650/2073-8803-2019-14-3-28-36.
4. Зенков Л.Р. Бессудорожные эпилептические энцефалопатии с психиатрическими, коммуникативными и поведенческими расстройствами. Вестник эпилептологии 2004;(2):7–11. [Zenkov L.R. Nonconvulsive epileptic encephalopathies with mental, communicative, and behavioral disorders. Vestnik epileptologii = Bulletin of Epileptology 2004;1(2):7–11. (In Russ.)].
5. Зенков Л.Р. Непароксизмальные эпилептические расстройства. М.: МЕДпресс-информ, 2007. 278 с. [Zenkov L.R. Non-paroxysmal epileptic disorders. Moscow: Medpress-Inform, 2007. Pp. 106–115. (In Russ.)].
6. Карлов В.А. Эпилепсия у детей и взрослых женщин и мужчин. М.: Медицина, 2010. 720 с. [Karlov V.A. Epilepsy in children and adult men and women. Moscow: Meditsina, 2010. 720 p. (In Russ.)].
7. Мухин К.Ю. Когнитивная эпилептиформная дезинтеграция: дефиниция, диагностика, терапия. Русский журнал детской неврологии 2012;7(1):3–20. [Mukhin K.Yu. Cognitive epileptiform disintegration: definition, diagnosis, therapy. Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2012;7(1):3–20. (In Russ.)]. DOI: 10.17650/2073-8803-2012-7-1-3-20.
8. Мухин К.Ю. Определение и классификация эпилепсии. Проект Классификации эпилептических приступов 2016 года. Русский журнал детской неврологии 2017;12(1):8–20. [Mukhin K.Yu. Definition and classification of epilepsy. Classification of epileptic seizures 2016. Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2017; 12(1):8–20. (In Russ.)]. DOI: 10.17650/2073-8803-2017-12-1-08-20.
9. Мухин К.Ю., Глухова Л.Ю., Макиевская Е.Р. Эпилепсия с электрическим эпилептическим статусом в фазу медленного сна с фокусом на электроэнцефалографические критерии. Русский журнал детской неврологии 2017;12(1):21–35. [Mukhin K.Yu., Glukhova L.Yu., Makievskaya E.R. Epilepsy with electrical status epilepticus during slow-wave sleep with a focus on electroencephalographic criteria. Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2017;12(1): 21–35. (In Russ.)]. DOI: 10.17650/2073-8803-2017-12-1-21-35.
10. Мухин К.Ю., Пылаева О.А. Формирование когнитивных и психических нарушений при эпилепсии: роль различных факторов, связанных с заболеванием и лечением (обзор литературы и описания клинических случаев). Русский журнал детской неврологии 2017;12(3):7–33. [Mukhin K.Yu., Pylaeva O.A. The formation of cognitive and mental disorders in epilepsy: the role of various factors associated with disease and treatment (a review of literature and case reports). Russkiy zhurnal detskoy nevrologii = Russian Journal of Child Neurology 2017;12(3):7–33. (In Russ.)]. DOI: 10.17650/2073-8803-2017-12-3-7-33.
11. Amin S., Majumdar A., Mallick A.A. Caregiver’s perception of epilepsy treatment, quality of life and comorbidities in an international cohort of CDKL5 patients. Hippokratia 2017;21:130–5.
12. Baba S., Sugawara Y., Moriyama K. Amelioration of intractable epilepsy by adjunct vagus nerve stimulation therapy in a girl with a CDKL5 mutation. Brain Dev 2017;39:341–4. DOI: 10.1016/j.braindev.2016.10.007.
13. Bahi-Buisson N., Bienvenu T. CDKL5- related disorders: From clinical description to molecular genetics. Mol Syndromol 2011;2:137–52. DOI: 10.1159/000331333.
14. Bahi-Buisson N., Kaminska A., Boddaert N. et al. The three stages of epilepsy in patients with CDKL5 mutations. Epilepsia 2008;49(6):1027–37.
15. Bahi-Buisson N., Nectoux J., RosasVargas R. et al. Key clinical features to identify girls with CDKL5 mutations. Brain 2008;131:2647–61. DOI: 10.1093/brain/awn197.
16. Barbiero I., Peroni D., Siniscalchi P. et al. Pregnenolone and pregnenolone-methylether rescue neuronal defects caused by dysfunctional CLIP170 in a neuronal model of CDKL5 Deficiency Disorder. Neuropharmacology 2019;164:107897. DOI: 10.1016/j.neuropharm.2019.107897.
17. Barbiero I., Peroni D., Tramarin M. et al. The neurosteroid pregnenolone reverts microtubule derangement induced by the loss of a functional CDKL5- IQGAP1 complex. Hum Mol Genet 2017;26:3520–30. DOI: 10.1093/hmg/ddx237.
18. Berg A.T., Berkovic S.F., Brodie M.J. et al. Revised terminology and concepts for organization of seizures and epilepsies: report of the ILAE Commission on Classification and Terminology, 2005– 2009. Epilepsia 2010;51:676–85.
19. Biagini G., Panuccio G., Avoli M. Neurosteroids and epilepsy. Curr Opin Neurol 2010;23(2):170–6. DOI: 10.1097/WCO.0b013e32833735cf.
20. Della Sala G., Putignano E., Chelini G. et al. Dendritic spine instability in a mouse model of CDKL5 disorder is rescued by insulin-like growth factor 1. Biol Psychiatry 2016;80:302–11. DOI: 10.1016/j.biopsych.2015.08.028.
21. Devinsky O., Verducci C., Thiele E.A. Open-label use of highly purified CBD (Epidiolex®) in patients with CDKL5 deficiency disorder and Aicardi, Dup15q, and Doose syndromes. Epilepsy Behav 2018;86:131–1. DOI: 10.1016/j.yebeh.2018.05.013.
22. Fehr S., Leonard H., Ho G. et al. There is variability in the attainment of developmental milestones in the CDKL5 disorder. J Neurodev Dis 2015;7:2. DOI: 10.1186/1866-1955-7-2.
23. Fehr S., Wong K., Chin R. Seizure variables and their relationship to genotype and functional abilities in the CDKL5 disorder. Neurology 2016;87:2206–13. DOI: 10.1212/WNL.0000000000003352.
24. Fehr S., Wilson M., Downs J. et al. The CDKL5 disorder is an independent clinical entity associated with early-onset encephalopathy. Eur J Hum Genet 2013;21(3):266–73. DOI: 10.1038/ejhg.2012.156.
25. Frullanti E., Papa F., Grillo E. et al. Analysis of the phenotypes in the Rett Networked Database. Int J Genom 2019;2019:6956934. DOI: 10.1155/2019/6956934.
26. Hanefeld F. The clinical pattern of the Rett syndrome. Brain Dev 1985;7:320–5. DOI: 10.1016/S0387-7604(85)80037-1.
27. Jakimiec M., Paprocka J., Smigiel R. CDKL5 deficiency disorder – a complex epileptic encephalopathy. Brain Sci 2020;10(2):107. DOI: 10.3390/brainsci10020107.
28. Kalscheuer V.M., Tao J., Donnelly A. Disruption of the serine/threonine kinase 9 gene causes severe X-linked infantile spasms and mental retardation. Am J Hum Genet 2003;72:1401–11. DOI: 10.1086/375538.
29. Khan S., Baradie R.A. Epileptic encephalopathies: A overview. Epilepsy Res Treat 2012;2012:403592. DOI: 10.1155/2012/403592.
30. Ko A., Jung D.E., Kim S.H. et al. Efficacy of ketogenic diet for specific genetic mutation in developmental and epileptic encephalopathy. Front Neurol 2018;9: 530–9. DOI: 10.3389/fneur.2018.0053.
31. Krishnaraj R., Ho G., Christodoulou J. RettBASE: Rett syndrome database update. Hum Mutat 2017;38:922–31. DOI: 10.1002/humu.23263.
32. Lim Z., Wong K., Downs J. et al. Vagus nerve stimulation for the treatment of refractory epilepsy in the CDKL5 Deficiency Disorder. Epilepsy Res 2018;146:36–40. DOI: 10.1016/j.eplepsyres.2018.07.013.
33. Lim Z., Wong K., Olson H.E. et al. Use of the ketogenic diet to manage refractory epilepsy in CDKL5 disorder: Experience of >100 patients. Epilepsia 2017;58:1415–22. DOI: 10.1111/epi.13813.
34. Mangatt M., Wong K., Anderson B. et al. Prevalence and onset of comorbidities in the CDKL5 disorder differ from Rett syndrome. Orphanet J Rare Dis 2016;11:39. DOI: 10.1186/s13023-016-0418-y.
35. Mei D., Darra F., Barba C. et al. Optimizing the molecular diagnosis of CDKL5 gene-related epileptic encephalopathy in boys. Epilepsia 2014; 55:1748–53. DOI: 10.1111/epi.12803.
36. Muller A., Helbig I., Jansen C. Retrospective evaluation of low long-term efficacy of antiepileptic drugs and ketogenic diet in 39 patients with CDKL5-related epilepsy. Eur J Paediatr Neurol 2016; 20:147–51. DOI: 10.1016/j.ejpn.2015.09.001.
37. Nabbout R., Dulac O. Epileptic encephalopathies: a brief overview. J Clin Neurophysiol 2003;20(6):393–7.
38. Olson H.E., Demarest S.T., PestanaKnight E.M. et al. Cyclin-dependent kinase-like 5 (CDKL5) deficiency disorder: Clinical review. Pediatr Neurol 2019;97:18–25. DOI: 10.1016/j.pediatrneurol.2019.02.015.
39. OMIM: Online Mendelian Inheritance in Man, an online catalog of human genes and genetic disorders. Available at: https://omim.org.
40. Russo S., Marchi M., Cogliati F. et al. Novel mutations in the CDKL5 gene, predicted effects and associated phenotypes. Neurogenetics 2009;10:241–50. DOI: 10.1007/s10048-009-0177-1.
41. Scala E., Ariani F., Mari F. CDKL5/STK9 is mutated in Rett syndrome variant with infantile spasms. J Med Genet 2005;42:103–7. DOI: 10.1136/jmg.2004.026237.
42. Scheffer I.E., Berkovic S., Capovilla G. et al. ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology. Epilepsia 2017;58(4):512–21.
43. Stosser M.B., Lindy A.S., Butler E. High frequency of mosaic pathogenic variants in genes causing epilepsy-related neurodevelopmental disorders. Genet Med 2018;20:403–10. DOI: 10.1038/gim.2017.114.
44. Swaiman K.F., Ashwal S., Ferriero D.M. et al. Swaiman’s Pediatric Neurology. Principles and Practice. 6th edn. Elsevier, 2017. 2969 p.
45. Tang S., Terzic B., Wang I.J. et al. Altered NMDAR signaling underlies autistic-like features in mouse models of CDKL5 deficiency disorder. Nat Commun 2019;10:2655. DOI: 10.1038/s41467-019-10689-w.
46. Tramarin M., Rusconi L., Pizzamiglio L. et al. The antidepressant tianeptine reverts synaptic AMPA receptor defects caused by deficiency of CDKL5. Hum Mol Genet 2018;27:2052–63. DOI: 10.1093/hmg/ddy108.
47. Weaving L.S., Christodoulou J., Williamson S.L. Mutations of CDKL5 cause a severe neurodevelopmental disorder with infantile spasms and mental retardation. Am J Hum Genet 2004;75: 1079–93. DOI: 10.1086/426462.
48. Wong V.C.-N., Kwong A.K.-Y. CDKL5 variant in a boy with Infantile Epileptic Encephalopathy: Case report. Brain Dev 2014;37:446–8. DOI: 10.1016/j.braindev.2014.07.003.
49. Zhao Y., Zhang X., Bao X. et al. Clinical features and gene mutational spectrum of CDKL5-related diseases in a cohort of Chinese patients. BMC Med Genet 2014;15:24. DOI: 10.1186/1471-2350-15-24.
Для цитирования:
Мухин К.Ю., Пылаева О.А., Бобылова М.Ю., Чадаев В.А. генетическая эпилепсия, вызванная мутациями в гене CDKL5, как пример эпилептической энцефалопатии и энцефалопатии развития: обзор литературы и собственные наблюдения. Русский журнал детской неврологии. 2021;16(1-2):10-41. https://doi.org/10.17650/2073-8803-2021-16-1-2-10-41
For citation:
Mukhin K.Yu., Pylaeva O.A., Bobylova M.Yu., Chadaev V.A. Genetic epilepsy caused by CDKL5 gene mutations as an example of epileptic encephalopathy and developmental encephalopathy: literature review and own observations. Russian Journal of Child Neurology. 2021;16(1-2):10-41. (In Russ.) https://doi.org/10.17650/2073-8803-2021-16-1-2-10-41