Ученые доказали, что носителем наследственной информации является ДНК
4 февраля 1944 года в США увидел свет номер «The Journal of Experimental Medicine» со статьей об одном из важнейших открытий в биологии. Освальд Эйвери (1877–1955) и его сотрудники Колин Маклауд и Маклин Маккарти в исследованиях, проведенных в лаборатории Рокфеллеровского медицинского института (Нью-Йорк), неопровержимо доказали, что носителем наследственной информации, «материалом» генов, является дезоксирибонуклеиновая кислота (ДНК).
ДНК была открыта Иоганном Фридрихом Мишером в 1869 году. Биологическая функция новооткрытого вещества была неясна, и долгое время ДНК считалась запасником фосфора в организме. Более того, даже в начале 20 века многие биологи считали, что ДНК не имеет никакого отношения к передаче информации, поскольку строение молекулы, по их мнению, было слишком однообразным и не могло содержать закодированную информацию.
Постепенно было доказано, что именно ДНК, а не белки, как считалось раньше, является носителем генетической информации. Одно из первых решающих доказательств принесли эксперименты О.Эйвери, К.Маклауда и М.Маккарти по трансформации бактерий (1944). Им удалось показать, что за так называемую трансформацию (приобретение болезнетворных свойств безвредной культурой в результате добавления в неё мёртвых болезнетворных бактерий) отвечают выделенные из пневмококков ДНК.
Вплоть до 1950-х годов точное строение ДНК, как и способ передачи наследственной информации, оставалось неизвестным. Хотя и было доподлинно известно, что ДНК состоит из нескольких цепочек, состоящих из нуклеотидов, никто не знал точно, сколько этих цепочек, и как они соединены.
Структура двойной спирали ДНК была предложена Френсисом Криком и Джеймсом Уотсоном в 1953 году на основании рентгеноструктурных данных, полученных Морисом Уилкинсом и Розалинд Франклин, и «правил Чаргаффа», согласно которым в каждой молекуле ДНК соблюдаются строгие соотношения, связывающие между собой количество азотистых оснований разных типов.
Позже предложенная Уотсоном и Криком модель строения ДНК была доказана, а их работа отмечена Нобелевской премией по физиологии и медицине 1962 года.
Прямые доказательства генетической роли ДНК: особенности, описание и интересные факты
В современном научном сообществе существует несколько теорий по поводу способа передачи информации от родителей потомкам: от волновых до футуристических типа сверхразума коллективов. Однако то, что именно молекулы ДНК являются материальной основой преемственности организмов, споров не вызывает. Понять, как в научной среде формировались доказательства генетической роли ДНК и что они собой представляют, – вот цель данной статьи.
Немного теории для не биологов
Для понимания предмета и самой сути доказательства роли ДНК в наследственности напомним лишь некоторые общие понятия и термины, применяемые в тексте. Молекулярные биологи и другие профессиональные биологи могут эту часть не читать – понятия даются в упрощенном варианте для интересующейся части читателей. Хотя современная специализация в биологии сегодня настолько возросла, что профессионал-эколог не всегда прорвется к пониманию сути эволюционных механизмов, а ботанику совсем не однозначно понятна специфика развития эмбриона лягушки. Итак, вот эти термины:
Немного истории
Швейцарский биолог Ф. Мишер в 1869 году увидел в ядрах клеток гноя (лейкоцитах) цепочки, которые назвал нуклеиновыми кислотами.
Немец А. Кассель как биохимик вычислил их состав: сахар, фосфорная кислота и пять разновидностей азотистых оснований. Он же в 1891 году доказал, что нуклеиновых кислот две – ДНК и РНК. В период от этих открытий до 1953 года велись исследования химического состава и структурной организации нуклеиновых кислот. Известные фамилии этого периода – Ф. Левен, А. Тодд, Э. Чаргафф. Опыты, начатые Ф. Гриффитом (1928) и продолженные О. Эвери, К. МакЛеодом и М. МакКарти (1944), представили доказательства роли ДНК в передаче генетической информации, о чем подробнее позже. В 1953 году американцы Дж. Уотсон и Ф.Крик предложили известную даже школьнику модель структуры ДНК в виде двойной закрученной спирали. Все, молекулярная биология родилась!
От белка к ДНК
На тот момент времени нуклеиновые кислоты представлялись странным материалом в ядре клетки. Для чего нужны эти образования, не знали, и тем более не искали доказательства генетической роли нуклеиновых кислот. Уже были открыты белки, состоящие из аминокислот и имеющие более сложную химическую структуру. Именно белки считали носителями наследственной информации.
В материале, который несет наследственную информацию, первым усомнился английский бактериолог Ф. Гриффит в 1928 году. И хотя он не смог представить убедительных доказательств генетической роли ДНК, его опыты заслуживают внимания.
Штаммы пневмококков Гриффита
Экспериментальные доказательства роли ДНК в передаче информации
Практически то же самое, что проделал Гриффит, только без бедных мышей, сделали в 1944 году О. Т. Эвери, К. М. МакЛеод и М. МакКарти. В Рокфеллеровском институте медицинских исследований в Нью-Йорке они получили in vitro (в пробирке) чистый трансформирующий агент Гриффита из убитых вирулентных форм и смешивали его, опять же в пробирке, с авирулентными формами. Получали капсулированных возбудителей. А потом изучали состав этого самого агента. Вначале они доказали, что это не белок, и это само по себе уже было новаторством. Ну а потом и пришли к тому, что этот агент и есть нуклеиновая кислота. Эти опыты американцев – прямые доказательства генетической роли ДНК в передаче наследственной информации. Но не единственные, которые наука считает классикой.
Второе из классических доказательств генетической роли ДНК
Классика биологии – еще два опыта как прямые доказательства генетической роли ДНК. Описание сократим до сути.
Американский генетик Альфред Херши получил Нобелевскую премию (1969) за эти опыты. Интересна и серия опытов Херши и Марты Чейз, проведенная в 1952 году в Университете Вашингтона в Сент-Луисе с бактериями и бактериофагами, меченными радиоактивным фосфором и серой. Их выводы о том, что именно ДНК бактериофага проникает в бактерии и дает начало новым бактериофагам, – классика доказательства генетической роли ДНК.
Третий опыт
Интересные современные доказательства
Современная молекулярная биология и генетика постоянно поставляют нам новые доказательства генетической роли ДНК. Несколько весьма занимательных, неожиданных и впечатляющих фактов из исследований современной науки, которые так или иначе доказывают роль ДНК в формировании организма, приведено далее.
В 2007 году ученые сумели выделить участок ДНК амфибий, который отвечает за формирование глаза. Сегодня уже есть саламандры с глазами на лапах и хвосте.
В геном коз ученые вживили ген паука, отвечающий за белок паутины, в результате этот белок появился в молоке коз. После специальной обработки и извлечения белка из молока образуется паучий шелк.
Голландцы вырастили коров с человеческим геном, отвечающим за специфический белок молока женщин – лактоферрин. Этот белок играет важную роль в первичном иммунитете младенцев. Тестирование молока коров продолжается, но перспективы применения его в медицине впечатляют.
Дополнив ген эмбриона поросят геном белка флуоресцентной медузы, китайские ученые вырастили двух светящихся зеленым цветом поросят.
В 2008 году мир облетело известие о рождении ребенка с искусственно измененным геномом. Произошло это в Лондоне, где женщина согласилась на эксперимент из-за обнаруженных генетических нарушений в геноме эмбриона.
Человеческие химеры существуют. В 2002 году при анализе ДНК на отцовство тест показал, что американка Лидия Фэйрчайлд не является матерью своего еще не рожденного ребенка. Исследования повторили, но анализ показал те же результаты. Оказалось, что организм Лидии развился из двух яйцеклеток, оплодотворенных разными сперматозоидами и слившихся на ранних стадиях онтогенеза. Поэтому ее тело состоит из тканей и клеток с разным набором хромосом.
О ДНК-тестировании на установление отцовства или в судебной практике знают все. Но ДНК-тесты используют и при проверке продуктов на подлинность. Например, можно установить место сбора икры или винограда для марочного вина.
В мире известно 4 семьи, члены которых не имеют отпечатков пальцев. Адерматоглифия вызвана редкой мутацией одного-единственного гена.
Чередование сна и бодрствования у человека контролирует ген hDEC2, его мутация сокращает необходимость сна до 4 часов.
Криогенетика достигла успеха в клонировании мыши, пробывшей замороженной 16 лет. Оживлять «полярников» ученые не научились, а вот клонировать их можно.
И немного о самой уникальной молекуле
Подведем итог
Несмотря на успехи молекулярной биологии и наши познания о ДНК, на многие вопросы человечество пока не знает ответов. Кто знает, какие открытия ждут нас в будущем, избавится ли человечество от наследственных болезней и будет ли побеждено старение.
История доказательства, что ДНК – носитель генетической информации
3.1. История доказательства, что ДНК – носитель генетической информации.
Явление это было открыто в опытах с пневмококками, то есть с бактериями, вызывающими воспаление легких. Известны две формы
пневмококков: А-форма с полисахаридной капсулой и Б-форма без капсулы. Оба эти признака наследственны.
Пневмококки А-формы при заражении ими мышей вызывают воспаление легких, от которого мыши погибают. Б-форма для них безвредна.
В 1928 году английский бактериолог Ф.Гриффитс заражал мышей смесью, состоящей из убитых нагреванием пневмококков А-формы и живых пневмококков Б-формы. Ученый предполагал, что мыши не заболеют. Но вопреки ожиданиям подопытные животные погибли. Ф. Гриффитсу удалось выделить из тканей погибших мышей пневмококки. Все они оказались капсулированными, то есть А-формы. Следовательно, убитая форма каким-то образом передавала свои свойства живым клеткам Б-формы. Но как? С помощью какого именно вещества: полисахарида, из которого состоит капсула, белка или ДНК?
От решения этого вопроса зависело многое, так как, установив вещество, передающее наследственный признак – образование капсулы, можно было получить нужный ответ. Однако сделать это не удавалось довольно долго. Лишь спустя 16 лет после опытов Ф. Гриффитса, в 1944 году, американский ученый А. Эвери с сотрудниками, поставив ряд четких экспериментов, сумел с полным обоснованием доказать, что полисахарид и белок не имеют никакого отношения к передаче наследственных свойств пневмококка А-формы.
В процессе этих экспериментов с помощью специального фермента растворили полисахаридную капсулу убитых пневмококков А-формы и проверили, продолжают ли остатки клетки формы А передавать наследственную информацию клеткам формы Б. Оказалось, что продолжают. Стало ясно, что полисахарид как источник генетической информации отпадает.
Далее ученые при помощи других ферментов удалили из остатков пневмококков А белки и снова проверили их действие. Передача наследственной информации от А к Б продолжалась. Следовательно, и белок ни при чем.
Таким образом, методом исключения было установлено, что наследственную информацию в клетке хранит и передает молекула ДНК. И действительно, когда разрушили ДНК, образование капсульных форм А из бескапсульных Б прекратилась.
Явление преобразования, то есть наследственного изменения свойств одной формы бактерий под воздействием веществ другой формы, было названо трансформацией. Вещество же, вызывающее трансформацию, получило название трансформирующего агента. Им, как было установлено, служит ДНК.
3.2. Расшифровка генетической информации.
Полимерные цепи белков состоят из мономерных звеньев – аминокислот и последовательность расположения их в белковой молекуле строго специфична. В связи с этим очевидно, Что в ДНК должна храниться информация не только о качественном и количественном составе аминокислот в молекуле данного белка, но и о последовательности их расположения. Соответственно каким-то образом должны быть закодированы в полинуклеотидной цепи ДНК каждая аминокислота и белок в целом.
Зная, что аминокислот всего 20, а нуклеотидов – 4, легко представить себе, что 4 нуклеотидов явно недостаточно для кодирования 20 аминокислот. Недостаточно также и кода из двух нуклеотидов на каждую кислоту (4 = 16). Для кодирования 20 аминокислот необходимы группы по меньшей мере из трех нуклеотидов (4 = 64). Подобная группа, несущая информацию об одной аминокислоте в молекуле белка, называется кодоном. Весь же участок ДНК, ответственный за синтез одной молекулы белка, в целом как раз и есть ген. Значит, в гене столько кодонов, сколько аминокислот входит в состав данного синтезируемого белка.
Синтез белков происходит на рибосомах. ДНК же локализована в ядре, в его хромосомах. Возникает вопрос: каким образом генетическая информация из ядра переносится в цитоплазму на рибосому? Предположить, что ДНК сама поступает через поры ядерной мембраны, нельзя: Ведь ДНК ядер обладает огромной молекулярной массой и в связи с этим просто не может проникнуть через крошечные поры ядерной мембраны. Поэтому должны быть какие-то более мелкие молекулы – посредники, передающие генетическую информацию от ДНК к белкам. А.Н. Белозерский и А.Г. Спирин выдвинули соображение, что эту роль играют молекулы РНК.
Но сразу же возникает другой вопрос: как копируется информация с ДНК на более короткие молекулы РНК? Чтобы ответить на него, надо вспомнить, что в строении нуклеотида ДНК и РНК много общего. В частности, из-за сходства азотистых оснований информация с ДНК на РНК может переноситься по принципу комплиментарности, согласно которому образовывать пары могут не только нуклеотиды в системе ДНК-ДНК, но и нуклеотиды в системе ДНК-РНК.
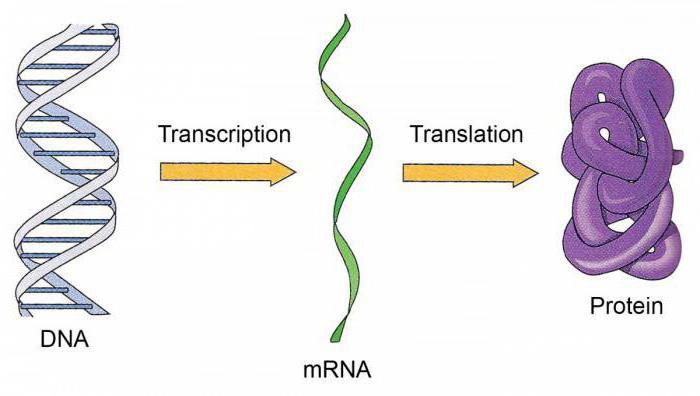
Поскольку РНК так же, как и ДНК, содержит пуриновые и пиримидиновые основания, на участках одной их цепей ДНК при помощи фермента РНК – полимеразы строятся комплиментарные короткие цепи РНК. Этот процесс синтеза РНК на матрице ДНК, происходящий с помощью ферментов, носит название транскрипции. В результате процесса транскрипции закодированная в ДНК последовательность нуклеотидов, которая и представляет собой определенную генетическую информацию, передается на РНК. Транскрипция происходит на отдельных участках ДНК – генах, каждый из которых содержит набор кодонов, программирующих последовательности аминокислот в данной молекуле белка.
Таким образом, в каждом кодоне ДНК транскрибируется в комплиментарный кодон РНК. В результате получается как бы негатив РНК с позитива – ДНК. Эта РНК, снимающая информацию с ДНК, называется информационной РНК (и-РНК).
К настоящему времени ученым удалось расшифровать кодоны для всех аминокислот. Оказалось, что одной аминокислоте зачастую соответствует несколько кодонов. Такой код называется вырожденным. Наряду с этим обнаружилось, что некоторые кодоны не кодируют ни одну аминокислоту. Их называют бессмысленными. Бессмысленные кодоны имеют очень важное значение, так как определяют границы начала и конца транскрипции, то есть границы генов в данной молекуле ДНК.
Если у прокариот гены по своей записи непрерывны, то у эукариот это далеко не так. Информация необходимая для синтеза белка, оказывается записанной с пропусками, прерывисто: гены составлены из кодирующих участков (экзонов), разделенных некодирующими последовательностями (интронами). При транскрипции таких генов интроны копируются вместе с экзонами в общую молекулу пре-мРНК. Последняя подвергается в ядре серии реакций, в ходе которых интроны вырезаются, а экзоны соединяются друг с другом своими краями. Получившаяся молекула м-РНК покидает ядро и оказывается уже во власти системы трансляции, дешифрующей нуклеотидную последовательность. Соединение аминокислот с образованием белка происходит в цитоплазме на особых частицах-рибосомах. Все это можно сравнить с фабрикой (клетка), в которой чертежи (гены) хранятся в библиотеке (ядро), а для выпуска продукции (белки) используются не сами чертежи (ДНК), а их фотокопия (мРНК). Копировальная машина (РНК-полимераза) выпускает или по одной страничке фотокопии (ген), или сразу целую главу (оперон). Изготовленные копии выдаются через специальные окошки (поры ядерной мембраны). Их затем используют на монтажных линиях (рибосомы) с дешифратором (генетический код) для получения из заготовок (аминокислот) окончательной продукции (белки).
Как же происходит сам процесс синтеза белка?
Первый его этап связан с функционированием транспортной РНК (т-РНК). Число разновидностей этих молекул РНК равно числу основных аминокислот, то есть их 20 видов. Каждой аминокислоте соответствует определенная т-РНК и определенный фермент.
В цитоплазме клетки всегда в достаточном количестве имеются разные аминокислоты. Из них молекула т-РНК отбирает соответствующую аминокислоту. Каждая аминокислота, прежде чем вступить в белковую цепь, с помощью специального фермента соединяется с АТФ и запасается энергией. «Подзарядившись» таким образом аминокислота связывается с т-РНК, которая переносит ее к рибосомам. Характерной чертой молекул т-РНК является наличие в их структурах антикодонов. Эта особенность обеспечивается расположением соответствующих аминокислот в той последовательности кодонов, которая зашифрована в молекуле и-РНК. Между рядом расположенными аминокислотами возникают пептидные связи и синтезируется молекула белка.
Таким образом, генетическая информация, заключенная в ДНК, реализуется разными видами РНК в молекулах соответствующих белков.
Процесс передачи программы, принесенной с собою молекулами и-РНК, получил название трансляции.
4. КАК ЖЕ РАБОТАЮТ ГЕНЫ?
При изучении вегетативно размножающихся растений получены доказательства того, что отдельные части организма, такие как клубень, лист, луковица, черенок и так далее, дают начало нормальному растению. А это значит, что все клетки данного организма несут полную генетическую информацию, так же как и исходная оплодотворенная яйцеклетка, из которой развивается животное. Вместе с тем в любом организме содержатся дифференцированные клетки с определенной формой и функцией. Например, у человека есть клетки нервные, мышечные, половые и т.д. Но, несмотря на то, что каждая клетка нашего тела несет полную генетическую информацию, то есть полный набор генов, полученных от родителей, функционируют лишь определенные гены, остальные находятся в неактивном состоянии. Каким же образом в клетке регулируется деятельность тех или иных генов?
Во всех процессах жизнедеятельности клетки роль биологических катализаторов играют ферменты. Без их участия не протекает практически ни одна химическая реакция синтеза или распада веществ. В каждой клетке (с ее характерными функциями) должны находиться регуляторные механизмы, контролирующие не только качественный состав ферментов, но и их количество. В противном случае беспрерывно синтезируемые макромолекулы белков накапливались бы в клетке ненужным балластом, загромождая ее.
И действительно, подобный регуляторный механизм был обнаружен в клетках бактерий в 1961 году французскими учеными Франсуа Жакобом и Жаком Моно.
Что же это за механизм?
Ф. Жакоб и Ж. Моно доказали, что не все гены бактерий одинаковы по своему назначению. Одна группа – структурные гены, выдающие информацию о синтезе определенных полипептидных цепей, другая – регуляторные гены, ведающие активностью структурных генов путем их «включения» и «выключения».
Регуляторные гены представлены геном-оператором, непосредственно сцепленным с группой структурных генов, и геном-регулятором, который может находиться в некотором отдалении от них.
Ген-оператор с группой регулируемых им структурных генов был назван опероном. Оперон служит единицей транскрипции, то есть с него списывается одна молекула и-РНК.
Ген регулятор действует не путем непосредственного контакта со структурными генами, а при помощи белка репрессора.
При наличии достаточно накопившихся молекул синтезируемого вещества белок-репрессор, соединяясь с этими молекулами, активизируется и связывается с геном-оператором. В результате синтез данного вещества прекращается. Свое название белок-репрессор получил из-за того, что подавляет деятельность гена-оператора, то есть ставит его в положение «выключено».
При малом количестве синтезируемых молекул белок-репрессор остается неактивным. В таких условиях действие оперона – гена-оператора и структурных генов – не подавляется, и синтез будет продолжаться беспрепятственно.
ДНК. Механизмы хранения и обработки информации. Часть II
Привет Хабр! Сегодня мы продолжим прошлый рассказ о ДНК. В нем мы поговорили о том, сколько ее бывает, как ДНК хранится и почему так важно то, как она хранится. Сегодня мы начнем с исторической справки и закончим основами кодирования информации в ДНК.
История
Сама по себе ДНК была выделена еще в 1869 году Иоганном Фридрихом Мишером из лейкоцитов, которые он получал из гноя. Лейкоциты это белые клетки крови, выполняющие защитную функцию. В гное их довольно много, ведь они стремятся к поврежденным тканям, где «поедают» бактериальные клетки. Он выделил вещество, в состав которого входят азот и фосфор. Вначале оно получило название нуклеин, однако, когда у него обнаружили кислотные свойства, название изменили на нуклеиновую кислоту. Биологическая функция новооткрытого вещества была неясна, и долгое время считалась, что в нем запасается фосфор. Даже в начале XX века многие биологи считали, что ДНК не имеет никакого отношения к передаче информации, поскольку строение молекулы, как тогда казалось, было слишком однообразным и не могло закодировать столько информации.
К 1901 году Альбрехт Коссель выделил и описал пять азотистых оснований, входящих в состав ДНК и РНК. А еще чуть позже Петр Левен установил, что углеводным компонентом нуклеиновых кислот являются дезоксирибоза и рибоза. Нуклеиновые кислоты, в состав которых входит рибоза стали называть рибонуклеиновыми кислотами или, сокращенно, РНК, а те, которые содержали дезоксирибозу, дезоксирибонуклеиновыми кислотами, или ДНК.
Теперь, встал вопрос, как отдельные звенья соединены между собой. Для этого цепи ДНК нужно было разрушить и посмотреть на то, что получится после разрушения. Для этого полимер ДНК подвергался гидролизу. Однако Левен изменил метод гидролиз. Теперь вместо многочасового кипячения в закисленной среде он использовал ферменты. На этот раз из гидролизатов удалось выделить не только отдельные аденин, гуанин, тимин, цитозин, дезоксирибозу и фосфорную кислоту, но и более крупные фрагменты, например соединения азотистых оснований с углеводом или углевода с фосфорной кислотой. Вместе с тем в гидролизатах нуклеиновых кислот не были обнаружены соединения, состоящие из двух азотистых оснований, или соединения типа основание – фосфорная кислота. То есть стало понятно, что фосфорная кислота соединяется с сахаром, а он в свою очередь, с азотистым основанием. Соединения азотистых оснований с углеводом было предложено называть нуклеозидами, а фосфорные эфиры нуклеозидов назвали нуклеотидами.
В результате этих работ Левен пришел к выводу, что нуклеиновые кислоты являются полимерами. В качестве мономеров служат нуклеотиды. Содержание каждого из четырех нуклеотидов в ДНК, или РНК, по данным химического анализа того времени, представлялось Левену равным. Поэтому Левен предложил следующую теорию строения нуклеиновых кислот: они являются полимерами, мономерами которых служат блоки из четырех нуклеотидов, соединенных последовательно.
Теория тетрануклеотидного строения в то время выглядела вполне обоснованно, войдя во все учебники довоенного времени. Однако вопрос функции ДНК оставался неясным. Чтобы прояснить этот вопрос понадобилось почти полвека.
Наступил период, во время которого биологи накапливали сведения об распространении нуклеиновых кислот в различных типах животных и растительных тканей, в бактериях и вирусах, в некоторых одноклеточных организмах.
В то время научное сообщество всерьез полагало, что за хранение генетической информации ответственны именно белки. Традиционное представление о первичной роли белков в жизненном процессе не позволяло и думать о том, что столь важное вещество, как вещество наследственности, могло быть чем-либо, кроме белка. Белки были крайне разнообразны по своей структуре, чего тогда не могли сказать о нуклеиновых кислотах. Известный советский генетик-цитолог Н. К. Кольцов подсчитал, что, варьируя последовательность 20 аминокислот, входящих в состав белковой молекулы, можно создать триллионы непохожих друг на друга белков.
Если бы мы захотели напечатать в самой упрощенной форме, как печатаются логарифмические таблицы, этот триллион молекул и предоставили для выполнения этого плана все ныне существующие типографии мира, выпуская в год 50000 томов по 100 печатных листов, то до конца предпринятой работы протекло б столько времени, сколько его прошло с архейского периода д наших дней.
Действительно много… 20 в 20й… А ведь последовательности бывают куда длиннее чем 20 аминокислот.
А вот как пишет по этому поводу А. Р. Кизель – один из наиболее эрудированных биохимиков того времени.
Из только что приведенных воззрений на роли нуклеиновой кислоты… вытекает ее непричастность к строению генов и следует, что гены составлены из какого-то другого материала. Этого материала мы еще достоверно не знаем, несмотря на то, что он в большинстве случаев прямо называется белком.
Первый успех пришел из микробиологии. В 1944 г. были опубликованы результаты опытов Эвери и сотрудников (США) по трансформации бактерий. Пару слов о трансформации.
Сама трансформация была открыта в 1928 году микробиологом Гриффитсом.
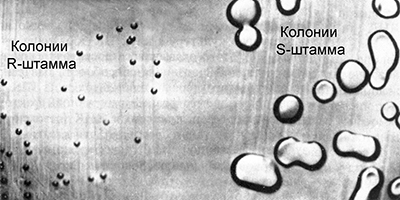
Гриффит работал с культурами пневмококка (Streptococcus pneumoniae) возбудителя одной из форм пневмонии. Некоторые штаммы этой бактерии являются вирулентными, вызывая воспаление легких. Их клетки покрыты полисахаридной капсулой, защищающей бактерию от действия иммунной системы. В культуре такие бактерии образуют крупные гладкие колонии правильной сферической формы. Благодаря этому, они получили название S–штаммы (от английского smooth – гладкий).
Существуют различные вирулентные штаммы пневмококка, они отличаются по антителам, которые вырабатываются в организме при попадании в него бактерий. Их называют IS, IIS, IIIS и т. д. Время от времени некоторые клетки вирулентных штаммов S мутируют, утрачивая способность синтезировать полисахаридную оболочку, и становятся авирулентными. В культуре они образуют мелкие шероховатые колонии неправильной формы, из-за этого получили название R–штаммов (от английского rough – шероховатый). Иногда происходят обратные мутации, восстанавливающие способность к синтезу полисахаридной оболочки, но только в группах соответствующих штаммов:
IIS — IIR
IIIS — IIIR
Это говорит о том, что авирулентные R–штаммы всегда соответствуют родительскому вирулентному S–штамму.
Гриффит вводил разным группам лабораторных мышей вирулентный и авирулентный штамм пневмококка. В первой контрольной группе инъекция вирулентного штамма IIIS приводила к гибели животных. Животные второй контрольной группы после инъекции авирулентного штамма IIR оставались живы. После этого Гриффит нагревал раствор с культурой вирулентого штамма IIIS при температуре 60 °С, что привело к гибели бактерий. Убитые нагреванием бактерии он ввел третьей группе подопытных мышей. Животные остались живы, что в принципе и ожидалось. Однако это не все. Он ввел части выживших мышей бактерии авирулентного штамма IIR.
Казалось, ни к каким страшным последствиям для мышей это не могло привести. Однако вопреки ожиданиям, животные погибли. Когда из их тел были выделены бактерии и высеяны в культуру, оказалось, что они относятся к вирулентному штамму IIIS.
Тот факт, что вызывающие гибель мышей клетки синтезировали полисахаридную оболочку типа III, а не II, свидетельствовал о том, что они не могли возникнуть в результате обратной мутации IIR — IIS. Из этого Гриффит сделал очень важный вывод. Авирулентные бактерии штамма IIR могут трансформироваться в вирулентные как-то взаимодействуя с убитыми нагреванием бактериями штамма IIIS, которые еще оставались в теле мышей. Другими словами, авирулентные бактерии штамма IIR получают от мертвых бактерий штамма IIIS некий фактор, превращающий их в вирулентные. Однако, что это за фактор, Гриффит не знал.
Собственно этот феномен и был назван бактериальной трансформацией. Он представляет собой однонаправленный перенос наследственных признаков от одной бактериальной клетки к другой.
Теперь вернемся к опытам Эвери. Схема их экспериментов несколько схожа с экспериментами Гриффитса. Эвери и сотрудники поставили перед собой задачу выяснить химическую природу трансформирующего агента. Они разрушали суспензию пневмококков и удаляли из экстракта белки, капсульный полисахарид и РНК, однако трансформирующая активность экстракта сохранялась. Трансформирующая активность препарата не терялась при его обработке кристаллическим трипсином или химотрипсином (разрушающими белки), рибонуклеазой (разрушает РНК). Было ясно, что препарат не являлся ни белком, ни РНК. Однако трансформирующая активность препарата полностью утрачивалась при обработке его дезоксирибонуклеазой (разрушающей ДНК), причем ничтожные количества фермента вызывали полную инактивацию препарата. Таким образом, было установлено, что трансформирующий фактор у бактерий является чистой ДНК. Этот вывод явился значительным открытием, и Эвери отлично сознавал это. Он писал, что это как раз то, о чем давно мечтали генетики, а именно вещество гена. Кажется вот оно доказательство. Но уж слишком сильна была вера в белок, как вещество наследственности. Некоторые считали, что трансформацию могут вызывать и те ничтожные примеси белка, которые оставались в препарате.
Новым доказательством прямой генетической роли ДНК явились опыты вирусологов Херши и Чейз. Они работали с бактериофагом Т2 (Бактериофаги — вирусы бактерий), который заражает бактерию Escherichia coli (кишечную палочку).
Собственно что они сделали. В состав ДНК одних бактериофагов они включили радиоактивный фосфор (P32), а в состав белков других — изотоп серы (S35). Для этого одни бактерии выращивались на среде с добавлением радиоактивного фосфора в составе фосфат иона, другие — на среде с добавлением радиоактивной серы в составе сульфат иона. Затем к этим бактериям добавлялся бактериофаг Т2, который, размножаясь в клетках бактерий, включал радиоактивную метку в свою ДНК (P есть в ДНК, но нет в белках), или белки (S есть в белках, но нет в ДНК).
После выделения радиоактивно-меченых бактериофагов их добавляли к культуре свежих (не содержащих изотопов) бактерий. Что приводило к инфицированию этих бактерий. Бактериофаг присоединяется к клетке бактерии и «впрыскивает» свою ДНК. После этого среду с бактериями подвергали энергичному встряхиванию в специальном смесителе (было показано, что при этом оболочки фага отделяются от поверхности бактериальных клеток), а затем инфицированных бактерий отделяли от среды. Когда в первом опыте к бактериям добавлялись меченые фосфором-32 бактериофаги, оказалось, что радиоактивная метка находилась в бактериальных клетках. Когда же во втором опыте к бактериям добавлялись бактериофаги, меченые серой-35, то метка была обнаружена во фракции среды с белковыми оболочками, но её не было в бактериальных клетках. Это подтвердило, что материалом, которым инфицировались бактерии, является ДНК. Поскольку внутри инфицированных бактерий формируются полные вирусные частицы, содержащие белки вируса, данный опыт стал одним из решающих доказательств того факта, что генетическая информация (информация о структуре белков) содержится в ДНК.
Эти открытия сильно повлияли на многих биологов того времени. В особенности на знаменитого своими правилами Чаргаффа. Он считал, что Эвери по сути открыл ‘новый язык’, или как минимум показал, где его искать.
Чаргафф принялся искать разницу в нуклеотидном составе и расположении нуклеотидов в препаратах ДНК, полученных из различных источников. И, поскольку методов позволяющих точно дать химическую характеристику ДНК, в то время не существовало… ему пришлось их придумать. Им было показано, что старая тетрануклеотидная теория строения нуклеиновых кислот неверна. ДНК у разных организмов по составу и строению сильно отличаются. При этом обнаружились новые факты, не установленные ранее для других природных полимеров, а именно регулярности в соотношении отдельных оснований в составе всех исследованных ДНК. Сейчас даже школьники знают их, как правила Чаргаффа.
Потихоньку мы подошли к двум легендарным людям, открывшим структуру ДНК. Фрэнсис Крик и Джеймс Уотсон встретились впервые в 1951 году. Уотсон тогда решил заняться структурой ДНК. Как биолог, он понимал, что при выборе определенной структуры ДНК нужно учитывать существование какого-то простого принципа удвоения молекулы ДНК, заложенного в ее структуре. Ведь одним из важнейших свойств генов является передача наследственной информации.
Криком же была создана теория дифракции рентгеновских лучей на спиралях, позволяющая определить, находится исследуемая структура в спиральной конформации или нет. В то время рентгенограммы ДНК уже существовали. Их получили в Лондоне Морис Уилкинс и Розалинд Фрэнклин.
По характеру рентгенограммы ДНК Уотсон и Крик поняли, что исследуемая структура находится в спиральной конформации. Они знали также, что молекула ДНК представляет собой длинную линейную полимерную цепь, состоящую из мономеров-нуклеотидов. Фосфодезоксирибозный костяк этого полимера непрерывен, а сбоку к дезоксирибозным остаткам присоединены азотистые основания. Для построения моделей оставалось решить вопрос, сколько цепей линейного полимера уложено в компактную структуру.
На основании рентгенограммы В-формы ДНК Уотсон и Крик предположили, что молекула ДНК состоит из двух линейных полинуклеотидных цепей с фосфодезоксирибозным остовом снаружи молекулы и азотистыми основаниями внутри ее. Что в последствии подтвердилось. Оставалось только решить вопрос о порядке расположения азотистых оснований двух цепей внутри биспирали.
Рассматривая возможные комбинации пар азотистых оснований, Уотсон обнаружил, что пары аденин–тимин и гуанин–цитозин имеют одинаковый размер и стабилизируются водородными связями. Сразу же объяснялись и правила Чаргаффа: если в биспирали ДНК аденин одной цепи всегда соединяется с тимином другой цепи, а гуанин всегда входит в паре с цитозином, то аденина в составе ДНК должно быть всегда столько же, сколько тимина, а гуанина – столько же, сколько цитозина. Ясно было также, как должно происходить удвоение молекулы ДНК. Каждая цепь комплементарна другой, и в процессе репликации ДНК цепи биспирали должны разойтись и на каждой полинуклеотидной цепи должна достроиться комплементарная к ней цепь. Тут тоже было несколько теорий, но о них через неделю, в следующей статье.
Кодирование информации
Итак, мы знаем, что ДНК — носитель информации, знаем из чего она состоит. Но как кодирует информацию — все еще не понятно.
Собственно у нас есть 64 варианта и 20 аминокислот. Аминокислоты могут кодироваться разными кодонами. Так же существуют старт и стоп кодоны, с которых начинается считывание.
Не забываем, что сначала ДНК считывается в РНК, с которой уже происходит считывание в белок.
Таблица внизу — соответствие кодонов РНК аминокислотам. Помним, что в РНК нет тимина, вместо него идет урацил.
Если вы не нашли в таблице старт кодон — поищите AUG. Он кодирует метионин и одновременно является стартовым. При трансляции генов прокариот, пластидных и митохондриальных генов стартовой аминокислотой является N-формилметионин (это просто для справки)).
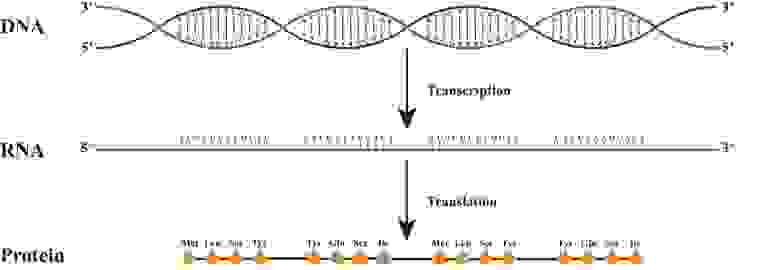
Если расписать весь путь от ДНК до белка, получим что-то такое.
На данном рисунке синтез идет с красной цепи. Как следствие РНК будет совпадать с синей цепью (не забываем про замену Т на У)
Как я уже говорил, каждую аминокислоту может кодировать несколько кодонов. На первый взгляд это кажется не особо нужным побочным эффектом избыточности числа кодонов. Но у него, на самом деле, довольно важная роль.
Тут мы немного затронем мутации. Они бывают разных типов. От хромосомных, когда целые куски хромосом удаляются из генома, меняются местами, дублируются, до точечных, когда происходит замена одного азотистого основания на другое. Сфокусируемся на точечных мутациях.
К чему могут привести точечные мутации?
Кодон может начать кодировать другую аминокислоту, что не всегда страшно. Такие мутации называются миссенс-мутацими (то есть со сменой смысла). Это может повлиять на структуру белка. Например если положительно заряженная аминокислота заменится на отрицательно заряженную — это может сделать белок нестабильным, или приведет к тому, что он свернется в другую конформацию (да, линейная последовательность аминокислот обычно сворачивается в определенную форму) и не сможет выполнять свои функции (или начнет делать это лучше, это уже попахивает эволюцией).
Если конкретно, то гемоглобин S имеет единичную замену нуклеотида (А на Т) в кодирующем гене. В результате триплет ГАГ, кодирующий глутамат, заменяется на ГТГ, кодирующий валин. Гемоглобин S тоже может транспортировать кислород, но делает это хуже чем обычный гемоглобин.
В молекуле гемоглобина Хикари аспарагин замещен на лизин, однако он все также хорошо перенести кислород.
Как пример с потерей функции рассмотрим гемоглобин M. Другая точечная мутация в гене гемоглобина приводит к полной утрате функции (гистидин меняется на тирозин в активном центре).
Кстати, сворачивание белка выглядит примерно так, если опустить все нюансы.
Что еще может произойти?
Замена одного азотистого основания может так же привести к появлению стоп кодона в центре последовательности, или наоборот стоп кодон в конце исчезнет. На выходе получится либо неполная цепь, либо экстремально длинная цепь, которые в любом случае не смогут нормально функционировать. Такие мутации называются нонсенс.
Есть еще третий тип мутации — сайленс-мутация. По сути происходит смена кодона на другой, кодирующий ту же аминокислоту. Свойства белка не меняются.
Подитожим общей схемой.
В завершение хотел бы еще рассказать об одной интересной особенности. Одну аминокислоту может кодировать несколько кодонов. Это мы знаем. Но что это значит? Организм использует сразу все кодоны для кодирования. Но какие-то чаще, какие-то реже.
Сравним человека и… кишечную палочку (Escherichia coli) по частоте использования кодонов кодирующих цистеин.
Он кодируется двумя кодонами UGU и UGC.
Человек
UGU 10.6
UGC 12.6
Кишечная палочка (штамм O127:H6)
UGU 19.1
UGC 0.0
Цифры это встречаемость триплета на тысячу. Видно, что мы используем оба кодона примерно с одинаковой частотой, в то время как E. coli почти не использует UGC кодон.
Об этой особенности нужно помнить, особенно когда ты занимаешься геноинженерией и хочешь нарабатывать продукт гена одного организма в другом. Если ген человека, с частой встречаемость UGC кодона попытаться вставить в кишечную палочку данного штамма — вас ждет разочарование. В клетке аминокислоты связаны с транспортными РНК, каждая из которых соответствует своему кодону. Так вот тРНК соответствующих UGC кодону будет крайне мало, что сильно замедлит синтез.
Если интересно, тут можно посмотреть отличия в кодонном составе у разных организмов.
Кодонный состав может сильно отличаться как у организмов разных видов, так и разных штаммов. Так у Escherichia coli O157:H7 EDL933 все более менее поровну в плане UGC и UGU. Или вот еще пример. У штаммов туберкулезной палочки выделенных в разных странах также отличается кодовый состав.
Подытожу
В этот раз было очень много истории и относительно мало биологии. Больше такого не будет. Мы поговорили о том, как стало понятно, что ДНК — носитель информации, как она хранится в самой ДНК. Поговорили об избыточности ген кода и о том, к чему это приводит. Немного затронули мутации и разницу в частоте использования определенных кодонов.
В следующий раз поговорим о репликации ДНК.