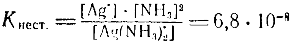Свойства и область применения серебра
Аргентум, или серебро — металл и химический элемент, которому присвоен атомный номер 47 в периодической таблице Менделеева. Химическая формула металла — Ag. Серебро было исследовано человечеством еще в четвертом тысячелетии до нашей эры. Открытие этого металла обошлось без помощи ученых, поскольку он был найден человеком как самородное серебро. Причем самородки достигали весьма впечатлительных размеров. К примеру, в пятнадцатом столетии был добыт самородок массой свыше 20 тонн.
Однако добыча серебра требовала больше усилий по сравнению с теми, которые приходилось прикладывать для добычи золота. По этой причине на протяжении нескольких столетий серебро стоило дороже золота. Запасы серебряной руды на Земле на сегодня составляют свыше 550 тонн, причем государствами-лидерами в добыче серебра считаются:
Драгоценный металл содержится в коре Земли в концентрации 70 миллиграммов на тонну. В условиях природы аргентум встречается в большинстве случаев в рудных залежах в комбинации с другими элементами. В природе находится свыше пятидесяти видов серебряных руд, однако эффективными, с точки зрения экономики, считаются такие:
Серебро может встречаться в природе совместно с золотом, и такое образование называется электрумом. Благородный металл в большом количестве сосредоточен в рудах, содержащих уран, висмут и никель.
Самородное серебро есть в сульфидных рудах, в которых оно образует мельчайшие кристаллы, распыленные среди других металлов, из которых состоят руды. На изломах кристаллы имеют неровную угловатую поверхность, что делает их похожими на крючки. Это находка, которая встречается в природных условиях гораздо реже золота. Причем внешний вид таких самородков весьма необычный. Из-за своей пластичности серебро образует самородки, напоминающие решетки, трубочки, ветви и жгуты. По этой причине такое серебро не используется в промышленных целях, а служит лишь экспонатом в музеях.
Физико-химические свойства
Серебро как металл характеризуется белым металлическим блеском. Среди всех существующих в природе металлов элемент аргентум обладает высокой электропроводностью и теплопроводностью. Твердость серебра составляет 25 килограмм-сил на кубический миллиметр. Именно это качество и определяет прочность и износостойкость металла.
Плотность — это еще одна характеристика, определяющая физические свойства драгоценного металла. Плотность серебра составляет 10,5 грамма на кубический сантиметр. Аргентум также отличается тугоплавкостью (температура плавления составляет 962 градуса). В то же время серебро невероятно пластичное, особенно в чистом виде. Так, из этого металла без труда можно изготовить тончайшую пластину или скрутить нить.
Металл выдерживает сильные нагрузки, поэтому из него изготавливаются контактные элементы для вычислительной техники, космических ракет, подводных лодок и других агрегатов. Серебро идеально отражает свет, из-за чего этот металл используется в изготовлении высокоточных зеркал.
Аргентум не вступает в реакцию с такими элементами:
Серебро вступает в реакцию с серой, при этом образуя сульфид серебра. В реакцию с галогенами аргентум вступает при нагревании. При контакте с концентрированной азотной кислотой превращается в нитрат серебра и диоксид азота. Серебро также реагирует на концентрированную серную кислоту. При высокой температуре аргентум может вступать в реакцию с соляной кислотой.
Применение серебра
Физико-химические свойства аргентума позволяют с успехом применять его в ювелирной промышленности, производстве технических приборов и в медицине.
При изготовлении ювелирных изделий и столовых приборов серебро никогда не используется в чистом виде, а все из-за пластичности этого металла. Добавление в сплав серебра более прочных металлов, к примеру, меди, позволяет придать ему устойчивость к деформации. Для оценки содержания драгоценного металла в сплаве используется такая мера, как проба. Она подается в виде трехзначного числа, демонстрирующего содержание серебра в килограмме сплава. К примеру, проба 925 означает, что масса серебра в килограмме сплава составляет 925 граммов, или 92,5 %.
Серебряное кольцо 925 пробы
В России официально признанными считаются такие пробы металла:
Серебро, которое используется для изготовления украшений и столовых приборов, со временем темнеет, а все из-за того, что оно окисляется под влиянием воздуха. Но правильный уход за изделиями позволит долго поддерживать их в идеальном состоянии.
Серебро
Быстрый поиск по тексту
Благородный металл белого цвета
Серебро относится к группе древнейших металлов. Человечеству оно знакомо уже около 6 тысяч лет. Тогда оно было найдено на территории Передней Азии. Такое раннее знакомство человека с серебром обусловлено нахождением серебра в виде самородков, иногда достаточно крупного размера. Его не приходилось добывать из руды.
Существует легенда о первом обнаружении металла. Во время охоты егерь, что служил при королевском дворе привязал коня и надолго его оставил одного. Конь долгое время бил копытом по одному и тому же месту. В итоге, раскопал небольшую яму из которой виднелся белый кусок непонятного происхождения. События происходили 968 году, при короле Оттоне 1 Великом, который на том месте заложил первый рудник.
Долгое время считалось, что белый металл дороже золота. Самым древним местом добычи серебра считается Сардиния, где металл был известен с эпохи энеолита.
Латинское название металла – аргентум происходит от индоевропейского корня.
Химический состав
В периодической системе Менделеева имеет название Argentum (Ag), атомный номер – 47, атомная масса – 107,8682, состоит из двух изотопов: 107Ag, 109Ag, период – 5, группа – 11.
Аргентум не растворяется и не реагирует с другими элементами. Исключение составляют:
В соляной и серной кислотах серебро не растворяется, однако, при определенных условиях это может произойти. Серебро может раствориться в концентрате серной кислоты под воздействием высоких температур. А также в условиях присутствия свободного кислорода в соляной кислоте.
Серебро не поддается воздействию кислорода.
Структура кристаллической решетки серебра – кубическая гранецентрированная. Параметры – 486 Å.
Физические свойства серебра
Серебро обладает высокой пластичностью, что позволяет раскатать его до толщины в 0,00025 мм. За счет своего цвета и блеска имеет хорошую склонность к полировке.
Основные физические свойства аргентума:
Серебро широко применяется во многих сферах промышленности благодаря своей электрической и теплопроводности.
Его применение незаменимо в изготовлении контактов для электротехники, для спаивания различных металлов.
Среди предметов, без которых современный человек не может обойтись – аккумуляторы для различных устройств. Они также изготавливаются при помощи аргентума с добавлением цинка и кадмия.
Металл используется как напыление различных поверхностей. Например, при изготовлении зеркал.
В промышленности применяется как катализатор, например, при изготовлении формальдегида метанола. Также как катализатор используется для противогазовых фильтров.
Йодид аргентума – инструмента управления погодой, если нужно «раздвинуть тучи».
Хлорид аргентума необходим для производства инфракрасной оптики.
Кроме того, металл имеет большой спрос в медицине, в изготовлении монет, в ювелирном деле.
Добыча серебра
Ученые сходятся во мнении, что добыча белого драгоценного металла в России началась при Петре I. Добыча велась на Урале и на Алтае.
Сегодня добывают драгоценный металл более, чем в 20 регионах нашей страны. Наибольшие запасы находятся в Магаданской области (19,4 тыс. тонн), в Красноярском крае (16,2 тыс. тонн), в Читинской области (16 тыс. тонн), в Республике Саха (10,1 тыс. тонн), в Республике Бурятия (9 тыс. тонн).
Примерно 80% от добытого серебра использует промышленность, остальное – ювелирная. Наиболее популярными методами добычи, которые используют по всему миру являются цианирование и амальгамирование.
По примерным подсчетам общее количество серебра в мире составляет 512 тонн. Лидерами по запасам являются:
Искусственное серебро
Запасы аргентума на Земле, которые доступны для добычи не так богаты, поэтому есть смысл искусственно синтезировать этот драгоценный металл. В отличие от золота, существуют как лабораторные способы, так и способы домашнего синтеза кристаллов аргентума.
Серебро можно синтезировать, вырастив кристалл аргентума. Такой металл будет аналогом настоящего. Вырастить кристалл можно методом электролиза. В результате, получится чистое серебро. По своим физическим свойствам металл, полученный таким способом практически идентичен природному.
10 самых дорогих металлов в мире
В мире множество самых разнообразных металлов. Стоимость металла напрямую зависит от его количеств на планете. Металлы делятся на природные и искусственно получаемые в лабораторных условиях. И безусловно, как можно предположить, искусственно созданные будут дороже.
В Топ-10 не попадает серебро, которое остаётся на 12 месте, немного опережая 13 место — индий и уступая 11 месту — рутению.
10 место СКАНДИЙ
Природный редкоземельный металл. Легкий и высокопрочный, серебристого цвета с желтым отливом. Впервые элемент был обнаружен в 1879 году шведским химиком Ларсом Нильсоном, который назвал его в честь Скандинавии. Скандий применяется в мире высоких и инновационных технологий. Его используют при конструировании роботов, ракет, самолетов, спутников и лазерной техники. Сплавы данного металла служат в спортивной сфере — для изготовления высококлассного инвентаря. Самые крупные месторождения богатых скандием минералов находятся в Норвегии и на Мадагаскаре.
Стоимость грамма скандия зависит от чистоты металла, но усреднённая стоимость 3-4 доллара. На биржах драгметаллов не продаётся. В ювелирной промышленности используют оксид скандия для производства фианитов.
9 место РЕНИЙ
Существование металла было предсказано Д.И.Менделеевым в 1871 году, но впервые его открыли в 1925 году немецкие химики и назвали в честь реки Рейн. Относительно чистый рений удалось получить только в 1928 году. Для получения 1 грамма рения требовалось переработать более 600 кг норвежского молибденита.
Рений — серебристо-белый металл, очень плотный, занимает третье место по температуре плавления среди металлов. Используется в электронной и химической промышленности. Имеет стратегическое значение, т.к. используется в космических и военных целях.
По природным запасам рения на первом месте в мире стоит Чили, на втором США, а на третьем Россия. Рений получают при переработке сырья с очень низким содержанием целевого компонента. Его запасы в России не более 15 тонн.
Цена на грамм рения в среднем 5 долларов.
В ювелирной промышленности не используется.
На международных биржах металл не продаётся.
8 место ОСМИЙ
Был открыт в 1803 году двумя британскими химиками. Название металл получил от греческого слова osme, что означает «запах». Осмию присущ довольно резкий и неприятный запах, напоминающий смесь чеснока и хлорки.
Осмий — голубовато-серебристый металл платиновой группы, характеризующийся высокой плотностью, тяжёлый, хрупкий. В чистом виде не существует, встречается только в связках с другим металлом из платиновой группы — иридием.
Добывают данный металл на Урале, в Сибири, Южной Африке, Канаде, США и Колумбии. Используется в сплавах в химической промышленности и фармакологии.
Цена одного грамма осмия на мировом рынке составляет 12-17 долларов.
В ювелирной промышленности не используется.
На биржах металл не продаётся.
7 место ПЛАТИНА
Цивилизации Анд доколумбовой Южной Америки добывала и использовала её с незапамятных времён. Первыми европейцами, познакомившимися с платиной в середине 16 века, были испанские конкистадоры, которые и дали ему пренебрежительное название, что означало в переводе «маленькое серебро», «серебришко». Отношение объясняется тугоплавкостью платины, которая не поддавалась переплавке и долгое время не находила применения, она ценилась вдвое ниже серебра.
Примечательно, что испанский король в 1735 году повелел платину в Испанию не ввозить, чтобы мошенники не могли расплачиваться ей вместо ценного серебра. При разработке россыпей в Колумбии повелевалось отделять её от золота и топить под надзором королевских чиновников в глубокой речке, которую стали именовать Платино-дель-Пинто. Королевское распоряжение было отменено через 40 лет, когда мадридские власти приказали доставлять платину в Испанию, чтобы самим фальсифицировать золотые и серебряные монеты. С нею познакомились алхимики, считавшие самым тяжёлым металлом золото, а оказавшаяся более тяжёлой платина была наделена адскими чертами.
В 1790 году во Франции из платины был изготовлен эталон метра, а позже эталон килограмма.
В России платину впервые обнаружили на Урале близ Екатеринбурга 1819 году, а в 1824 году были открыты платиновые россыпи в Нижнетагильском округе. Разведанные запасы платины были столь велики, что Россия на долгие годы заняла первое место в мире по добыче этого металла. В настоящее время лидером является ЮАР.
В природе платина встречается только как сплав с другими металлами.
Металл отличается особым блеском и пластичностью. Активно используют в ювелирной, оружейной, медицинской промышленности. В России и СССР платина применялась при изготовлении монет и знаков отличия за выдающиеся заслуги.
Российский спрос на ювелирную платину в настоящее время составляет 0,1 % от мирового уровня.
Ещё несколько лет назад платина была дороже золота, но в настоящее время цена её составляет не более 28-30 долларов за грамм.
Платина торгуется на международной бирже драгметаллов.
6 место ИРИДИЙ
Мир впервые узнал о нем в 1803 году благодаря британскому химику С. Теннанту, который его открыл одновременно с осмием.
Иридий- металл платиновой группы, тяжелый, твердый и одновременно хрупкий, серебристо-белого цвета. Имеет высокую коррозийную стойкость даже при температуре 2000 °C.
В чистом виде в земных породах не встречается, поэтому высокая концентрация иридия в образцах породы является индикатором космического метеоритного происхождения последних.
Самостоятельно иридий практически нигде не применяется и используется для создания сплавов. Ювелиры добавляют его к платине, поскольку он делает её твёрже, а украшение из такого сплава становится практически вечным. Также он востребован при изготовлении хирургических инструментов, электроконтактов, точных лабораторных весов. Из него делают кончики для дорогих авторучек. Иридий применяется в аэрокосмической технике, биомедицине, стоматологии, химической промышленности.
В течение года мировая металлургия расходует приблизительно одну тонну данного металла. Основное месторождение иридия находится в ЮАР.
Его стоимость равняется около 47-50 долларам за грамм.
Иридий продаётся на биржах драгметаллов.
5 место ЗОЛОТО
Люди добывают золото с незапамятных времён, археологи находят его в обиходе человека с 5 тысяч лет до н.э. в эпоху неолита в самородках. Начало системной добычи было положено на Ближнем Востоке, откуда поставлялись золотые украшения, в т.ч. в Египет.
В России до Елизаветы золото не добывалось. Оно ввозилось из-за границы в обмен на товары и взималось в виде ввозных пошлин. Первое открытие запасов золота было сделано в 1732 году в Архангельской губернии, где вблизи одной деревни была обнаружена золотая жила.
Латинское aurum означает «жёлтое».
Золото — один из немногих металлов, встречающихся исключительно в чистом виде. Чистое золото — металл жёлтого цвета, тяжёлый плотный металл, мягкий, высокопластичный.
Традиционным и самым крупным потребителем золота является ювелирная промышленность. Все ювелирные изделия изготавливают не из чистого золота, а из его сплавов с другими металлами, значительно превосходящими золото по механической прочности и стойкости.
Запасы золота в мире распределено так: около 10 % — в промышленных изделиях, остальное делится приблизительно поровну между централизованными запасами (в основном, в виде стандартных слитков химически чистого золота), собственностью частных лиц в виде слитков и ювелирными изделиями.
США, Китай и Австралия — лидеры по золотодобыче.
Стоимость грамма золота на мировом рынке около 45-50 долларов. Золото и иридий постоянно соперничают в цене, меняясь местами в рейтинге самых дорогих металлов.
4 место ПАЛЛАДИЙ
Назван в честь астероида Паллада, открыт во время изучения платиновых руд в 1803 году.
Палладий — легкий, пластичный серебристо-белый металл из платиновой группы. Он очень легкоплавкий, хорошо полируется, не тускнеет и довольно стоек к коррозии.
Главное направление использования палладия — ювелирная промышленность. Мастера ценят его гибкость и легковесность, что позволяет создавать из него самые удивительные произведения ювелирного искусства.
Металл широко применяется в химической промышленности, медицине, для создания электроники и пр.
Крупнейшее месторождение палладия находится в России.
Стоимость палладия за последние несколько лет сильно возросла и составляет около 60 долларов за грамм.
Палладий торгуется на международной бирже драгметаллов.
3 место РОДИЙ
Открыт в Англии в 1803 году (плодородный год на открытие металлов. ) в ходе работ с самородной платиной. Назван в честь розы (греч.), т.к. типичные соединения родия имеют глубокий тёмно-красный цвет.
Родий — это твердый благородный металл, обладающий мощнейшими отражающими свойствами, стойкостью к окислению и коррозии. За год во всем мире добывается всего лишь 30 тонн родия.
Применяют для изготовления зеркал и фар, в автомобильной и химической промышленности.
Ювелиры используют электролиты родия для получения износостойких и коррозионно-устойчивых покрытий. В дорогой и высококачественной бижутерии можно встретить родированное покрытие.
Монеты из родия выпускает США, но не как платёжное средство, а в качестве объекта инвестирования средств.
Руанда выпускает монету из чистого родия как платёжное средство.
Самые крупные месторождения находятся в России, Канаде и ЮАР.
Родий торгуется на международной бирже драгметаллов.
2 место ОСМИЙ-187
Металл осмий-187 изотоп, является результатом распада изотопа рения с огромнейшем периодом полураспада. Соотношение изотопного состава осмия и рения позволяет определять возраст горных пород и метеоритов.
Изотопов осмия множество и их разделение представляет собой сложную задачу. Именно поэтому некоторые изотопы довольно дороги.
Самый редкий среди них осмий-187, процесс добычи которого отличается особой сложностью и занимает около девяти месяцев. В результате его получают в виде черного мелкокристаллического порошка с фиолетовым оттенком. Его считают самым плотным на планете. При этом он очень хрупок, его можно растолочь в обычной ступе на мелкие частички. Он имеет важное научно-исследовательское значение, его используют как катализатор химических реакций, для изготовления измерительных приборов высокой точности и в медицинской отрасли.
Казахстан — первое и единственное государство, продающее чистый Осмий-187 на мировом рынке.
Стоимость Осмия-187 оценивается в 200 тысяч долларов за 1 грамм.
Этот изотоп не торгуется на бирже драгметаллов и более того, его международная торговля строго контролируется, пресекается любая контрабандная продажа.
Лидер рейтинга! 1 место КАЛИФОРНИЙ-252
На земле сегодня нет металла, который стоил бы дороже. Рекорд стоимости зафиксирован в Книге Гиннеса. Он является одним из изотопов калифорния.
Баснословная цена составляет 10 миллионов долларов за грамм.
Мировой запас — 8 граммов, а ежегодная добыча –30-40 микрограмм. Получают редкий металл путем сложнейшей и долговременной работы в лабораторных условиях. В чистом природном виде не встречается, полностью искусственного происхождения. Впервые был получен учёными в 1950 году в США.
Главная ценность калифорния-252 состоит в его невероятной энергии, сравнимой с энергией среднего атомного реактора. Применяется в ядерной физике и в медицине в качестве лучевой терапии раковых новообразований. С его помощью научились определять месторождения золота и серебра. Используют для выявления дефектов в реакторах и самолетах, которые невозможно выявить даже при помощи рентгена.
В мировом рейтинге самых дорогих веществ калифорний-252 занимает 2 место, уступая по цене лишь Антиматерии.
Серебро (Argentum) всё о ювелиром металле
Серебро (Argentum) это
В 1956 г. добыча серебра в капиталистических странах составила 5,7 тыс: т. Из этого количества почти половина добыта в Мексике и США.
Добыча Ag
В СНГ серебро добывается из серебро-свинцовых руд, месторождения которых имеются на Урале, Алтае, Северном Кавказе, в Казахстане и некоторых других местах.
Первый способ заключается в том, что содержащий серебро свинец (так называемый «веркблей») плавят и дают ему медленно остывать. При охлаждении на поверхности сплава выделяются кристаллы чистого свинца, которые вычерпывают ковшами. Когда таким образом остаток обогатится серебром, его подвергают окислению, продувая через него сильную струю воздуха. Свинец переходит при этом в окись свинца, а серебро остается в чистом виде.
Второй способ основан на том, что расплавленный цинк не смешивается с расплавленным свинцом, а серебро гораздо лучше растворяется в расплавленном цинке, чем в свинце.
При прибавления цинка к расплавленному свинцу, содержащему серебро, все серебро почти полностью переходит в цинк, который затем вычерпывают и подвергают перегонке. Оставшееся после отгонки цинка серебро очищают от небольшой примеси свинца так же, как при первом способе.
Чистое серебро это
Чистое серебро — очень мягкий, тягучий металл уд. ; веса 10,49, плавящийся при 960,8°. Оно лучше всех металлов проводит тепло и электрический ток.
В последнее время серебро расходуют в значительных количествах на изготовление аккумуляторов.
В серебряно-цинковых аккумуляторах положительными электродами являются пластинки из чистого серебра, а отрицательными — пластинки из окиси цинка. Электролитом служит раствор едкого кали. Эти аккумуляторы имеют ряд преимуществ перед железо-никелевыми и свинцовыми аккумуляторами и, несмотря на сравнительно высокую стоимость, получили значительное распространение.
Основными преимуществами серебряно-цинковых аккумуляторов являются:
1) большая емкость при сравнительно малом весе;
2) возможность работы в широком интервале температур (от —60 °)
3) хорошая хранимость в заряженном состоянии;
4) возможность использования в значительных пределах изменения атмосферного давления.
Химические свойства металла
Серебро принадлежит к наименее активным металлам, занимая в ряду напряжений одно из последних мест. Оно не окисляется на воздухе ни при обыкновенной температуре, ни при нагревании. Наблюдаемое часто почернение серебряных предметов происходит вследствие образования черного сульфида серебра Ag2 S под влиянием содержащегося в воздухе сероводорода, а также при соприкосновении с пищевыми продуктами, содержащими сернистые соединения.
Соляная и разбавленная серная кислоты не действуют на серебро. Растворяют серебро обычно в азотной кислоте.
Серебро образует только один ряд солей, растворы которых содержат бесцветные катионы Ag •
Соли серебра
Окись серебра Ag 2О. При действии щелочей на растворы серебряных солей можно было бы ожидать получения гидрата окиси серебра AgOH, но вместо него выпадает бурый осадок окиси серебра:
В большом количестве воды окись серебра заметно растворяется, сообщая раствору щелочные свойства. Такой раствор окрашивает лакмус в синий цвет и, подобно щелочам, осаждает гидраты окисей многих металлов из растворов их солей. Очевидно, в растворе содержится некоторое количество гидрата окиси серебра AgOH, представляющего собой довольно сильное основание. Последнее обстоятельство подтверждается также тем, что соли серебра не гидролизуются.
Кроме окиси серебра, известна также перекись серебра Ag2O2, образующаяся при действии на серебро озона.
Из солей серебра наиболее важными являются следующие:
1. Нитрат серебра, или азотнокислое серебро AgNO3, называемое также ляписом. Образует бесцветные прозрачные кристаллы, легко растворимые в воде. Получается путем растворения серебра в азотной кислоте. Применяется в медицине для прижигания, так как ион серебра действует на органические вещества окисляющим образом, восстанавливаясь сам до металлического серебра. Служит исходным веществом при получении других соединений серебра. Применяется в фотографической промышленности, в производстве зеркал, в гальванопластике.
2. Хлорид серебра, или хлористое серебро AgCl. Образуется в виде белого, творожистого, нерастворимого в воде и кислотах осадка при встрече ионов Ag • с ионами Сl. На свету хлористое серебро постепенно темнеет, разлагаясь с выделением металлического серебра. Такими же свойствами обладают бромистое и йодистое серебро, имеющие, в отличие от хлористого серебра, желтоватый цвет. Напротив, фтористое серебро AgF растворимо в воде.
Комплексные соединения серебра. Подобно меди, серебро обладает ярко выраженной склонностью к образованию комплексных соединений.
Многие нерастворимые в воде соединения серебра как, например, Ag2O, AgCl и др., легко растворяются в водном аммиаке. Причиной растворения является образование комплексных аммиачно-серебряных ионов [Ag(NH3)2] • при встрече молекул аммиака с ионами серебра.
Происходящий процесс в случае, например, хлористого серебра можно изобразить в виде следующей схемы:
Хлористое серебро посылает в раствор некоторое количество ионов Ag • после чего между ними и осадком устанавливается динамическое равновесие. При прибавлении аммиака молекулы его связываются с ионами серебра в комплексные ионы [Ag(NH3)2] • и равновесие непрерывно смещается вправо, пока весь осадок не растворится. Таким образом, в аммиачном растворе серебро находится в виде комплексных катионов [Ag(NH3)2] • . Но наряду с ними в растворе всегда остается и некоторое, хотя и незначительное, количество ионов Ag • вследствие диссоциации комплексного иона по уравнению
Диссоциация ионов [Ag(NH3)2] • согласно приведенному выше уравнению,, как и диссоциация всякого слабого электролита, подчиняется закону действия масс и может быть охарактеризована соответствующей константой, называемой константой нестойкости комплексного иона:
Константы нестойкости для различных комплексных ионов весьма различны и могут служить мерой устойчивости комплекса.
Особенной устойчивостью обладают комплексные анионы, об разующиеся путем соединения ионов Ag • с ионами CN’.
Если к раствору AgNО3 прибавить цианистого калия, то выпадает белый осадок цианистого серебра:
В избытке цианистого калия осадок легко растворяется, переходя в комплексную соль K[Ag(CN)2], существующую в растворе в виде ионов К • и [Ag(CN)2]’: AgCN + KCN = К[ Ag(CN)2]
или в ионной форме
При выпаривании раствора K[Ag(CN)2] выделяется в твердом виде.
Применение металла
Все соединения серебра легко восстанавливаются с выделением металлического серебра.
Если к аммиачному раствору окиси серебра, находящемуся в стеклянном сосуде, прибавить в качестве восстановителя немного глюкозы или формалина, то металлическое серебро выделяется в виде плотного блестящего зеркального слоя на поверхности стекла. Этим способом в настоящее время готовят зеркала, а также серебрят внутреннюю поверхность стеклянных сосудов в термосах для уменьшения потери тепла путем лучеиспускания.
Фотография. Соли серебра, особенно хлористая и бромистая, ввиду их способности разлагаться под влиянием света с выделением металлического серебра, широко используются в фотографии для приготовления светочувствительных пластинок, пленок и бумаг.
Фотографические пластинки и пленки изготовляются следующим образом. К теплому раствору азотнокислого серебра прибавляют некоторое количество желатины и смешивают его с раствором КВr. Образуются бромистое серебро и азотнокислый кглий согласно уравнению
Вследствие защитного действия желатины бромистое серебро не выпадает в осадок, а остается в растворе в виде тончайшей мути. Полученная мутная жидкость носит название «бромосеребряной эмульсии» (правильнее было бы сказать — суспензии). Так как в очень мелко раздробленном виде AgBr мало светочувствительно, то эмульсию оставляют на некоторое время в теплом месте, пока не произойдет так называемый процесс созревания, состоящий в уменьшении степени дисперсности бромистого серебра и образовании более крупных частиц: от этого светочувствительность AgBr увеличивается в сотни раз.

По окончании процесса созревания эмульсию охлаждают, полученный студень желатины дробят и промывают водой для удаления KNO3, затем, расплавив студень, обливают им стеклянные пластинки или целлулоидные пленки. Все эти процессы ведутся при красном све те, который не действует на бромистое серебро.
Если фотографическую пластинку выставить на свет, то потемнение ее происходит довольно медленно. Однако этот процесс может быть чрезвычайно ускорен действием на пластинку различных веществ, называемых проявителями. Замечательно, что проявитель может разлагать (восстанавливать) бромистое серебро лишь после того, как оно подвергалось освещению, хотя бы даже очень непродолжительное время (доли секунды).
Чтобы получить на фотографической пластинке изображение снимаемого предмета, ее помещают в фотографическую камеру и в течение очень короткого времени подвергают действию лучей, проходящих через объектив аппарата (систему собирающих линз) и дающих на пластинке изображение предмета. Если затем опустить пластинку в раствор какого-нибудь проявителя (это делается в темной комнате при красном свете), то подвергшиеся освещению места пластинки довольно быстро темнеют и на пластинке появляется изображение снятого предмета. Такой, процесс называется проявлением.

Таким образом получается негатив, т. е. обратное изображение, на котором светлые части снятого предмета являются темными и, наоборот, темные — светлыми (рис. 145).
С негатива можно получить нормальное изображение или позитив (рис. 146) на светочувствительной бумаге, приготовляемой так же, как пластинки Для этого негатив накладывают на бумагу и на короткое время выставляют на свет. Затем бумагу проявляют и фиксируют.
Существуют также бумаги, светочувствительный слой которых содержит хлористое серебро. На таких бумагах печатают без последующего проявления, выдерживая бумагу под негативом на свету, пока на Ней не получится видимое изображение, после чего отпечаток фиксируют.
Вы читаете, статья на тему Серебро (Argentum)
Похожие страницы:
Понравилась статья поделись ей